Клинический случай успешного применения ниволумаба у пациентки с рецидивом В-клеточного острого лимфобластного лейкоза после терапии CAR-T клетками
Автор: Зикунова И.А., Кручинкина Ю.А., Субора А.Ю., Кисиличина Д.Г., Луговая А.М., Скурихина В.Е., Булусов М.П., Юнусов А.У., Урнова Е.С., Шалаев С.А., Кручинкин А.А., Жеребцова В.А., Бутаев Л.С., Отморская А.А., Капланов К.Д., Птушкин В.В.
Журнал: Вестник гематологии @bulletin-of-hematology
Рубрика: Клинический случай
Статья в выпуске: 1 т.22, 2026 года.
Бесплатный доступ
Острый лимфобластный лейкоз (ОЛЛ) – злокачественное заболевание системы кроветворения, характеризующееся неконтролируемой пролиферацией незрелых лимфоидных клеток в костном мозге с последующим выходом в периферическую кровь и возможным экстрамедуллярным распространением. У взрослых пациентов ОЛЛ имеет неблагоприятный прогноз. Согласно данным регистров, ежегодная частота ОЛЛ увеличивается с 0,39 случая на 100 000 населения в возрасте 35-39 лет, до 2,1 случая на 100 000 населения – в возрасте ≥85 лет. Несмотря на значительный прогресс в лечении ОЛЛ, проблема резистентности заболевания и развития рецидивов сохраняет свою актуальность. В данной работе приводится описание случая молодой пациентки с рецидивирующим/рефрактерным (р/р) ОЛЛ, получавшей лечение Т-клетками с химерным антигенным рецептором (CAR-T) после двух неудачных трансплантаций периферических стволовых клеток. Через девять месяцев после CAR-T у пациентки возник молекулярный рецидив, в связи с чем было принято решение о терапии препаратом ниволумаб. Биологическим обоснованием для применения ингибиторов PD-1 при ОЛЛ служит экспрессия лиганда PD-L1 на бластных клетках, что было показано в ряде исследований. После первого введения ниволумаба измеримая остаточная болезнь не выявлялась и сохранялась В-клеточная деплеция. Согласно нашим данным, это первый успешный случай применения ниволумаба у пациентки с ОЛЛ в качестве преодоления резистентности после терапии CAR-T-клетками.
Ниволумаб, острый лимфобластный лейкоз, трансплантация костного мозга, CAR-T
Короткий адрес: https://sciup.org/170211665
IDR: 170211665
A clinical case of successful use of nivolumab in a patient with relapsed B‑cell acute lymphoblastic leukemia after CAR‑T cell therapy
Acute lymphoblastic leukemia (ALL) is a malignant disease of the hematopoietic system characterized by the uncontrolled proliferation of immature lymphoid cells in the bone marrow, followed by their release into the peripheral blood and possible extramedullary spread. In adults, ALL has a poor prognosis. According to registry data, the annual incidence of ALL increases from 0.39 cases per 100,000 people aged 35-39 years to 2.1 cases per 100,000 people aged 85 years or older. Despite significant progress in the treatment of ALL, the problem of disease resistance and relapse remains relevant. This paper describes the case of a young patient with relapsed/refractory (r/r) ALL who received chimeric antigen receptor T-cell (CAR-T) therapy after two failed peripheral stem cell transplants. Nine months after CAR-T, the patient was diagnosed with minimal residual disease (MRD), and a decision was made to begin treatment with nivolumab. The biological rationale for the use of PD-1 inhibitors in ALL is the expression of the PD-L1 ligand on blast cells, as demonstrated in several studies. After the first administration of nivolumab, no measurable MRD was detected and B-cell depletion persisted. According to our data, this is the first successful case of nivolumab being used in a patient with ALL to overcome resistance after CAR-T cell therapy.
Текст научной статьи Клинический случай успешного применения ниволумаба у пациентки с рецидивом В-клеточного острого лимфобластного лейкоза после терапии CAR-T клетками
Введение . Острый лимфобластный лейкоз (ОЛЛ), характеризующийся аномальной клональной пролиферацией ранних лимфоидных стволовых клеток или клеток-предшественников и истощением нормальных гемопоэтических клеток в костном
(CAR-T) therapy after two failed peripheral stem cell transplants. Nine months after CAR-T, the patient was diagnosed with minimal residual disease (MRD), and a decision was made to begin treatment with nivolumab. The biological rationale for the use of PD-1 inhibitors in ALL is the expression of the PD-L1 ligand on blast cells, as demonstrated in several studies. After the first administration of nivolumab, no measurable MRD was detected and B-cell depletion persisted. According to our data, this is the first successful case of nivolumab being used in a patient with ALL to overcome resistance after CAR-T cell therapy.
Терапия химерными антигенными рецепторами (CAR-T) представляет собой прорывной метод лечения р/р В-клеточных злокачественных новообразований, включая ОЛЛ [2–5]. Несмотря на успех CAR-T-терапии, варианты лечения рецидивов ограничены. Одним из механизмов ускользания опухоли является индукция иммуносупрессивных путей, в частности пути PD-1/PD-L1 [6]. Биологическим обоснованием для применения ингибиторов PD-1 при ОЛЛ служит экспрессия лиганда PD-L1 на бластных клетках, что было показано в ряде исследований [7, 8]. Первые клинические данные, включая исследование комбинации CAR-T и пембролизумаба, указывают на перспективность данного направления [8, 9].
В связи с этим ингибиторы иммунных контрольных точек, такие как анти-PD-1 моноклональные антитела, рассматриваются в качестве стратегии для преодоления резистентности и продления ремиссии после терапии CAR-T [8–10]. В данном сообщении представлен клинический случай длительного ответа на терапию ниволумабом у пациентки с рецидивом В-ОЛЛ после неудачи аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК) и терапии CAR-T.
Клинический случай
Пациентка дала согласие на использование своих деперсонифицированных медицинских данных в научных исследованиях и публикациях.
Пациентка, 27 лет, поступила в стационар с жалобами на выраженные боли в области спины с иррадиацией в левую нижнюю конечность. В клиническом анализе крови лейкоцитоз до 32 × 10⁹/л, лимфоцитоз 13 × 10⁹/л, бластоз 37%.
В аспирате костного мозга бласты 83%, по данным иммунофенотипирования (ИФТ) костного мозга (КМ) фенотип соответствует В-клеточной линейной направленности (пре-пре-В клеточному варианту (В-II-common) ОЛЛ.
По результатам FISH и цитогенетического исследований выявлен ОЛЛ с транслокацией t(1;19) и химерным геном TCF3-PBX1 (89% клеток). Отмечаются дополнительные прогностически неблагоприятные изменения: делеция локуса CDKN2A (9p21) в 43% клеток и сложные перестройки хромосомы 1q (дупликации, маркерные хромосомы).
Таким образом верифицирован В-II острый лимфобластный лейкоз, группа высокого риска.
Этапы лечения и динамика заболевания
Сентябрь 2022 года – начало терапии с предфа-зы (преднизолон) с последующей индукционной терапией по протоколу ALL-2016 (1-я фаза индукции: преднизолон, даунорубицин, винкристин, L-аспарагиназа; 2-я фаза: меркаптопурин, циклофосфамид, цитарабин, L-аспарагиназа). Люмбальные пункции с введением химиопрепаратов (метотрексат, цитарабин, десаметазон).
С декабря 2022 года консолидация I–V: дексаметазон, доксорубицин, винкристин, меркаптопурин, циклофосфамид, цитарабин, метотрексат, L-аспарагиназа. Люмбальные пункции в соответствии с указанным протоколом. Достижение молекулярной ремиссии на 133-й день курса. Курсы химиотерапии прерывались в связи с развитием нейтропении, фебрильной лихорадки. После купирования симптомов, восстановления показателей крови продолжалась химиотерапия.
В июле 2023 года закончен второй курс поддерживающей терапии – даунорубицин, винкри-стин, дексаметазон, меркаптопурин, метотрексат, L-аспарагиназа. На момент завершения второго курса поддерживающей терапии у пациентки МОБ-отрицательная ремиссия, данных за нейролейкоз не получено.
В августе 2023 года выполнена алло-ТГСК от HLA-идентичного неродственного донора. Спустя два месяца по данным ИФТ КМ выявлена популяция бластов В-линейной направленности в количестве 21% от лейкоцитов. У пациентки первый сверхранний костномозговой рецидив.
С ноября 2023 года начат курс химиотерапии ALL-R3. На 7 день курс прерван в связи с появлением возможности применения препарата инотузумаб озогамицин. В период терапии препаратом иноту-зумаб озогамицин № 3 выполнялись люмбальные пункции с интратекальным введением химиопрепаратов: цитарабин, метотрексат, дексаметазон.
В декабре 2023 года выполнена повторная алло-ТГСК от гаплоидентичного родственного донора (мать).
13.05.24 появились жалобы на слабость, боль в правом тазобедренном суставе. По данным ми-елограммы в аспирате костного мозга выявлены бластные клетки в количестве 11% от лейкоцитов. По результатам ИФТ популяция опухолевых бластов В-линейной направленности выявлена в КМ (22% от лейкоцитов) и в ликворе.
Таким образом, у пациентки диагностирован комбинированный рецидив. Учитывая наличие экспрессии маркеров CD19 и CD22 на опухолевых клетках, принято решение о выполнении CAR-Т-терапии с анти-CD19 и анти-CD22 лимфоцитами от родственного донора (мать).
На фоне стандартной сопроводительной терапии проведена трансплантация донорских CAR-T-клеток от родственного донора (мать).
26.06.2024 – лимфодеплетирующая терапия: флу-дарабин, циклофосфамид.
02.07.2024 – трансфузия донорских CAR-T-лимфоцитов, перелито 1,0 × 105 CD19+ и CD22+ CAR-T клеток/кг массы тела (МТ) реципиента.
09.07.2024 – трансфузия донорских CAR-T-лимфоцитов, перелито 5,68 × 105 CD19+ и 9,63 × 105 CD22+ CAR-T клеток/кг МТ реципиента.
После введения CAR-Т-клеток (02.07.24) у пациентки развился синдром выброса цитокинов I степени тяжести. СВЦ был купирован введением глюкокортикостероидов и тоцилизумаба. В течение первого месяца пациентка наблюдалась еженедельно, затем 2 раза в месяц.
В марте 2025 выполнено контрольное обследование: по результатам ИФТ костного мозга выявлен опухолевый клон – 0,009% от лейкоцитов. В спинномозговом ликворе популяция бластов не обнаружена.
В качестве косвенного маркера сохраняющейся персистенции CAR-Т-лимфоцитов определяли отсутствие В-клеток в периферической крови с помощью метода проточной цитометрии. По результатам данного исследования получено подтверждение сохранения В-клеточной аплазии [11, 12].
Терапия ниволумабом в монорежиме
С учётом развития молекулярного рецидива, было принято решение о назначении ниволумаба в монорежиме с целью преодоления резистентности к терапии и реактивации донорского иммунитета и/или остаточных CAR-T-клеток.
14.03.2025 выполнено первое введение ниволу-маба 180 мг (3 мг/кг МТ), которое пациентка перенесла без осложнений. Далее при контрольном исследовании костного мозга и ликвора с помощью проточной цитометрии (26.03.2025) популяция опухолевых бластов не выявлялась. Следующие введения ниволумаба проводились через 28 дней и далее каждые 14 дней в дозе 240 мг.
В мае 2025 у пациентки развилась диарея до 3-4 раз за сутки. Анализ кала на Cloctridium difficile положительный. Терапия: ванкомицин перорально. На фоне терапии – купирование жалоб, клостридиальный токсин отрицательный.
В июне 2025 появилась макулопапулёзная сыпь на коже туловища, верхних конечностях, сухость глаз, что было расценено как реакция «трансплантат против хозяина» (РТПХ) 1-2 степени. Симптомы успешно контролировались топическими стероидами, топическими ингибиторами кальциневрина, эмолентами и инстилляциями увлажняющих капель.
В сентябре 2025 развился рецидив РТПХ с поражением кожи. На фоне местной терапии сохранялись жалобы на сыпь, зуд кожи. Продолжена местная терапия топическими стероидами, топическими ингибиторами кальциневрина, эмолентами. В связи с развитием РТПХ на фоне сохранения стойкой ре- миссии, принято решение о снижении дозировки ниволумаба до 40 мг каждые 28 дней. На фоне снижения дозы ниволумаба, местной терапии купирование симптомов РТПХ.
При контрольном иммунофенотипировании костного мозга 11.12.25 популяция опухолевых клеток не определялась. Чувствительность анализа 0,001%. В период с марта 2025 по декабрь 2025 проводилось исследование В-клеточной аплазии методом ИФТ, полученные данные свидетельствовали об отсутствии В-лимфоцитов в периферической крови.
Таким образом, у пациентки с р/р В-II-ОЛЛ, получившей лечение CAR-T после двух неудачных алло-ТГСК, назначение ниволумаба позволило преодолеть резистентность к CAR-T и сохранить глубокий молекулярный ответ в течение более 9 месяцев наблюдения (Рисунок 1).
Обсуждение. Ингибирование передачи сигналов PD-1/PD-L1 оказалось эффективным при широком спектре злокачественных новообразований. В исследовании Cassaday R.D. et al. описывается опыт применения пембролизумаба в качестве монотерапии у взрослых пациентов с острым лимфобластным лейкозом и минимальной остаточной болезнью, который показал минимальную, но не нулевую эффективность. В исследование были включены 12 пациентов, троим из которых была выполнена CART-терапия. У 1 из 12 пациентов наблюдался полный ответ после введения пембролизумаба. Пациент до введения пебролизумаба получил алло-ТГСК и CART-терапию. В связи с этим в исследование решено включить еще 9 пациентов для более точной оценки частоты ответа на лечение. Поскольку ответ на терапию был кратковременным, исследование прекращено после завершения первого этапа набора пациентов. Отмечено пять нежелательных явлений ≥3-й степени тяжести: 3 случая артериальной гипертензии 3-й степени тяжести, 1 случай синдрома Стивенса – Джонсона 3-й степени тяжести и 1 случай снижения количества нейтрофилов 4-й степени тяжести [9].
Несмотря на небольшую выборку и кратковременный эффект от терапии в данном исследовании, полученные результаты могут послужить основанием для дальнейшего изучения применения этих препаратов в более конкретных ситуациях.
В работе Chan T.S.Y. et al. описываются 2 случая рецидива ОЛЛ с экстрамедуллярными очагами после алло-ТГСК. На фоне терапии низкими дозами ниволумаба у 1-й пациентки – уменьшение размеров экстрамедуллярных очагов со стабилизацией состояния и в дальнейшем развитие РТПХ с поражением печени, что послужило причиной для отмены терапии ниволумабом. На момент публикации пациентка находилась в бессимптомном состоянии без проведения химиотерапии более 13 месяцев. У 2-й пациентки после 1 введения развился синдром лизиса опухоли с уменьшением количества бласт-
25%
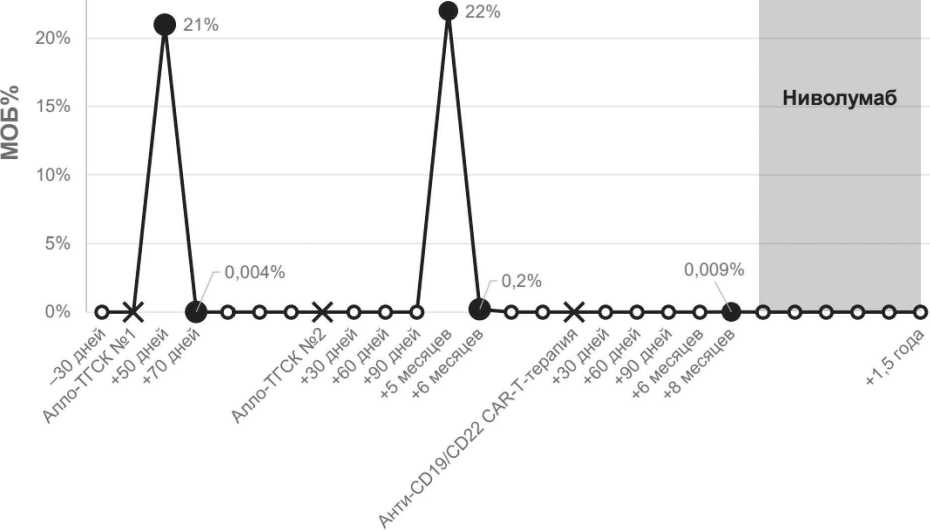
Рисунок 1. Молекулярный ответ у больной получившей ниволумаб после терапии CAR-T- клетками
ных клеток в костном мозге. После пятого введения количество бластов увеличилось. Пациентка оставалась жива в течение 16 недель после введения ниво-лумаба с последующим проведением других курсов химиотерапии [10].
Низкие дозы ниволумаба способны индуцировать значимый противоопухолевый ответ у определенной доли пациентов c рецидивом ОЛЛ после алло-ТГСК, CAR-T-терапии. Кроме того, нельзя исключить, что низкие дозы ниволумаба обладают эффективностью, сопоставимой с высокими дозами. При этом монотерапия ниволумабом может быть менее эффективна в отношении рецидивов, сопровождающихся экстрамедуллярным поражением. Долгосрочный ответ после терапии CAR-T ассоциирован с персистенцией модифицированных клеток, на эффективность которой может негативно влиять истощение CAR-T-клеток, опосредованное активацией пути PD-1 / PD-L1. Ингибиторы PD-1 теоретически способны реактивировать как врожденную иммунную резистентность, так и адаптивный, CART-опосредованный противоопухолевый иммунитет [6].
В представленном нами случае ниволумаб в монорежиме, назначенный в качестве терапии рецидива после терапии CAR-T, позволил добиться и сохранить глубокий молекулярный ответ в течение более 9 месяцев наблюдения. Важно отметить, что терапия проводилась в амбулаторных условиях и характеризовалась управляемым профилем безопасно- сти. Развившиеся иммуноопосредованные явления (инфекционная диарея, кожная и офтальмологическая РТПХ) были своевременно диагностированы и эффективно купированы стандартными подходами, не потребовав отмены основного лечения. На момент публикации пациентка жива.
Полученные данные демонстрируют необходимость проведения более масштабных проспективных исследований для точной оценки частоты ответов, оптимального дозирования, долгосрочной безопасности и выживаемости. Также необходимо изучение комбинации ниволумаба с другими методами (таргетной и химиотерапией).
Заключение. Данное клиническое наблюдение демонстрирует эффективность терапии ниволума-бом для поддержания длительной ремиссии у пациентов с р/р -ОЛЛ после терапии CAR-T-клетками. Предлагаемый подход позволяет минимизировать токсичность, связанную с высокодозной химиотерапией, и может быть рассмотрен в рамках персонализированной стратегии лечения. Для определения оптимальных сроков назначения, схем дозирования и оценки долгосрочных результатов необходимы дальнейшие проспективные исследования на более крупных когортах пациентов.


