Клинико-генетическая характеристика больных ишемическим инсультом молодого и среднего возраста
Автор: Овсянникова Анна Николаевна, Машин Виктор Владимирович, Белова Людмила Анатольевна, Саенко Юрий Владимирович, Бырина Анна Вадимовна
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Клиническая медицина
Статья в выпуске: 3, 2016 года.
Бесплатный доступ
С целью изучения полиморфизма генов системы гемостаза как предиктора развития ишемического инсульта проведен анализ генетических факторов риска острой ишемии мозга путем исследования полиморфных вариантов генов свертывающей системы крови у больных ишемическим инсультом (ИИ) молодого и среднего возраста. Материалы и методы. Обследовано 172 пациента. Для исследования выбраны описанные в литературе полиморфизмы генов-кандидатов ишемического поражения головного мозга: полиморфизм 20210G>A гена FII, 1691G>A гена FV, 10976G>A гена FVII, -455G>A гена FGB, -675 5G>4G гена PAI-1, 807C>T гена ITGA2, 1565Т>С гена ITGB3. Использовалась технология выявления и идентификации однонуклеотидных полиморфизмов (SNP) с анализом кривых температуры плавления («ДНК-Технология»). Изучено влияние генетических факторов на особенности течения острого периода, а также исход ИИ в обследуемой группе больных. Результаты. У больных ИИ по сравнению с контрольной группой статистически значимо преобладают полиморфные варианты генов FBG, FII, F5, ITGB3. Наиболее часто встречаемым является полиморфизм -455G гена фибриногена. Наличие полиморфных вариантов генов свертывающей системы крови определяет клинические особенности течения острого периода ишемического инсульта (патогенетический подтип инсульта, количество очагов ишемии, тяжесть неврологического дефицита) и не влияет на функциональный исход к концу острого периода заболевания. Установлено наличие генетической детерминированности ИИ у лиц молодого и среднего возраста.
Гены-кандидаты, факторы риска, ишемический инсульт, тромбофилия
Короткий адрес: https://sciup.org/14113176
IDR: 14113176 | УДК: 616.831-005.1:616-052:575
Clinical and genetic characteristics of young and middle-aged patients with ischemic stroke
Analysis of genetic risk factors for acute cerebral ischemia was conducted to study the gene polymorphism of hemostasis system (as a predictor of ischemic stroke). Polymorphic variants of the genes of blood coagulation were studied in young and middle-aged patients with ischemic stroke (IS). Materials and Methods. 172 patients were enrolled in the trial. Genetic polymorphisms, which contributed to ischemic brain damage and were literature reported, were chosen for the study, namely: FII gene polymorphism 20210G>A, FV gene polymorphism 1691G>A, FVII gene polymorphisms 10976G>A, FGB gene polymorphism -455G>A, PAI-1 gene polymorphism -675 5G>4G, ITGA2 gene polymorphism 807C>T, and ITGB3 gene polymorphism 1565T>C. The authors used the technology of detecting and identifying single nucleotide polymorphisms (SNPs) using melting temperature curve analysis (“DNA-technology"). The influence of genetic factors on the acute phase as well as ischemic stroke (IS) outcome in the examined group of patients was studied. Results. In patience with IS polymorphic variants of FBG, FII, F5, ITGB3 genes predominated (as compared to a control group). The most frequent was 455G>A fibrinogen gene polymorphism. Polymorphic variants of blood coagulation genes determined clinical features of acute ischemic stroke (pathogenic stroke subtype, number of ischemic sites, severity of neurological deficit). Moreover, they did not affect the functional outcome by the end of the acute phase of the disease. It was found that genetic predisposition to thrombophilic states played an essential role in the development of ischemic stroke in young and middle-aged people.
Текст научной статьи Клинико-генетическая характеристика больных ишемическим инсультом молодого и среднего возраста
Введение. Ишемическая цереброваскулярная патология представляет собой актуальную проблему современной медицины, являясь одной из основных причин смертности и инвалидизации населения [1–4]. Высокая доля в структуре заболеваемости и смертности населения, значительные показатели временных трудовых потерь и первичной инвалидности обусловливают большое медико-социальное значение сосудистых заболеваний головного мозга [3].
Основное место в структуре цереброваскулярных заболеваний занимают инсульты.
В последние годы во всем мире отмечается рост распространенности заболеваний острыми нарушениями мозгового кровообращения, при этом увеличивается количество инсультов среди лиц трудоспособного возраста – до 64 лет [2, 5].
В России заболеваемость и смертность от инсульта остаются одними из самых высоких. Так, частота инсультов в Российской Федерации составляет, по разным данным, 350–400 случаев на 100 тыс. населения [1–3, 5]. По данным Регистра инсульта (2009), в г. Ульяновске среднегодовая заболеваемость инсультом составляла 2,1 на 1000 населения в год [6]. Смертность в остром периоде инсульта составляет 35 % и достигает к концу года почти 50 % [2, 7]. Наряду с высокой смертностью, социально значимыми являются и последствия инсультов: развитие стойкой инвалидности с потерей трудоспособности, высокий риск повторных нарушений мозгового кровообращения, сосудистой деменции.
Известно, что большинство ишемических инсультов относятся к мультифакториальным заболеваниям: их развитие, клиническое течение и исход во многом обусловлены комплексным влиянием факторов внешней среды и наследственной предрасположенностью [6].
Одной из актуальных проблем современного здравоохранения является выяснение молекулярно-генетических основ развития сердечно-сосудистых заболеваний. На современном этапе одним из наиболее плодотворных подходов к изучению наследственной предрасположенности к ишемическому инсульту является исследование ассоциаций полиморфных вариантов генов-кандидатов с риском развития заболевания. В первую очередь это гены, продукты которых либо вовлечены в липидный гомеостаз, либо оперируют в системе свертывания крови, либо влияют на физиологию стенки сосудов [8].
Обнаружение генетических маркеров тромбофилических состояний позволит значительно повысить возможности проведения своевременной профилактики, адекватного патогенетического лечения, а также правильной оценки риска развития повторного инсульта и дальнейшего прогноза.
Цель исследования. Изучить полиморфизм генов системы гемостаза как предиктора развития ишемического инсульта у лиц молодого и среднего возраста.
Материалы и методы. Клинико-инструментальные методы. Обследовано 172 пациента в остром периоде ишемического инсульта в возрасте от 25 до 60 лет включительно, находившихся на лечении в неврологическом отделении для больных с острыми нарушениями мозгового кровообращения ГУЗ «Центральная клиническая медико-санитарная часть им. заслуженного врача России В.А. Егорова» г. Ульяновска с 2012 по 2015 г. В числе обследованных – 69 женщин (40,1 %) и 103 мужчины (59,9 %). Средний возраст пациентов – 58 (56; 60) лет, средний возраст женщин – 56 (48; 58) лет, мужчин – 60 (58; 60) лет.
В ходе обследования пациента выяснялись его анамнестические данные (с учетом сопутствующей патологии).
Всем больным проводилось тщательное клинико-инструментальное обследование с целью выявления факторов риска цереброваскулярной патологии, верификации сосудистой патологии головного мозга, а также ус- тановления патогенетического механизма развития ишемического инсульта. Обследование включало: неврологический осмотр, терапевтический осмотр, проведение рентгеновской компьютерной томографии (РКТ) головного мозга, дуплексного сканирования экстракраниальных артерий, транскраниальной эхокардиографии, электрокардиографии, лабораторное исследование с оценкой липидного спектра, исследование гемореологических показателей и параметров системы гемостаза. Всем пациентам проводился генетический анализ с целью выявления полиморфизмов генов системы гемостаза, ассоциированных с повышенным риском развития тромбофилии.
Оценка степени тяжести ишемического инсульта проводилась с использованием шкалы тяжести инсульта Национального института здоровья США (the National Institutes of Health Stroke Scale – NIHSS) с интерпретацией результатов данной шкалы по критериям L.B. Goldstein et al. [9]. При суммарном результате менее 6 баллов определяется легкий инсульт; 7–12 баллов – инсульт средней степени тяжести; более 14 баллов – тяжелый инсульт. Оценка тяжести состояния и степени нарушения сознания проводилась с использованием шкалы Глазго (Glazgow). Для оценки функционального исхода использовалась шкала Рэнкин.
Диагноз ишемического инсульта у всех пациентов подтверждался методом нейровизуализации: всем пациентам проводилась РКТ головного мозга при поступлении и через 24 ч от начала заболевания.
Распределение пациентов по группам в зависимости от размера очага ишемии проводилось в соответствии с классификацией Н.В. Верещагина, Л.К. Брагиной (1983): обширные инфаркты – инфаркты, распространяющиеся на весь бассейн внутренней сонной артерии или на весь бассейн артерий вертебрально-базилярной системы; к большим относят инфаркты, распространяющиеся на весь бассейн основных ветвей (передней, средней, задней мозговых, базилярной и мозжечковой артерий); средние инфаркты – это инфаркты бассейна корковых и глубоких ветвей; малые – инфаркты в бассейнах внут- римозговых артерий, отходящих от передней, задней, средней мозговых, позвоночной и базилярной артерий, размер не превышает 1–1,5 см.
Группу контроля (ГК) составили 90 практически здоровых лиц (39 (43,3 %) женщин и 51 (56,7 %) мужчина; средний возраст – 57 (54; 59) лет), не имеющих цереброваскулярной патологии, по полу и возрасту сопоставимых с группой обследованных больных.
Молекулярно-генетическое исследование осуществлялось в лаборатории молекулярной и клеточной биологии Научно-исследовательского технологического института имени С.П. Капицы ФБГОУ ВО «Ульяновский государственный университет». Экстракция геномной ДНК проводилась из лейкоцитов замороженной венозной крови с использованием набора «Ампли Прайм ДНК-сорб-АМ». Генетические полиморфизмы определялись с использованием комплекта реагентов для определения генетических полиморфизмов, ассоциированных с риском развития тромбофилии, методом полимеразной цепной реакции (ПЦР) в режиме реального времени «Кардио-ГенетикаТромбофилия», разработанным компанией «ДНК-Технология» (регистрационный номер 2010/08414 от 22.07.2010). ПЦР проводились на ДНК-амплификаторе CFX96.
Проводился анализ полиморфизмов генов, кодирующих белки системы свертывания крови и гемостаза. Для исследования были выбраны описанные в литературе полиморфизмы генов, которые с теоретических позиций могут иметь отношение к повышенному риску ишемического поражения головного мозга: полиморфизм 20210G>A гена FII, полиморфизм 1691G>A гена FV, полиморфизм -455G>A гена FGB, полиморфизм -675 5G>4G гена PAI-1, полиморфизм 807C>T гена ITGA2, полиморфизм 1565Т>С гена ITGB.
Статистическая обработка полученных данных проводилась с применением пакета прикладных программ «Статистика 6.1» (StatSoft, 2003, США). Группы сравнивались по качественным данным с помощью критерия χ2, точного критерия Фишера. Также при описательной статистике количественных признаков использовались методы оценки непараметрических данных с вычислением медианы и межквартильного интервала (25–75-й процентили), при сравнении двух связанных признаков – критерий Уилкоксо-на. При сравнении двух несвязанных признаков для проверки гипотезы о различии выборок групп больных применялся тест Манна– Уитни (Mann–Whitney U-test). Данные представлены в виде медианы, 25 и 75 % квартилей (Me (25; 75 %)). При проверке гипотез статистически значимыми считались результаты при уровне вероятности более 95 % (p<0,05).
Результаты и обсуждение. Клиническая характеристика больных. Согласно возрастной классификации ВОЗ (2009) все больные ИИ были разделены на две группы. Первую группу составили больные ИИ молодого возраста (25–44 года), вторую группу – больные среднего (зрелого) возраста (45–60 лет). Распределение больных по возрастным группам показало преобладание больных ИИ среднего (зрелого) возраста (р<0,001).
Распределение больных по десятилетиям жизни показало преобладание пациентов с ИИ в возрасте 50–59 лет – 41,9 % (72 чел.) и в возрасте 60 лет – 40,1 % (69 чел.) (р<0,001). В возрасте 20–29 лет было выявлено 1,7 % больных (3 чел.), в возрастной группе 30–39 лет – 4,1 % (7 чел.), 12,2 % (21 чел.) составили больные ИИ в возрасте 40–49 лет (р>0,05).
Среди обследованных пациентов преобладали мужчины (р<0,001).
По локализации ишемического очага отмечалось преобладание полушарных инсультов – 70,9 % (n=122) (р<0,01). Из них в бассейне левой средней мозговой артерии – 54,1 % (n=66), в бассейне правой средней мозговой артерии – 31,9 % (n=39), в бассейне левой задней мозговой артерии – 7,4 % (n=9), в бассейне правой передней мозговой артерии – 4,1 % (n=5), в бассейне левой передней мозговой артерии – 2,5 % (n=3). Локализация ишемического инсульта в вертебральнобазилярном бассейне выявлена у 19,8 % обследованных пациентов (n=34), из них у 70,6 % (n=24) очаг ишемии располагался в стволе головного мозга, у 29,4 % (n=10) – в мозжечке. В 9,3 % случаев (n=16) было вы- явлено два «свежих» ишемических очага: у всех пациентов один очаг ишемии локализовался в мозжечке, второй – в полушариях головного мозга.
Среди мужчин чаще встречалась локализация очага ишемии в бассейне левой средней мозговой артерии – 44,6 % (n=46), а также в мозжечке – 8,7 % (n=9). У женщин инфаркт мозга чаще развивался в бассейне правой средней мозговой артерии – 34,8 % (n=24) (р<0,05).
Отмечено преобладание полушарного ишемического инсульта среди лиц молодого возраста – 87,1 % (n=27) (р<0,05).
Различий по локализации зоны инфаркта в правом или левом полушарии головного мозга, а также в различных долях у больных не выявлено (р>0,05).
По результатам РКТ головного мозга в соответствии с классификацией, принятой в НЦ неврологии РАМН (Верещагин Н.В. с со-авт., 1983), отмечалось преобладание средних инфарктов – у 50 % (n=86), малые (лакунарные) инфаркты наблюдались в 22,7 % случаев (n=39), большие ишемические инфаркты – в 20,9 % (n=36), обширные инфаркты – в 6,4 % случаев (n=11) (рис. 1).
Отмечено достоверное преобладание очагов инфаркта средних размеров среди мужчин – 57,3 % (р=0,029) и больших инфарктов у женщин – 28,9 % (р=0,037) и у пациентов молодого возраста (младше 45 лет) – 35,5 % (р=0,048). Обширные инфаркты диагностированы только у пациентов среднего возраста (45–60 лет) – 7,8 %. Лакунарные инфаркты наблюдались одинаково часто в двух возрастных группах – 19,4 и 23,4 % (p>0,05).
Среди обследованных больных с ишемическим инсультом чаще была диагностирована болезнь крупных сосудов (атеротромботи-ческий инсульт, АТИ) – у 75 пациентов (43,6 %) (р<0,023), из них 53 (70,6 %) мужчины и 22 женщины (29,3 %) (р<0,00001). У 47 больных (27,3 %) имел место кардиоэмболический подтип ишемического инсульта (КЭИ): у 31 мужчины (69,5 %) и 16 женщин (34,1 %) (р<0,001). Лакунарный инсульт (ЛАИ) выявлен у 39 пациентов (22,7 %): 27 женщин (69,2 %) и 12 мужчин (30,8 %) (р<0,001). Гемодинамический подтип ИИ
(ГДИ) отмечен у 11 пациентов (6,4 %), одинаково часто у мужчин и женщин – 7 (63,6 %) и 4 (36,4 %) случая соответственно (р>0,05).
Инсульта по типу гемореологической микроокклюзии в группе обследованных пациентов не выявлено (рис. 2).
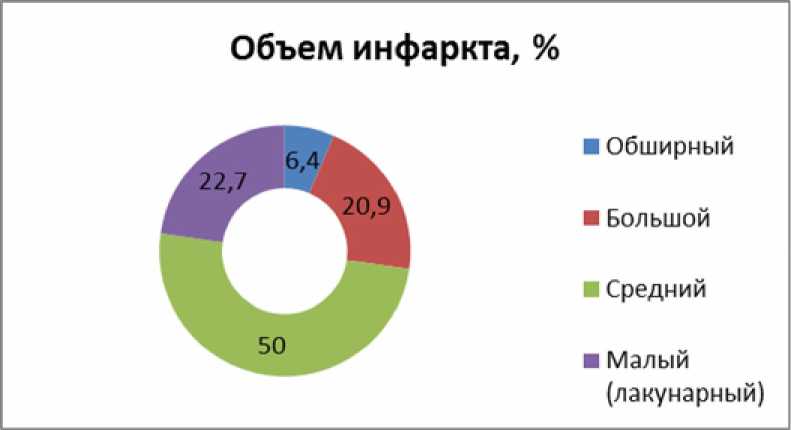
Рис. 1. Объем инфаркта в группе обследованных больных
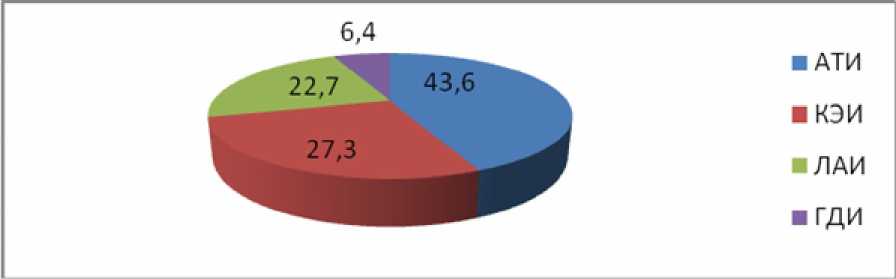
Рис. 2. Распределение патогенетических подтипов ИИ у обследованных больных
Получены гендерные и возрастные различия по частоте встречаемости подтипов ИИ. Отмечено преобладание АТИ у лиц среднего (зрелого) возраста – 48,9 % (р=0,002), а также у мужчин – 51,5 % (р=0,012). У пациентов в возрасте младше 45 лет (48,4 %) (р=0,0005) и у женщин (39,1 %) достоверно чаще преобладал ЛАИ (р=0,00035).
Распределение больных в зависимости от патогенетического подтипа и объема очага поражения показало преобладание среди пациентов с АТИ больших инфарктов – 40 % (n=30) (р<0,05). Средние инфаркты чаще раз- вивались при КЭИ – 57,3 % (n=43) (p<0,05). Лакунарные инфаркты соответственно выявлены у пациентов с лакунарным подтипом инсульта – 100 % (n=39) (p=0,001). Обширные ишемические инфаркты, распространяющиеся на весь бассейн внутренней сонной артерии или на весь бассейн артерий вертебрально-базилярной системы, диагностированы только у больных с АТИ – 14,7 % (n=11). Различий по частоте встречаемости ишемических очагов различного объема у пациентов с ГДИ не выявлено (р>0,05).
Отмечено достоверное преобладание очагов ишемии средних размеров у мужчин –
57,3 % (р=0,029) и больших инфарктов у женщин – 28,9 % (р=0,037) и у пациентов молодого возраста (младше 45 лет) – 35,5 % (р=0,048). Обширные инфаркты диагностированы только у пациентов среднего возраста (45–60 лет) – 7,8 %, одинаково часто у мужчин и у женщин – 7 (6,8 %) и 4 (5,8 %) соответственно (р>0,05). Лакунарные очаги и инфаркты средних размеров диагностированы одинаково часто у мужчин и женщин – 21 (20,4 %) и 18 (26,1 %) (р>0,05).
Нарушение сознания различной глубины в остром периоде ИИ зарегистрировано у 58 пациентов (33,7 %). Из них в оглушении (13–14 баллов по шкале Глазго) находились 34 пациента (58,6 %), в сопоре (9–12 баллов по шкале Глазго) – 20 больных (34,5 %), кома (менее 8 баллов по шкале Глазго) диагностирована у 4 пациентов (6,9 %). 114 (68 %) больных находились в состоянии ясного сознания (15 баллов).
Независимо от подтипа инсульта большая часть пациентов в остром периоде заболевания находилась в состоянии ясного сознания (15 баллов по шкале Глазго) – 66,3 %, а также в состоянии оглушения (13–14 баллов) – 58,6 % пациентов. Наибольшую степень нарушения сознания (оглушение, сопор, кома) имели пациенты с АТИ – 56 %, по сравнению с пациентами других патогенетических подтипов инсульта (р<0,05).
Получены различия в состоянии уровня сознания пациентов в зависимости от объема инфаркта мозга. Отмечена тенденция к усугублению степени нарушения сознания до сопора и комы у больных с большими (23,7 и 2,6 %) и обширными (36,4 и 27,3 %) инфарктами мозга, в то время как пациенты с лакунарными и средними инфарктами находились в состоянии ясного сознания (92,3 и 68,6 %) или оглушения (5,4 и 24,4 % соответственно) (р<0,05).
При оценке неврологического статуса пациентов в остром периоде ИИ в 41,9 % случаев (n=72) ведущими неврологическими синдромами были нарушения двигательной сферы, при этом у 31,9 % пациентов (n=23) была выявлена плегия, у 20,9 % (n=15) – глубокие парезы (до 2 баллов), умеренные парезы (3 балла) встречались в 33,3 % случаев
(n=24), легкие парезы (4 балла) – в 13,8 % (n=10). Нарушения в сфере чувствительности наблюдались у 2,9 % обследованных пациентов (n=5). Вестибуло-мозжечковый синдром являлся ведущим синдромом у 8,2 % больных (n=14). Изолированная афазия также диагностирована у 14 пациентов (8,2 %), у 6 (42,9 %) из которых выявлена тотальная афазия, у 3 (21,4 %) – моторная, у 5 (35,7 %) – cен-сомоторная. Бульбарный синдром являлся ведущим у 6,9 % пациентов (n=12), глазодвигательные нарушения диагностированы в 4,7 % случаев (n=8). У 47 пациентов (27,3 %) наблюдалось сочетание неврологических синдромов, равноценных по степени выраженности. Так, сочетание тотальной афазии и гемиплегии отмечено у 55,3 % больных (n=26), бульбарного синдрома и нарушений двигательной сферы – у 36,2 % (n=17), нарушений в координаторной сфере и гемипареза – у 8,5 % (n=4).
По степени тяжести ИИ с оценкой по шкале NIHSS отмечалось преобладание инсульта средней тяжести – у 75 пациентов (43,6 %), тяжелый инсульт наблюдался у 32 чел. (18,6 %), у 65 больных (37,8 %) инсульт расценивался как легкий. Средняя оценка по шкале NIHSS в группе обследованных пациентов составила 8 (4,5; 12) баллов, в группе мужчин – 5 (4; 12) баллов, в группе женщин – 10 (7; 13) баллов. Обращало на себя внимание преобладание тяжелого инсульта в группе мужчин по сравнению с группой обследованных женщин (20 и 12 больных соответственно), но данные различия не достигали уровня статистической значимости (p>0,05).
Различий по степени тяжести течения инсульта у больных в различных возрастных группах не выявлено.
При оценке степени тяжести инсульта по шкале NIHSS у пациентов с различными патогенетическими подтипами инсульта получено достоверное преобладание инсульта средней тяжести при АТИ и КЭИ по сравнению с другими подтипами инсульта (41 (57,3 %) и 22 (59,6 %) (р<0,05)). В случае ЛИ и ГДИ достоверно чаще развивался легкий инсульт (30 (76,9 %) и 8 (63,6 %) (р<0,05)). Тяжелый инсульт (более 14 баллов)
был диагностирован только при АТИ и КЭИ и встречался одинаково часто в обеих группах (21 (21,3 %) и 11 (14,9 %) соответственно (р>0,05)).
Наиболее тяжелое течение инсульта в остром периоде заболевания имели пациенты с наличием обширных – 90,9 % (n=10) и больших инфарктов – 50 % (n=18) по данным РКТ головного мозга (p=0,00003).
Получены различия в степени тяжести острого периода инсульта в зависимости от локализации ишемического очага. Более тяжелое течение имело место при локализации инфаркта в больших полушариях мозга, особенно при развитии патологического процесса в бассейне ЛСМА – 16 (24,3 %) (р<0,05).
Молекулярно-генетическая характеристика больных. Полиморфные варианты исследуемых генов системы гемостаза выявлены у 140 из 172 больных с ИИ (81,4 %), у 32 чел. (18,6 %) изменений генотипа по исследуемым генам не выявлено (р>0,001). Полиморфные варианты генов встречались одинаково часто у мужчин и женщин (76 (54,3 %) и 64 (45,7 %) случая соответственно), в независимости от возрастной группы (24 (77,6 %) и 116 (82,3 %)) (р>0,05).
Выявлены как одиночные, так и сочетанные полиморфизмы. Одиночные полиморфные варианты исследуемых генов определены у 53 чел. (37,9 %). Из них у 14 чел. (26,4 %) диагностирован полиморфизм -455G>A гена фибриногена, у 12 (22,6 %) пациентов – полиморфизм -675 5G>4G гена PAI-1 и полиморфизм 1691G>A гена FV. Полиморфный вариант 20210G>A гена FII выявлен у 8 чел. (15,1 %), одиночный полиморфизм 807 C>T гена ITGA2 – у 6 (11,3 %), полиморфизм 1565T>C гена ITGB3 – у 1 пациента (2 %).
У 87 (62,1 %) обследованных пациентов обнаружены сочетанные полиморфные варианты генов системы гемостаза (р>0,05). Полиморфные варианты в двух исследуемых генах системы гемостаза встретились у 47 (33,6 %) чел., в трех – у 40 (28,6 %).
Были выявлены следующие комбинации полиморфных вариантов исследуемых генов:
-
1) -455G>A гена FGB+1691G>A гена FV+20210G>A гена FII – 4 чел.;
-
2) -455G>A гена FGB+ -675 5G>4G гена PAI-1+1565 T>C гена ITGB3 – 18 чел.;
-
3) -675 5G>4G гена PAI-1+807C>T гена ITGА2+1565 T>C гена ITGB3 – 18 чел.;
-
4) -455G>A гена FGB+ -675 5G>4G гена PAI-1 – 22 чел.;
-
5) -455G>A гена FGB+1691G>A гена FV – 4 чел.;
-
6) -675 5G>4G гена PAI-1+807 C>T гена ITGА2 – 5 чел.;
-
7) -675 5G>4G гена PAI-1+1565T>C гена ITGB3 – 7 чел.;
-
8) 1565T>C гена ITGА2+1565T>C гена ITGB3 – 8 чел.;
-
9) -675 5G>4G гена PAI-1+1565T>C гена ITGB3 – 1 чел.
По сравнению с ГК среди пациентов с ИИ получено достоверное преобладание полиморфных вариантов следующих генов: полиморфизм -455G>A гена FGB – 33,7 %, полиморфизм 20210G>A гена FII – 6,9 %, полиморфизм 1691G>A гена FV – 11,6 %, полиморфизм -675 5G>4G гена PAI-1 – 12,8 %, полиморфизм 1565T>C гена ITGB3 – 29,7 %.
Анализ полиморфизма 1565Т>С гена ITGВ3 не показал статистически значимых различий в общем распределении наблюдаемых частот генотипов между группой больных с ИИ и ГК (табл. 1, 2).
Отмечена наибольшая частота встречаемости полиморфного варианта -455G>A гена фибриногена (33,7 % больных). Ведущие позиции данный полиморфизм занимает как при одиночном носительстве (26,4 %), так и в сочетании с полиморфными вариантами других генов системы гемостаза (55,2 %). Кроме того, только в группе обследованных пациентов с ИИ диагностирован редко встречающийся гомозиготный генотип А/А гена фибриногена, ассоциированный с наибольшим риском тромбофилических состояний (1,2 % больных).
Таблица 1
Частота встречаемости генотипов по исследованным генам системы гемостаза (FGB, FII, FV)
|
Обследованные группы |
Исследованные гены, выявленные генотипы, n (%) |
||||||||
|
Ген FGB (-455G>A) |
Ген FV (1691G>A) |
Ген FII (20210G>A) |
|||||||
|
G/G |
G/A |
A/A |
G/G |
G/A |
A/A |
G/G |
G/A |
A/A |
|
|
Больные ИИ |
112 (65,1) |
58 (33,7)* |
2 (1,2) |
152 (88,4) |
20 (11,6)* |
- |
160 (93,1) |
12 (6,9)* |
- |
|
Группа контроля |
82 (91,1) |
8 (8,9) |
- |
89 (98,9) |
1 (1,1) |
- |
89 (98,9) |
1 (1,1) |
- |
Примечание. * – статистически значимые различия с группой контроля (р<0,05).
Таблица 2
Частота встречаемости генотипов по исследованным генам системы гемостаза (PAI-1, ITGA2, ITGB3)
|
Обследованные группы |
Исследованные гены, выявленные генотипы, n (%) |
||||||||
|
Ген PAI-1 (-675 5G>4G) |
Ген ITGA2 (807C>T) |
Ген ITGB3 (1565T>C) |
|||||||
|
5G/5G |
5G/4G |
4G/4G |
C/C |
C/T |
T/T |
T/T |
C/T |
C/C |
|
|
Больные ИИ |
107 (62,2) |
43 (25,0) |
22 (12,8)* |
133 (77,3) |
25 (14,6) |
14 (8,1) |
121 (70,3) |
51 (29,7)* |
- |
|
Группа контроля |
64 (71,1) |
26 (28,9) |
- |
83 (92,2) |
5 (5,6) |
2 (2,2) |
82 (91,1) |
8 (8,9) |
- |
Примечание. * – статистически значимые различия с группой контроля (р<0,05).
Таким образом, полученные результаты проведенного исследования, а именно достоверное преобладание полиморфных вариантов исследуемых генов системы гемостаза у лиц с ишемическим поражением головного мозга, свидетельствуют о наличии ассоциации генотипов G/A и А/А (FGB), G/A (FII), G/A (FV), 4G/G/4G (PAI-1), С/Т ITGB3 генов системы гемостаза с повышенным риском развития тромбофилических состояний, в частности ишемического инсульта у лиц молодого и среднего возраста.
Результаты молекулярно-генетического исследования пациентов в остром периоде ИИ подтверждают существующие предположения о значительном вкладе генетических факторов в развитие ишемических нарушений мозгового кровообращения.
Анализ клинических и инструментальных данных выявил особенности клинического течения острого периода ИИ у пациентов с сочетанными полиморфными вариантами генов системы гемостаза. Только в данной группе больных имели место тромбоэмболические осложнения различных локализаций – у 28,7 % больных, в то время как у лиц с одиночными полиморфизмами тромбоэмболических ос- ложнений не наблюдалось (р=0,001). Наиболее часто острый период ИИ осложнялся развитием инфаркта миокарда – у 14,9 % больных, тромбозы глубоких вен развились у 10,3 % больных, тромбоэмболия легочной артерии – у 4,6 % больных с сочетанными полиморфизмами. У одного пациента, являющегося носителем сочетания полиморфных вариантов генов FGB, FII и FV, острый период ИИ осложнился развитием острого инфаркта миокарда в сочетании с тромбозом глубоких вен нижних конечностей. Следует отметить, что у 96 % больных с тромбоэмболическими осложнениями при генетическом исследовании диагностирован полиморфизм -455G>A гена FGB.
Результаты данного исследования показывают, что носительство полиморфных аллелей генов, кодирующих белки свертывающей системы крови, определяет клиникопатогенетический подтип ИИ, количество ишемических очагов, а также тяжесть неврологического дефицита и не влияет на функциональный исход инсульта.
У пациентов с полиморфным вариантом генов системы гемостаза достоверно преобладал АТИ (48,1 %), у пациентов с «нейтральным» генотипом – ГДИ (18,8 %). Выяв- лена зависимость патогенетического подтипа инсульта от полиморфного варианта гена. При наличии полиморфизма гена FGB преобладал АТИ (83,3 %), гена PAI-1 – АТИ и ЛАИ (50 и 35,7 %), гена ITGA2 – ЛАИ (66,7 %). При наличии сочетанного полиморфного варианта генотипа имели место АТИ и КЭИ (44,8 и 35,9 % соответственно (р<0,05)).
Среди пациентов с полиморфным вариантом генов системы гемостаза отмечено преобладание лиц с сочетанными ишемическими очагами (12,2 %) (р=0,043), а также с высокой балльной оценкой по шкале NIHSS, что соответствует тяжелому течению инсульта (16,8 %) (р=0,04).
Наибольшую балльную оценку тяжести инсульта имели пациенты с диагностированными полиморфными вариантами FGB, FII и FV (17,70±7,12; 9,60±2,77; 10,50±2,94), а также при сочетании полиморфизмов в генах PAI-I и ITGB3 (17,70±2,81). При этом достоверных различий балльной оценки степеней тяжести неврологического дефицита у пациентов с одиночными и сочетанными полиморфизмами исследуемых генов не выявлено (р>0,05).
При динамическом обследовании пациентов на 21-й день заболевания снижение баллов имело место у пациентов как с «нейтральным», так и с полиморфным генотипами, однако наибольший регресс баллов получен в группе пациентов без полиморфизма генов (-2,10±3,24 и -3,60±3,04 балла соответственно).
Среди пациентов с одиночными полиморфизмами наибольший регресс баллов в динамике получен у лиц с полиморфизмом в гене PAI-1 (-4,20±2,25 балла), наименьший – с полиморфизмом в гене FII (-1,00±1,41 балла). У пациентов с сочетанными полиморфизмами наибольший регресс баллов отмечен у лиц с сочетанием полиморфизма гена PAI-1 и гена ITGB3 (-12,40±4,07 балла), наименьший – с сочетанием полиморфизмов в генах FGB и PAI-1 (-0,1±2,49 балла).
В единственной группе пациентов с сочетанием полиморфных вариантов генов FGB, FII, FV получен прирост баллов в динамике к концу острого периода инсульта
(2,00±2,24 балла), что, вероятно, обусловлено наличием экстрацеребральных тромоэмболи-ческих осложнений в указанной группе больных. Однако данная динамика баллов оказалась статистически не значима (р=0,14).
Улучшение функционального исхода с оценкой по шкале Рэнкин на 21-й день от начала заболевания статистически значимым было как в группе больных с полиморфизмом генов, так и в группе без него.
Выводы:
-
1. Установлено наиболее тяжелое течение инсульта при атеротромботическом и кардиоэмболическом подтипах, при обширных и больших инфарктах мозга, а также при локализации инфаркта в больших полушариях мозга, особенно в левом каротидном бассейне.
-
2. Среди пациентов с ишемическим инсультом молодого и среднего возраста по сравнению с группой контроля преобладают полиморфные варианты генов фибриногена, V фактора свертывания крови (фактора Лейдена), протромбина, гена плазминогена I типа и гена бета-3 субъединицы тромбоцитарного рецептора фибриногена. Наиболее часто встречаемым является полиморфизм -455G>A гена фибриногена. Полиморфный вариант гена фибриногена занимает лидирующие позиции как при одиночном носительстве, так и в сочетании с полиморфными вариантами других генов системы гемостаза.
-
3. Наличие полиморфных вариантов генов, кодирующих белки свертывающей системы крови, определяет клинические особенности течения острого периода ишемического инсульта: клинико-патогенетический подтип инсульта, количество очагов ишемии, а также тяжесть неврологического дефицита, – и не влияет на функциональный исход к концу острого периода заболевания.
У пациентов с полиморфным вариантом генов системы гемостаза достоверно преобладал АТИ. Выявлена зависимость патогенетического подтипа инсульта от полиморфного варианта гена. При наличии полиморфизма гена FGB преобладает АТИ, гена PAI-1 – АТИ и ЛАИ, гена ITGA2 – ЛАИ. При наличии сочетанного полиморфного варианта генотипа имеют место АТИ и КЭИ. Среди пациентов с полиморфным вариантом генов системы гемостаза преобладают лица с сочетанными ишемическими очагами, а также с высокой балльной оценкой по шкале NIHSS. Грубый неврологический дефицит, соответствующий тяжелому течению инсульта, имеют пациенты с полиморфными вариантами генов фибриногена, V фактора свертывания крови и гена протромбина. Сочетание поли- морфизмов данных трех генов ассоциировано с нарастанием неврологического дефицита, а также с утяжелением общего состояния пациентов к концу острого периода заболевания, вероятно, за счет развития экстрацеребральных тромбоэмболических осложнений.
Список литературы Клинико-генетическая характеристика больных ишемическим инсультом молодого и среднего возраста
- Воробьев П.А. Инсульт. Нормативные документы. М.: Ньюдиамед; 2010.
- Гусев Е.И., Мартынов М.Ю., Камчатнов П.Р. Ишемический инсульт. Современное состояние проблемы//Доктор.ру. 2013; 5 (83): 2-7.
- Суслина З.А., Пирадов М.А., Домашенко М.А. Инсульт: оценка проблемы (15 лет спустя). Журнал неврологии и психиатрии им. С.С. Корсакова. 2014; 11: 5-13.
- Alan S. AHA Statistical Update: Heart Disease and Stroke Statistics -2013 Update. A Report From the American Heart Association. Circulation. 2013; 127: 6-245.
- Скворцова В.И., Стаховская Л.В. Эпидемиология церебрального инсульта в РФ. Материалы Всероссийской научно-практической конференции «Нарушения мозгового кровообращения». Иркутск; 2011: 7-15.
- Машин В.В., Котова Е.Ю., Пинкова Е.А. Заболеваемость и факторы риска инсульта. Возможности профилактики. Неврологический вестник. Журнал им. В.М. Бехтерева. Т. XXXIX. Вып. 1. Материалы научного конгресса «Бехтерев -основоположник нейронаук: творческое наследие, история и современность» (приложение к журналу). 2007: 156-157.
- Lloyd-Jobes D., Adams R., Brown T. et al. Heart disease and stroke statistics-2010 update: a report from the American Heart Association. Circulation. 2010; 121: 46-215.
- Кобылина О.В., Гехт А.Б., Фаворова О.О., Гусев Е.И., Николаева Т.Я. Генетические аспекты ишемического инсульта. Инсульт, приложение к Журналу неврологии и психиатрии им. Корсакова. 2008; 23: 49-55.
- Goldstrein L., Bertels C., Davis J.N. Interrater reliability of the NIH Stroke Scale. Arch. Neurol. 1989; 46: 660-622.


