Клинико-генетические детерминанты генов ФНО-ОС, ИЛ-1/3 и ИЛ-1РА в инициации и развитии хронической сердечной недостаточности у больных ишемической болезнью сердца
Автор: Тепляков А.Т., Шилов С.Н., Березикова Е.Н., Яковлева Н.Ф., Торим Ю.Ю., Кистенева И.В., Кузнецова А.В., Воронина Е.Н., Маянская С.Д., Карпов Р.С.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 1 т.24, 2009 года.
Бесплатный доступ
Хроническая сердечная недостаточность (ХСН) - одна из актуальных проблем клинической кардиологии. Смертность от ХСН сопоставима с таковой онкологических больных. В экономически развитых странах отмечается неуклонное нарастание частоты этой патологии. Поэтому актуальны ранняя диагностика и современная эффективная профилактика ХСН. Цель работы - изучить клиникогенетические аспекты влияния полиморфных вариантов генов фактора некроза опухолиα (ФНО-α), интерлейкина-1β (ИЛ-1β) и рецепторного антагониста ИЛ-1 на инициацию и развитие ХСН у больных ИБС. Обследовано 165 больных ИБС I-IV ФК ХСН (121 мужчина и 44 женщины, в среднем возрасте 56,7±5,3 лет). Для количественного определения цитокинов в сыворотке использовался электрохемилюминесцентный метод (ЭХЛ). Идентификацию генотипов проводили с помощью ПДРФ-анализа ПЦРпродуктов. Группу контроля составили 114 практически здоровых лиц (54 мужчины и 60 женщин, средний возраст 53,2±4,9). Установлено, что уровень провоспалительного цитокина ФНО-α в крови пациентов с ХСН ассоциирован с высоким риском развития и ФК тяжести клинических проявлений ХСН. Показано, что аллель G полиморфного локуса G-308A ФНО-α ассоциирован с повышенным риском развития и тяжестью клинических проявлений ХСН; аллель А полиморфного локуса G-308A ФНО-α, напротив, не ассоциировался с повышенным риском развития ХСН. Кроме того, аллель С полиморфного локуса С+3953Т гена ИЛ-1β ассоциирован с риском развития, тяжестью и неблагоприятным характером течения ХСН у больных ИБС, тогда как аллель Т полиморфного локуса С+3953Т гена ИЛ-1β ассоциирован с благоприятным характером течения ХСН. В ходе исследования не было обнаружено тесных ассоциативных взаимосвязей между полиморфными вариантами гена ИЛ-1Ра (VNTR intron 2) и характером течения ХСН. Таким образом, установлены ассоциативные взаимосвязи между уровнем содержания ФНО-α в сыворотке крови, а также полиморфизмом генов ФНО-α и ИЛ-1β с высоким риском развития и тяжестью течения ХСН.
Сердечная недостаточность, ишемическая болезнь сердца, генетический полиморфизм, гены фно-α, ил-1β, ил-1ра
Короткий адрес: https://sciup.org/14919000
IDR: 14919000 | УДК: 616.12-008.46-02:616.127-005.4]:575
Clinical-genetic determinants of TFN, IL-1b and IL-1RA genes in the initiation and development of chronic heart failure in coronary artery disease patients
Clinical-genetic aspects of polymorphic variants of TNF-? gene, interleukin-1? gene and interleukin-1 receptor antagonist gene influence on the initiation and development of CHF in patients with CHD are presented in the article. We studied 165 CHD patients with NYHA Class I-IV CHF (121 males and 44 females, mean age - 56,7±5,3 years). Control group consisted of 114 persons (54 males and 60 females, mean age 53,2±4,9 years). The level of proinflammatory cytokine TNF-? in CHF patients was shown to be associated with high risk of CHF development and severity degree of CHF clinical manifestations. Associations between polymorphous variants of IL-1Ra gene (VNTR intron 2) and CHF development were not revealed. Association between serum TNF-? level and polymorphism of TNF-? and IL-1? genes with high risk of CHF development and severity of disease was found as well.
Текст научной статьи Клинико-генетические детерминанты генов ФНО-ОС, ИЛ-1/3 и ИЛ-1РА в инициации и развитии хронической сердечной недостаточности у больных ишемической болезнью сердца
E-mail: sergei@rnp.ru
КЛИНИКО-ГЕНЕТИЧЕСКИЕ ДЕТЕРМИНАНТЫ ГЕНОВ ФНО-А, ИЛ-1В И ИЛ-1РА В ИНИЦИАЦИИ И РАЗВИТИИ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА
-
* ГУ НИИ кардиологии Томского научного центра СО РАМН;
-
* * Новосибирский государственный медицинский университет;
-
* ** Новосибирский институт химической биологии и фундаментальной медицины СО РАН
Несмотря на значительные достижения в лечении сердечно-сосудистых заболеваний, распространенность хронической сердечной недостаточности (ХСН) не только не снижается, но, наоборот, возрастает. Самыми частыми причинами развития ХСН в экономически развитых странах мира являются ишемическая болезнь сердца (ИБС) и артериальная гипертензия (АГ). По данным эпидемиологических исследований, проведенных в нашей стране, оказалось, что у 4/5 всех больных с СН это заболевание ассоциируется с АГ и у 2/3 больных – с ИБС [1]. Прогноз при ХСН остается крайне неблагоприятным, поэтому своевременная профилактика и ранняя диагностика данной патологии является самой актуальной проблемой современной кардиологии.
Недавно была предложена новая концепция развития ХСН, в основе которой лежит парадигма о системном воспалении как об одном из важных независимых факторов высокого кардиоваскулярного риска [2, 3].
Согласно этой концепции, неспецифическая активация макрофагов и моноцитов, реализующаяся при тяжелых стрессорных нарушениях микроциркуляции, является индуктором синтеза провоспали-тельных цитокинов (в частности фактора некроза опухоли-α (ФНО-α), который ранее называли ка-хексином, а также интерлейкина-1α (ИЛ-1α), интер-лейкина-^З (ИЛ-1З), интерлейкина-6 (ИЛ-6) и др.), определяющих неблагоприятное развитие либо регресс ишемической и/или постинфарктной дисфункции сердца, ремоделирование левого желудочка (ЛЖ) и развитие ЛЖ-сердечной недостаточности [2-4]. При этом повышение экспрессии провоспали-40
тельных цитокинов напрямую связана с ФК тяжести ХСН и тесно коррелирует с концентрацией предсердного натрийуретического пептида, а также некоторых других нейрогормонов [3, 5].
Молекулярные механизмы, лежащие в основе ци-токининдуцируемых нарушений инотропной способности и ремоделирования ишемизированного миокарда, до конца неясны. Предполагают, что про-воспалительные цитокины играют важную роль в прогрессировании ХСН, опосредуя характер и интенсивность процессов ремоделирования миокарда и сосудов уровнем апоптоза кардиомиоцитов, который рассматривают в качестве фундаментального механизма, способного вызвать необратимые нарушения сократительной способности миокарда при ХСН [6, 7].
Провоспалительные цитокины являются важным и достаточно хорошо изученным классом биологических локальных клеточных патофизиологических регуляторов, способных инициировать и обострять развитие ХСН [8-11].
Показано, что уровень ФНО-α в сыворотке больных с тяжелой сердечной недостаточностью (III-IV ФК по NYHA) на порядок выше, чем у здоровых лиц. Причем повышенное содержание ФНО-α регистрировалось у пациентов с более тяжелыми клиническими проявлениями декомпенсации, большей степенью кахексии (с массой тела 82% от идеального веса) и повышенной активностью ренин-ангиотензин-альдостероновой системы [12]. В других работах обращено внимание на тесную корреляционную взаимосвязь высоких уровней ФНО-а, ИЛ-1З и ИЛ-6 с тяжестью клинических проявлений [13, 14] и нейро-гуморальной активацией у больных ХСН [15, 16].
Существует семейство цитокинов ИЛ-1, которое включает три цитокина с высокой степенью гомологии: ИЛ-1а, ИЛ-1З и рецепторный антагонист ИЛ-1 (ИЛ-1Ра). ИЛ-1а и ИЛ-1З обладают фактически идентичной активностью. Если ИЛ-1α является в основном медиатором местных защитных реакций, то ИЛ-10 представляет собой секреторный цитокин, который реализует свое действие как местно, так и на системном уровне. ИЛ-1Ра характеризуется тем, что он блокирует биологическую активность ИЛ-1 [17].
Уже более 10 лет существует такое направление как генетическая кардиология, которая интегрирует концепции и технологии молекулярной генетики для познания этиологии, патогенеза и механизмов клинического полиморфизма сердечно-сосудистых заболеваний человека [18, 19].
В общей картине этиологии и патогенеза некоторых мультифакториальных заболеваний может преобладать эффект одного или нескольких генов. Существуют десятки тысяч полиморфных генетических систем, эволюционной основой возникновения которых является большая приспособительная ценность определенных сочетаний наследственных факторов. Но наряду с хорошо приспособленными ин- дивидами существуют и индивиды с «неблагоприятными» сочетаниями наследственных факторов. Именно они и составляют группу лиц с наследственной предрасположенностью к болезням [20].
В последние годы в кардиологии проведен ряд научных исследований, посвященных оценке вклада генетических факторов в развитие недостаточности кровообращения [21-24]. Благодаря исследованиям генома человека, идентификации его генов, в том числе и генов, мутации которых приводят к наследственным болезням либо предрасполагают к наиболее частым полигенным (мультифакториальным) заболеваниям, впервые появилась реальная возможность не только проводить точную молекулярную диагностику, но и прогнозировать предрасположенность человека к тому или иному заболеванию [19, 25]. Исследования ассоциаций основаны на поиске популяционных корреляций в частотах аллелей. В классическом случае они представляют собой сравнение больных индивидов со здоровыми из той же популяции. Генетический маркер считается ассоциированным с болезнью, если его частота встречаемости среди больных значимо выше, чем в контрольной выборке.
Хорошо известно, что своевременная профилактика и ранняя диагностика различных заболеваний являются самыми актуальными проблемами современной медицины. Примечательно, что использование современных достижений в исследовании генома человека в клинической кардиологии сделали реальной раннюю, досимптомную диагностику не только генных, но и многих мультифакториальных заболеваний [25].
В клинической практике такая цель достигается посредством молекулярного тестирования генов, получивших название генов «предрасположенности» или кандидатных генов [25, 26]. Последние можно определить как гены, наследственные полиморфизмы которых совместимы с жизнью, но в сочетании с неблагоприятными внешними факторами (например, с лекарствами, продуктами питания, вредными привычками, инфекциями, загрязнением окружающей среды) могут послужить причиной различных, в том числе и таких частых патологических состояний и заболеваний, как атеросклероз, ИБС, сахарный диабет и т.д.
Таким образом, из приведенных данных следует, что такое направление в кардиологии подвергается интенсивному изучению и исследованию с целью выявления генетического риска и прогнозирования осложнений заболевания до появления клинических проявлений. Учитывая современные достижения в изучении патогенеза ХСН, можно предположить влияние полиморфизмов генов, кодирующих про-воспалительные цитокины, в частности цитокинов ФНО-α и ИЛ-1, на развитие и прогрессирование ХСН.
Для понимания механизмов развития и прогрессирования ХСН научные исследования в последние годы направлены на оценку генетических факторов развития этого синдрома. Это перспективный подход в связи с тем, что выявляется генетический риск и прогнозируются осложнения заболевания до появления клинических проявлений. Учитывая современные достижения в изучении патогенеза ХСН, целью нашей работы было изучить влияние полиморфных вариантов гена ФНО-а, ИЛ-1/З и гена ИЛ-1Ра, а также уровня ФНО-α в сыворотке на развитие и характер течения ХСН у больных с ИБС и АГ.
МАТЕРИАЛ И МЕТОДЫ
В исследование включено 165 больных ИБС со стенокардией напряжения I-III ФК (по классификации Канадской ассоциации кардиологов) – 121 мужчина и 44 женщины в возрасте от 45 до 65 лет (в среднем возрасте 56,7±5,3) с ХСН I-IV по NYHA. Фракция выброса (ФВ) левого желудочка колебалась в пределах 63-40% по данным эхокардиографии (ЭхоКГ). Обследовали пациентов, состояние которых сохранялось стабильным в течение не менее 23 недель на постоянной базовой терапии, включающей ингибиторы АПФ, диуретик, при необходимости антагонист альдостерона, дигоксин, а также 3—адре— ноблокаторы.
Критериями исключения являлись: острый коронарный синдром, острый инфаркт миокарда, острое нарушение мозгового кровообращения (перенесенное ранее 6 месяцев до исследования), гемодинамически значимые нарушения функции клапанного аппарата сердца, неконтролируемая артериальная гипертония, сахарный диабет типа II, желудочковые тахи- и брадиаритмии (обусловленные синдромом слабости синусового узла), фибрилляция предсердий, АВ-бло-кады II-III степени, онкологическая патология.
Диагноз верифицировался на основании тщательного анализа клинических данных, а также клинико-инструментальных исследований, включавших ЭКГ и рентгенографию грудной клетки по общепринятым методикам, ЭхоКГ, тест 6-минутной ходьбы, общеклинических и биохимических исследований крови и мочи.
Всех пациентов, включенных в исследование, разделили на 3 группы, сопоставимые по возрасту, длительности патологии и ФК ХСН. В 1-ю группу вошли 37 (22,4%) больных с I ФК ХСН, во 2-ю – 69 (41,8%) пациентов со II ФК ХСН, в 3-ю – 59 (35,8%) больных с III-IV ФК ХСН. Группу контроля составили 114 пациентов (54 мужчины и 60 женщин) в возрасте от 45 до 65 лет (в среднем возрасте 53,2±4,9) без клинических проявлений ИБС и ХСН.
На каждого больного заполнялась специально разработанная клиническая карта. Все пациенты давали свое письменное информированное согласие для участия в проспективном исследовании.
Состояние больных оценивали исходно и проспективно в течение 12 месяцев с анализом частоты комбинированной конечной точки, включающей: летальность, повторные госпитализации по поводу 41
обострений ХСН, эпизоды ухудшения течения сердечно-сосудистой патологии и ХСН.
В динамике проводили ЭхоКГ на аппарате «SONOS-2500» (США) по стандартной методике. Регистрировали конечные диастолический и систолический объемы (КДО и КСО) ЛЖ, ударный объем (УО), рассчитывали фракцию выброса (ФВ) ЛЖ. Методом допплерэхокардиографии оценивалось диастолическое наполнение ЛЖ с определением скорости раннего (√е) и позднего (√а) диастолического наполнения желудочков, отношения этих скоростей (√е/√а), времени замедленного раннего диастолического наполнения, времени изоволюмического расслабления ЛЖ. Физическую толерантность оценивали посредством теста 6-минутной ходьбы.
У всех пациентов забирался генетический материал (букальный эпителий) с последующим типиро-ванием аллелей гена ФНО-а (G-308A), ИЛ-1уЗ (С+3953Т) и гена ИЛ-1Ра (VNTR intron 2). Для выделения ДНК использовали метод фенол-хлороформной экстракции [28].
Генотипирование проводилось методом ПЦР; использовали праймеры, синтезированные в Институте химической биологии и фундаментальной медицины (ИХБФМ СО РАН).
Генотипирование ФНО-α проводилось в режиме реального времени с использованием конкурирующих TaqMan-зондов, комплементарных полиморфному участку ДНК.
Каждый образец амплифицировался с использованием пары праймеров (TNF308-R 5’-TTCCGAGGGGGGTCTTCTG-3’ и TNF-308U 5’-GTTCTATCTTTTTCCTGCATCCTGT-3’, размер ПЦР-продукта – 167 пар оснований) и двух зондов, несущих «гаситель» на 3’-конце и разные флуоресцентные красители (FAM либо R6G) на 5’-конце (FAM-зонд, 5’-FAM-CCCGTCCTCATGCCC-RTQ-3’ и R6G -зонд, 5’-R6G-CCCGTCCCCATGCCC-FQ-3’). Общий объем реакционной смеси составлял 25 мкл, смесь содержала 40-100 нг ДНК; 300 нМ каждого праймера; 100 нМ Taqman-зонда, конъюгированного с FAM; 200 нМ TaqМan-зонда, конъюгированного с R6G; 200 мкМ-ные dNTP, амплификационный буфер (65 mM Tris-HCl (pH8,9); 0,05% Tween 20; 16 mM (NH4)2SO4; 2,4 mM MgCl2), термостабильную Taq-полимеразу – 0,5 ед.акт./реакц.
ПЦР проводилась в следующих условиях: начальная денатурация 3’ при 96°С; затем 40 циклов, включавших денатурацию при 96°С-8”, отжиг праймеров и последующую элонгацию при 60°С-35” (каждый шаг сопровождался регистрацией флуоресцентного сигнала в диапазонах, соответствовавших интервалам флуоресценции флуорофоров FAM и R6G).
Структуры праймеров гена ИЛ-1уЗ (С+3953Т): прямой – TCCCTACTGGTGTTGTCATCAG; обратный – CTTGGGTGGACATGGTCCTG.
ПЦР проводили в конечном объеме 12 мкл, содержащем 650 мМ трис.-HCl (рН 8,9), 160 мМ суль-42
фат аммония; 20 мМ MgCl2; 0,05% Tween 20; 2 mM dNTP; 0,5 мкМ растворы олигонуклеотидных праймеров, 20-100 нг ДНК и 1 ед. Taq-полимеразы. Реакцию проводили на амплификаторе «Eppendorff» с начальной денатурацией при 95°С 3 мин., далее в течение 35 циклов с денатурацией 10 сек при 95°С, отжигом 10 сек при 62°С и синтезом 15 сек при 72°С. Финальная элонгация проводилась при 72°С 5 мин.
Для проведения ПДРФ-анализа полученных фрагментов ДНК рестрикцию осуществляли следующим образом. К амплификационной смеси добавляли 1/10 V 10х буфера для рестрикции и эндонуклеазу рестрикции (1-3 ед. акт. фермента) и инкубировали 2 часа при 65°С. Буфер для рестрикции использовали с учетом рекомендаций производителя эндонуклеазы рестрикции. Фермент инактивировали добавлением 1мкл 0,5М ЭДТА.
При гидролизе амплификационного фрагмента гена ИЛ-1^3 эндонуклеазой рестрикции TaqI выявлялось три фрагмента размером 550 п.н., 440 п.н. и 110 п.н. Фрагмент 550 п.н. соответствует амплифика-ционному фрагменту, не подвергнувшемуся гидролизу, что указывает на присутствие аллеля Т (+3953Т) гена ИЛ-1^3. При наличии аллеля C (C+3953) происходило разрезание амплификационного фрагмента ДНК на два, размером 440 п.н и 110 п.н.
Исследование полиморфизма ИЛ-1Ра проводили с помощью ПЦР с праймерами, фланкирующими полиморфный регион в пределах второго интрона, в котором находится вариабельное количество тандемных повторов – 86 п.н. (VNTR). В результате амплификации детектировали фрагменты ДНК размером 438, 610, и 696 п.н. с 2, 4 или 5 тандемными повторами соответственно. Эти аллели были обозначены как 2R, 4R и 5R в данном исследовании и соответствовали аллелям ИЛ-1Ра 2, 1, 4 [16] и IL1RN* 2, 1, 3 [29].
Структуры праймеров, синтезированных в Институте химической биологии и фундаментальной медицины СО РАН: ИЛ-1Ра-U– CCCACTCATGGCCTTGTTC; ИЛ-1Ра-R – GGCTCAATGGTACCACATC.
Амплификацию проводили в буфере, содержащем 10 мМ Трис-НСl (рН 8.9), 50 мМ KCl, 1,7 мМ MgCl, 0,05% Tween 20, с добавлением 0,2 мМ-го раствора dNTP, 0,5 мкМ-го раствора праймеров, 20 нг ДНК и 1,0 ед. акт. Taq-полимеразы. Реакционную смесь в объеме 20 мкл покрывали 40 мкл минерального масла. ПЦР проводили на амплификаторе «Терцик» («ДНК-Технология», Москва) с начальной денатурацией при 95°С – 2 мин, далее в течение 35 циклов при следующих режимах: денатурация – 7 с при 95°С; отжиг праймеров – 10 с при 64°С; элонгация – 20 с при 72°С.
Для количественного определения цитокинов в сыворотке был использован электрохемилюминесцентный метод (ЭХЛ) [27].
ЭХЛ метод основан на реакции электронного переноса, в которой молекула прекурсор-трипопила- мин (ТПА) и рутений трис-бипиридина хелат (Ru (bpy2+3) или TAG) при контакте с электродом теряют электрон и активируются, в результате чего рутений приобретает способность в момент восстановления Ru2+ до Ru3+ испускать фотон специфичной длины волны 620 нм. Источником электрона необходимого для восстановления Ru2+ служит активированный ТПА. Реакция может протекать только непосредственно у поверхности электрода, благодаря этому достигается высокое разрешение и низкий уровень фона. Свойство рутения образовывать N-гидроксисукцинимидэфир (NHS) рутения (II) трис-бипиридина хелат или TAG-NHS Ester, способного эффективно реагировать с депротонированны-ми алифатическими остатками аминокислот на Fc фрагменте антител, позволяет использовать реакцию электронного переноса с последующей эмиссией света для количественной оценки TAG меченых молекул в растворе.
Для осуществления всех инкубаций и детекции сигнала использовался электрохемилюминометр ORIGEN Analyzer, разработанный фирмой IGEN, Inc/ (USA). Для количественного определения цитокинов пара антител, не конкурирующих за эпитопы связывания на антигене, метятся TAG и биотином.
Исследуемую группу инкубировали с TAG мечеными антителами. После инкубации в раствор добавляли биотинилированные антитела. К образовавшимся в растворе структурам антиген- антитело (сэндвич) добавляют парамагнитные микробусы, покрытые ковалентно связанным с поверхностью бус стрептавидином. Реакция стрептосидина с биотином приводит к образованию конъюгата бусы/сэндвич, в таком виде конъюгат поступает в камеру люминато-ра Analyzer. Подвижный магнит притягивает конъюгат к электроду, на поверхности которого протекает реакция электрохемилюминесценции, в результате которой освобождается фотон длиной волны 620 nm, регистрируемый люминометром. Калибровочная кривая (КК) строится по нескольким стандартным разведениям рекомбинантного цитокина. Полученные данные обрабатывали на компьютере.
Статистическая обработка результатов проводилась с помощью стандартного статистического пакета программ SPSS 13,0. Сравнение частот встречаемости генотипов полиморфных локусов в различных популяциях проводили по критерию χ2. Сравнение средних значений анализируемых показателей проводили с помощью t-критерия Стьюдента или U-критерия Манна-Уитни.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Оценка уровня ФНО-α показала, что в начале наблюдения ФНО-α во всех группах был статистически значимо выше контроля (р<0,01-0,001) группы контроля (рис. 1). Так, у пациентов 1-й группы с I ФК ХСН уровень ФНО-α был в 1,8 раза выше группы контроля (р<0,01), при этом в 2,1 раза меньше, чем у пациентов 3-й группы с III-IV ФК ХСН (р<0,01). У пациентов 2-й группы с II ФК ХСН ФНО-α составил 81,6±8,2 пг/мл, в 2,6 раза превышая таковой в группе контроля (р<0,001). Наиболее высокий исходный уровень ФНО-α регистрировался в крови пациентов 3-й группы с III-IV ФК ХСН, достигая 119±12,3 пг/мл, в 3,7 раза превышая таковой контрольной группы (р<0,001).
Таблица 1
Частота встречаемости аллелей и генотипов полиморфного локуса G-308A гена ФНО-α в группе больных ХСН и в группе контроля
|
Выборка |
Аллели, n (%) |
Генотипы, n (%) |
|||
|
G |
A |
G/G |
G/A |
A/A |
|
|
Группа контроля, n=114 |
181 (79,4) |
47 (20,6) |
79 (69,3) |
23 (20,2) |
12 (10,5) |
|
Группы больных, n=165 |
292 (88,5)* |
38 (11,5)* |
129 (78,2)* |
34 (20,6) |
2 (1,2)* |
|
Мужчины (группа контроля), n=54 |
85 (78,7) |
23 (21,3) |
36 (66,7) |
13 (24,1) |
5 (9,2) |
|
Мужчины (группы больных), n=121 |
219 (90,5)* |
23 (9,5)* |
99 (81,8)* |
21 (17,4)* |
1 (0,8)* |
|
Женщины (группа контроля), n=60 |
96 (80,0) |
24 (20,0) |
43 (71,7) |
10 (16,7) |
7 (11,6) |
|
Женщины (группы больных), n=44 |
73 (82,9) |
15 (17,1) |
30 (68,2) |
13 (29,5) * |
1 (2,3)* |
Примечание. * – различия статистически значимы по сравнению с группой контроля, р<0,05.
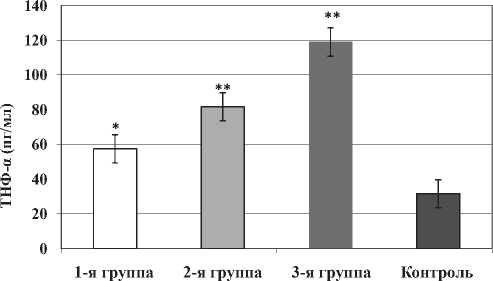
Рис. 1. Сравнительная оценка уровней экспрессии ФНО-а в крови пациентов в зависимости от тяжести ХСН.
Примечание. * - различия статистически значимы по сравнению с группой контроля, р<0,01, ** - различия статистически значимы по сравнению с группой контроля, р<0,001
Распределение частот встречаемости генотипов гена ФНО-α в 1-й-3-й группах больных и в контрольной группе соответствовало ожидаемому при равновесии Харди-Вайнберга. Результаты исследования полиморфного локуса G-308A гена ФНО-α в целом в группе контроля и в группах больных (с учетом влияний пола) представлены в табл. 1.
Оказалось, что в целом у больных частота аллеля G и генотипа G/G была статистически значимо выше (соответственно на 9,1% и 8,9%), а частота аллеля A и генотипа А/А была статистически значимо ниже (соответственно на 9,1% и 9,3%) по сравнению с группой контроля. Следовательно, аллель G (p<0,05) и генотип G/G (p<0,05) являются факторами риска развития ХСН, а аллель A (p<0,05) и генотип A/A (p<0,05) проявили себя как протективный генетический фактор. Однако при исследовании полиморфного локуса G-308A гена ФНО-α в зависимости от пола оказалось, что аллель G и генотип G/G ассоциировались с риском развития ХСН (p<0,05), а аллель A проявил себя как протективный фактор (p<0,05) только у лиц мужского пола, тогда как среди женщин по данным аллелям и генотипам статистически значимых различий между группами контроля и больных не обнаруживалось.
Распределение частот встречаемости генотипов гена ИЛ-13 в группах больных с ХСН соответствова- ло ожидаемому при равновесии Харди-Вайнберга, а в контрольной группе в целом и у мужчин наблюдалось значимое отклонение от ожидаемого распределения генотипов (р=0,032 и р=0,015 соответственно), что, вероятнее всего, было обусловлено тем, что группа контроля не являлась случайной выборкой. Результаты исследования полиморфного локуса С+3953Т гена ИЛ-13 в целом в группе контроля и в группах больных с ХСН, а также в зависимости от пола представлены в табл. 2.
Установлено, что в целом у больных частота аллеля С и генотипа С/С была статистически значимо выше (соответственно на 12,2% и 20,6%), а частота аллеля Т и генотипов С/Т и Т/Т была статистически значимо ниже (соответственно на 12,2%, 16,8% и 3,8%), чем в группе контроля. Следовательно, аллель (p<0,05) и генотип С/С (p<0,05) являются факторами генетического риска развития ХСН, а аллель Т (p<0,05) и генотипы С/Т (p<0,05) и Т/Т (p<0,05) проявили себя как протективные факторы. Вместе с тем исследование полиморфного локуса С+3953Т гена ИЛ-13 в зависимости от пола показало, что аллель С был ассоциирован с риском развития ХСН (p<0,05), а аллель Т проявил себя как протективный фактор (p<0,05) только у лиц мужского пола, тогда как среди женщин статистически значимых различий между группами контроля и больных мы не обнаружили.
Таблица 2
Частота встречаемости аллелей и генотипов полиморфного локуса С+3953Т гена ИЛ-1β в группе больных ХСН и в группе контроля
|
Выборка |
Аллели, n (%) |
Генотипы, n (%) |
|||
|
С |
Т |
С/С |
С/Т |
Т/Т |
|
|
Группа контроля, n=114 |
154 (67,5) |
74 (32,5) |
47 (41,2) |
60 (52,6) |
7 (6,2) |
|
Группы больных, n=165 |
263 (79,7)* |
67 (20,3)* |
102 (61,8)* |
59 (35,8)* |
4 (2,4)* |
|
Мужчины (группа контроля), n=54 |
76 (70,4) |
32 (29,6) |
23 (42,6) |
30 (55,6) |
1 (1,8) |
|
Мужчины (группы больных), n=121 |
198 (81,8)* |
44 (18,2)* |
78 (64,5)* |
42 (34,7)* |
1 (0,8) |
|
Женщины (группа контроля), n=60 |
78 (65) |
42 (35) |
24 (40) |
30 (50) |
6 (10) |
|
Женщины (группы больных), n=44 |
65 (73,9) |
23 (26,1) |
24 (54,5) |
17 (38,6) |
3 (6,9) |
Примечание. * – различия статистически значимы по сравнению с группой контроля, р<0,05.
Таблица 3
Частота встречаемости аллелей и генотипов полиморфного локуса VNTR intron 2 гена ИЛ-1Ра в группе больных ХСН и в группе контроля
|
Выборка |
Аллели, n (%) |
Генотипы, n (%) |
||||
|
2R |
4R |
2R/2R |
2R/4R |
4R/4R |
2R/5R+4R/5R |
|
|
Группа контроля, n=114 |
67 (29,4) |
160 (70,2) |
14 (12,3) |
39 (34,2) |
60 (52,6) |
1 (0,9) |
|
Группы больных, n=165 |
108 (32,7) |
208 (63) |
25 (15,2) |
55 (33,3) |
71 (43) |
14 (8,5) |
|
Мужчины (группа контроля), n=54 |
29 (26,9) |
79 (73,1) |
5 (9,2) |
19 (35,2) |
30 (55,6) |
0 |
|
Мужчины (группы больных), n=121 |
81 (33,5) |
151 (62,4) |
19 (15,7) |
40 (33,1) |
53 (43,8) |
8 (6,6) |
|
Женщины (группа контроля), n=60 |
38 (31,7) |
81 (67,5) |
9 (15) |
20 (33,3) |
30 (50) |
1 (1,7) |
|
Женщины (группы больных), n=44 |
27 (30,7) |
57 (64,8) |
6 (13,7) |
15 (34,1) |
18 (40,9) |
6 (13,6) |
Результаты исследования полиморфного локуса VNTR (intron 2) гена ИЛ-1Ра в целом в группе контроля и у больных (с учетом влияния пола) представлены в табл. 3.
Распределение частот встречаемости генотипов гена ИЛ-1Ра во всех представленных группах соответствовало ожидаемому при равновесии Харди-Вайнберга, кроме группы больных в целом (р=0,015). Для удобства анализа в одну группу были объединены генотипы 2R/5R и 4R/5R полиморфного локуса VNTR (intron 2) гена ИЛ-1Ра.
Статистически значимых различий в распределении частот встречаемости генотипов и аллелей гена ИЛ-1Ра (полиморфизм VNTR intron 2) в целом у больных с ХСН и в группе контроля, а также в зависимости от пола получено не было.
Результаты исследования взаимосвязи генетических маркеров гена ФНО-а, гена ИЛ-1^3 и гена ИЛ-1Ра со степенью тяжести ФК ХСН (по NYHA) представлены в табл. 4.
Установлены статистически значимые различия по частоте встречаемости генетических маркеров генов ФНО-а ИЛ-1^3 в зависимости от тяжести ФК ХСН. Частота генотипа G/G во 2-й (82,6%, р<0,05) и
Таблица 4
Распределение частот встречаемости генотипов и аллелей гена ФНО-α (G-308A), гена ИЛ-1β (С+3953Т) и гена ИЛ-1Ра (VNTR intron 2) в зависимости от ФК ХСН (NYHA)
|
Генетический маркер |
1-я группа (I ФК), n=37 |
2-я группа (II ФК), n=69 |
3-я группа (IIIIV ФК), n=59 |
|
Генотип G/G |
20 (54,1%) |
57 (82,6%)* |
52 (88,1%)* |
|
Генотип G/A |
15 (40,5%) |
12 (17,4%)** |
7 (11,9%)**# |
|
Генотип A/A |
2 (5,4%) |
0 (0%) |
0 (0%) |
|
АллельG |
55 (74,3%) |
126 (91,3%)* |
111 (94,1%)** |
|
Аллель A |
19 (25,7%) |
12 (8,7%)** |
7 (5,9%)** |
|
Генотип С/C |
12 (32,4%) |
41 (59,4%)* |
49 (83,1%)**# |
|
Генотип C/T |
23 (62,2%) |
27 (39,1%)* |
9 (15,2%)**# |
|
Генотип Т/Т |
2 (5,4%) |
1 (1,5%) |
1 (1,7%) |
|
Аллель С |
47 (63,5%) |
109 (79%)* |
107 (90,7%)* |
|
АллельТ |
27 (36,5%) |
29 (21%)* |
11 (9,3%)**# |
|
Генотип 2R/2R |
7 (18,9%) |
10 (14,5%) |
8 (13,6%) |
|
Генотип 2R/4R |
11 (29,7%) |
26 (37,7%) |
18 (30,5%) |
|
Генотип 4R/4R |
18 (48,6%) |
23 (33,3%) |
30 (50,8%) |
|
Генотип 2R/5R+4R/5R |
1 (2,7%) |
10 (14,5%) |
3 (5,1%) |
|
Аллель 2R |
25 (33,8%) |
48 (39,3%) |
35 (29,7%) |
|
Аллель 4R |
48 (64,7%) |
80 (58%) |
80 (67,8%) |
Примечание. * – различия статистически значимы по сравнению с 1-й группой c I ФК, p<0,05; ** – различия статистически значимы по сравнению с 1-й группой c I ФК, p<0,001; # – различия статистически значимы по сравнению со 2-й группой с II ФК, p<0,05.
3-й группе (88,16%, р<0,05) была статистически значимо выше, чем в 1-й группе (54,1%). Частота же генотипа G/A существенно преобладала в 1-й группе (40,5%, р<0,001) по сравнению со 2-й и 3-й группами (17,4% и 11,9% соответственно). Различия по частоте аллеля G (I ФК – 74,3%, II ФК – 91,3% и IIIIV ФК – 94,1%), а также аллеля А (I ФК – 25,7%, II ФК – 8,7% и III-IV ФК – 5,9%) оказались статистически значимыми.
Частота генотипа С/С в 3-й группе статистически значимо преобладала над таковыми во 2-й и в 1-й группах (83,1%, 59,4% и 32,4%, р<0,05 и p<0,001 соответственно), а во 2-й группе она значимо превышала ее по сравнению с 1-й группой (р<0,05). Вместе с тем генотипы, содержащие аллель Т, во 2-й группе встречались чаще, чем в 3-й (40,6% и 16,9%, р<0,001), но реже, чем в 1-й группе (40,6% против 67,6%, р<0,05). Различия по частоте аллеля С (I ФК – 63,5%, II ФК – 79% и III-IV ФК – 90,7%) и аллеля Т (I ФК – 36,5%, II ФК – 21% и III-IV ФК – 9,3%) также оказались статистически значимыми.
По данным распределения частот встречаемости генотипов и аллелей гена ИЛ-1Ра (VNTR intron 2) в зависимости от ФК ХСН (NYHA) статистически значимых различий получено не было.
С целью выявления возможности ассоциации уровня ФНО-α в сыворотке крови, полиморфизмов генов ФНО-а, ИЛ-1уЗ и ИЛ-1Ра с характером течения ХСН больные были разделены по итогам 12-месячного проспективного наблюдения на две группы: группа А – пациенты с благоприятным течением ХСН и группа Б – пациенты с неблагоприятным течением заболевания. При этом в течение периода наблюдения оценивались: состояние гемодинамических показателей, частота нарастания симптомов и признаков ХСН, частота госпитализаций по поводу СН, динамика ФВ ЛЖ. В результате в группу А вошли 95 человек, в группу Б – 70 человек (табл. 5).
В начале проспективного наблюдения во всех группах уровень ФНО-α у пациентов с неблагоприятным течением был статистически значимо выше (р<0,05), чем у пациентов с благоприятным течением. В динамике наблюдения в 1-й группе отмечалось статистически значимое снижение уровня ФНО-α как у пациентов с благоприятным течением ХСН, так и у пациентов с неблагоприятным течением (р<0,05). Во 2-й группе статистически значимое снижение ФНО-α в 1,6 раза отмечалось только у пациентов с благоприятным течением (р<0,05), в подгруппе Б, напротив, наблюдалась тенденция прироста уровня ФНО-α. В 3-й группе с III-IV ФК ХСН не произошло существенного снижения уровня ФНО-α к концу наблюдения.
Таблица 5
Уровень ФНО-а у больных в подгруппах А и Б (М±м)
|
ФНО |
1-я группа ХСН (I ФК 1), n=37 |
2-я группа ХСН (II ФК 2), n=69 |
3-я группа ХСН (ПЛУФК), n=59 |
||||||
|
Группа А n=27 |
Группа Б n=10 |
А % |
Группа А n=41 |
Группа Б n=28 |
А % |
Группа А n=27 |
Группа Б n=32 |
А % |
|
|
1 точка |
42,3±7,0 |
67,2±8,2* |
24,9 |
67,4±8,6 |
92,3±10,4* |
24,9 |
111,4±9,3 |
137,4±11,3* |
26,0 |
|
2 точка |
34,8±10,8# |
49,7±6,2*# |
14,9 |
41,2±7,1# |
97,8±12,9* |
56,6 |
98,4±5,3 |
141,5,4±12,3* |
43,1 |
Примечание. * – различия показателя статистически значимы по отношению к группе А (р<0,05); # –различия показателя статистически значимы по сравнению с исходными данными внутри группы (р<0,05).
Таким образом, статистически высокозначимое и существенное повышение в крови ключевого про-воспалительного цитокина ФНО-α ставит его в ряд важнейших маркеров, способных объективно характеризовать степень тяжести ХСН у больных ИБС.
Анализ распределения частот встречаемости генотипов и аллелей генов ФНО-а, ИЛ-18 и Л-1Ра в зависимости от характера течения ХСН показал (табл. 6), что среди пациентов с неблагоприятным характером течения ХСН (группа Б) статистически значимо чаще (р<0,05) встречались аллель С и носители генотипа С/С и статистически значимо реже (р<0,01) – аллель Т и носители генотипов, содержащих аллель Т в гомо- и гетерозиготном состоянии. Следовательно, аллель С и генотип С/С являются факторами неблагоприятного течения ХСН, а ал-
Таблица 6
Распределение частот встречаемости генотипов и аллелей гена ФНО-а, гена ИЛ-1в и гена ИЛ-1Ра в зависимости от характера течения ХСН
|
Генетический маркер |
Группа А (n=95) |
Группа Б (n=70) |
|
ГенотипG/G |
74 (77,9%) |
55 (78,6%) |
|
Генотип G/A |
19 (20,0%) |
15 (21,4%) |
|
ГенотипA/A |
2 (2,1%) |
0 (0%) |
|
АллельG |
167 (87,9%) |
125 (89,3%) |
|
Аллель A |
23 (12,1%) |
15 (10,7%) |
|
Генотип С/C |
44 (46,3%) |
58 (82,9%)* |
|
Генотип C/T |
47 (49,5%) |
12 (17,1%)** |
|
Генотип Т/Т |
4 (4,2%) |
0 (0%) |
|
Аллель С |
135 (71,1%) |
128 (91,4%)* |
|
АллельТ |
55 (28,9%) |
12 (8,6%)** |
|
Генотип 2R/2R |
15 (15,8%) |
10 (14,3%) |
|
Генотип 2R/4R |
39 (41,1%) |
32 (45,7%) |
|
Генотип 4R/4R |
33 (34,7%) |
22 (31,4%) |
|
Генотип 2R/5R+4R/5R |
8 (8,4%) |
6 (8,6%) |
|
Аллель 2R |
71 (37,4%) |
53 (37,9%) |
|
Аллель 4R |
111 (58,4%) |
12 (57,9%) |
Примечание. * – р<0,05; ** – p<0,01.
лель Т и генотипы С/Т и Т/Т проявили себя как про-тективные факторы.
По данным распределения частот встречаемости генетических маркеров гена ФНО-α и гена ИЛ-1Ра (VNTR intron 2) в зависимости от характера течения ХСН статистически значимых различий получено не было.
Результаты проведенного исследования убедительно продемонстрировали, что уровень в крови про-воспалительного цитокина ФНО-α у пациентов с ХСН ассоциирован с высоким индивидуальным риском развития и тяжестью клинических проявлений, а также с характером течения ХСН. Это подтверждается данными литературы о неблагоприятном влиянии провоспалительных цитокинов на инициацию, становление и прогрессирование ишемической дисфункции, ЛЖ-сердечной недостаточности и глобальной ХСН [2-4].
В литературе данных об исследованиях ассоциаций полиморфизмов генов цитокинов ФНО-α (G-308A), ИЛ-18 (+3953) и ИЛ-1Ра (VNTR intron 2) с сердечно-сосудистой патологией имеется относительно немного, а исследования о связи этих полиморфизмов с риском развития и характером прогрессирования ХСН у больных с ИБС и АГ вообще отсутствуют.
Francis S.E. et al. в 1999 г. обнаружили ассоциацию аллеля 2R гена ИЛ-1Ра с атеросклеротическим поражением коронарных артерий, установленным на основании коронароангиографии (Р=0,005) [30]. Однако в ряде других исследований не обнаруживались ассоциации между данным полиморфизмом генов и коронарным атеросклерозом и таким осложнением ИБС, как инфаркт миокарда [31-34]. Kastrati А. et al. [35] при исследовании 1850 пациентов обнаружили статистически значимо меньший риск возникновения рестенозов у носителей аллеля 2R (+2018 in exon 2) после стентирования.
Latkovskis G. et al. при исследовании взаимодействия между уровнем С-реактивного белка и полиморфизмами генов, кодирующих ИЛ-18 (-511), ИЛ-18 (+3953), ИЛ-1Ра (VNTR intron 2), ИЛ-6 (-174) и ИЛ-6 (-572), у 160 пациентов с атеросклеротическим поражением коронарных артерий обнаружили: высокие уровни СРБ у носителей Т-аллеля гена ИЛ-18 (+3953) (Р<0,05) и низкие показатели
СРБ у носителей аллеля 2R гена ИЛ-1Ра (Р<0,01) [36]. В другом исследовании у 674 пациентов с такой же коронарной патологией авторы не обнаружили ассоциаций между полиморфизмами генов, кодирующих ИЛ-1а (-889), ИЛ-1^3 (-511 и +3953) с риском прогрессирования ИБС [30]. Подобный же результат был получен в отношении полиморфизма гена ИЛ-1уЗ (-511) у 335 пациентов с атеросклерозом коронарных артерий, подтвержденным ангиографически [34].
В целом, все эти данные показывают неоднозначность результатов, касающихся ассоциации полиморфных вариантов вышеперечисленных генов, поэтому данная проблема требует дальнейшего целенаправленного изучения и тщательного планирования на соответствующих солидных клинически контролируемых популяциях.
Таким образом, в ходе проведенного исследования установлено, что аллель G полиморфного локуса G-308A ФНО-α ассоциируется у больных ИБС мужского пола с индивидуально высоким риском развития ХСН, а также с ФК тяжести клинических проявлений ХСН. Аллель А полиморфного локуса G-308A ФНО-α, наоборот, ассоциируется с низким риском развития ХСН. У женщин с ИБС, отягощенной ХСН, подобной закономерности не обнаружено.
Установлено также, что аллель С полиморфного локуса С+3953Т гена ИЛ-1уЗ ассоциируется с риском развития, тяжестью клинических проявлений и неблагоприятным характером течения ХСН у больных с ИБС, тогда как аллель Т полиморфного локуса С+3953Т гена ИЛ-1уЗ ассоциировался с низким риском развития данной патологии и с благоприятным характером течения ХСН. Также в ходе исследования не было обнаружено тесных ассоциативных взаимосвязей между полиморфными вариантами гена ИЛ-1Ра (VNTR intron 2) и риском развития, тяжестью течения ХСН.
Резюмируя полученные данные, следует особо подчеркнуть, что клинико-генетические исследования, доступные в настоящее время для кардиологической практики, могут сыграть важную роль в раннем выявлении той или иной сердечно-сосудистой патологии (и в частности ХСН) до ее клинической мани-фистации и, таким образом, определять большую значимость для эффективной профилактики риска возникновения, прогрессирования и серьезных осложнений заболевания, а также объективной надежной оценки перспектив лечения. Такой же точки зрения придерживается ряд авторитетных исследователей [20, 24, 25, 37-40].
Список литературы Клинико-генетические детерминанты генов ФНО-ОС, ИЛ-1/3 и ИЛ-1РА в инициации и развитии хронической сердечной недостаточности у больных ишемической болезнью сердца
- Агеев Ф.Т., Даниелян М.О., Мареев В.Ю. и др. Больные с хронической сердечной недостаточностью в российской амбулаторной практике: особенности контингента, диагностики и лечения (по материалам исследования ЭПОХА-О-ХСН). Сердечная недостаточность 2004; 5(1): 4-7.
- Ольбинская Л.И., Игнатенко С.Б. Роль цитокиновой агрессии в патогенезе синдрома сердечной кахексии у больных хронической сердечной недостаточностью. Сердечная недостаточность 2001; 2: 132-134.
- Тепляков А.Т., Дибиров М.М., Болотская Л.А. и др. Модулирующее влияние карведилола на активацию цитокинов и регресс сердечной недостаточности у больных с постинфарктной дисфункцией сердца. Кардиология 2004; 9: 50-57.
- Насонов Е.Л., Самсонов М.Ю., Беленков Ю.Н. и др. Иммунопатология застойной сердечной недостаточности: роль цитокинов. Кардиология 1999; 3: 66-73.
- Henriksen P.A., Newby D.E. Therapeutic inhibition of tumor necrosis factor α in patients with Heart failure: cooling an inflamed Heart. Heart 2003; 89: 14-18.
- Макарков А.И., Салмаси Ж.М., Санина Н.П. Апоптоз и Сердечная недостаточность. Сердечная недостаточность 2003; 6: 312-314.
- Кang P.M., Izumo S. Apoptosis and Heart Failure. A Critical Review of the Literature. Circ Res 2000; 86: 1107-1113.
- Мann D.L. Inflammatory mediators and the failing heart: past, present, and the foreseable future. Circulat Res 2002; 91: 988-998.
- Ребров А.П., Толстов С.Н. Клинико-диагностическое значение активации цитокинов и изменения морфо-функциональных параметров сердца у больных с хронической сердечной недостаточностью и возможности коррекции выявленных нарушений симвастатином. Кардиология 2007; 5: 14-18.
- Blum A., Miller H. Pathophysiological role of cytokines in congestive heart failure. Annu Rev Med 2001; 52: 15-27.
- von Haehling S., Jankowska E.A., Anker S.D. Tumour necrosis factor-alpha and the failing heart: pathophysiology and therapeutic implications. Basic Res Cardiol 2004; 99: 18-28.
- Levine B., Kalman J., Mayer L. Elevated circulating levels of tumor necrosis factor in severe chronic heart failure. N Engl J Med 1990; 323: 236-241.
- Teasta M., Yeh M., Lee P. Circulating levels of cytokines and their endogenous modulators in patients with mild to severe congestive heart failure due to coronary artery disease or hypertension. J Am Coll Cardiol 1996; 28: 964-971.
- Comini L., Bachetti T., Agnoletti L. et al. Induction of functional inducible nitric oxide synthase in monocytes of patients with congestive heart failure. Link with tumor necrosis factor-alpha. Eur Heart J 1999; 20(20): 1503-1513.
- МacGowan G., Mann D.L., Kormos R.L. Circulating interleukin-6 in severe congestive heart failure. Am J Cardiol 1997; 79: 1128-1131.
- Rauchhaus M., Koloczek V., Florea V. The relationship between tumor necrosis factor-a and natriuretic peptides in patients with chronic heart failure. Eur J Heart Failure 1999; 1 (Suppl): 203.
- Dinarello C.A. Interleukin-1. Cytokine and Growth Factor Reviews 1997; 8 (4): 253-265.
- Schwartz K. On the pulse of genetic cardiology. Nat. Genet 1994; 8: 110-111.
- Cambien F., Tiret L. Genetics of cardiovascular diseases. Circulation 2007; 116: 1714-1724.
- Бочков Н.П. Клиническая генетика. М., «Гэотар-Мед.», 2001, 440 с.
- Bleumink G.S., Schut A.F., Sturkenboom M.C. et al. Genetic polymorphisms and heart failure. Genet Med 2004; 6 (6): 465-474.
- Кitsios G., Zintzaras E. Genetic variation associated with ischemic heart failure: a HuGE review and meta-analysis. Am J Epidemiol 2007; 166 (6): 619-633.
- Snyder E.M., Olson T.P., Johnson B.D. Genetics and pharmacogenetics in heart failure. Curr Heart Fail Rep 2007; 4(3): 139-144.
- Губаев К.И., Насибуллин Т.Р., Карамова И.М. и др. Анализ ассоциаций полиморфизма -344Т/С гена альдостеронсинтазы с хронической сердечной недостаточностью ишемической этиологии. Сердечная недостаточность 2007; 8(5): 236-238.
- Баранов В.С., Хавинсон В.Х. Определение генетической предрасположенности к некоторым мультифакториальным заболеваниям. Генетический паспорт. СПб., «Фолиант», 2001, 48 с.
- Le Convoisier P., Park H.Y., Carlson K.M et al. Impact of genetic polymorphisms on heart failure prognosis. Arch Mal Coeur Vaiss 2003; 96(3): 197-206.
- Крысов С.В., Курамшин Д.Х., Силков С.В. и др. Использование электрохемилюминесцентного метода для количественного определения цитокинов в различных средах. Клиническая лабораторная диагностика 2000; 12: 39-43.
- Маниатис Т., Фрич Э., Сэмбрук Дж. Молекулярное клонирование. М., «Мир», 1984, 480 с.
- Смольникова М.В., Коненков В.И. Клиническая иммуногенетика заболеваний человека. Медицинская иммунология 2001; 3: 379-389.
- Francis S.E., Camp N.J., Dewberry R.D. et al. Interleukin-1 receptor antagonist gene polymorphism and coronary artery disease. Circulation 1999; 99: 861-866.
- Manzoli A., Andreotti F., Varlotta C. et al. Allelic polymorphism of the interleukin-1 receptor antagonist gene in patients with acute or stable presentation of ischemic heart disease. Cardiologia 1999; 44: 825-830.
- Iacoviello L., Donati M.B., Gattone M. Possible different involvement of interleukin-1 receptor antagonist gene polymorphism in coronary single vessel disease and myocardial infarction. Circulation 2000; 101: E193.
- Zee R.Y., Lunze K., Lindpaintner K. et al. A prospective evaluation of the interleukin-1 receptor antagonist intron 2 gene polymorphism and the risk of myocardial infarction. Thromb Haemost 2001; 86: 1136-1138.
- Vohnout B., Di Castelnuovo A., Trotta R. et al. Interleukin-1 gene cluster polymorphisms and risk of coronary artery disease. Haematologica 2003; 88 (1): 54-60.
- Kastrati A., Koch W., Berger P., et al. Protective role against restenosis from an interleukin-1 receptor antagonist gene polymorphism in patients treated with coronary stenting. J A m Coll Cardiol 2000; 36: 2168-2173.
- Latkovskis G., Licis N., Kalnins U. C-reactive protein levels and common polymorphisms of the interleukin-1 gene cluster and interleukin-6 gene in patients with coronary heart disease. Eur J Immunogenet 2004; 31 (5): 207-213.
- Tерещенко С.Н., Джаиани Н.А., Моисеев В.С. Генетические аспекты хронической сердечной недостаточности. Тер архив 2000; 4: 75-77.
- Коган-Пономарев М.Я. Клиническое значение некоторых факторов транскрипции генов при болезнях сердца. Кардиология 2004; 1: 66-70.
- Затейщиков Д.А., Чумакова О.С., Затейщикова А.А. и др. Генетические предикторы неблагоприятного течения заболевания у больных ИБС высокого риска по данным 2-летнего наблюдения. Кардиология 2004; 12: 16-22.
- Valen G., Yan Z., Hansson G.K. Nuclear factor kappa-B and the heart. J Am Coll Cardiol 2001; 38: 307-314.


