Комплексный подход в лечении хронического инкрустирующего цистита
Автор: Васин Р.В., Ионов Е.Н., Жиборев А.Б., Васин А.Р.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Инфекционно-воспалительные заболевания
Статья в выпуске: 4 т.18, 2025 года.
Бесплатный доступ
Введение. Инкрустирующий цистит (ИЦ) – редкое хроническое воспалительное заболевание мочевого пузыря с поражением слизистой оболочки инкрустациями и формированием конкрементов. Цель исследования: повысить эффективность лечения пациентов с хроническим инкрустирующим циститом. Материалы и методы. Рандомизированное проспективное одноцентровое исследование включило 33 пациента с ИЦ: І группа – 18 пациентов, которым проводилось оперативное лечение (эндоскопическое удаление конкрементов и инкрустаций из полости мочевого пузыря), антибактериальная терапия по результатам посева мочи, L-метионин внутрь 1 месяц и инстилляции мочевого пузыря раствором с кислым рН; II группа – 15 пациентов, которым проводилось тоже лечение, но без инстилляций мочевого пузыря. Результаты. Возраст пациентов варьировал от 39 до 78 лет. В 32 (96,9%) случаях в анамнезе имелся факт катетеризации мочевого пузыря. В обеих группах была выявлена щелочная реакция мочи, гематурия и лейкоцитурия. Бактериурия выявлена у 24 (72,7%) пациентов с ИЦ. Corynebacterium urealyticum (CU) не была выявлена ни у одного пациента. Динамика общего анализа мочи через 1 месяц после лечения в обеих группах продемонстрировала достоверное улучшение в сравнение с предоперационными данными, так: в I группе лейкоцитурия уменьшилась с 88,8±23,3 в п/з до 8,6±5,7 в п/з, уровень рН мочи уменьшился с 7,9±0,2 до 6,0±0,4; во II группе лейкоцитурия – с 67,8±7,0 в п/з до 29,1±17,0 в п/з; уровень рН мочи – с 8,2±0,3 до 7,0±0,7 (р<0,05). Через 3 месяца в I группе эффективность достигнута в 18 (100%) случаях, во II группе рецидив ИЦ выявлен в 13 (86,7%) случаях. Заключение. Комплексный подход в лечении инкрустирующего цистита (эндоскопическое удаление инкрустаций/конкрементов в просвете мочевого пузыря, проведение внутрипузырных инстилляций растворов с кислым рН, проведение антибактериальной терапии по результатам посева и прием пероральных препаратов, снижающих рН мочи) позволил повысить эффективность лечения пациентов, страдающих этой нозологией.
Инкрустирующий цистит, Corynebacterium urealyticum, уреазопродуцирующие микроорганизмы, закисление мочи
Короткий адрес: https://sciup.org/142246985
IDR: 142246985 | DOI: 10.29188/2222-8543-2025-18-4-136-145
An integrated approach to the treatment of chronic encrusting cystitis
Introduction. Encrusting cystitis (IC) is a rare chronic inflammatory disease of the bladder with damage to the mucous membrane by incrustations and formation of stones. Objective: to improve the efficiency of treatment of patients with chronic incrusting cystitis. Materials and methods. A randomized, prospective, single-center study included 33 patients with IC: Group I – 18 patients who underwent surgical treatment (endoscopic removal of stones and incrustations from the bladder cavity), antibacterial therapy based on urine culture results, oral L-methionine for 1 month, and bladder instillations with a solution with an acidic pH; Group II – 15 patients who underwent the same treatment, but without bladder instillations. Results. The age of patients ranged from 39 to 78 years. In 32 (96.9%) cases, there was a history of bladder catheterization. In both groups, alkaline urine reaction, hematuria and leukocyturia were detected. Bacteriuria was detected in 24 (72.7%) patients with IC. CU was not detected in any patient. The dynamics of the general urine analysis 1 month after treatment in both groups demonstrated a reliable improvement in comparison with the preoperative data, thus: in group I, leukocyturia decreased from 88.8±23.3 in field of view to 8.6±5.7 in field of view, the urine pH level decreased from 7.9±0.2 to 6.0±0.4; in group II, leukocyturia – from 67.8±7.0 in field of view to 29.1±17.0 in field of view; urine pH level – from 8.2±0.3 to 7.0±0.7 (p<0.05). After 3 months, efficacy was achieved in 18 (100%) cases in Group I, while in Group II, recurrence of IC was detected in 13 (86.7%) cases. Conclusion. A comprehensive approach to the treatment of encrusting cystitis (endoscopic removal of encrustations/calculi in the bladder lumen, intravesical instillations of solutions with an acidic pH, antibacterial therapy based on culture results, and oral medications that lower urine pH) has improved the effectiveness of treatment for patients with this disease.
Текст научной статьи Комплексный подход в лечении хронического инкрустирующего цистита
экспериментальная и клиническая урология № 4 2025
Инкрустирующий цистит (ИЦ) – редкое хроническое воспалительное заболевание мочевого пузыря, характеризующееся поражением слизистой оболочки с появлением конкрементов и инкрустаций. Патологический процесс непосредственно обусловлен активностью микроорганизмов,вырабатывающих уреазу в моче. Главной причиной данной патологии является грамположительная бактерия Corynebacterium ure-alyticum (CU), в норме являющаяся естественным колонизатором кожи человека преимущественно в зоне промежности и паховых складок. Впервые стали говорить о том,что коринеформные микроорганизмы выявляются у больных пожилого возраста,страдающих хроническими заболеваниями органов мочевыделительной системы в середине 30 х годов ХХ века [1, 2]. В будущем идентифицировали данную бактерию как CU. У ослабленных пациентов с тяжелой сопутствующей патологией,длительно использующих антибактериальные препараты, CU может приводить к инкрустирующим пиелитам,циститам и даже выявлялись случаи бактеремии и сепсиса [3, 4]. У этой бактерии очень высокая тропность к уротелию,а урологические процедуры (катетеризация мочевого пузыря на протяжении длительного времени, трансуретральные оперативные вмешательства и др.)являются причиной колонизации бактериями мочевыводящих путей [5]. Помимо этого, в некоторых источниках имеются указания на то,что подобные виды инкрустирующей патологии мочевыводящих путей могут быть связаны с другими уреазопродуцирующими микроорганизмами: Escherichiа coli, Pseudomonas aeruginosa, Ure-aplasma urealyticum, Streptococcus (viridans, haemolyticus) Proteus, Staphylococcus, Corynebacterium glucuronolyticum и Arcanobacterium pyogenes [6–8]. Инкрустации образуются в щелочной среде (при рН свыше 7,16) за счет отложений фосфата аммония,магния и струвита на поверхности эпителия мочевыводящих путей [9].
Ранняя диагностика этого заболевания служит ключевым аспектом эффективного лечения.
В последнее время инкрустирующий цистит встречается все чаще,но диагностика этой уропатии во многих случаях несвоевременна [10]. Отмечается нарастание количества публикаций на данную тему: всего в отечественном источнике eLibrary.ru по запросу «инкрустирующий цистит» найдено 80 публи- каций за все время, причем только 19 результатов из данной подборки имели отношение непосредственно к проблемам инкрустирующей уропатии нижних мочевых путей у людей. Остальные результаты относятся к осложнениям после трансплантации почки, лучевой терапии,при «забытых урологических стентах» и при инородных телах мочевой системы, а также большое количество статей относится к области ветеринарии.
По данным поиска в международном ресурсе PubMed по запросу «encrusting cystitis» найдено всего 122 публикации; за последние 10 лет (с 2015 по 2025 год) опубликовано 32 статьи, но из них только 15 статей относились к области медицины,остальные – к ве-теринарии.Причем пик публикаций приходится на 2021 год – 4 статьи.
Был отмечен рост числа инкрустирующих уроинфекций в «эпоху» пандемии COVID-19, т.е. в период 2020-2022 гг. Во многих публикациях даже стал фигурировать термин «постковидный цистит», ковид-ассо-циированный цистит [11–16]. Указывается, что у вируса SARS-COV-2 повышенная аффинность к рецепторам ангионтензин-превращающего фермента 2 (АПФ-2 или АСЕ2) уротелия, что может способствовать развитию инкрустирующего цистита [17, 18].
Лечение ИЦ осложняется полирезистентностью CU. Это свойство определяет необходимость в подборе терапии на основании посева мочи с определением чувствительности к антибиотикам [19]. В связи с патогенезом ИЦ (рост инкрустаций и конкрементов в щелочной среде) необходимо проводить мероприятия, направленные на снижение рН мочи (подкисление с использование как пероральных препаратов, так и внутрипузырных инстилляций) [10].
В связи с этим существует необходимость комплексных подходов в лечении ИЦ с учетом этиологических и патогенетических подходов, с целью уменьшения рисков рецидива.Все вышеизложенное и определило цель исследования.
Цель исследования: повысить эффективность лечения пациентов с хроническим инкрустирующим циститом.
МАТЕРИАЛЫ И МЕТОДЫ
Рандомизированное проспективное одноцентровое исследование по сравнению способов лечения

ИЦ выполнено на клинической базе кафедры урологии с курсом хирургических болезней Рязанского государственного медицинского университета в Городской клинической больнице № 11 (г. Рязань) в период 2022-2025 гг. В исследование были включены 33 пациента, соответствовавших критериям включения: возраст старше 18 лет, подтвержденный диагноз инкрустирующий цистит,согласие пациента на участие в данном исследовании.Критерии невключения: беременность, облучение малого таза и забрюшинного пространства в анамнезе,наличие любого вида дренажей в мочевыделительной системе на момент включения в исследование,сопутствующие заболева-ния,являющиеся абсолютным противопоказанием к оперативному лечению,тяжелые сопутствующие за-болевания,онкологические заболевания в процессе лечения, ВИЧ-инфекция, трансплантация органа в анамнезе, прием иммуносупрессоров, прием лекарственных препаратов, влияющих на pH мочи, невозможность соблюдения протокола исследования, наличие в анамнезе аллергических реакций на лекарственные препараты,используемые в исследовании, выраженные когнитивные нарушения или психические заболевания, препятствующие соблюдению протокола исследования.
Добровольное информированное согласие на участие в исследование было получено от всех участников.
Пациенты были рандомизированы на 2 группы: 1) I группа (экспериментальная) – 18 пациентов, которые получали следующее лечение:
-
• оперативное лечение (эндоскопическое удаление конкрементов и инкрустаций из полости мочевого пузыря);
-
• антибактериальную терапию по результатам микробиологического исследования мочи;
-
• инстилляции мочевого пузыря стерильным раствором для снижения рН мочи (лимонная кислота 32,3 г + натрия гидрокарбонат 4,4 г + магния оксид 3,8 г в 1000 мл дистиллированной воды) с экспозицией 5 минут 7 раз (первый раз через 2 дня после операции, затем с интервалом 2 дня дважды, после 2 раза с интервалом 3 дня и затем дважды через неделю);
-
• L-метионин в дозе 500 мг внутрь каждые 12 ч 1 месяц.
-
2) II группа (контрольная) – 15 пациентов, которые получали лечение:
-
• оперативное лечение (эндоскопическое удаление конкрементов и инкрустаций из полости мочевого пузыря);
-
• антибактериальную терапию по результатам микробиологического исследования мочи;
-
• L-метионин в дозе 500 мг внутрь каждые 12 ч 1 месяц.
Всем пациентам в предоперационном периоде было проведено комплексное клиническое,лабора-торное и инструментальное обследование.Клиниче-ское обследование включало сбор жалоб и анамнеза, общий осмотр пациентов с оценкой эндокринной, нервной, сердечно-сосудистой, дыхательной, пищева-рительной,мочевыделительной и половой систем.
Инструментальное обследование включало: ультразвуковое исследование мочевыделительной системы (УЗИ), компьютерную томографию (КТ) органов забрюшинного пространства и органов малого таза без контрастного усиления, цистоскопию.
УЗИ мочевыделительной системы и мочевого пузыря было выполнено на ультразвуковом сканере Samsung HS70 (Южная Корея). Проводили абдоминальное и влагалищное сканирование с использованием датчиков микроконвексного 2-11 МГц и кон-вексного 1-7 МГц. При исследовании оценивали форму, размеры, положение мочевого пузыря, структуру и толщину его стенок,наличие образований и взвеси в его просвете. КТ органов забрюшинного пространства и органов малого таза при наполненном мочевом пузыре,без контрастного усиления с трехмерной реконструкцией и 3D-моделированием выполняли на аппарате томограф рентгеновский компьютерный Supria Hitachi 128 срезов (Япония). При КТ оценивали форму, положение, размеры мочевого пузыря, толщину стенки,наличие отека,инкрустаций и воспалительных изменений,содержимое,наличие в просвете газа, конкрементов как фиксированных, так и свободно лежащих, новообразований, анатомическое взаимоотношение органов малого таза,наличие травматических изменений, врожденных аномалий разви-тия,состояние региональных лимфоузлов и жировой клетчатки.
Цистоскопию проводили на эндоскопической стойке Karl Storz (Германия) под местной анестезией. При цистоскопии оценивались количество остаточной мочи, состояние оптической среды, слизистой мочевого пузыря и уретры (гиперемия,сосудистый рисунок, наличие язвенных дефектов; наличие инкрустаций, конкрементов, объемных образований; оценивалось положение устьев мочеточника).
Верификация возбудителей ИЦ и их выделение выполнялись в бактериологической лаборатории с использованием тест-системы Enterotest 16 (Erba Lachema, Чехия), микробиологического анализатора Labsystems iEMS Reader, программного обеспечения BACT, а также индикаторных бумажных систем для идентификации микроорганизмов, произведенных АО «НПО» «Микроген», Россия, и иммунологического латексного метода для обнаружения антигенов стрептококков групп А, В, С, D (Oxoid Ltd., Соединенное Королевство Великобритании и Северной Ирландии). Чувствительность микроорганизмов к антибиотикам оценивалась с использованием фенотипи-
ческого диско-диффузионного метода (ДДМ) и аналитического метода инактивации карбопенемов (Car-bapenem Inactivation Method, CIM) [20].
С целью выявления CU выполнялись посевы мочи на кровяной агар (с использованием донорской крови), инкубация на протяжении 72 часов.
Техника операции. Оперативное лечение проводилось на эндоскопической стойке Karl Storz (Германия) под спинномозговой анестезией или внутривенным наркозом. Во время операции трансуретрально в мочевой пузырь вводился монополярный или биполярный резектоскоп, оценивалось состояние слизистой мочевого пузыря и уретры, размеры конкрементов, наличие инкрустаций и их локализация. Производилась механическая цистолитотрипсия крупных конкрементов с помощью литотриптора Karl Storz с последующим отмыванием фрагментов с помощью шприца Reiner-Alexander. Во всех случаях конкременты были «рыхлыми» и легко поддавались дроблению. На следующем этапе проводилось удаление инкрустаций с помощью монополярных или биполярных режущих электродов путем «соскабливания» или резекции вместе с подлежащей пораженной слизистой. Резецированные участки стенки мочевого пузыря направлялись на патогистологическое исследование. Выполнялся гемостаз электрокоагуляцией. Операция завершалась установкой уретрального катетера.
Отдаленные результаты лечения были прослежены у пациентов в срок до 3 лет. Контрольное обследование пациентов,включавшее оценку жалоб,общий осмотр, лабораторное обследование (общий анализ мочи, посев мочи на флору) проводили в сроки 14 дней, 1, 3, 6 и 12 месяцев после операции, затем ежегодно. В сроки наблюдения, начиная с 3-его месяца, добавлялось инструментальное обследование (УЗИ, цистоскопия).
Под рецидивом ИЦ понимали наличие у пациента симптомов цистита,сопровождающихся лейко-цитурией и/или бактериурией, и/или гематурией, и подтвержденным инструментальными методами диагностики поражением слизистой мочевого пузыря инкрустацией и/или конкрементами.
Статистическую обработку массива данных проводили на персональном компьютере с помощью электронных таблиц «Microsoft Excel 2024» и пакета прикладных программ «Statistica for Windows» v. 10, StatSoft Inc. (США). Рассчитывали следующие показатели: среднее арифметическое (М); стандартное отклонение (СО); коэффициент вариации; асимметрию и эксцесс с оценкой их репрезентативности по t-критерию Стьюдента; коэффициент корреляции (r); степень вероятности возможной ошибки ( p ). При оценке существенности различий между средними величинами вычисляли коэффициент достоверности по критериям Стьюдента.За уровень достоверности была принята вероятность различия 95,0% ( р ≤0,05).
РЕЗУЛЬТАТЫ
В ходе исследования установлено, что возраст пациентов варьировал от 39 до 78 лет, средний возраст составил в I группе 66,0±9,0 лет, во II группе 67,8±7,0 лет ( р >0,05). В обеих группах преобладали женщины: в I группе – 88,8%, во II – 80% ( p >0,05). Основные характеристики обеих групп представлены в таблицах 1 и 2.
Анализ жалоб у пациентов с ИЦ показал,что во всех случаях пациенты предъявляли жалобы на дизурию (поллакиурию, странгурию), периодическое отхождение конкрементов и макрогематурию.Острая задержка мочеиспускания на фоне обструкции уретры камнем диагностирована у 2 (11,1%) пациентов I группы.
Оценка сопутствующей патологии не выявила достоверных различий в группах. В структуре заболеваемости преобладала гипертоническая болезнь и сахарный диабет.
Средняя продолжительность ИЦ в группах составила от 3 до 13 месяцев: в I группе 7,2±1,1 месяца, а во II группе 8,1±1,2 месяца ( р >0,05). В обеих группах отмечается связь с ранее перенесенной COVID-инфекцией: 28 (84,8%) пациентов переносили COVID-инфекцию перед началом заболевания: 17 (94,4%) пациентов в I группе; 11 (73,3%) пациентов во II группе. Анамнестически установлено, что в 32 (96,9%) случаях имелся факт катетеризации мочевого пузыря перед началом заболевания ИЦ: 17 (94,4%) пациентов в I группе, 15 (100%) пациентов во II группе. Длительность периода катетеризации колебалась от 3 до 10 дней, в среднем в I группе составила 6,8±1,2 дня; во II группе – 7,1±1,4 дня ( р >0,05). Все пациенты в обеих группах получали до госпитализации амбулаторно антибактериальную терапию, но во всех случаях в течение 10-14 дней после окончания лечения симптомы рецидивировали.
При физикальном обследовании у всех пациентов отмечалась болезненность в нижних отделах живота и над лоном.
Известно, что патогномоничными признаками ИЦ являются щелочная реакция мочи, микро- или макрогематурия, лейкоцитурия. Во всех случаях в обеих группах это утверждение было верно. В протокол исследования вносилось максимальное значение уровня лейкоцитов по данным общего анализа мочи. Лейкоцитурия выявлена во всех случаях, при этом в I группе среднее число лейкоцитов составило – 88,8±23,3 в поле зрения (п/з), во II группа – 69,1±18,2 в п/з ( р <0,05). Микро- или макрогематурия также выявлены у всех пациентов. Щелочная реакция мочи выявлена во всех исследованиях,средняя кислотность мочи составила в I группе – 7,9±0,22, во II группе – 8,2±0,28 ( р >0,05).
Таблица 1. Ключевые характеристики группы обследуемых больных основной (эксперименальной) группы (I)
Table 1. Key characteristics of the group of examined patients of the main (experimental) group (I)
|
№ |
Ф.И.О. Initials of the full name |
Пол: М/Ж Gender М/F |
Возраст Age |
рН мочи, изначально Urine pH, initially |
рН мочи, через 1 месяц Urine pH, after 1 month |
Лейкоциты в моче, и значально White blood cells in the urine, initially |
Лейкоциты в моче, через 1 месяц UWhite blood cells in the urine, after 1 month |
Посев мочи на флору, изначально Urine culture for flora, initially |
Посев мочи, через 1 месяц Urine culture, 1 month later |
Предшествующее заболевание Previous illness |
Устанавливался уретральный катетер в анамнезе: да/нет Has a urethral catheter been inserted in the past: yes/no |
|
1 |
СГВ |
Ж/F |
71 |
8 |
6,5 |
100 |
20 |
K.pneumoniae |
Нет роста/sterile |
COVID-19 |
да/yes |
|
2 |
КТВ |
Ж/F |
75 |
7,5 |
6 |
80 |
10 |
E.coli |
Нет роста/sterile |
COVID-19 |
да/yes |
|
3 |
БАА |
Ж/F |
63 |
8 |
6 |
75 |
7 |
E.coli |
Нет роста/sterile |
COVID-19 |
да/yes |
|
4 |
ФТС |
Ж/F |
65 |
8,1 |
5,5 |
100 |
5 |
K.pneumoniae |
Нет роста/sterile |
COVID-19 |
да/yes |
|
5 |
KBB |
Ж/F |
69 |
8 |
5,8 |
120 |
1 |
Нет роста sterile |
Нет роста/sterile |
COVID-19 |
да/yes |
|
6 |
ФНБ |
Ж/F |
58 |
7,5 |
6 |
90 |
5 |
K.pneumoniae |
E.coli |
COVID-19 |
да/yes |
|
7 |
ГЗВ |
Ж/F |
62 |
7,8 |
5,5 |
25 |
12 |
K.pneumoniae |
Нет роста/sterile |
COVID-19 |
да/yes |
|
8 |
НВМ |
Ж/F |
73 |
7,5 |
6 |
120 |
20 |
E.coli |
Нет роста/sterile |
COVID-19 |
да/yes |
|
9 |
ГММ |
М/М |
78 |
7,8 |
6,5 |
100 |
10 |
K.pneumoniae |
E.coli |
Простатэтомия, недержание мочи Prostatectomy, urinary incontinence |
да/yes |
|
10 |
КВФ |
М/М |
75 |
8 |
6,2 |
120 |
15 |
K.pneumoniae |
Нет роста/sterile |
Простатэтомия, недержание мочи Prostatectomy, urinary incontinence |
да/yes |
|
11 |
ЮАС |
Ж/F |
39 |
8 |
5,5 |
70 |
1 |
E.faecalis |
Нет роста/sterile |
COVID-19 |
нет/no |
|
12 |
КНМ |
Ж/F |
62 |
7,8 |
6 |
100 |
10 |
E.faecium |
Нет роста/sterile |
COVID-19 |
да/yes |
|
13 |
АРВ |
Ж/F |
70 |
8,1 |
6,2 |
80 |
7 |
E.coli |
Нет роста/sterile |
COVID-19 |
да/yes |
|
14 |
ИВК |
Ж/F |
75 |
8 |
6,5 |
70 |
10 |
E.coli |
Нет роста/sterile |
COVID-19 |
да/yes |
|
15 |
РНС |
Ж/F |
63 |
8,2 |
6 |
100 |
7 |
E.faecalis |
Нет роста/sterile |
COVID-19 |
да/yes |
|
16 |
КИИ |
Ж/F |
67 |
8 |
5,5 |
80 |
0 |
K.pneumoniae |
Нет роста/sterile |
COVID-19 |
да/yes |
|
17 |
ЛДВ |
Ж/F |
59 |
7,8 |
5,5 |
70 |
5 |
E.faecalis |
Нет роста/sterile |
COVID-19 |
да/yes |
|
18 |
ИСЮ |
Ж/F |
65 |
8,1 |
6 |
100 |
10 |
Нет роста sterile |
Нет роста/sterile |
COVID-19 |
да/yes |
Напротив, по результатам посевов мочи бакте-риурия выявлена только у 24 (72,7%) пациентов с ИЦ, при этом во всех случаях в диагностически значимом титре >104 КОЕ/мл: в I группе у 16 (88,8%) пациентов; во II группе у 8 (53,3%) пациенток ( р <0,05).
Спектральный состав микроорганизмов, выявленных при посеве мочи,был следующий:
-
• Enterococcus faecalis и faecium – 5 (15,2%) случаев: 4 (12,1%) случая – в I группе; 1 (3,1%) случай – во II группе;
-
• Escherichiа coli –8 (24,2%) случаев: 5 (15,2%) случая – в I группе; 3 (9,0%) случая – во II группе;
-
• Streptococcus agalactiae – 1 случай в I группе;
-
• Kiebsiella pneumoniaе – 8 (24,2%) пациентов (в I
группе у 6 (18,2%) пациентов; во II группе – 2 (6,1%) пациентов);
-
• Pseudomonas aeruginosa – 1 случай в I группе;
-
• Proteus mirabilis – 1 случай во II группе.
CU, несмотря на связь развития ИЦ с этим мик-роорганизмом,не была выявлена ни у одного пациента при исследовании мочи на специализированной среде – на кровяном агаре (с использованием донорской крови)в микроаэрофильных условиях.
При оценке результатов УЗИ у всех пациентов обеих групп выявлено патологическое утолщение стенки наполненного мочевого пузыря свыше 4 мм [21], гиперэхогенная слизистая мочевого пузыря за счет инкрустации, наличие гиперэхогенных фиксиро-
Таблица 2. Ключевые характеристики обследуемых больных контрольной группы (II)
Table 2. Key characteristics of the group of examined patients in the control group (II)
По данным КТ органов малого таза у всех пациентов выявлено утолщение стенки наполненного мочевого пузыря свыше 4 мм,инкрустация слизистой на различных по площади участках; наличие конкрементов в просвете мочевого пузыря,как фиксированных, так и свободно лежащих (рис. 2).
При цистоскопии у всех пациентов была выявлена гиперемия слизистой с эрозированными участками, множественные конкременты, фиксированные к стенке мочевого пузыря и свободно
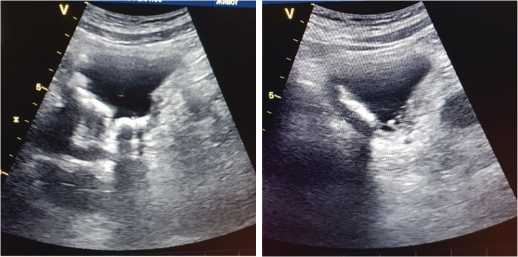
Рис. 1. Ультразвуковая картина — гиперэхогенные образования в просвете мочевого пузыря
Fig. 1. Ultrasound pattern. Hyperechoic formations in the lumen of the bladder

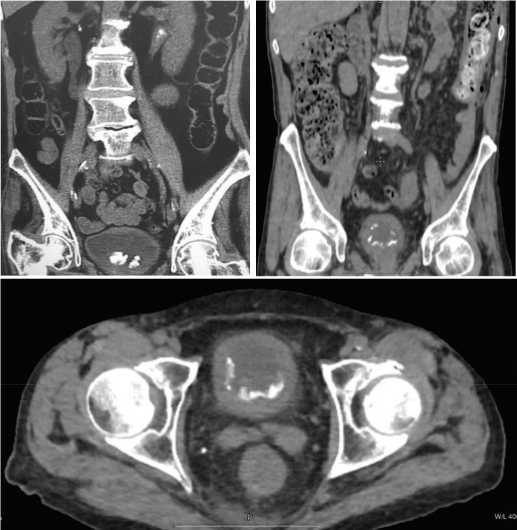
Рис. 2. Компьютерная томография. Картина конкрементов в просвете мочевого пузыря при инкрустирующем цистите
Fig. 2. Computed tomography. The picture of concretions in the lumen of the bladder with encrusting cystitis
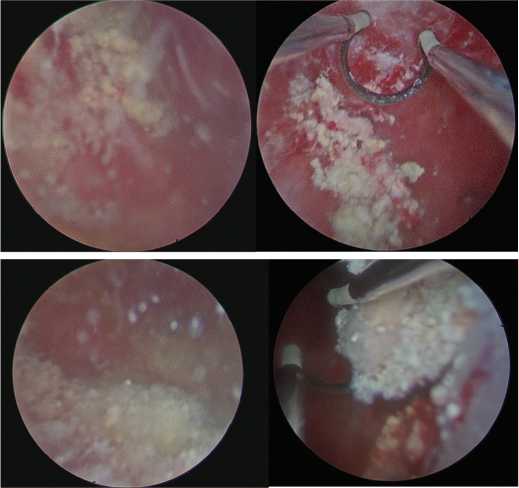
Рис. 3. Цистоскопическая картина инкрустирующего цистита Fig. 3. Cystoscopic picture of encrusting cystitis перемещающиеся в полости мочевого пузыря.При этом емкость мочевого пузыря у всех пациентов была достаточная – 200,0±46,0 мл (рис. 3, 4).
Средняя длительность оперативного вмешательства составила 50,9±15,9 и 55,7±14,7 мин в I и II группах соответственно ( p >0,05). Интра- и послеоперационных осложнений не было в обеих группах.
По результатам патогистологического исследования стенки мочевого пузыря выявлялась картина продуктивного воспаления с выраженным ангиома-тозом,слабой лимфо-и плазмоцитарной инфильтрацией по типу незрелой грануляционной ткани;
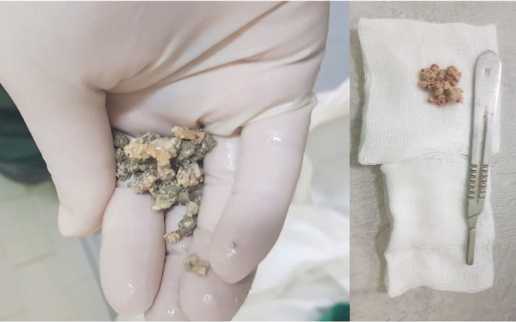
Рис. 4. Удаленные конкременты из просвета мочевого пузыря при инкрустирующем цистите
Fig. 4. Removed concretions from the lumen of the bladder in case of encrusting cystitis реактивная гиперплазия переходного эпителий с хорошо выраженной интраэпителиальной лейкоцитарной инфильтрацией,отложения кальция в слизистой В некоторых образцах выявлялся папилломатоз (2 случая, 11,1%, основной группы), в контрольной не выявлялся (рис. 5).
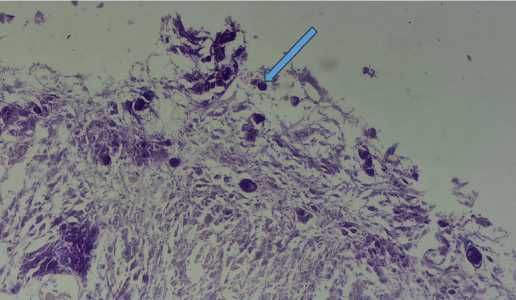
Рис. 5. Гистологическая картина при инкрустирующем цистите картина продуктивного воспаления с выраженным ангиоматозом, слабой лимфо- и плазмоцитарной инфильтрацией по типу незрелой грануляционной ткани; реактивная гиперплазия переходного эпителий с хорошо выраженной интраэпителиальной лейкоцитарной инфильтрацией. Отложения кальция в слизистой мочевого пузыря.
Fig. 5. Hystological picture in encrusting cystitis: picture of productive inflammation with pronounced angiomatosis, weak lymphocytic and plasmacytic infiltration of immature granulation tissue; reactive hyperplasia of the transitional epithelium with well-defined intraepithelial leukocyte infiltration. Calcium deposits in the bladder mucosa
Антибактериальная терапия проводилась в обеих группах по результатам микробиологического исследования мочи.
В I группе в 12 (66,6%) случаях в лабораторных исследованиях отмечалась чувствительность к аминогли-казидам, в связи с чем назначен амикацин по 1,0 г внутримышечно 1 раз в сутки 7 дней; в 1 (5,5%) случае отмечалась высокая чувствительность к цефалоспоринам 2 и 3 поколений, в связи с чем назначался цефтриаксон по 1,0 г внутримышечно 2 раза в день 7 дней; в 3 (16,6%) случаях отмечалась чувствительность к це-фоперазону/сульбактаму, который назначался внутримышечно по 1,0 г 2 раза в день 7 дней; при отсутствии бактериурии в 2 (11,1%) случаях назначался цефтриаксон по 1,0 г внутримышечно 2 раза в день 7 дней.
Во II группе по результатам посевов мочи с определением чувствительности к антимикробным препаратам в 5 случаях (33,3%) назначены аминогликозиды (амикацин по 1,0 г внутримышечно 1 раз в сутки 7 дней); в 3-х (20%) случаях отмечалась чувствительность к цефоперазону/сульбактаму, который назначался внутримышечно по 1,0 г 2 раза в день 7 дней; при отсутствии бактериурии – 7 (46,6%) пациентам назначался в цефтриаксон по 1,0 г внутримышечно 2раза в день 7 дней.
Средняя длительность госпитализации составила в I группе 8,7+3,1 дня (от 7 до 14 дней), во II группе – 9,2+4,3 дня (от 9 до 17 дней).
Динамика общего анализа мочи через 1 месяц после лечения в обеих группах продемонстрировала достоверное улучшение в сравнении с предоперационными данными,так;в I группе лейкоцитурия уменьшилась с 88,8±23,3 в п/з до 8,6±5,7 в п/з, уровень рН мочи уменьшился с 7,9±0,2 до 6,0±0,4; во II группе лей-коцитурия уменьшилась с 67,8±7,0 в п/з до 29,1±17,0 в п/з; уровень рН мочи уменьшился с 8,2±0,3 до 7,0±0,7 ( р <0,05). Межгрупповой сравнительный анализ показал статистически достоверные различия в результатах общего анализа мочи: в экспериментальной группе показатели достигли референсных значений, в контрольной сохранялась лейкоцитурия ( р <0,05).
Бактериурия через 1 месяц после лечения выявлена в I группе у 2 пациентов (11,2%) в титре не более 104 КОЕ/мл; во II группе у 3 пациентов (20,0%) в титре более 105 КОЕ/мл. Во всех этих случаях была назначена антибактериальная терапия.
Оценка ультрасонографии мочевого пузыря через 1и 3 месяца выявила,что в экспериментальной группе во всех 18 случаях в просвете мочевого пузыря конкременты не были выявлены, толщина стенки мочевого пузыря при наполнении до 200 мл была 2-3 мм, гиперэхогенные участки слизистой не выявлялись; в контрольной группе у 13 (86,7%) пациентов в просвете мочевого пузыря отмечается гиперэхогенная слизистая, инкрустации с эхо-тенью, у 2 (13,3%) пациентов были выявлены конкременты,толщина стенки мочевого пузыря при наполнении до 200 мл была до 4-6 мм.
Контрольная цистоскопия выполнена всем пациентам через 3 месяца после лечения: в экспериментальной группе у всех пациентов в просвете мочевого пузыря не было инкрустированных участков, у 2 (11,1%) пациентов определялись участки буллезного отека слизистой, в зонах резекции, также определялся или налет фибрина в 8 (44,4%) случаях, или рубцовое втяжение – в 10 (55,6%) случаях; в контрольной группе в 13 (86,7%) случаях выявлена гиперемия и отек слизистой с эрозивными участками и инкрустацией солями; мелкие конкременты в просвете мочевого пузыря, в 2-х (13,3%) случаях в просвете мочевого пу- зыря не было инкрустированных участков, в зонах резекции определялось рубцовое втяжение.
Таким образом, оценивая результаты лечения пациентов с ИЦ в течение 3 месяцев,в экспериментальной группе эффективность достигнута в 18 (100%) случаях,в отличие от контрольной группы,в которой рецидив ИЦ выявлен в 13 (86,7%) случаях.
ОБСУЖДЕНИЕ
В литературе наиболее частым этиологическим фактором развития ИЦ описывается CU [1–4]. Однако в нашем исследовании ни у одного из пациентов не выявлено данной бактерии в результатах посевов мочи.Возможно,что развитие ИЦ у пациентов,вклю-ченных в наше исследование связано с другими уреазопродуцирующими микроорганизмами, что также описано многими авторами [6–8]. Также известно, что использование неселективных сред в диагностике CU малоэффективно,так как при этом данная бактерия высевается с частотой 0,04-0,2% в популяции. При использовании специализированных сред (среда с 5 % содержанием СО 2 кровяной агар или цистеиноволак-тозно-обогащенный агар)частота высева составляет до 1,17% (в популяции) [21, 22]. При этом у пациентов, находящихся на стационарном лечении при использовании неспециализированных сред,данная бактерия высевается с частотой 1,32%, а на специализированных в 4,64% случаев [23]. Резко повышается частота положительных посевов у пациентов после трасплан-тации почки (вплоть до 10%), причем как при использовании специализированных сред,так и не специализированных [24]. В нашем исследовании, несмотря на использование специализированных сред, ни в одном из случаев не была обнаружена CU. Эти факты полностью не исключают ее участие в развитии ИЦ в исследуемых группах, даже при использовании специальных сред.
ИЦ наиболее часто поражает ослабленных пациентов или перенесших оперативные вмешательства на мочевых путях,что подтверждается и нашей работой [10]. 28 (84,8%) пациентов перенесли COVID-инфекцию, из них у 24 пациентов (72,7%) COVID-пневмония протекала тяжело,что повлекло за собой нахождение в реанимационном отделении,длительную катетеризацию мочевого пузыря.У остальных пациентов отмечалось вмешательство на мочевых путях или также длительное нахождение в палате интенсивной терапии в связи с острой сосудистой патологией.
В большом количестве исследований указывается на преобладание инкрустирующего цистита у мужчин 66-75% [4, 24]. Однако в нашем исследовании отмечается преобладание женщин 84,8% случаев.
От начала заболевания до госпитализации на стационарное лечение у всех пациентов, вошедших в исследование,прошло более 6 месяцев.По данным других авторов также указывается на длительные периоды времени от момента начала заболевания,как правило после «инструментальной интервенции» (эндоскопические вмешательства на мочевых путях), до диагностики и назначения лечения – от 5 дней до 3-х лет [25].
Необходимость комплексного подхода в лечении ИЦ нашло отражение в ряде научных публикациях [10]. Особое место в терапии ИЦ, помимо назначения антибактериальных препаратов по посеву мочи,за-нимает трансуретральное удаление конкрементов и инкрустаций, снижение уровня рН мочи (ацидифи-кация мочи),что нашло подтверждение в нашем исследовании. Подкисление мочи способствует удалению остаточных инкрустаций, при снижении рН мочи менее 5,5 растворимость струвита значительно увеличивается [26].
ЗАКЛЮЧЕНИЕ
Комплексный подход в лечении инкрустирующего цистита (эндоскопическое удаление инкруста-ций/конкрементов в просвете мочевого пузыря, проведение внутрипузырных инстилляций растворов с кислым рН,проведение антибактериальной терапии по результатам посева и прием пероральных препа-ратов,снижающих рН мочи)позволил повысить эффективность лечения пациентов, страдающих этой нозологией.


