Коррекция нарушений метаболизма суставного хряща и морфологическая оценка эффективности внутрисуставной озонотерапии при экспериментальном посттравматическом артрите
Автор: Захватов Алексей Николаевич, Беляев Александр Назарович, Кузнецов Сергей Иванович, Аткина Наталья Алексеевна
Журнал: Инженерные технологии и системы @vestnik-mrsu
Рубрика: Фундаментальная медицина
Статья в выпуске: 3, 2016 года.
Бесплатный доступ
Введение. Повреждение коленного сустава занимает одно из первых мест среди травм опорно-двигательного аппарата, составляя по разным источникам от 4,9 % до 24,0 % всех случаев травм и от 40 % до 50 % - среди повреждений суставов [1-3]. По данным Берглезова М. А. [1] и Насоновой В. А. [4], остеоартрозом крупных суставов страдает от 48 до 67,5 % трудоспособного (лица среднего и молодого возраста) населения России, причем 64-80% случаев имеет посттравматический характер. Таким образом, очевидна актуальность разработки современных методов диагностики, лечения травм коленного сустава и профилактики последующего прогрессирования посттравматического гонартроза. Цель исследования - изучить влияние внутрисуставной озонотерапии на некоторые показатели обмена коллагена и морфологические изменения тканей сустава при экспериментальном посттравматическом артрите. Материалы и методы. В ходе эксперимента на 132 белыгх нелинейных крысах было определено содержание фракций оксипролина в сыворотке крови и проведено морфологическое исследование суставного хряща, синовиальной оболочки и субхондрального слоя кости на фоне применения нимесулида, внутрисуставной озонотерапии и их комбинации. Результаты исследования. Комбинированное применение нимесулида и внутрисуставной озонотерапии при травматическом повреждении коленного сустава в большей степени способствует уменьшению альтерации коллагеновых элементов экстрацеллюлярного матрикса хряща и коррекции синтетических процессов в обмене коллагена (снижение БСО и отношения ПСО/СО), что предупреждает процессы избыточного фибриллогенеза и склерозирования тканей поврежденного сустава. При гистологическом исследовании хрящ вне зоны поражения и синовиальная оболочка существенно не отличались от хряща интактных животных. Зональность структуры хрящевой ткани вне очага повреждения четко прослеживалась. Фибрилляция поверхностной и промежуточной зоны не наблюдалась. При исследовании субхондральной кости деструкции и склероза костных балок обнаружено не было. Обсуждение и заключения. Экспериментальным путем было установлено, что сочетанное применение нимесулида и внутрисуставной озонотерапии при посттравматическом артрите препятствует развитию деструктивно-дистрофических изменений сустава, уменьшая биодеструкцию коллагеновых волокон и блокируя избыточную пролиферацию соединительной ткани, а также способствует регенерации дефекта.
Посттравматический артрит, оксипролин, коллаген, нимесулид, внутрисуставная озонотерапия
Короткий адрес: https://sciup.org/14720220
IDR: 14720220 | УДК: 616.72-002:612.014.464 | DOI: 10.15507/0236-2910.026.201603.359-369
Correction of metabolic disorders of the articular cartilage and morphological evaluation of intra-ozone therapy in experimental post-traumatic arthritis
Introduction. Currently, increased medical and social significance of the problem of traumatic injuries of the knee joint. High prevalence, social losses due to temporary disability at a substantial cost of treatment and the risk of subsequent development of post-traumatic arthrosis, arthritis due to lack of pathogenetic approach to the conservative treatment of post-traumatic disorders in the joints make it extremely urgent the development of modern methods of diagnosis and treatment of knee joint injuries and prevent further progression of posttraumatic gonarthrosis. Materials and Methods. In the experiment on 132 white non-linear rats studied the content of hydroxyproline fractions in serum and morphological investigation of the articular cartilage, synovial membrane and subchondral bone layer during treatment with nimesulide, intra-articular ozone therapy, and combinations therapy. Results. The combined use of nimesulide and intra-ozone therapy in traumatic injury of the knee to a greater extent reduces alterations of collagen components of the extracellular matrix of cartilage and correction of synthetic processes in the metabolism of collagen, which prevents the processes of excessive fibrillogenesis and sclerosis of tissues damaged joint. Histological examination of the cartilage is affected areas and synovium were not significantly different from the cartilage of intact animals. The zoning of the structure of cartilage lesion is clearly discernible. Fibrillation of the surface and the intermediate zone was observed. In the study of subchondral bone degradation and bone sclerosis beams were found. Discussion and Conclusions. It was found that the combinations therapy of nimesulide and intra-ozone therapy in post-traumatic arthritis in the experiment prevents of destructive and degenerative changes in the joint, reducing biodegradation of the collagen fibers and blocking excessive proliferation of connective tissue and so promotes regeneration of the defect.
Текст научной статьи Коррекция нарушений метаболизма суставного хряща и морфологическая оценка эффективности внутрисуставной озонотерапии при экспериментальном посттравматическом артрите
В настоящее время проблема травматических повреждений крупных суставов является актуальной, несмотря на разнообразие современных методов лечения [5–6]. Обеспокоенность данной проблемой объясняется тем, что в отдаленные сроки после травм суставов у 92 % больных имеется рентгенологическая картина деформирующего остеоартроза, приводяще- го к стойкой утрате нетрудоспособности [7–8].
В состав гиалинового хряща входят клетки – хондроциты и хондробласты, а также межклеточное вещество, которое представлено белково-поли-сахаридными комплексами и коллагеновыми волокнами [2; 9–12]. Известно, что травматическое повреждение сустава, сопровождающееся кровоизлиянием в его полость, в ранние сро- ки приводит к возникновению внутри-и внесуставных изменений и в первую очередь – развитию синовита. Хро-низация экссудативного процесса является одной из основных причин формирования вторичных пролиферативных и дегенеративно-дистрофических изменений [6; 11; 13].
Воспалительный процесс в суставе приводит к дисбалансу между катаболическими и анаболическими реакциями, протекающими в хрящевой ткани, в сторону увеличения активности распада коллагена и протеогликанов межклеточного матрикса. Их фрагменты попадают в синовиальную жидкость и усиливают воспалительную реакцию, в условиях которой наблюдается нарушение белоксин-тезирующей функции хондроцитов, в результате чего ими образуется короткоцепочечный нефибриллярный коллаген [14–15]. Оксипролин является специфической аминокислотой коллагена, поэтому может использоваться в качестве маркера его метаболизма [10; 16–19].
При развитии посттравматического артрита (ПА) наблюдается увеличение содержания оксипролина в сыворотке крови за счет его свободной (СО) и пептидосвязанной (ПСО) фракции [9; 20–21]. Синтез коллагена, напротив, характеризуется увеличением фракции белковосвязанного оксипролина (БСО). В настоящее время важную роль в патогенезе посттравматического остеоартроза отводится активации процессов перекисного окисления липидов, продукты которых усугубляют деструкцию хондроцитов и межклеточного матрикса суставного хряща [3–4; 22–23]. При этом патогенетически обоснованный подход к профилактике посттравматического остеоартроза в настоящее время отсутствует.
Учитывая механизмы развития острого асептического ПА, наиболее целесообразным в комплексном лечении является применение локаль- ной внутрисуставной озонотерапии, поскольку озон обладает широким спектром воздействия: анальгетическим, противовоспалительным, иммуномодулирующим; улучшает микроциркуляцию, оптимизирует про- и антиоксидантные системы, потенцируя действие других лекарственных препаратов [5; 16].
Цель исследования – изучить влияние внутрисуставной озонотера-пии на некоторые показатели обмена коллагена и морфологические изменения тканей сустава при экспериментальном ПА.
Материалы и методы
Эксперименты были проведены на 132 белых нелинейных крысах обоего пола массой 180–200 г., содержавшихся в стандартных условиях вивария ФГБОУ ВО «МГУ им. Н. П. Огарёва». Протокол экспериментов был составлен в соответствии с Конвенцией по защите животных, используемых в эксперименте и других научных целях (принятой Советом Европы в 1986 г.), с приказом МЗ РФ № 267 от 19.06.2003 «Об утверждении правил лабораторной практики»; он соответствует требованиям Хельсинкской декларации о гуманном отношении к животным (2000 г.), одобрен локальным этическим комитетом ФГБОУ ВО «МГУ им. Н. П. Огарёва».
Животные были разделены на 5 групп. Первую серию составили интактные животные в количестве 12 крыс. В контрольной (30 животных) и опытных группах под ингаляционным наркозом моделировали повреждение коленного сустава механическим путем в модификации Г. М. Дубровина [2]. Во II контрольной группе лечение не проводилось. Животным III группы (30 крыс), начиная со дня моделирования травмы, проводился курс лечения нимесулидом через зонд в среднетерапевтической дозе 2 мг/кг ежедневно в течение 10 дней. В IV группе (30 животных) проводилось внутрисуставное введение озоно-кислородной смеси в концентрации озона на выходе из аппарата 15 мг/л через день в количестве 5 сеансов. На животных V группы (30 крыс) изучалось комбинированное влияние нимули-да в дозе 2 мг/кг и внутрисуставного введения озоно-кислородной смеси в концентации 15 мг/л по указанной выше схеме введения. Для исследования от животных получали периферическую кровь и поврежденные коленные (скакательные) суставы конечностей.
Оценку метаболизма коллагена проводили по содержанию СО, ПСО и БСО в сыворотке крови по методу П. Н. Шараева [24] (на данную методику оценки интенсивности деструктивных процессов в суставе нами был получен патент № 2463000 от 10.10.2012 г.). Гистологическим методом изучали морфологию суставного хряща, синовиальной оболочки и субхондрального слоя костной ткани. Серийные срезы окрашивались гематоксилином и эозином. Исследование было проведено с использованием светового биологического микроскопа «Humascope Advanced Led» (Германия).
Животных выводили из эксперимента на 28-е сутки. Статистическая обработка результатов исследований была проведена с помощью t-критерия Стьюдента. Изменения считали достоверными при р < 0,05 (0,01; 0,001).
Результаты исследования
При исследовании сыворотки крови животных контрольной группы после моделирования травмы коленного сустава относительно интактной серии выявлено увеличение содержания
СО и БСО на 188,9 % и на 135,1 % соответственно; содержание ПСО выросло в 2,76 раза; коэффициент ПСО/ СО повышался и составил 1,38 ± 0,15 усл. ед. (p < 0,001).
На фоне внутрижелудочной нестероидной противовоспалительной терапии нимесулидом содержание СО в сыворотке крови было снижено на 20,5 %; ПСО – на 47,8 %; БСО – на 26,8 % по сравнению с соответствующими показателями в контрольной группы (p1 < 0,001). Коэффициент ПСО/СО был равен 0,91 ± 0,09 усл. ед.
При внутрисуставном введении газообразной озоно-кислородной смеси относительно данных контрольной серии наблюдалось снижение фракций оксипролина: уровень СО – на 25,0; концентрация ПСО – на 59,0%; БСО – на 39,4 % (p1 < 0,001). Коэффициент ПСО/СО составил 0,76 ± 0,05 усл. ед.
При комбинированном применении нестероидной противовоспалительной терапии нимесулидом и внутрисуставной озонотерапии фракции оксипролина в сыворотке крови по сравнению с данными контрольной серии изменились следующим образом: СО снизился на 35,1%; ПСО – на 66,4 %; БСО – на 47,8 %; коэффициент ПСО/СО – на 47,8 % (p1 < 0,001) (таблица).
При макроскопической оценке гиалиновый хрящ коленного сустава интактных животных имел беловаторозовую окраску, гладкую, блестящую поверхность и упругую структуру. Микроскопически гиалиновый хрящ эпифиза бедренной кости крысы имел сходство с человеческим, в нем выделялись 3 зоны: поверхностная, средняя (промежуточная) и глубокая.
Т а б л и ц а
T a b l e
Динамика некоторых показателей обмена коллагена при экспериментальном посттравматическом артрите на фоне комбинированного применения нимесулида и озона, 28-е сутки (M ± m)
Dynamics of some indicators of collagen metabolism in experimental post-traumatic arthritis by combination of nimesulide and ozone, 28 day (M ± m)
|
Показатель / Index |
Интактные животные (n = 12) / Intact animals (n = 12) |
Контрольная группа (n = 30) / Control group (n = 30) |
НПВС (n = 30) / NSAID (n = 30) |
В/с озон (n = 30) / Ozone (n = 30) |
НПВС + в/с озон (n = 30) / NSAID + ozone (n = 30) |
|
СО, мкмоль/л / FO, mmole/l |
13,74 ± 0,51 |
28,31 ± 0,94 (p < 0,001) |
22,51 ± 0,52 (p < 0,001; p1< 0,001) |
21,23 ± 0,45 (p < 0,001; p1< 0,001) |
21,23 ± 0,45 (p < 0,001; p1< 0,001) |
|
ПСО, мкмоль/л / PBO, mmole/l |
7,42 ± 0,42 |
39,36 ± 1,43 (p < 0,001) |
20,53 ± 1,07 (p < 0,001; p1< 0,001) |
16,13 ± 1,22 (p < 0,001; p1< 0,01) |
16,13 ± 1,22 (p < 0,001; p1< 0,01) |
|
БСО, мкмоль/л / PBH, mmole/l |
51,26 ± 0,89 |
123,93 ± 1,89 (p < 0,001) |
91,76 ± 1,20 (p < 0,001; p1< 0,001) |
75,19 ± 1,13 (p < 0,001; p1< 0,001) |
75,19 ± 1,13 (p < 0,001; p1< 0,001) |
|
ПСО/СО, усл. ед. / PBO/FO, mmole/l |
0,54 ± 0,02 |
1,38 ± 0,15 (p < 0,001) |
0,91 ± 0,09 (p < 0,01; p < 0,05) |
0,76 ± 0,05 (p < 0,001; p < 0,001) |
0,76 ± 0,05 (p < 0,001; p < 0,001) |
Примечания: p – достоверность отличий к данным интактных животных; р1 – достоверность отличий к данным контрольной группы / Note: p – reliatibility of differences in the data intact animals; р1 – significance of differences in the control group
При визуальной оценке у крыс контрольной серии в области коленного сустава наблюдался отек, стойкая сгибательная контрактура; при передвижении животные хромали и щадили травмированную конечность. Макроскопическое исследование суставной поверхности бедренной кости выявило в области медиального мыщелка дефект в виде углубления с нечеткими границами. Поверхность хряща имела желтовато-белую окраску без характерного блеска.
При световой микроскопии определялось нарушение цитоархитектоники хрящевой ткани, распространяющееся далеко от экспериментально нанесенной травмы. Отмечалось разволокнение поверхностной зоны и образо- вание узур, уменьшение количества клеточных элементов в лакунах и их дегенеративные изменения. В субхондральной кости обнаруживались признаки остеосклероза. Толщина суставного хряща была значительно ниже, чем у интактных животных, с одновременным сокращением численной плотности функционально активных хондроцитов, что способствовало дезорганизации коллагеновых фибрилл и формированию фиброзного хряща (рис. 1).
Деструктивно-дистрофические изменения обнаруживались также в синовиальной оболочке: атрофия и фиброз стромы, склероз сосудов микроцирку-ляторного русла и очаговая инфильтрация лейкоцитами.
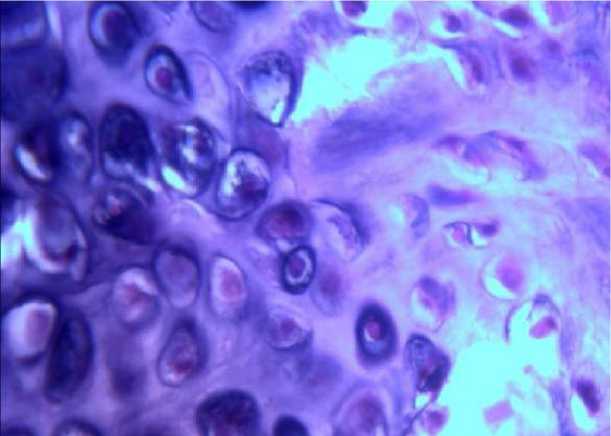
Р и с. 1. Гистологический препарат. Суставной хрящ коленного сустава крысы. Группа контрольная. (Посттравматический артрит). Увеличение 10х40. Окраска гематоксилином и эозином.
F i g 1. Histological preparation. Articular cartilage of rat knee joint. Group control. (Post-traumatic arthritis). Increased 10x40. Hematoxylin and eosin stain.
Суставы животных, получавших нимесулид, внешне были в удовлетворительном состоянии. Макроскопическое исследование выявило, что хрящ был тусклым, имел желтоватую окраску с участком организации в области травматического повреждения. При световой микроскопии были определены уменьшение количества хондроцитов поверхностной зоны, а также деструктивные изменения части клеточных элементов, деструкция межклеточного матрикса с образованием узур.
Аналогичные изменения наблюдались также в более глубоких слоях хрящевой ткани вплоть до субхондральной кости, где определялись признаки остеосклероза. Нарушение цитоархитектоники распространялось за пределы экспериментальной травмы. С морфологической точки зрения, в синовиальной оболочке была обнаружена картина хронического посттравматического синовита – фиброз, умеренная лимфоцитарная инфильтрация стромы и реактивные изменения синовиальных клеток.
У животных, получавших озон внутрисуставным способом введения, внешний вид сустава мало отличался от здорового. Макроскопически суставной хрящ имел свойственные ему цвет и блеск, область дефекта была покрыта соединительнотканным регенератом. Деструктивные изменения хряща ограничивались незначительным числом трещин поверхностной зоны в смежных с дефектом областях. Склеротические изменения субхондральной кости затрагивали отдельные трабекулы в зоне повреждения. Морфологическая структура синовиальной оболочки характеризовалась незначительной степенью воспаления в виде периваскулярной лейкоцитарной инфильтрации.
Наиболее выраженная регрессия морфологических изменений по сравнению с контрольными данными наблюдалась при комбинации перорального применения нимесулида и внутри- суставного введения озона. Отека в области коленного сустава не наблюдалось. Макроскопически участок хряща, соответствующий экспериментальной травме, отличался от другой локализации небольшим углублением и отсутствием типичного блеска. При гистологическом исследовании было выявлено, что сам дефект заполнен зрелой соединительной тканью, в которой определялось большое количество хондроцитов. Зональность структуры хрящевой ткани вне очага повреждения четко прослеживалась. Фибрилляции поверхностной и промежуточной зоны не наблюдалось. При исследовании субхондральной кости деструкции и склероза костных балок обнаружено не было (рис. 4). В синовиальной оболочке при морфологическом изучении редкой находкой были периваскулярные инфильтраты.
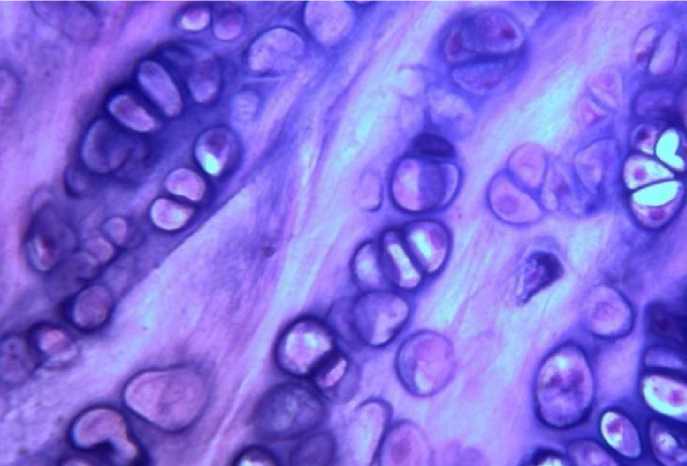
Р и с. 2. Гистологический препарат. Суставной хрящ коленного сустава крысы (Посттравматический артрит). Группа с комбинированным применением нимесулида и внутрисуставным введением озона. Увеличение 10х40. Окраска гематоксилином и эозином.
F i g 2. Histological preparation. Articular cartilage of rat knee joint (Post-traumatic arthritis). Group with the combined use of nimesulide and intra-articular injection of ozone. Increased 10x40. Hematoxylin and eosin stain.
Обсуждение и заключения
Моделирование ПА коленного сустава приводит к дисбалансу метаболизма коллагена, характеризующегося значительным ростом всех фракций оксипролина, свидетельствующем о деструктивных процессах коллагена с одновременной высокой активностью неполноценного фибриллогенеза, приводящего к избыточному накоплению соединительной ткани с развитием склерозирования хряща и субхондральной кости.
Нестероидная противовоспалительная терапия, уменьшая воспаление, препятствовала деградации биополимеров соединительной ткани сустава, однако не ограничивала избыточные процессы фибриллогенеза, о чем свидетельствует высокий уровень БСО сыворотки на поздних стадиях экспериментального ПА.
Комбинированное применение ни-месулида и внутрисуставной озонотера-пии при травматическом повреждении коленного сустава в большей степени способствует уменьшению альтерации коллагеновых элементов экстрацеллюлярного матрикса хряща и коррекции синтетических процессов в обмене коллагена (снижение БСО и ПСО/СО), в отличие от лечения нимесулидом и внутрисуставного введения озоно-кислородной смеси в качестве монотерапии.
Данный эффект обусловлен воздействием препаратов на различные звенья патогенеза ПА: с одной стороны, нимесулид подавляет хемотаксис нейтрофилов и макрофагов в очаг воспаления, снижая синтез простагландинов и провоспалительных цитокинов. С другой, озон устраняет тканевую гипоксию, оказывает иммуномодулирующий, противовоспалительный эффект, модифицирующее действие на структурно-функциональное состояние клеточных мембран, усиливая метаболические процессы в клетках. Это пре- дупреждает избыточный фибриллогенез и склерозирование тканей сустава.
Выявленные данные обосновывают комбинированное применение нестероидной противовоспалительной терапии и внутрисуставной озоноте-рапии, позволяющее в ранние сроки купировать воспалительный процесс в пораженном суставе, стимулировать заживление травматического дефекта и уменьшить развитие дегенеративнодистрофических процессов.
Полученные результаты обусловливают необходимость дальнейшего проведения углубленных доклинических исследований и планирования клинических испытаний эффективности комбинированного применения нимесулида и внутрисуставной озо-нотерапии у больных с травматическими повреждениями коленного сустава с целью предупреждения прогрессирования ПА.
Список литературы Коррекция нарушений метаболизма суставного хряща и морфологическая оценка эффективности внутрисуставной озонотерапии при экспериментальном посттравматическом артрите
- Берглезов М. А., Андреева Т. М. Остеоартроз: этиология, патогенез. Вестник травматологии и ортопедии им. Н. Н. Приорова. 2006. № 4. С. 79-86.
- Обоснование применения миелопида для профилактики посттравматического остеоартроза (экспериментальное исследование)/Г. М. Дубровин //Вестник травматологии и ортопедии им. Н. Н. Приорова. 2005. № 2. С. 60-62.
- Шостак Н. А. Остеоартроз: актуальные вопросы диагностики и лечения. Русский медицинский журнал. 2014. № 4. С. 278-281. URL: http://www.rmj.ru/articles/aktualnaya_problema/Osteoartroz%3A_aktualynye_voprosy_diagnostiki_i_lecheniya.
- Насонова В. А. Остеоартроз коленного сустава: причины развития, диагностика и профилактика. Consilium medicum. 2003. №2. С. 90-96. URL: http://old.consilium-medicum.com/media/consilium/03_02/90.shtml.
- Бархоткина Т. М., Томашевский Е С. Метод оценки эффективности озонотерапии. Медицинский альманах. 2013. № 3. С. 31-32. URL: http://cyberleninka.ru/article/n/metod-otsenki-elfektivnosti-ozonoterapii.
- Бурьянов А. А. Структурно-функциональные изменения костной ткани при неспецифических воспалительных поражениях суставов. Боль: суставы: позвоночник. 2013. № 1. С. 87-88. URL: http://www.mif-ua.com/archive/article/35770.
- Гришина Е. И., Бабинец О. М., Шулика С. А. Провоспалительные цитокины у больных остеоартрозом с метаболическим синдромом. Травма. 2011. Т. 12, № 4. C. 113-117. URL: http://www. mif-ua.com/archive/article/25645.
- Changes in serum and synovial fluid biomarkers after acute injury (NCT00332254)/J. B. Catterall //Arthritis Research & Therapy. 2010. Vol. 12, No. 6. P. 229.
- Зупанец И. А., Тюляков В. А., Шебеко С. К. Влияние комбинации глюкозамина гидрохлорида с парацетамолом на апоптоз хондроцитов в условиях развития системного стероидного артроза у крыс. Экспериментальная и клиническая фармакология. 2012. Т. 75, № 4. С. 34-37.
- Корочина К. В., Полякова В. С., Корочина И. Э. Реорганизация структур коленных суставов крыс с хронической сердечной недостаточностью. Фундаментальные исследования. 2014.
- Фундаментальная медицина № 10. С. 1335-1340. URL: http://cyberleninka.ru/article/n/reorganizatsiya-struktur-kolennyh-sustavov-krys-s-hronicheskoy-serdechnoy-nedostatochnostyu.
- Содержание АТФ и 2,3-ДФГ в эритроцитах при консервации и воздействии озона/B. Н. Крылов //Биомедицина. 2014. № 2. C. 37-12. URL: http://cyberleninka.ru/article/n/soderzhanie-atf-i-2-3-dfg-v-eritrotsitah-pri-konservatsii-i-vozdeystvii-ozona.
- Лечение локального глубокого дефекта хряща коленного сустава, сочетающегося с медиальным гонартрозом I стадии и варусной деформацией нижней конечности/Т. А. Куляба //Травматология и ортопедия России. 2011. № 1. С. 92-95.
- Биохимические изменения в синовиальной жидкости больных с остеоартрозом коленного сустава различной этиологии/Е. Л. Матвеева //Бюллетень ВСНЦ СО РАМН. 2013. № 5. С. 60-63.
- Роль интерлейкина-1В и интерлейкина-4В в патогенезе деформирующего артроза голеностопного сустава в разные сроки катамнестического периода наблюдения/А. О. Момбеков //Фундаментальные исследования. 2013. № 9. С. 1073-1076.
- Новочадов В. В., Гайфуллин Н. М., Фролов Д. М. Ремоделирование суставного хряща в условиях эндогенной интоксикации. Фундаментальные исследования. 2012. № 10-2. С. 271-275.
- Перетягин П. В., Мартусевич А. К., Перетягин С. П. Экспериментальная оценка состояния микроциркуляции при системном введении озонированного физиологического раствора. Биорадикалы и антиоксиданты. 2015. Т. 2, № 1. С. 54-61. URL: http://cyberleninka.ru/article/n/eksperimentalnaya-otsenka-sostoyaniya-mikrotsirkulyatsii-pri-sistemnom-vvedenii-ozonirovannogo-fiziologicheskogo-rastvora.
- Самойлов В. В., Мироманов А. М., Самойлова С. И. Значение цитокинов в патогенезе остеоартроза. Забайкальский медицинский вестник. 2014. № 2. С. 119-125.
- Ударцев Е. Ю. Морфогистохимические аспекты консервативного лечения больных с посттравматическим остеоартрозом крупных суставов нижних конечностей. Фундаментальные исследования. 2011. № 6. С. 182-187.
- Федоров В. Г. Структурная единица «синовиальный сустав» и основные принципы лечения остеоартроза и других дегенеративных заболеваний синовиального сустава. Успехи современного естествознания. 2015. № 1. С. 594-600. URL: http://www.natural-sciences.ru/ru/article/view?id=34862.
- Elvis A. M., Ekta J. S. Ozone therapy: a clinical review. Journal of Natural Science, Biology and Medicine. 2011. Vol. 2, No. 1. P. 66-70.
- Human knee synovial fluid cytokines correlated with grade of knee osteoarthritis -a pilot study/C. T. Vangsness //Bulletin of the NYU Hospital for Joint Diseases. 2011. Vol. 69, No. 2. P. 122-127.
- К вопросу моделирования остеоартроза коленного сустава у собак для изучения патогенеза (экспериментально-морфологическое исследование)/В. И. Шевцов //Гений ортопедии. 2012. № 1. С. 38-42.
- Oxidative stress in secondary osteoarthritis: from cartilage destruction to clinical presentation/C. Ziskoven //Orthopedic Reviews. 2010. Vol. 2, No. 2. P. 95-101.
- Шараев П. Н. Методы исследования обмена коллагена в клинике//Актуальные проблемы теоретической и прикладной биохимии: мат-лы науч. конф. Ижевск, 2001. С. 150-153.


