Квантово-химическое изучение молекулярной структуры микотоксинов зерна пшеницы
Автор: Потороко И.Ю., Малинин А.В., Руськина А.А.
Рубрика: Биохимический и пищевой инжиниринг
Статья в выпуске: 2 т.13, 2025 года.
Бесплатный доступ
В настоящее время на фоне глобального изменения климата все более наблюдается активная динамика распространения на зерновых культурах токсинообразующих грибов и роста их вторичных метаболитов. На масштабы загрязнения оказывают влияние температура и влажность, что определяет активность опасных микромицетов сельсхозяйственных культур, что проявляется при нарушении условий хранении урожая. Микотоксины создают серьёзные риски для зерновых культур, так как являются продуктами жизнедеятельности плесневых грибов и могут загрязнять зерно. Содержание микотоксинов в сельскохозяйственном пищевом сырье, продуктах питания и кормах строго регламентируется. Микотоксины оказывают негативное воздействие на организм человека и животных. В связи с представленной выше проблемой являются актуальным поиск и разработка инновационных методов обеззараживания и более детального изучения микотоксинов на квантово-химическом уровне. Цель данного исследования была направлена на изучение геометрических параметров, стабильности, реактивности молекул микотоксинов (Афлатоксина B1, Дезоксиниваленола (ДОН), Зеараленона, Т-2 токсина), определяющих риски снижения качества и безопасности зерна пшеницы, полученного в экстремальных погодных условиях. В рамках исследования микотоксинов учитывались такие показатели, как общая энергия (Total energy), энергия молекулярных орбиталей HOMO и LUMO, размер энергетического зазора HOMO-LUMO (Homo-LUMO gap), энергия отталкивания электронов (Repulsion energy), вибрационные частоты ИК-спектров, карты электростатического потенциала. В ходе квантово-химических вычислений был сформирован массив данных, который будет полезен для дальнейшего изучения взаимодействия микотоксинов с белками зерна пшеницы. Таким образом, квантово-химические методы открывают новые возможности для исследования микотоксинов и их свойств благодаря применению принципов квантовой механики.
Микотоксины, квантово-химические расчеты, метод gfn2-xtb, молекулярные орбитали, карты электростатического потенциала
Короткий адрес: https://sciup.org/147250724
IDR: 147250724 | УДК: 658.788.462+547.458.1 | DOI: 10.14529/food250210
Quantum-chemical study of the molecular structure of wheat grain mycotoxins
Currently, against the background of global climate change, there is an increasingly active dynamics of the spread of toxin-forming fungi on grain crops and the growth of their secondary metabolites. The scale of pollution is affected by temperature and humidity, which determines the activity of dangerous micromycetes of agricultural crops, which manifests itself when the storage conditions of the crop are violated. Mycotoxins create serious risks for grain crops, as they are the products of the vital activity of mold fungi and can contaminate grain. The content of mycotoxins in agricultural food raw materials, food products and feed is strictly regulated. Mycotoxins have a negative impact on the body of humans and animals. In connection with the problem presented above, the search for and development of innovative methods of disinfection and a more detailed study of mycotoxins at the quantum-chemical level is relevant. The aim of this study was to investigate the geometric parameters, stability, and reactivity of mycotoxin molecules (Aflatoxin B1, Deoxynivalenol (DON), Zearalenone, T-2 toxin) that determine the risks of reducing the quality and safety of wheat grain obtained in extreme weather conditions. The mycotoxin study took into account such indicators as total energy, the energy of HOMO and LUMO molecular orbitals, Homo-LUMO gap, electron repulsion energy, vibration frequencies of IR spectra, and electrostatic potential maps. Quantum-chemical calculations generated a data array that will be useful for further studying the interaction of mycotoxins with wheat grain proteins. Thus, quantum-chemical methods open up new opportunities for studying mycotoxins and their properties through the use of quantum mechanics principles.
Текст научной статьи Квантово-химическое изучение молекулярной структуры микотоксинов зерна пшеницы
Агропромышленный комплекс Уральского федерального округа (АПК УрФО) является важным социально-экономический сектором, который обеспечивает лидерские позиции в части устойчивого развития сельских территорий. В настоящее время на фоне глобального изменения климата все более наблюдается активная динамика распространения на зерновых культурах токсинообразующих грибов и роста их вторичных метаболитов. На масштабы загрязнения оказывают влияние температура и влажность, что определяет активность опасных микромицетов сельскохозяйственных культур, что проявля- ется при нарушении условий хранения урожая. Представленная выше ситуация большей частью применительно к зерновому сырью требует глубокого изучения с целью готовности производителей сырья к сохранению объемов полученного урожая на всех этапах товародвижения в цепочке от поля до конечного потребителя [3].
Стоит отметить, что плесневые грибы родов Aspergillus, Penicillium и Fusarium продуцируют микотоксины. Например, Афлатоксин B1 продуцируется некоторыми видами микроскопических плесневых грибов (микроми-цетов) рода Аспергилл (Aspergillus flavus, Aspergillus parasiticus). Микотоксины, такие как дезоксиниваленол (ДОН), зеараленон, Т-2 токсин продуцируются некоторыми видами микроскопических плесневых грибов Fusarium [4, 5, 7]. Важно понимать, что основная проблема обеспечения безопасности продуктов переработки зерна связана с негативным воздействием даже низких концентраций различных микотоксинов, как индивидуально, так и при их совместном присутствии в продукции. Микотоксины имеют накопительный эффект в организме человека, попадая по пищевой цепи даже при минимальном содержании, через десятилетия могут провоцировать тяжелые заболевания, в том числе онкологические.
Особую опасность представляют маскированные и модифицированные микотоксины. Маскированные микотоксины являются продуктами биохимических реакций, в которых микотоксины связываются с гликозидами, глюкуронидами, сложными эфирами жирных кислот и белками. Реакции происходят в организме растения-хозяина для снижения токсичности микотоксинов. Благодаря таким модификациям маскированные микотоксины не обнаруживаются с помощью обычных методов. В организме человека и животных маскированные микотоксины расщепляются с высвобождением микотоксинов. Проблема поиска новых эффективных и в то же время экологически безопасных способов снижения загрязненности сельскохозяйственной продукции токсигенными плесенями и продуктами их метаболизма остается чрезвычайно актуальной. В связи с этим возникает необходимость разработки инновационных методов обеззараживания зерновых масс, но обоснование возможности трансформации токсиген-ных микромицетов и продуцируемых микотоксинов требует детализированного изучения на молекулярном уровне. Квантовохимические методы позволяют на основе законов квантовой механики изучить объект (молекулу, систему), а также поведение электронов и ядер внутри атомов и молекул, определять электронную структуру, прогнозировать свойства и моделировать химические реакции. В квантовой химии существует множество методов, которые можно разделить на несколько групп (неэмпирические, полуэмпи-рические, методы теории функционала плотности (DFT), гибридные методы) [1, 2].
Целью исследования является изучение геометрических параметров, стабильности, реактивности молекул микотоксинов, определяющих риски для качества и безопасности зерна пшеницы.
Объекты и методы исследования
В качестве объектов исследований определены вторичные метаболиты токсигенных микромицетов - Афлатоксин B1, Дезоксиниваленол (ДОН), Зеараленон (ЗЕН) и Т-2 токсин, нормируемые в зерне пшеницы и продуктах переработки.
Для изучения геометрических параметров, стабильности, реактивности молекул проводились квантово-химический расчеты с использованием полуэмпирических методов теории функционала плотности, в программном обеспечении xTB версия 6.7.1 (метода плотного связывания). Исходные данные о микотоксинах для квантово-химических расчетов были получены при помощи базы данных PubChem. На первом этапе была проведена оптимизации геометрии с последующим расчетом молекулярной энергии молекул микотоксинов.
В рамках программного обеспечения xTB был выбран полуэмпирический метод жёсткой связи GFN2-xTB, предназначенный для быстрого расчёта энергии молекулярных систем, включающих десятки или сотни атомов [10]. В рамках исследования микотоксинов учитывались такие показатели, как общая энергия ( Total energy ), энергия молекулярных орбиталей HOMO и LUMO, размер энергетического зазора HOMO-LUMO ( Homo-LUMO gap), энергия отталкивания электронов (Repulsion energy), вибрационные частоты ИК-спектров, карты электростатического потенциала .
Далее проводилась статистическая обработка полученных данных квантовохимических расчётов молекул, включающая методы анализа результатов вычислений для выявления закономерностей и прогнозирования свойств объектов исследования.
Результаты и их обсуждение
На первом этапе исследования после оптимизации геометрии, которая позволяет найти наиболее стабильную структуру, которая имеет наименьшую энергию, осуществлялся расчет молекулярной энергии молекул микотоксинов (афлатоксин B1, дезоксиниваленол (ДОН), зеараленон, Т-2 токсин). Результаты квантово-химических расчетов микотоксинов с использованием метода GFN2-xTB представлены в табл. 1.
Таблица 1
Результаты квантово-химических расчетов микотоксинов с использованием метода GFN2-xTB
|
Расчетный параметр |
Исследуемые микотоксины |
|||
|
афлатоксин В1 |
ДОН |
зеараленон |
T-2 токсин |
|
|
Total energy, Eh |
–66,91 |
–66,64 |
–70,04 |
–95,94 |
|
Energy (HOMO), eV |
–10,5590 |
–10,2796 |
–10,2924 |
–10,7203 |
|
Energy (LUMO), eV |
–8,4061 |
–7,3719 |
–7,3905 |
–6,3588 |
|
HOMO-LUMO gap, eV |
2,1529 |
2,9076 |
2,9018 |
4,361 |
|
Repulsion energy, Eh |
0,789 |
0,673 |
0,899 |
1,022 |
Представленные результаты показывают, что наибольшая общая энергия ( Total energy ) наблюдается у Т-2 токсина и составляет – 95,94 Eh (является наиболее стабильной молекулой по сравнению с представленными выше микотоксиноми). В то время как наименьшая общая энергия была выявлена у де-зоксиниваленола и составляла –66,64 Eh (что демонстрирует более низкую стабильность молекулы).
Стоит отметить, что под HOMO-LUMO gap понимается разница в энергии между высшей занятой молекулярной орбиталью (HOMO) и нижней незанятой молекулярной орбиталью (LUMO) в молекуле.
Наибольшее значение HOMO-LUMO gap наблюдается у Т-2 токсина и составляет 4,361 eV (ед. измерения электронвольты). Таким образом, Т-2 токсин обладает более высокой кинетической стабильностью молекулы и низкой химической реактивностью, так как для возбуждения электрона с HOMO на LUMO требуется больше энергии. В то время как афлатоксин B1 обладает наименьшим значением HOMO-LUMO gap, которое составляет 2,1529 eV (ед. измерения электронвольты). Меньший HOMO-LUMO gap часто коррелирует с повышенной реактивностью, так как для возбуждения требуется меньше энергии. Некоторая локализация молекулярных орбиталей HOMO и LUMO микотоксинов представлена в табл. 2. Представленные данные позволяют фиксировать связывающие, несвязывающие и разрыхляющие молекулярные орбитали.
Наибольшее значение энергии отталкивания (Repulsion energy) определено для Т-2 токсина и составляет 1.022 Eh (Энергия Хар- три). Последовательность, выстроенная по значению показателя, Eh: Т-2 (1,022) > зеара-ленон (0,899) ˃ афлотоксин В1 (0, 789) ˃ ДОН (0,673).
В то же время значение Total energy, Eh определяет аналогичную последовательность: Т-2 (–95,94) > зеараленон (–70,4) ˃ афлоток-син В1 (–66,91) ˃ ДОН (–66,64).
Наибольшее значение Homo-LUMO gap (см. табл. 2) рассчитана для Т-2 ‒ 4.361 eV (ед. измерения электронвольты). Следовательно, Т-2 в составе углеводно-белкового комплекса зерна обладает высокой кинетической стабильностью молекул и низкой химической реактивностью, так как для возбуждения электрона с HOMO на LUMO требуется больше энергии. Таким образом, данный показатель позволяет понять, как энергия отталкивания влияет на стабильность молекул. Чем ближе атомы и чем больше электронов у них, тем выше будет энергия отталкивания [6].
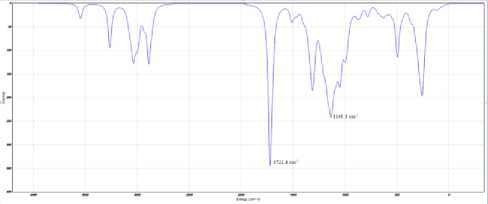
На втором этапе исследования рассчитывались и оценивались теоретически вибрационные частоты ИК-спектров для изучения свойств молекул. Стоит отметить, что вибрационные частоты ИК-спектров важны для изучения стабильности и реакционной способности веществ. Вибрационные частоты ИК-спектров – это частоты, при которых происходит поглощение инфракрасного излучения молекулами вещества в силу колебательных движений атомов и связей. Каждый пик или полоса соответствует определённому типу молекулярных колебаний. Исследуемые теоретически вибрационные частоты ИК-спектров микотоксинов представлены на рисунке.
Таблица 2
Некоторая локализация молекулярных орбиталей HOMO и LUMO микотоксинов с использованием метода GFN2-xTB
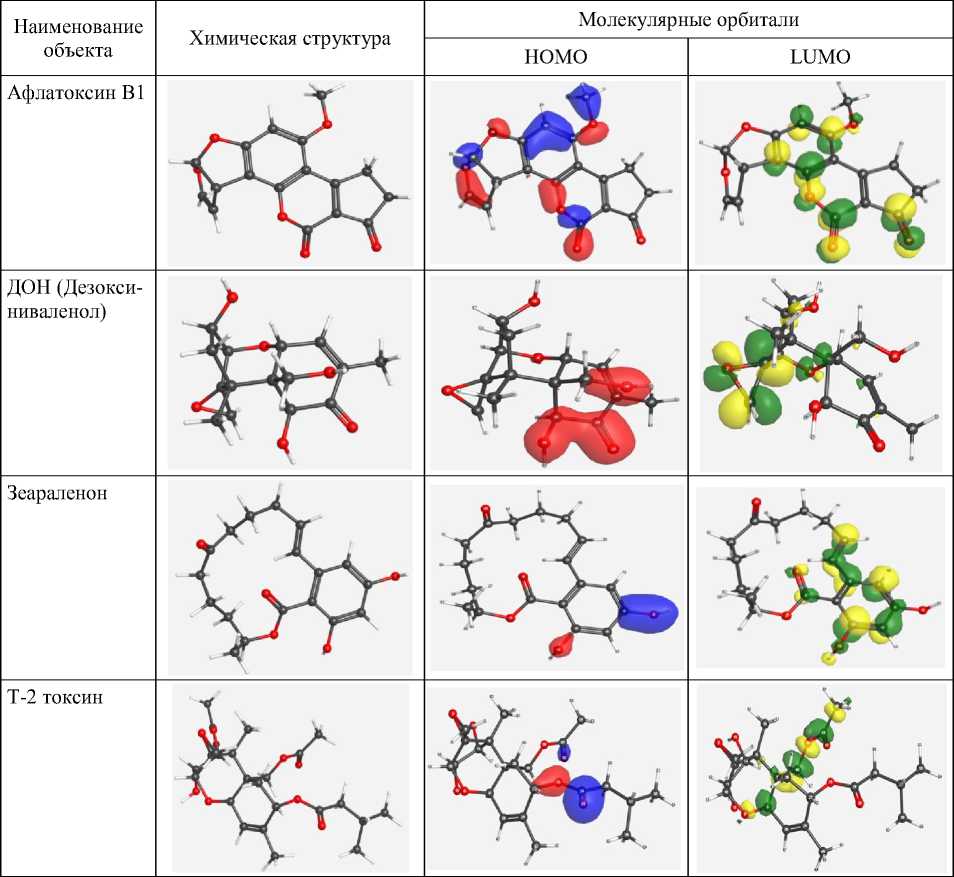
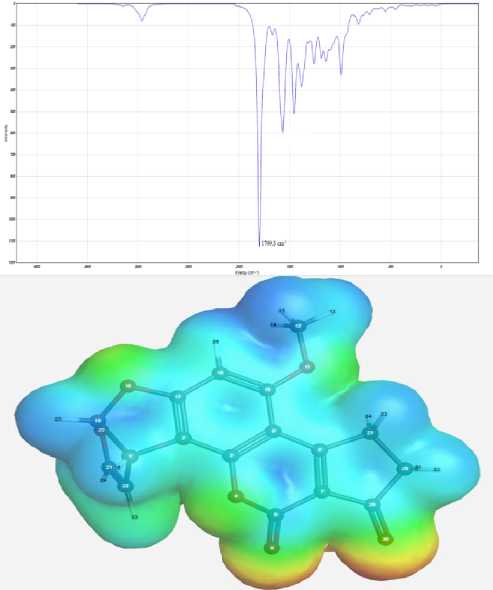
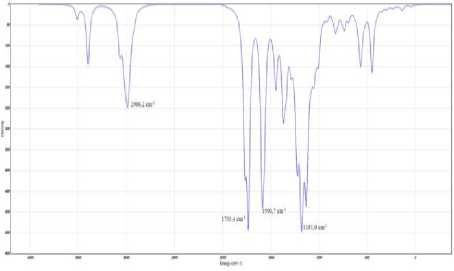
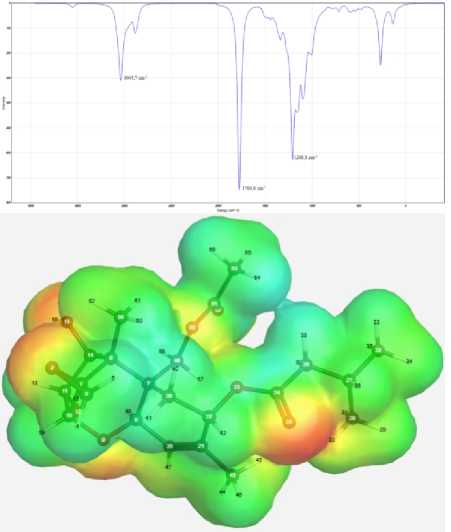
Теоретический ИК-спектр афлатоксина В1 демонстрирует выраженную полосу поглощения при волновом значении 1799,8 см–1, что соответствует для растяжения C=O, характерного для вибрации двойной связи углерод – кислород. В то время как для ДОН вибрационные частоты ИК-спектра демонстрируют полосы поглощения при волновых значениях 1722,4 см–1, что характерно для колебаний C=O связи, а также 1141,1 см–1, что демонстрирует колебания C-O связи (полярная ковалентная связь). Зеараленон проявил вибрационные частоты ИК-спектров при волновых числах 2986,2 см–1, что характерно для колебаний C-H группы, 1733,4 см–1 характерно для колебаний C=O связи (двойная ковалентная связь), 1590,7 см–1 – для деформационных колебаний C=С связи, 1181,0 см–1 демонстрирует колебания C-O связи. Для Т-2 токсина вибрационные частоты ИК-спектров находятся при волновых числах 3045,7 см–1, относится к вибрации C-H растяжения, 1769,8 см–1 демонстрирует колебания C=O связи, 1208,8 см–1 демонстрирует колебания C-O связи [8].
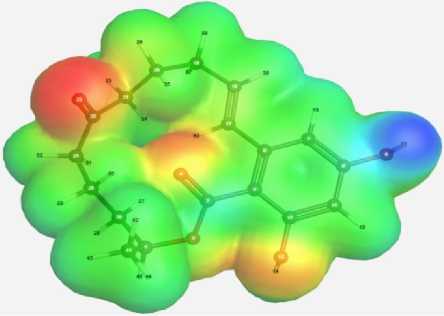
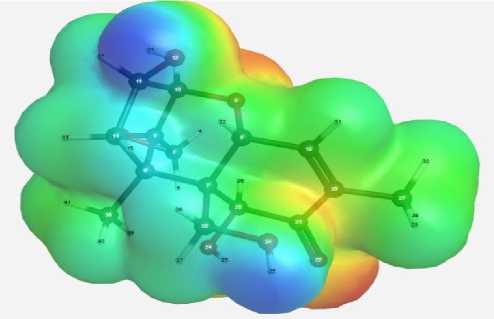
Карты электростатического потенциала микотоксинов, демонстрирующие трёхмерное распределение зарядов молекул, позволяют визуализировать чередующиеся заряженные области молекулы. Величину электростатического потенциала отражает интенсивность цвета, позволяя визуально анализировать распределение и силу электростатических сил
c)
a)
b)
d)
Вибрационные частоты ИК-спектров и карты электростатического потенциала микотоксинов: a – афлатоксин В1; b – ДОН (дезоксиниваленол); c – зеараленон; d – Т-2 токсин внутри молекулы [1, 2, 6, 9]. На картах показан максимальный уровень электростатического потенциала для Т-2 токсина (преобладает в большей степени зеленый цвет). Для всех микотоксинов наблюдается красный цвет, что свидетельствует об участках с минимальным электростатическим потенциалом молекул, характеризующим слабую связь или избыток электронов. Также наблюдаются синие участки на картах электростатического потенциала афлатоксина В1, дезоксиниваленола, зеарале-нона, указывающие на положительный электростатический потенциал. Представленные карты показывают трёхмерное распределение зарядов молекул, что важно для изучения их структуры и свойств. Полученные теоретически рассчитанные вибрационные частоты ИК-спектров микотоксинов важны для понимания природы колебаний отдельных функциональных групп в сложных молекулярных системах.
Выводы по результатам работы
Квантово-химические методы открывают новые возможности для исследования микотоксинов и их свойств благодаря применению принципов квантовой механики. Полученный массив данных с использованием квантовохимических расчетов методом GFN2-xTB позволил изучить не только геометрические параметры конструкций изученных микотоксинов, но также стабильность, реактивность молекул афлатоксина B1, дезоксиниваленола, зеараленона, Т-2 токсина, оказывающие риски снижения качества и безопасности зерна пшеницы, полученного в экстремальных погодных условиях.
Кроме того, полученные данные будут полезны для дальнейшего изучения силы взаимодействия микотоксинов с клейковинными белками зерна пшеницы.
Список литературы Квантово-химическое изучение молекулярной структуры микотоксинов зерна пшеницы
- Игнатов С.К. Квантовхимическое моделирование атомно-молекулярных процессов. Н. Новгород: Нижегородский государственный университет им. Н.И. Лобачевского, 2019. С. 79.
- Основы квантовой механики и квантовой химии. Методы расчёта электронной структуры и свойств молекул: учеб. пособие для студентов хим. фак. / С.П. Муштакова Н.А. Бурмистрова, И.Ю. Горячева и др. Саратов: Изд-во Новый ветер, 2009. 107 с. ISBN: 978-5-9758-1036-6
- Потороко И.Ю., Руськина А.А., Анйум В. Прогнозирование рисков присутствия микотоксинов в пищевых системах, полученных на основе зернового сырья // Вестник ЮУрГУ. Серия "Пищевые и биотехнологии". 2024. Т. 12, № 2. С. 38-47. DOI: 10.14529/food240205
- Alshannaq A., Yu J-H. Occurrence, toxicity, and analysis of major mycotoxins in food // Int J Environ Res Public Health. 2017. V. 14. P. E632. DOI: 10.3390/ijerph14060632
- Atoui A., Khoury A.I., Kallassy M. et al. Quantification of Fusarium graminearum and Fusarium culmorum by real-time PCR system and zearalenone assessment in maize // Int J Food Microbiology. 2012. Vol. 154(1-2). P. 59-65. DOI: 10.1016/j.ijfoodmicro.2011.12.022
- Feride Akman. Spectroscopic investigation, HOMO-LUMO energies, natural bond orbital (NBO) analysis and thermodynamic properties of two-armed macroinitiator containing coumarin with DFT quantum chemical calculations // Canadian Journal of Physics. 2016. Vol. 94(6). P. 583-593. DOI: 10.1139/cjp-2016-0041
- Jundi Liu, Jundi Liu, Todd Applegate. Zearalenone (ZEN) in Livestock and Poultry: Dose, Toxicokinetics, Toxicity and Estrogenicity // Toxins. 2020. Vol. 12(6). P. 377. 10.3390/toxins 12060377. DOI: 10.3390/toxins12060377
- John A. Agwupuye, Peter A. Neji, Hitler Louis et al. Investigation on electronic structure, vibrational spectra, NBO analysis, and molecular docking studies of aflatoxins and selected emerging mycotoxins against wild-type androgen receptor // Heliyon. 2021. Vol. 7, Iss. 7. e07544. DOI: 10.1016/j.heliyon.2021.e07544
- Markus Bursch et al. Best Practice DFT Protocols for Basic Molecular Computational Chemistry / Markus Bursch, Jan-Michael Mewes, Andreas Hansen, Stefan Grimme // Angewandte Chemie International Edition. 2022. Vol. 61(42). DOI: 10.1002/anie.202205735
- Valdemir Ludwig, Zélia Maria da Costa Ludwig, Marlon de Assis Modesto et al. Binding energies and hydrogen bonds effects on DNA-cisplatin interactions: a DFT-XTB study // Journal of Molecular Modeling. 2024. Vol. 30. Art. No. 187. DOI: 10.1007/s00894-024-05983-4


