Методические подходы к экспертному исследованию растений эфедры как объекта контролируемого оборота
Автор: Заер Е.В., Лебеденко С.Е., Мунгалов Е.А.
Журнал: Криминалистика: вчера, сегодня, завтра @kriminalistika-vsz
Рубрика: Уголовно-правовые науки
Статья в выпуске: 2 (26), 2023 года.
Бесплатный доступ
В настоящей статье на основе обобщения и систематизации сведений о способах и методах исследования растений эфедры (растений рода Ephedra L) предложен комплексный подход к решению экспертных задач по их отнесению к объектам незаконного оборота - растениям, содержащим прекурсоры наркотических средств или психотропных веществ. Рассмотрены анатомо - морфологические признаки представителей рода Ephedra L., условия и способы применения различных методов физико - химического анализа для определения основных алкалоидов эфедры.
Незаконное производство наркотических средств, растение эфедра, анатомо - морфологические признаки, хромато масс спектрометрия, тонкослойная хроматография, инфракрасная спектроскопия
Короткий адрес: https://sciup.org/143180747
IDR: 143180747 | УДК: 343.983.4+343.983.7 | DOI: 10.55001/2587-9820.2023.73.89.006
Methodological approaches to the expert study of ephedra plants as an object of controlled traffic
In this article, on the basis of generalization and systematization of information on methods and techniques of research of ephedra plants (plants of the genus Ephedra L), a comprehensive approach to solving expert problems on their attribution to objects of illicit trafficking - plants containing precursors of narcotic drugs or psychotropic substances is proposed. Anatomical and morphological features of representatives of the genus Ephedra L., conditions and modes of application of various methods of physico - chemical analysis to determine the main alkaloids of ephedra are considered.
Текст научной статьи Методические подходы к экспертному исследованию растений эфедры как объекта контролируемого оборота
Экспертные исследования психоактивных веществ в рамках расследования преступлений в сфере незаконного оборота наркотических средств, психотропных веществ и их прекурсоров достаточно сложны, так как предусматривают не только применение знаний в области химии, химического и физико-химического анализа, но и свободное оперирование нормативной базой в виде соответствующих федеральных законов и постановлений Правительства Российской Федерации.
Ситуация еще более усложняется при необходимости проведения экспертизы в отношении достаточно редко встречающихся в экспертной практике контролируемых растений, содержащих наркотические средства, психотропные вещества или их прекурсоры. В этом случае требуется применение специальных знаний не только из области химии, но и из области ботаники. Одним из таких объектов является эфедра, различные виды которой содержат в своем составе помимо прочих такие алкалоиды, как эфедрин, псевдоэфедрин, фенилпропаноламин (норэфедрин) [1, с. 20], отнесенные отечественным законодательством к числу прекурсоров1. На этом основании эфедра (растение рода Ephedra L) включена в Перечень растений, содержащих наркотические средства или психотропные вещества либо их прекурсоры и подлежащих контролю в Российской Федерации2.
Интерес к экспертному исследованию эфедры обусловлен ее относительно широким ареалом распространения, в том числе и на территории Российской Федерации, а также сообщениями специализированных органов по борьбе с незаконным оборотом наркотиков иностранных государств и межгосударственных образований. В частности, Европейский центр мониторинга наркотиков и наркомании (EMCDDA) в специальной публикации, посвященной ситуации с наркопроизводством в Афганистане, отмечает, что с 2019 года на территории его западных и юго-западных регионов наблюдается устойчивый рост культивации и заготовки эфедры с целью выделения эфедрина и дальнейшего использования его для синтеза метамфетамина. Исследователи EMCDDA отмечают, что в указанных регионах производство метамфетамина практически вытеснило традиционное для этих местностей производство героина3. Ареал распространения различных видов эфедры на территории бывшего СССР включает в себя страны Средней Азии, юг Европейской части России, юг Западной Сибири и восточную часть главного Кавказского хребта [2, с. 79]. Таким образом, на отдельных территориях Российской Федерации весьма вероятно появление очагов незаконного производства метамфетамина с использованием растительного сырья, что приведет к увеличению количества изъятий и назначений экспертиз и исследований травы эфедры.
При производстве судебных экспертиз с целью отнесения изъятых объектов к наркосодержащему растению эфедра (растение рода Ephedra L) эксперты сталкиваются с отсутствием единой методики экспертного исследования растений эфедры и их частей, которые обычно и поступают в экспертные подразделения в рамках уголовных дел или проверок сообщений о преступлениях. Для решения этой проблемы в настоящей статье приводятся и обобщаются сведения об анатомии и морфологии растений рода эфедра и исследовании алкалоидов эфедры физико-химическими методами.
Основная часть
На первом этапе экспертного исследования объектов растительного происхождения выявляются морфологические и анатомические особенности их строения, которые в рассматриваемом нами случае должны сопоставляться с аналогичными признаками эфедры. Рассмотрим подробнее признаки растений рода Ephedra L. и особенности систематизации последних.
Род эфедра (хвойник) Ephedra L – единственный род семейства Эфедровые Ephedraceae Dumort., представитель класса Гнетовые Gnetopsida из отдела Голосеменные Pinophyta . По мнению различных ученых, в роде эфедра насчитывается от 40 до 73 различных видов [3, с. 523; 4, с. 85; 5, с. 2].
Растения рода эфедра4 – это кустарники, реже деревья или лианы, высотой от 2–7 см до 5–7 м, с членистыми стеблями, напоминающими хвощ (рис. 1).

Рисунок 1. Эфедра хвощевая ( Ephedra equisetina Bunge)
Особый интерес представляет строение стеблей, так как в качестве источника алкалоидов (эфедрин, псевдоэфедрин) собираются именно неодревесневшие верхушечные части растения эфедра. Стебли серозеленого, желто-зеленого цвета, имеют сочлененный вид из-за наличия на них отдельных узлов и междоузлий. Междоузлия продольно ребристые, а гребни на последующих междоузлиях чередуются. Листья, расположенные в основании узла, редуцированные, пленчатого типа, лишенные хлорофилла, часто коричневого цвета, на 1/3 или почти полностью сросшиеся от основания в пленчатое влагалище, у отдельных видов листья опадающие (рис. 2). Поскольку листья чешуйчатые и редуцированные, процесс фотосинтеза осуществляется через поверхность стеблей, кора которых состоит в частности из клеток, содержащих хлорофилл. Растение двудомное, реже однодомное, с невзрачными раздельнополыми цветами, собранными в небольшие почти сидячие колоски. Мужские колоски одиночные или скученные по 2–3 штуки, двух-, четырехцветковые, почти шаровидные, длиной 4–5 мм; тычиночные (мужские) цветы состоят из тычинок, сросшихся в колонку, едва выдающуюся из чешуевидных прицветников. Наружные прицветники округлоэллиптические, на 1/3 сросшиеся с узкой окраиной у основания; внутренние округлые, более длинные. Пыльники, числом 6–8, почти сидячие. Женские колоски мелкие, на коротких ножках, одноцветковые, с двумя (тремя) парами прицветников. Зрелые плоды представляют собой либо ложную ягоду желтоватую или красную, мясистую (рис. 3), либо сухие плоды, окруженные пленчатыми прицветниками.

Рисунок 2. Стебель с листьями растения эфедра

Рисунок 3. Ложные ягоды растения эфедра
Пыльцевые зерна эфедры эллипсоидальные и отмечены чередующимися гребнями и бороздками, параллельными длинной оси. Этот необычный полипликативный тип пыльцы также называется «эфедро-идным» [6, с. 41].
Эпидермальный слой стеблей эфедры по периметру состоит из чередующихся гребней и бороздок, что хорошо заметно при изучении их поперечных срезов. Внешний слой эпидермиса с толстым слоем кутикулы. В эпидермисе имеются многочисленные и вдавленные устьица, расположенные в бороздках. Устьица гап-лохейльные, и каждое устьице состоит из двух защитных клеток и выступающей субстоматальной полости. Кора представлена столбчатой и губчатой паренхимой с неравномерно распределенными участками склеренхимы. В центре стебля находится паренхиматозная сердцевина.
Исследование анатомоморфологического строения растений эфедры и их частей проводится в соответствии с методикой исследования объектов растительного происхождения [7, с. 156-176], в ходе которого выявляется комплекс перечисленных выше признаков.
На следующем этапе экспертного исследования необходимо устано- вить наличие в исследуемых объектах алкалоидов, отнесенных к прекурсорам наркотических средств и психотропных веществ. В большинстве видов эфедры основным алкалоидом является эфедрин, содержание которого может составлять до 65 % от общего количества (суммы) алкалоидов [2, с. 83; 8, с. 250].
Эфедрин (l-эфедрин; (1R, 2S)-2-метиламино-1-фенилпропан-1-ол) схож как по строению молекулы, так и по действию на организм человека с псевдоэфедрином
(d-псевдоэфедрином, (1S, 2S)-2- метиламино-1-фенилпропан-1-олом) [9, с. 248], который является диастереомером эфедрина. Между собой эти соединения соотносятся как трео- и эритро-формы молекулы с брутто-формулой C10H15NO соответственно
(рис. 4).
Основные алкалоиды эфедры (l-эфедрин и d-псевдоэфедрин) являются прекурсорами такого распространенного наркотического средства, как метамфетамин (рис. 5). Получаемый с их использованием оптически активный d-метамфетамин обладает гораздо более высокой биологической активностью, чем смесь его оптических изомеров, получаемая при синтезе с использованием иных исходных компонентов [10, с. 14].
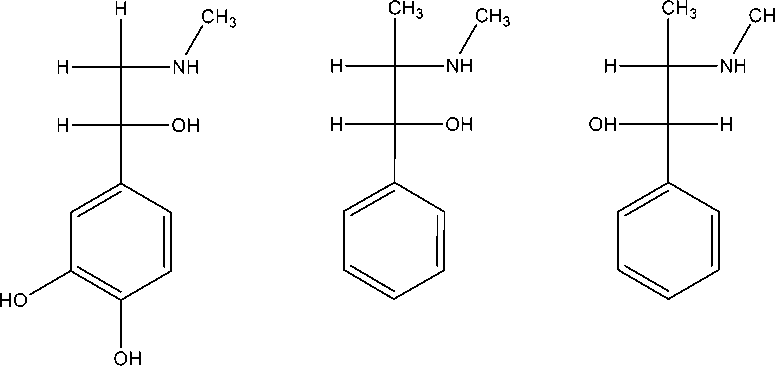
Рисунок 4. Структурные формулы соединений: а) адреналин, б) l-эфедрин, в) d-псевдоэфедрин
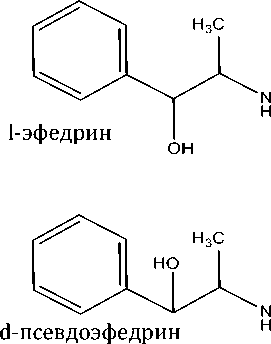
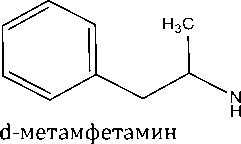
Рисунок 5. Схема восстановительной реакции получения метамфетамина из l-эфедрина или d-псевдоэфедрина
Как и большинство диастереомеров, l-эфедрин или d-псевдоэфедрин имеют схожие химические свойства, но несколько различаются по физическим свойствам, что позволяет проводить их обнаружение методами физико-химического анализа. В различных работах для исследований такого рода рекомендуется использовать тонкослойную хроматографию [10, с. 45–46], высокоэффективную жидкостную хроматографию [11, с. 353], капиллярный электрофорез [12, с. 8], хромато-масс-спектрометрию с хиральной и ахиральной дериватизацией [13, с. 89– 90], либо сочетание нескольких из перечисленных и иных методов [14, с. 5–9].
Отметим, что в случае исследования растительных объектов непосредственно анализу определяемых компонентов предшествует стадия их выделения из растительной матрицы. В качестве наиболее эффективного способа извлечения алкалоидов может быть предложена экстракция предварительно высушенной и измельченной растительной массы эфедры диэтиловым эфиром (при его отсутствии – хлороформом) с добавлением раствора гидроксида натрия до достижения значения pH, равного 12, в течение 30 минут в ультразвуковой ванне при соотношении массы образца и объема растворителя 1:10 [10, с. 45; 11, с. 352]. Полученный экстракт необходимо отделить от растительных частиц путем фильтрации, упарить досуха в токе воздуха, после чего исследовать сухой остаток выбранным методом анализа.
В целях надежной идентификации соединений следует применять два независимых метода исследования, аналитический сигнал по меньшей мере одного из которых определяется химической структурой анализируемого компонента [15, с. 15– 17]. Также возможно применение схем исследования, в которых используются три метода исследования, аналитические сигналы двух из которых определяются физическими или химическими свойствами искомого компонента, а третий метод се- лективен по отношению к группе или классу соединений (например, метод качественных цветных реакций).
Для реализации первой из упомянутых схем в экспертных подразделениях чаще всего используется метод газовой хроматографии с масс-селективным детектированием, так как он по своей сути является комплексным и позволяет проводить идентификацию соединений как на основе спектральной информации, так и по хроматографическим параметрам. Однако в случае одновременного присутствия в исследуемых образцах эфедрина и псевдоэфедрина данный метод оказывается ограниченно применим, так как параметры удерживания эфедрина и псевдоэфедрина совпадают, а масс-спектры этих веществ и их дериватов практически неразличимы (рис. 6, 7).
39 42 51 56 63 73 77 91 105 117 131
39 42 51 56 63 74 91 105 117 130
40 50 60 70 80 90 100 110 120 130 140 150 160 170
Pseudoephedrine Head to Tail MF=903 RMF=906 Ephedrine
Рисунок 6. Масс-спектр псевдоэфедрина из библиотеки NIST Mainlib (вверху) в сравнении с масс-спектром эфедрина из библиотеки NIST Replib (внизу)
29 42 56 69 7784 91 105 115 127 136 145 159 173 185 196 213 222 231 244 254 288
29 56 77 84 91 105 115 127 138 159 174 185 196 213 224 244 288
338 357
338 357
20 30 40 50 60 70 80 90 100 110 120 130 140 150 160 170 180 190 200 210 220 230 240 250 260 270 280 290 300 310 320 330 340 350 360 370
Pseudoephedrine 2TFA Head to Tail MF=957 RMF=957 Ephedrine 2TFA
Рисунок 7. Масс-спектр трифторацетильного производного псевдоэфедрина (вверху) в сравнении с масс-спектром трифторацетильного производного эфедрина (внизу).
Приведены масс-спектры из библиотеки EKBDRUGS-17
Изменение времени, а соответственно, и индексов удерживания возможно при дериватизации исследуемых образцов в среде хлороформа, например путем ацетилирования [16, с. 121] или силилирования [17, с. 117].
Масс-спектры ацетильных, три-фторацетильных и некоторых силильных производных эфедрина и, в меньшей степени, псевдоэфедрина содержатся в наиболее распространенных в экспертных подразделениях библиотеках масс-спектров, таких как NIST, EKBDRUGS-17, а также в библиотеках модулей масс-спектрометрического анализа информационно-поисковой системы «АИПСИН Антинаркотики». Кроме того, в библиотеке масс-спектров EKBDRUGS-17 приведены экспериментальные значения индексов удерживания (RI) трифторацетиль-ных производных эфедрина и псевдоэфедрина для хроматографической колонки HP-5ms: для производного эфедрина RI = 1409, для производного псевдоэфедрина RI = 1459.
Так как малое различие масс-спектров в данном случае не позволяет проводить идентификацию исследуемых компонентов, целесообразно использовать метод добавок. Он заключается в проведении не менее двух последовательных анализов в одинаковых условиях, при этом в ходе повторного в аналит до дерива-тизации вносится навеска стандартного образца эфедрина или псевдоэфедрина массой не более 1 мг. По изменению площади хроматографического пика можно судить о химической структуре соответствующего ему компонента.
Аналогичным образом может быть проведено и исследование методом газожидкостной хроматографии с пламенно-ионизационным детектированием.
Рекомендуемые экспертным подразделениям органов внутренних дел условия анализа методами хро-мато-масс-спектрометрии и газожидкостной хроматографии в целях обнаружения эфедриноподобных алкалоидов приведены в работе коллектива авторов ЭКЦ МВД России [14, с. 6, 8].
Также при наличии стандартных образцов псевдоэфедрина и/или эфедрина может быть применен метод тонкослойной хроматографии. Для разделения указанных веществ в слое силикагеля предложены по меньшей мере две системы растворителей: хлороформ – метанол – ацетон – 25 %-ный раствор аммиака (система 1) в соотношении 40:20:6:3 [10, с. 46] и циклогексан – толуол – диэтиламин (система 2) в соотношении 75:15:10 [16, с. 121]. В качестве растворителей для нанесения образцов могут быть использованы этанол, метанол, хлороформ с добавлением триэтиламина (диэтиламина). В качестве проявителя целесообразно использовать 1 %-ный раствор нингидрина в ацетоне с нагреванием хроматографических пластин при температуре 70° до появления синефиолетового окрашивания зон стандартных образцов.
В случае отсутствия стандартных образцов эфедрина, псевдоэфедрина для их обнаружения может быть применен метод инфракрасной (ИК) спектроскопии в различных исполнениях (прессование таблеток с галогенидами щелочных металлов, использование приставок нарушенного полного внутреннего отражения, ИК-микроскопия и т. д.), так как инфракрасные спектры эфедрина и псевдоэфедрина достаточно информативны для их идентификации и дифференциации этих соединений между собой (рис. 8).
Следует учитывать, что метод ИК-спектроскопии применим в качестве идентифицирующего только к относительно чистым веществам. При исследовании объектов сложного состава, таких как экстракты растительных масс, необходимо предварительное выделение определяемых компонентов. Для этого может быть использована препаративная тонкослойная хроматография в системах растворителей, указанных ранее. Как показывает практика, при выделении веществ методом препаративной тонкослойной хроматографии удовлетворительные результаты достигаются с использованием пластин с тонким слоем силикагеля на алюминиевой фольге без УФ-индикатора, например «Sorbfil ПТСХ-АФ-В» (ООО «ИМИД», Россия).
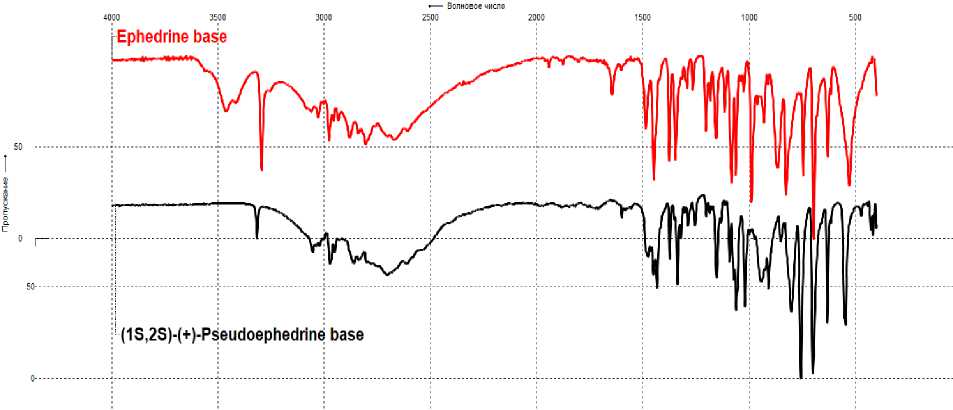
Рисунок 8. Инфракрасные спектры эфедрина (вверху) и псевдоэфедрина (внизу) из спектральной библиотеки SWGDRUG IR Library Version 2.1, полученные в программном обеспечении ZaIR 3.5
Для выделения эфедрина и псевдоэфедрина экстракт исследуемого образца растения эфедры небходимо наносить на стартовую линию предварительно очищенной хроматографической пластины в виде непре- рывной полосы. После хроматографирования в выбранной системе растворителей пластину следует высушить в токе воздуха, отрезать от нее участки шириной до 2 сантиметров с левого и правого края и обработать их раствором нингидрина. В упомянутых ранее работах указывается, что Rf (показатель хроматографической подвижности) эфедрина и псевдоэфедрина соответственно составляет 0,55 и 0,97 в системе 1 и 0,05 и 0,54 в системе 2. После проявления хроматографических зон отрезанные участки нужно приложить к оставшейся части пластины и по проявленным зонам на ней отметить участки локализации разделенных компонентов. Далее с отмеченных участков необходимо поочередно удалить силикагель и подвергнуть его экстракции диэтиловым эфиром с последующим отделением экстрактов фильтрацией или центрифугированием. Полученные экстракты следует высушить в токе воздуха, после чего инфракрасные спектры их сухих остатков могут быть зарегистрированы одним из указанных ранее способов и сопоставлены в автоматическом или ручном режиме с имеющимися в библиотеках программного обеспечения ИК-спектрами эфедрина и псевдоэфедрина.
Выводы и заключение
Рассмотренные нами анатомические и морфологические признаки растений эфедры и их частей, приемы и методы выявления, идентификации и дифференциации основных алкалоидов эфедры образуют комплекс исследований, осуществление которого необходимо и достаточно для решения вопроса об отнесении объектов растительного происхождения в рамках судебной экспертизы или исследования к наркосодержащему растению эфедра (растению рода Ephedra L) или его частям.
Список литературы Методические подходы к экспертному исследованию растений эфедры как объекта контролируемого оборота
- Особенности производства экспертиз наркотических средств и психотропных веществ растительного происхождения, а также наркосодержащих растений и их частей: информационное письмо ЭКЦ МВД России от 18.06.2013 № 37/3739. 26 с.
- Моргункова, Ю. М., Сорокин, В. И., Любецкий, Г. В. Анатомо-морфологическое исследование наркотических средств растительного происхождения: учебное пособие. М.: ЭКЦ МВД России, 2008. 215 с.
- Мусаев, И. Ф. О географии и филогении представителей рода эфедра // Ботанический журнал, 1978. Т. 63, № 4. С. 523–543.
- Сосков, Ю. Д. Три линии развития в секции Ephedra рода Ephedra L. во флоре СССР // Ботанический журнал, 1968. Т. 53, № 1. С. 85–91.
- Ramírez A, Pastor-Palacios G, Pérez-Miranda S, Ramírez-Hernández A, Trujillo J, Bautista, E. A Review of the Ephedra genus: Distribution, Ecology, Ethnobotany, Phytochemistry and Pharmacological Properties // Molecules, 2020 Jul 20; 25(14):3283.
- Robert A. Price Systematics of the Gnetales: A Review of Morphological and Molecular Evidence // International Journal of Plant Sciences 1996, Volume 157. pp. 40–49.
- Мусин, Э. Ф., Мелешев, Р. С., Виноградова, М. М. Типовые экспертные методики исследования вещественных доказательств: в 2 ч. Ч. II / под ред. А. Ю. Семёнова; общ. ред. канд. техн. наук В. В. Мартынова. М.: ЭКЦ МВД России, 2012. 800 с.
- Кожамжарова, Л. С., Аблайханова, Н. Т., Есимсиитова, З. Б. Биоэкология и компонентный состав эфедриновых алкалоидов у видов E.equisetina в Джунгарском Алатау // Вестник КазНМУ: науч.-практич. журн. Алматы: Казахский Национальный мед. ун-т им. С. Д. Асфендиярова, 2021. № 2. С. 246–252.
- Машковский, М. Д. Лекарственные средства: пособие для врачей / 16-е изд., перераб., испр. и доп. М.: Новая волна: Изд. Умеренков, 2012. 1216 с.
- Журинов, М. Ж., Газалиев, А. М, Фазылов, С. Д. Химия эфедриновых алкалоидов. Алма-Ата: Наука, 1990. 144 с.
- Chang, C. W., Hsu, S. Y., Huang, G. Q. [et al.]. Ephedra alkaloid contents of Chinese herbal formulae sold in Taiwan // Drug Testing and Analysis, 2018. Vol.10, № 2, P. 350–356.
- Lloyd A, Russell M., Blanes L. Lab-on-a-chip screening of methamphetamine and pseudoephedrine in samples from clandestine laboratories // Forensic science international, 2013. Vol. 228. P. 8–14.
- Wang S. M., Lewis R. J., Canfield D. Enantiomeric determination of ephedrines and norephedrines by chiral derivatization gas chromatography-mass spectrometry approaches // Journal of chromatography. B, Analytical technologies in the biomedical and life sciences, 2005. Vol. 825, № 1. P. 88–95.
- Гладырев, В. В., Дроздов, М. А., Дротьев, В. М. Вопросы криминалистического исследования псевдоэфедрина. М.: ЭКЦ МВД России, 2007. 13 с.
- Rodriguez-Cruz S. E., Matchett C., Iera J. Scientific working group for the analysis of seized drugs (SWGDRUG) recommendations. Edition 8.1. Washington: SWGDRUG, 2023. 85 p. URL: https://www.swgdrug.org/Documents/SWGDRUG%20Recommendations%20Version%208.1_FINAL_ForPosting_Rev%201-23-23.pdf (дата обращения: 24.04.2023). Режим доступа: свободный.
- Сурнина, О. В. Обнаружение эфедрина и псевдоэфедрина в БАД // Избранные вопросы судебно-медицинской экспертизы. Избранные вопросы судебно-медицинской экспертизы: сб. науч. трудов / ГБОУ ВПО ДВГМУ Минздрава России; под ред. А. И. Авдеева, И. В. Власюка. Хабаровск: Ред.-изд. центр ИПКСЗ, 2009. Вып. 10. С. 120–123.
- Cui, J. F., Zhou, T. H. C. Q., Zhang, J. S. [et al.]. Analysis of Alkaloids in Chinese Ephedra Species by Gas Chromatographic Methods // Phytochemical Analysis, 1991. Vol. 2. pp. 116–119.


