Методика определения текучести крови при тромбоэмболии легочной артерии
Автор: Начкебия С.Д., Кандашвили Т.И., Момцелидзе Н.Г., Кучава Г.Т., Джаркава М.В., Гоцадзе М.Ш., Манцкава М.М.
Журнал: Российский журнал биомеханики @journal-biomech
Статья в выпуске: 2 т.29, 2025 года.
Бесплатный доступ
Тромбоэмболия легочной артерии является одним из наиболее опасных заболеваний. Полная или частичная окклюзия легочной артерии (или её мелких ветвей) эмболами или тромбом вызывает повреждения, часто не совместимые с жизнью. Большй процент летальности и инвалидизации делает болезнь еще более опасной с точки зрения фундаментальной и клинической биомедицины. В данной статье предложена методика исследования текучести крови у пациентов с тромбоэмболией легочной артерии. В ходе работы были определены прямые и непрямые реологические параметры у пациентов с диагностированной тромбоэмболией легочной артерии, а также были определены параметры в венозном отделе у контрольной группы. В рамках работы был рассчитан градиент изменения параметров, равнявшийся отношению параметров в артериальном отделе к среднему арифметическому значению в разных локациях венозного отдела. При помощи данной методики было подчеркнуто, что изменение текучести крови происходит на фоне реорганизации всех прямых и непрямых параметров, но с ярко выраженным изменением агрегируемости эритроцитов и Dдимера. В итоге было определено, что снижение агрегации эритроцитов при тромбоэмболии легочной артерии может быть необходимо для достижения лучшего результата лечения.
Текучесть, реология, агрегация, фибриноген, D-димер
Короткий адрес: https://sciup.org/146283143
IDR: 146283143 | УДК: 531/534: [57+61] | DOI: 10.15593/RZhBiomeh/2025.2.15
The method of determining blood fluidity in pulmonary embolism
Pulmonary embolism is one of the dangerous diseases. Complete or partial occlusion of the pul-monary artery or small branches by an embolus or thrombus causes damage that is often incompatible with life. A large number of fatalities and disabilities makes the disease even more significant from the point of view of fundamental and clinical biomedicine. We have proposed a new algorithm for studying blood fluidity in patients with pulmonary embolism. We have studied the so-called direct and indirect (rheological) parameters in patients with pulmonary embolism in different locations (venous and arterial compartments) and in the control. In this work, for the first time, we introduced a gradient of parameter change, which was equal to the ratio of parameters in the arterial compartment to the arithmetic mean value in different locations of the venous compartment of the blood. Using this algorithm, it was empha-sized that the change in blood fluidity occurs against the background of changes in all direct and indirect parameters, but with a pronounced change in the aggregability of erythrocytes. In summary, it is neces-sary to regulate the aggregation of erythrocytes in pulmonary embolism to obtain a better treatment result.
Текст научной статьи Методика определения текучести крови при тромбоэмболии легочной артерии
Тромбоэмболия представляет собой острое патологическое состояние, развивающееся в результате отрыва и миграции тромба, образованного на стенке кровеносного сосуда.
По характeру развития тромб может иметь различную структуру и поверхностные физико-пространственные свойства, однако чаще всего эмболия формируется в глубоких венах нижних конечностей, что впоследствии приводит к значительному нарушению газообмена и гемодинамическим расстройствам.
0000-0001-7558-6083
0000-0002-4632-3097


Эта статья доступна в соответствии с условиями лицензии Creative Commons Attribution-NonCommercial 4.0 International
License (CC BY-NC 4.0)
This work is licensed under a Creative Commons Attribution-NonCommercial 4.0 International License (CC BY-NC 4.0)
Благоприятными условиями для тромбообразова-ния и перемещения эмбола в легочную артерию является нарушение целостности сосудистой стенки, гиперкоагуляция, замедление кровотока. Но, с другой стороны, физико - пространственное понятие текучести связано с функциональным состоянием сосудов регуляторов, микроциркуляторной проницаемости, интенсивности микроциркуляции; противовеса коагуляци-онно/антикоагуляционных и реологической систем.
Таким образом, очевидно, существование прямой зависимости между тромбообразованием и текучестью крови. Как следствие, совокупность составляющих триады Вирхова коррелирует с вероятностью развития тромбоэмболии. Текучесть крови является мультиком-понентной проблемой, и, естественно, существует большое количество эндофакторов, которые влияют на характер изменения текучести [1; 2].
Однако кровь по гидродинамическим свойствам является промежуточным вариантом между суспензией и эмульсией. Поэтому текучесть крови определяется тем набором компонентов, из которых она состоит. Оторвавшийся тромб перемещается в правую часть сердца и попадает в легочную артерию, закупоривая ее. Результаты этого процесса зависят от размера, плотности тела (эмболы), коагуляционной/антикоагуляцион-ной системы [3].
Тромбоэмболия с гидродинамической точки зрения зависит от текучести. Текучесть в первую очередь определяется реологическими свойствами крови, коа-гуляцией/антикоагуляцией и свойствами кровеносных сосудов, каждый из этих факторов является детерминантом гемодинамических и биомеханических результатов [4–6].
Текучесть в основном обеспечивается реологическим статусом крови, которая, в свою очередь, зависит от деформационных свойств крови и составляющих ее частей. Поведение крови зависит от радиуса сосудов мы рассматриваем ее в венозном или артериальном отсеке. На математическом языке реологический статус крови состоит из тотальной суммы необратимой остаточной деформации и вязкопластичной деформации. Таким образом, реологический статус крови – это совокупность физико-химических свойств релаксации, последействия удлинения, качества стенки сосуда и включений в утяжеленном или неутяжеленном состоянии.
Одновременные реологические исследования на разных уровнях, в микроциркуляторном и макроцирку-ляторном русле, чрезвычайно важны, поскольку кровоток полностью определяет текучесть крови и ее движение [7].
Особенно важно исследование реологических свойств крови в случае тромбоэмболии легочной артерии. Здесь изучение реологии имеет дуальную роль. С одной стороны, реология крови участвует или не участвует в тромбообразовании, и сдругой стороны, реология крови обеспечивает перенос уже сформированного тромба. Траектория движения тромба также зависит от реологического статуса крови.
Таким образом, реологические подходы представляют собой многопрофильную современную задачу, включающую многочисленные концепции, постулаты и законы из областей физики, физиологии, патофизиологии, теоретической и клинической медицины.
Описание легочной тромбоэмболии возможно благодаря комплексной оценке деформируемости, упругости, пластичности, компонентов крови, сосудистой сети. Несмотря на наличие многочисленных клинических и экспериментальных исследований в направлении изучения тромбоэмболии легочной артерии, до сих пор не удалось проанализировать, какое влияние кровоток, зависящий одновременно от различных факторов, оказывает на тяжесть тромбоэмболии. Неясно, как именно влияют биомеханические свойства тромбо-массы на исход тромбоэмболии.
Независимо от особого научного интереса к тромбоэмболии легочной артерии, в современной литературе нет четко обозначенной позиции относительно того, какие предпосылки обеспечивают успешность терапии, не описаны случаи, когда на основании доклинических исследований можно было бы говорить о наличии тромба или эмбола. Также нет данных, какие конкретно изменения претерпевают реологические параметры крови в разных отсеках кровообращения.
На фоне плачевной эпидемиологической обстановки все вопросы, связанные с изучением тромбоэмболии легочной артерии, являются особенно актуальными [8–10].
Целью данной работы является исследование реологических параметров крови у пациентов с диагности-рованнной тромбоэмболией легочной артерии, в рамках которого полученные результаты и их обсуждение должны пролить свет на неизученные реологические характеристики в венозных и артериальных отсеках.
Материалы и методы
В исследовании приняли участие 20 пациентов с подтвержденным в день госпитализации диагнозом «тромбоэмболия легочной артерии». Средний возраст пациентов составляет 67 ± 8 лет. Критериями исключения служили сопутствующие онкологические заболевания легких, пневмонэктомия в анамнезе, ранее подтвержденная хроническая легочная гипертензия, заболевания крови. Контрольную группу составили добровольцы соответствующего возраста без сопутствующих болезней.
При поступлении всем пациентам проводили электрокардиографию, эхокардиографию, цветное дуплексное картирование вен нижних конечностей и малого таза, рентгеноконтрастное исследование легочной артерии, КТ-ангиографию.
В рамках работы все определенные параметры, которые напрямую или косвенно влияют на текучесть крови, далее в тексте будут обозначаться как «прямые» и «непрямые» параметры текучести.
Для определения текучести крови испытуемых был составлен алгоритм исследования. Для начала были получены прямые и непрямые параметры, определяющие текучесть крови у больных с тромбоэмболией легочной артерии в венозной и артериальной крови на периферии. Далее у этих же пациентов и у контрольной группы были исследованы непрямые параметры в венозной крови. После был рассчитан градиент изменения прямых параметров в венозных и артериальных отделах.
Локация эмбола и его габаритные размеры были идентичны друг другу. Анализировались следующие показатели пациентов: мера кислотности и щелочности ( pH ), парциальное давление кислорода и углекислого газа (pO 2 и рСО 2), сатурация крови кислородом ( SaO 2), уровень оксигемоглобина ( FO 2 Hb ), отношение парциального давления кислорода к концентрации вдыхаемого кислорода ( pO 2(a)/ FO 2), концентрация истинного бикарбоната ( cHCO 3 ( P )) и гемоглобина ( Hb ) в венозной крови, а также параметры, которые формируют структуру крови: индекс агрегации эритроцитов ( EAI), индекс деформируемости эритроцитов ( EDI) , вязкость плазмы ( VP ), фибриноген ( FIB ), D -димер ( D-d ), гематокрит ( Hct ), реологический коэффициент ( RC) в венозной и артериальной крови [12-14].
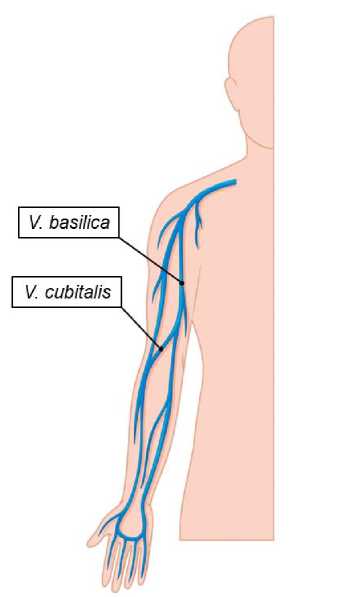
У представителей контрольной группы были исследованы прямые и непрямые параметры венозной крови только в области локтевой вены (v. cubitalis). У пациентов с тромбоэмболией легочной артерии были определены прямые и непрямые параметры венозной и артериальной крови в областях медиальной подкожной вены, локтевой вены (v. basilica и v. cubitalis) и в лучевой артерии (v. radialis) (рис. 1).
Были введены градиенты исследуемых величин в венозном и артериальном отделах кровеносной системы для следующих параметров ARC , A EAI , A EDI , APV , AHct . Данные градиенты рассчитывались согласно следующей формуле:
Avb + Avc
АЛ = A :-----------, ar 2
где Aar - параметр, определенный в лучевой артерии; Avb - параметр, определенный в медиальной подкожной вене; Avc - параметр, определенный в локтевой вене.
При выполнении работы были использованы следующие лабораторные приборы ABG ( Siemens ), Bekman ( Midrey ).
Для исследования реологической системы была использована оригинальная методика из работ [16-18].
Статистический анализ был проведен при помощи пакета программ Origin 8.1. Исследование проводилось в рамках Хельсинкской декларации, дано разрешение на проведение исследования от этического комитета, получены индивидуальные информационные согласия от всех испытуемых.
а
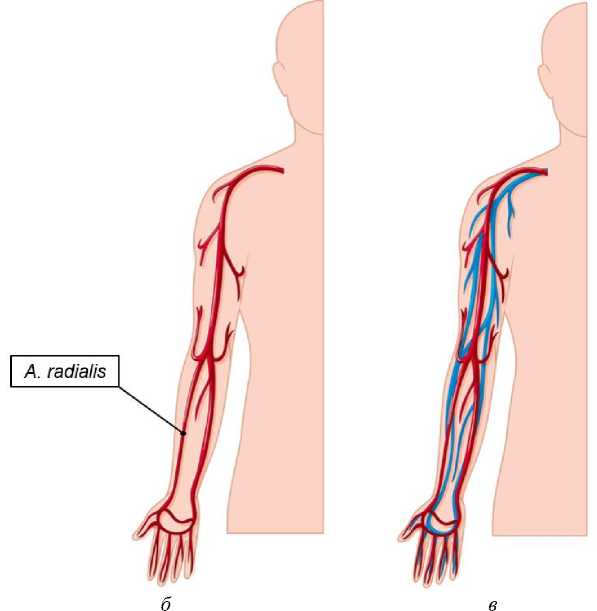
Рис. 1. Анатомическое расположение кровеносных сосудов в руке человека: а - вены; б - артерии; в - общее изображение [11]
Таблица 2
Средние значения непрямых параметров
|
Параметр |
Пациент |
Контрольная группа |
|
pH |
7,30 ± 0,12 |
7,35-7,45 |
|
pO 2, мм рт. ст. |
40,00 ± 9,20 |
30,00-50,00 |
|
рСО 2, мм рт. ст. |
36,00 ± 12,50 |
40,00-52,00 |
|
SaO 2 , % |
68,00 ± 7,90 |
60,00-85,00 |
|
FO 2 Hb , % |
85,00 ± 16,90 |
23,00-94,00 |
|
pO 2 ( a )/ FO 2 |
252,00 ± 62,00 |
400,00-500,00 |
|
cHCO 3 ( P ) ммоль/л |
15,00 ± 7,00 |
26,00-32,00 |
|
Hb , г/л |
126,30 ± 39,00 |
132,00-173,00 |
Таблица 1
Средние значения прямых параметров
|
Параметр |
Локализация |
|||
|
Пациент |
Контрольная группа |
|||
|
A. radialis |
V. basilica |
V. cubitalis |
V. cubitalis |
|
|
FIB , мг/мл |
700,00 ± 60,20 |
705,00 ± 50,80 |
682,00 ± 55,80 |
280,00 ± 30,00 |
|
D-d , нг/мл |
1182,50 ± 59,00 |
1176,50 ± 64,00 |
1172,50 ± 65,00 |
100,70 ± 8,80 |
|
EAI , % |
62,00 ± 4,50 |
54,00 ± 6,00 |
55,00 ± 5,00 |
29,00 ± 5,00 |
|
EDI , % |
2,20 ± 0,05 |
2,20 ± 0,05 |
2,20 ± 0,05 |
2,10 ± 0,05 |
|
PV , Па^с |
1,30 ± 0,04 |
1,30 ± 0,06 |
1,30 ± 0,04 |
1,10 ± 0,03 |
|
RC , Ед |
1,10 ± 0,05 |
1,10 ± 0,05 |
1,00 ± 0,05 |
1,00 ± 0,05 |
|
Hct , % |
41,20 ± 1,80 |
42,20 ± 1,50 |
42,60 ± 1,20 |
38,80 ± 0,45 |
Результаты
Все полученные результаты были обработаны с помощью методов математической статистики.
Средние значения прямых и непрямых параметров для пациентов и контрольной группы были рассчитаны как сумма/разность математического ожидания и среднеквадратичного отклонения ( M ± m )
(см. табл. 1, 2).
Кроме того, были рассчитаны градиенты изменения параметров, которые равнялись отношению параметров в артериальном отделе к среднему арифметическому значению в разных местах венозного отдела кровеносной системы (см. табл. 3).
Обсуждение
-
У пациентов с тромбоэмболией легочной артерии
происходило смещение рН в сторону увеличения кислотности, что указывает на субкомпенсированный негазовый ацидоз. Хотя основные газовые показатели рО 2 и рСО 2 были в пределах норм, но SaO 2, FO 2 Hb и индекс pO 2( a )/ FO 2 у пациентов с тромбоэмболией легочной артерии изменялся по сравнению с контрольными значениями. На фоне развития легочно-артериальной гипоксии это может быть связано с прогрессирующим нарушением вентиляционно-перфузионного соотношения, вызванного увеличением давления заклинивания в легочных капиллярах, что ведет к шунтированию справа налево и манифестации признаков легочной гипертензии [19].
Снижение уровня cHCO 3 ( P ) в венозной крови у пациентов с тромбоэмболией по сравнению с данными контрольной группы указывает на появление вторичного метаболического ацидоза [20-22].
Градиент изменения параметров. В основном это касалось величин, отражающих прямые параметры, влияющие на текучесть, так как непрямые параметры менялись адекватно [23-26]. То есть измеряемые нами параметры (водородный показатель ( pH ), парциальное давление кислорода и углекислого газа (pO 2 и рСО 2), сатурация крови кислородом ( SaO 2), уровень оксигемоглобина ( FO 2 Hb ), отношение парциального давления кислорода к концентрации вдыхаемого кислорода ( pO 2 ( a )/ FO 2 ), а также концентрации актуального бикарбоната ( cHCO 3 ( P )) и гемоглобина ( Hb )) изменялись предсказуемо и соответственно патофизиологии болезни. Что касается прямых параметров текучести, здесь изменения не были однородными. Точнее, при тромбоэмболии легочной артерии фибриноген у пациентов значительно увеличивался по сравнению с данными контрольной группы и в венозном, и в артериальном отделах. То же самое наблюдалось с D -димером. Подобные тенденции обнаружились у деформируемости эритроцитов и гематокрита.
-
■ Пациенты ■ Контрольная группа
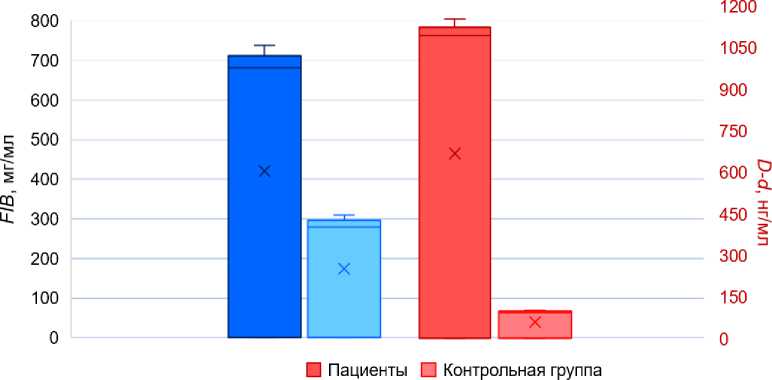
Рис. 2. Сравнение среднего значения фибриногена и D -димера у обследованных и лиц контрольной группы в области локтевой вены ( v. cubitalis )
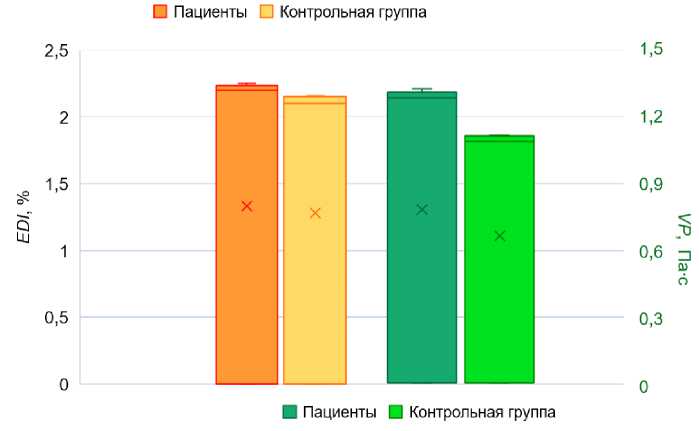
Рис. 3. Сравнение среднего значения показателя деформируемости эритроцитов и вязкости плазмы крови у обследованных и лиц контрольной группы в области локтевой вены ( v. cubitalis )
Таблица 3
Градиенты изменения параметров
|
Градиент Δ |
Δ FIB |
Δ D-d |
Δ EAI |
Δ EDI |
Δ PV |
Δ RC |
|
Значение |
1,01 |
1,01 |
1,14 |
1,00 |
1,00 |
1,05 |
В то же время изменения показателя агрегации эритроцитов в артериальной и венозной крови существенно отличались от контрольных значений. Это свидетельствует, что именно гиперагрегация способствует нарушению текучести крови и провоцирует ускорение, которое обусловливает миграцию тромба в венозную артерию [27-29].
Именно этот факт может объяснить то, что частота развития тромбоэмболии легочной артерии напрямую связана с тромбозом глубоких вен нижних конечностей [20; 21; 30; 31]. Агрегационная способность эритроцитов больше усиливается в артериальной крови, так как все компенсаторные механизмы направлены на упорядочение деформируемости мембран, что, в свою очередь, обеспечивается отсутствием градиента давления, которое связано с постоянным количеством фибриногена и D-димера в венозных и артериальных отделах.
Также был обнаружен параметр, меняющийся на протяжении всего пути перемещения крови от венозного отдела к артериальному. Для того чтобы обнаружить подобный параметр, был введен специальный градиент, равняющийся отношению прямого параметра в артериальном отделе к среднему арифметическому из разных вен венозного отдела (табл. 3). Оказалось, что агрегация эритроцитов
-
□ Пациенты □ Контрольная группа
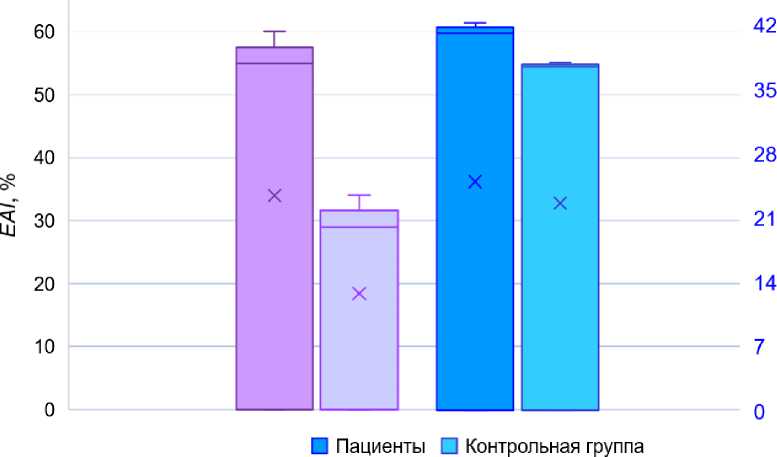
Рис 4. Сравнение среднего значения агрегации эритроцитов и гематокрита у обследованных и лиц контрольной группы в области локтевой вены ( v. cubitalis )
меняется на пути от венозного к артериальному отделу кровеносной системы. Таким образом, можно заключить, что именно агрегация эритроцитов отвечает за изменение текучести крови, что впоследствии может привести к тромбоэмболии легочной артерии [32; 33] .
Для наглядности на отдельные графики были выведены средние значения фибриногена и D -димера (см. рис. 2), деформируемости эритроцитов и вязкости плазмы (см. рис. 3), показателя агрегации эритроцитов и гематокрит (см. рис. 4) у пациентов с тромбоэмболией легочной артерии и в контрольной группе в области локтевой вены (см. рис. 1). Наибольшие отличия у пациентов и контрольной группы наблюдаются в значениях у фибриногена, D -димера и индекса агрегации эритроцитов.
Заключение
Составленный алгоритм исследования прямых и непрямых параметров, влияющих на текучесть крови в артериальном и венозном отделах, может использоваться в качестве первичной диагностики с целью оценки тяжести состояния пациентов с тромбоэмболией легочной артерии, в особенности ее острых форм, прогноза и выбора оптимального метода лечения.
В ходе исследования было обнаружено, что агрегация эритроцитов однозначно влияет на изменение текучести крови и может свидетельствовать о развитии тромбоэмболии.
Все диагностические тесты должны в большей или меньшей степени иметь предикторную роль. Высокая чувствительность тестов на основе прогностических функций может помочь в описании роли текучести крови при формировании тромбоэмболии. Это необходимо в клинической практике для установления диаг- ноза и выбора оптимального метода лечения.
В современной биомедицине особенно возросла роль превенционных мероприятий. Прогностические функции могут быть использованы при скрининге лабораторных показателей крови здоровых людей.


