Микроэкологические и иммунологические аспекты формирования нарушений репродуктивной функции
Автор: Сетко Нина Павловна, Михайлова Елена Алексеевна, Воронина Людмила Григорьевна, Штиль Ольга Олеговна, Генелес Лариса Нахимовна
Рубрика: Влияние экологии на внутренние болезни
Статья в выпуске: 1-7 т.13, 2011 года.
Бесплатный доступ
Изучены особенности микробиоценоза и локального иммунитета репродуктивного тракта фертильных и бесплодных мужчин. Были выявлены отличия в видовом составе, пенетрантности и экспрессии иммунодепрессивных свойств микрофлоры изучаемого биотопа, а также в уровне факторов антимикробной защиты. Результаты могут быть использованы в ранней диагностике патоспермии.
Микроэкология, иммунитет, эякулят, бесплодие
Короткий адрес: https://sciup.org/148100722
IDR: 148100722 | УДК: 616:612.017.1
Microecological and immunological aspects of formation the infringements of reproductive function
Features of microbiocenosis and local immunity of reproductive tract at fertile and infertile men are studied. Differences in specific structure, penetrance and expression of immunosuppressive properties of studied biotope microflora, and also in level of factors of antimicrobic protection have been revealed. Results can be used in early diagnostics of pathospermia.
Текст научной статьи Микроэкологические и иммунологические аспекты формирования нарушений репродуктивной функции
Состояние репродуктивного здоровья населения России привлекает все большее внимание специалистов, что обусловлено неблагоприятной демографической ситуацией. По данным ВОЗ [11] в 32,1% бесплодных супружеских пар репродуктивная функция нарушена у мужчин. Одним из факторов нарушения фертильности и развития патоспермии является инфицирование внутренних гениталий различными микроорганизмами [10]. При этом частым явлением оказывается формирование смешанной инфекции, обусловленной одновременным присутствием в урогенитальном тракте трех и более возбудителей, являющихся представителями нормальной микрофлоры. Показано снижение оплодотворяющей способности сперматозоидов под действием внутриклеточно паразитирующих возбудителей (хламидий, уреаплазм) и их метаболитов [5]. В то же время вопрос о роли условно-патогенных бактерий в патофизиологических механизмах развития бесплодия остается открытым. С одной стороны, данные микроорганизмы являются представителями эубиоза репродуктивной системы и, препятствуя заселению патогенов, обеспечивают колонизационную резистентность экологической ниши. С другой стороны, приобретая агрессивные потенции, они могут явиться этиологическим фактором воспалительного процесса в гениталиях [3, 4].
Особое место при рассмотрении роли смешанной урогенитальной инфекции в развитии бесплодия принадлежит выяснению механизмов,
Сетко Нина Павловна, доктор медицинских наук, заведующая кафедрой эпидемиологии и гигиены
Генелес Лариса Нахимовна, заведующая лабораторией Оренбургского центра планирования семьи определяющих восходящий характер инфекционного процесса и, таким образом, ведущих к формированию осложнений, непосредственно ведущих к утрате или снижению репродуктивной функции. Длительный симбиоз с макроорганизмом предполагает наличие у возбудителя факторов противостояния механизмам защиты хозяина, приводящее к формированию иммунодефицитного состояния, что, в свою очередь, также способно негативно сказываться на оплодотворяющей способности спермы.
Цель работы: изучение видового состава, иммунонейтрализующих свойств микрофлоры эякулята и факторов местной противоинфекци-онной защиты эякулята фертильных мужчин и больных бесплодием.
Материалы и методы. Обследовано 50 здоровых фертильных мужчин и 68 мужчин репродуктивного возраста, находящихся в бесплодном браке 1 год и более. У бесплодных мужчин на момент исследования не было клинических данных, свидетельствующих о воспалительных процессах в гениталиях. Женский фактор бесплодия был исключен. Отсутствие специфического инфекционного процесса устанавливали при проведении бактериологического исследования на гонококк в соответствии с приказом МЗ РФ № 415 «Об утверждении протокола ведения больных «Гонококковая инфекция» от 20.08.2003 г. Наличие микоплазм и уреаплазм определяли как с помощью ПИФ, так и путем посева на официнальные элективные питательные среды. Хламидии выявляли методом прямой иммунофлюоресценции и ПЦР, трихомонады – окраской мазков по Граму. Больные с положительными результатами тестов были исключены из дальнейшего обследования. Лабораторное исследование эякулята проводили согласно рекомендациям ВОЗ [11]. Лизоцим в эякуляте определяли по скорости лизиса М. luteus [2], функциональную активность комплемента – по лизису эритроцитов барана [1]. Для бактериологического исследования эякулята материал засевали на плотные питательные среды. Идентификацию выделенных микроорганизмов до уровня вида осуществляли общепринятыми методами на основании морфологических, тинкториальных, культуральных, биохимических и антигенных свойств. Биохимический профиль оценивали с помощью тест-систем «Lachema» («Lachema diagnostica», Брно, Чехия) и определителя бактерий Bergey [7]. Способность микроорганизмов к инактивации лизоцима – антилизоцимную активность (АЛА) – определяли кинетическим методом [2]. Для изучения антикомплементарной активности (АКА) исследуемых штаммов применялась методика, основанная на способе кинетического титрования комплемента [1] с измерением максимальной скорости лизиса сенсибилизированных эритроцитов барана. Источником комплемента служил препарат комплемента для РСК.
Результаты и обсуждение. При лабораторном исследовании установлено, что у здоровых мужчин объем эякулята составил 3,6±0,7 мл (2,5-6,2 мл), общее количество сперматозоидов (х106/мл) – 70,0±3,2 (62-75), из них активно подвижных 61,8±6,6% (50-75%). У больных бесплодием объем эякулята составил 3,3±0,8 мл (1,0-5,1 мл), общее количество сперматозоидов (х106/мл) – 45,0±4,2 (10-70), из них активно подвижных форм 12,3±3,7% (0-25%). Уровень лизоцима в эякуляте здоровых мужчин был равен 6,1±0,33 (4,5-7,2) мкг/мл. Содержание лизоцима в сперме больных бесплодием составило 0,73±0,14 (0,41,2) мкг/мл. При исследовании уровня комплемента в эякуляте выявлено, что у здоровых данный фактор антимикробной защиты составлял 4180±430 ед. СН 50. В сперме бесплодных мужчин концентрация комплемента была 3880±401 ед. СН 50.
Изучение взаимоотношений между анализируемыми лабораторными данными позволило выявить достоверную (p<0,01) положительную корреляционную зависимость (r=0,8) между содержанием лизоцима в эякуляте и подвижностью сперматозоидов. В тоже время было установлено отсутствие зависимости между уровнем лизоцима, комплемента, объемом эякулята и общим количеством сперматозоидов. Показатель микробной обсемененности (ПМО) эякулята здоровых мужчин не превышал 101 КОЕ/мл, тогда как интенсивность бактериоспермии у больных бесплодием колебалась в пределах 103-104 КОЕ/мл. Изучение микрофлоры эякулята показало, что от здоровых мужчин выделялась грампозитивная флора (рис. 1). При анализе видового состава микроорганизмов, выделенных из эякулята здоровых мужчин, было установлено, что коагула-зоотринательные стафилококки (S. epidermidis, S. capitis, S. saprophyticus, S. hominis) и стрептококки (Str. agalactiae) составляли 46,5%, a энтерококки (E. faecalis, E. faecium) – 21,3% микробиоценоза. Коринеформные микроорганизмы и лактобактерии составляли соответственно 10,5% и 8,2% микрофлоры эякулята здоровых мужчин. Высевались также анаэробные микроорганизмы (5,1%) и дрожжевые грибы (1,1%). В спектре микрофлоры эякулята больных бесплодием преобладали коагулазоотрицательные представители рода Staphylococcus (S. epidermidis, S. haemo-lyticus, S. hominis) и Streptococcus (Str. agalactiae), которые составляли 57,9% микробиоценоза. Появились энтеробактерии (Е. coli, Kl. pneimoniae, Е. cloacae. Proteus spp.) – 12,5%, а энтерококки (Е. faecalis, С. faecium, Е. gallinaiuu) и микрококки составляли соответственно 12,1% и 2,8% микрофлоры эякулята больных бесплодием. По сравнению со здоровыми из эякулята бесплодных обследуемых с большей частотой высевались анаэробы (2,4%) грибковая флора (12,3%).
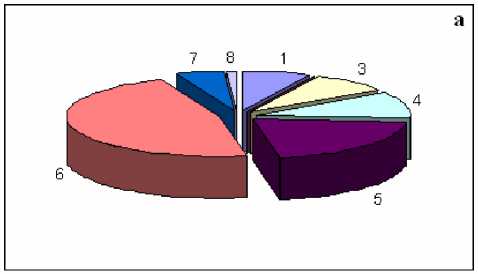
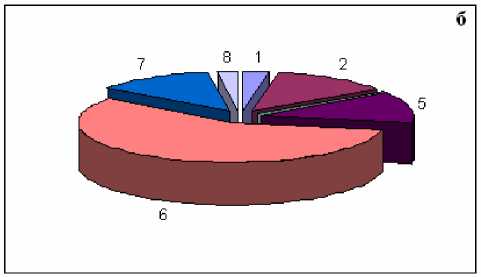
Рис. 1. Видовая характеристика микрофлоры эякулята здоровых мужчин (а) и больных бесплодием (б):
1 – микрококки, 2 – энтеробактерии, 3 – лактобактерии, 4 – коринебактерии, 5 – энтерококки, 6 – стафилококки и стрептококки, 7 – анаэробный микроорганизмы, 8 – дрожжевые грибы
Представленные результаты традиционного бактериологического исследования эякулята обследованных мужчин позволили сделать заключение, что: во-первых, несмотря на различия в микробной обсемененности эякулята здоровых мужчин и больных бесплодием, степень бактериоспермии у инфертильных мужчин в большинстве случаев не достигала диагностически значимого уровня; во-вторых, в видовой структуре изолированной микрофлоры у групп обследованных мужчин доминировали условно-патогенные грампози-тивные микроорганизмы, представленные коагулазоотрицательными стафилококками, условно патогенными стрептококками и энтерококками. Указанные обстоятельства, безусловно, осложняют клиническую оценку бактериологических данных и обусловливают необходимость поиска дополнительных информативных критериев индикации этиологически и диагностически значимых показателей.
В связи с этим нами был проведен сравнительный анализ частоты встречаемости и выраженности иммунонейтрализующих свойств у изолированных аэробных штаммов бактерий. У выделенных из исследуемого материала штаммов микроорганизмов от двух групп обследованных были определены антилизоцимная, антикомпле-ментарная активности (табл. 1), которые участвуют в формировании микробного биоценоза [2]. При анализе частоты встречаемости и уровня выраженности АЛА у штаммов бактерий, выделенных из эякулята здоровых и больных бесплодием, были установлены существенные межвидовые различия. У стафилококков, стрептококков и энтеробактерий в 100% случаев выявлялась АЛА, а ее выраженность была в 2,5-4 раза выше, чем у микрококков и энтерококков. Так, средние (2-3 мкг/мл) и высокие (3-5 мкг/мл) значения АЛА были отмечены у подавляющего количества штаммов энтеробактерий, стафилококков и стрептококков, при этом микрококки и энтерококки в большинстве случаев обладали АЛА, равной 0-1 мкг/мл.
Таблица 1. Уровень экспрессии АЛА (мкг/мл.ед.ОП) и АКА у бактериальной микрофлоры эякулята здоровых и бесплодных мужчин
|
Группа обследуемых |
Здоровые мужчины |
Бесплодные мужчины |
||
|
Биологическое свойство |
Уровень АЛА (мкг/мл) |
Уровень АКА (106анти-ЛЕК) |
Уровень АЛА (мкг/мл) |
Уровень АКА (106анти-ЛЕК) |
|
условнопатогенные стрептококки |
0,09±0,20 |
1,21±0,30 |
3,11±0,20* |
1,30±0,33 |
|
коринебактерии |
0,19±0,10 |
0,74±0,05 |
нет роста |
|
|
КОС |
0,60±0,19 |
1,18±0,40 |
4,61±0,51* |
1,13±0,11 |
|
лактобактерии |
0,32±0,10 |
0,54±0,04 |
Нет роста |
|
|
энтеробактерии |
нет роста |
нет роста |
3,74±0,59 |
2,89±0,41* |
|
энтерококки |
0,28±0,10 |
0,64±0,05 |
1,03±0,20* |
0,58±0,10 |
|
микрококки |
0,19±0,10 |
- |
0,15±0,09 |
- |
Примечание: * - р < 0,05
Кроме лизоцима микроорганизмы способны деградировать комплемент, который среди прочих факторов естественной резистентности организма усиливает силу проявления защитных свойств хозяина в отношении патогена. Из таблицы видно, что этой способностью обладали все (кроме микрококков) микроорганизмы, выделенные из биоценоза здоровых мужчин. Наиболее высокий уровень активности (табл. 1), определялся у энтеробактерий, которые обладали АКА в 58,8% случаев. Условно-патогенные стафилококки, изолированные от мужчин с бесплодием, по сравнению со штаммами, выделенными от здоровых, не отличались по частоте встречаемости и выраженности АКА. Выраженность АКА и встречаемость этого признака у энтерококков была такой же, как и у штаммов от здоровых лиц. Как и в группе здоровых, у энтерококков, изолированных от бесплодных мужчин, уровень выраженности АКА был самым низким среди всех видов. Стрептококки имели АКА в половине случаев, уровень активности был таким же, как у микроорганизмов данного таксона, выделенных от здоровых мужчин.
Проведенный анализ данных выявил достоверную (р<0,05) связь между выраженностью АЛА персистирующей флоры и низкой концентрацией лизоцима в эякуляте (рис. 2). В отношении АКА микроорганизмов и уровня комплемента в сперме выявлена аналогичная тенденция, однако достоверно значимая зависимость не определена.
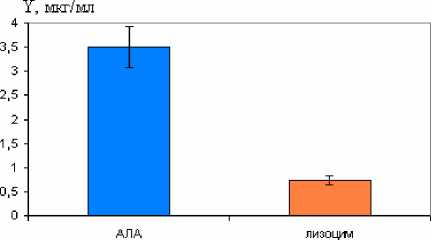
Рис. 2. Сравнительная характеристика содержания лизоцима в сперме и уровня АЛА микрофлоры эякулята у больных бесплодием
Как видно из представленных результатов, сперма больных бесплодием характеризуется более высокой степенью обсемененности микроорганизмами, что может косвенно указывать на этиологическую роль бактерий в формировании патоспермии. В микробиоценозе эякулята больных с бесплодием выявлены существенные различия в видовом многообразии, частоте встречаемости и силе выраженности свойств микроорганизмов, обеспечивающих инактивацию локальных антимикробных факторов защиты слизистой оболочки урогенитального тракта. Однако количество микроорганизмов в сперме может повышаться по причинам, не связанным с инфертильностью, например, вследствие контаминации во время сбора материала, при недиагностированных уретритах и др. [6, 8]. Изменения в видовой структуре микрофлоры эякулята (дефицит лактобактерий и коринеформных микроорганизмов, увеличение коагулазоотрицательных стафилококков и энтеробактерий) позволяют сделать вывод о развитии урогенитального дисбиоза у больных бесплодием. Широкая распространенность и выраженность антилизоцимного признака обеспечивает микроорганизмам возможность длительного переживания в организме хозяина [2]. В то же время персистенция бактерий, способных инактивировать лизоцим, по-видимому, формирует дефицит лизоцима в сперме. С одной стороны, снижение концентрации лизоцима в сперме вследствие его деградации микроорганизмами отражается на подвижности сперматозоидов, с другой – лизоцимдефицитное состояние эякулята, возможно, уменьшает вероятность прохождения сперматозоидов через цервикальную слизь [4, 9].
Выводы: у больных бесплодием высокая обсемененность спермы микроорганизмами, их видовое разнообразие, широкая распространенность и выраженность антилизоцимного признака, высокая антикомплементарная активность свидетельствуют об определенной роли перси-стируюшей микрофлоры в формировании патос-пермии и ухудшении фертильной функции. Определение низкого уровня лизоцима в сперме может служить диагностическим признаком при оценке её фертильности.
Список литературы Микроэкологические и иммунологические аспекты формирования нарушений репродуктивной функции
- Брудастов, Ю.А. Антикомплементарная активность бактерий: автореф. дис.. канд. мед. наук/Ю.А. Брудастов. -Челябинск, 1992. 22 с.
- Бухарин, О.В. Механизмы выживания бактерий/О.В. Бухарин, А.Л. Гинцбург, Ю.М. Романова, Г.И. Эль-Регистан. -М.: Медицина, 2005. 366 с.
- Зиганшин, О.Р. Механизмы антимикробной резистентности репродуктивных органов мужчин/О.Р. Зиганшин, И.И. Долгушин. -Челябинск: Изд-во «Челябинская Государственная медицинская академия», 2001. 188 с.
- Репродуктивное здоровье/Под ред. Л.Г. Кейта, Г.С. Бергера, Д.А. Эдельмана: Пер. с англ. -М., 1988, Т. 1-2. C. 312-390/
- Тиктинский, О.Л. Заболевания половых органов у мужчин/О.Л. Тиктинский, П.Ф. Новиков, В.В. Михайличенко. -Л., 1985. 293 с.
- Щеплев, П.А. Простатит/П.А. Щеплев, Л.С. Страчунский, В.В. Рафальский и др. -М., 2004. C.1-254.
- Bergey's Manual of Determinative Bacteriology/F.d J.G. Hull. 9-th Ed. Vol. 1-2. -Baltimore. 2004.
- Galdiero, F. Toxic effect on human spermatozoa by Chlamydia trachomatis purified lipopolysacchide/F. Galdiero, L. Sommesc, F. Gorga el al.//FEMS Microbiol Lett. 1994. Vol. 115, N 2-3. P. 197-200.
- Kelly, D. Commensal gut bacteria: mechanism of immune modulation/D. Kelly, S. Conway, R. Aminov//Trends Immunol. 2005. Vol. 26, № 6. P. 326-333.
- Nickel, J.C. The Prostatitis Manual: A Practical Guide to Management of Prostatitis/Chronic Pelvic Pain Syndrome. -Bladon Medical Publishing, 2002. P.1-116.
- WHO. Laboratory Manual for the Examination of Human Semen and Semen Cervical Mucus Interaction. Fifth edition -Cambridge, 2010. 125 p.


