Моделирование процесса роста кристаллов сахарозы в сахарсодержащем растворе
Автор: Семенов Е.В., Славянский А.А., Грибкова В.А., Митрошина Д.П., Антипов С.Т.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Процессы и аппараты пищевых производств
Статья в выпуске: 1 (87), 2021 года.
Бесплатный доступ
Кристаллизация сахарозы представляет собой один из наиболее важных этапов в технологическом потоке получения товарного сахара. По своей природе - это развивающийся в достаточно широком температурном диапазоне, условиях изменяющейся концентрации раствора, его пептизации и другого массообменный процесс образования и роста кристаллов сахара в сахарном растворе путем диффузионного переноса в нем молекул сахарозы. К этому нужно добавить еще и такие осложняющие физико-математическую формализацию явления, влияющие на кристаллизацию, как форма кристалла, чистота, вязкостные свойства и поверхностное натяжение раствора, наличие в нем несахаров и т.п. Поэтому среди обусловливающих в целом протекание процесса факторов обычно проводят, сохраняя среди них лишь приоритетные и наиболее важные с позиций исследования. С точки зрения классической диффузионной теории явление кристаллизации трактуется как молекулярный с бесконечной скоростью распространения возмущения от источника диффузионный перенос в растворе молекул сахарозы, вследствие чего концентрация в сахарсодержащей жидкостной системе также полагается изменяющейся мгновенно в каждой точке. Однако, поскольку в реальных условиях этот эффект не наблюдается, то, с целью разрешить это противоречие, вводят понятия возмущенного и невозмущенного, разделенных называемым диффузионным фронтом концентрации областей этих фазовых состояний. Используя кинематические характеристики фронта, определяют время протекания процесса кристаллизации в целом по обеим фазам. Что позволяет с большей, по сравнению с полученными на базе классической теорией результатами, точностью рассчитать период обработки раствора.
Вакуум-аппарат, концентрация раствора, затравка, кинетика кристаллизации, сахароза
Короткий адрес: https://sciup.org/140257366
IDR: 140257366 | УДК: 664.1.054 | DOI: 10.20914/2310-1202-2021-1-62-70
Simulation of the growth of sucrose crystals in a sugar-containing solution
Crystallization is one of the most important steps in the technological flow of commodity sugar. By its nature, it develops in a fairly wide temperature range, conditions of varying concentration of the solution, its peptization and other mass-exchange process of formation and growth of sugar crystals in a sugar solution by diffusion transfer in it sucrose molecules. To this it is necessary to add such complicating physical and mathematical formalization phenomena, affecting crystallization, such as the shape of the crystal, purity, viscous properties and surface tension of the solution, the presence of non-sugars, etc. Therefore, among the factors that determine the whole process, the factors usually take place, keeping among them only priority and most important from the point of view of the study. The article, unlike known analogues, provides justification and quantitative analysis of the kinetics of the sucrose crystallization process, taking into account the features of the crystal shape and diffusion properties of the solution. From the point of view of classical diffusion theory, the phenomenon of crystallization is interpreted as molecular with infinite rate of perilation from the source of diffusion transfer in the solution of sucrose molecules, so that the concentration in the sugar-containing liquid system is also supposed to change instantly at each point. However, since in the real world this effect is not observed, in order to resolve this contradiction, introduce the concepts of the indignant and unperturbed, separated by the diffusion front of the concentration of the regions of these phase states. Using the kinematic characteristics of the front, determine the time of the crystallization process in general in both phases. This allows us to calculate the processing period of the solution with greater accuracy than the results obtained on the basis of classical theory.
Текст научной статьи Моделирование процесса роста кристаллов сахарозы в сахарсодержащем растворе
This is an open access article distributed under the terms of the Creative Commons Attribution 4.0 International License
Семенов Е.В. и др.Вестник ВГУИТ, 2021, Т. 83, №. 1, С. 62-70 Введение
Хотя в настоящее время известно четыре научные гипотезы кристаллизации сахарозы, в число которых входит термодинамическая, диффузионная, молекулярно-кинетическая и дислокационная, по нашему мнению, наиболее простой и эффективной для прогнозирования протекания процесса кристаллизации является диффузионная гипотеза П.М. Силина [1–6]. В ней кристаллизация определяется как двухстадийное физическое явление: сначала инициация в чистом сахарсодержащем растворе в виде центров кристаллизации (первая стадия процесса), затем их эволюция – рост кристаллов (вторая стадия). По завершении интродукции в пересыщенный раствор затравочного материала, представляющего собой первую стадию процесса, сам процесс кристаллизации (вторая стадия) осуществляется при температуре Т > 50 °С в условиях градиента концентрации сахарозы в растворе на границе раздела фаз: “жидкость (раствор сахарозы) + твердое (кристалл)”, когда молекулы сахарозы адсорбируются на поверхности кристалла и встраиваются в кристаллическую решетку.
Следует отметить, что современная диффузионная теория процесса кристаллизации не учитывает влияния формы кристаллов на динамику кристаллообразования. Авторы статьи считают наиболее близкой к истине концепцию П.М. Силина [1], полагавшего, что на 1 м2 поверхности кристаллов конденсируется одинаковое количество сахара независимо от их размера.
Стоит обратить внимание на то, что в процессе кристаллизации условия роста кристаллов изменяются беспрерывно. Так, уменьшение объема и толщины слоя межкристального пространства, а также его концентрации наблюдается при росте размеров кристаллов. Помимо этого, вследствие имеющего место возрастания температуры в вакуум-аппарате в результате конденсации, интенсифицируется и собственно диффузионный перенос молекул сахарозы к поверхности кристалла.
Обзор посвященных научно-техническому обоснованию проблемы кристаллообразования сахарозы в вакуум-аппарате зарубежных литературных источников, с одной стороны, показывает, что по-прежнему, усилия специалистов-сахарников в большой степени направлены на изучение традиционной для сахарного производства задачи количественного анализа, в условиях изменения размера кристалла, процесса кристаллообразования в вакуум-аппарате. Так, работы [8, 9] посвящены оценке кинетики кристаллизации сахарозы на основе полученных в кристаллизаторах опытных данных при равномерно-монотонном убывании температуры раствора. Для чего при измерении размера кристалла был применен оптический микроскоп совместно со сканирующим электронным микроскопом типа SEM. При этом рассчитанные результаты сравниваются с полученными в других работах данными.
С другой стороны, особенность литературных источников, с очевидностью, указывает на ускорение перехода научного сообщества в области сахарного производства к использованию в исследованиях углубленного научного анализа, основанного на проведении опытов с использованием новейших образцов в области экспериментального оборудования [10–20]. Это связано с тем, что на практике в растворах, в том числе, и сахарсодержащих, явление кристаллообразования часто протекает в условиях, при которых, увеличивая свой размер, кристалл по габитусу отклоняется от своей классической формы в чистом растворе, т. е. становится дефектообразным. Данный фактор во многих исследованиях служит предметом пристального внимания ученых. Причем, поскольку этот процесс может инициироваться и выступающими в качестве центров кристаллизации имеющими размеры порядка одного нанометра молекулами сахарозы, то в статьях [10, 11] были изучены темпы роста кристаллизации сахарозы в чистых растворах при температуре в кристаллизаторе 313 К и пересыщении 0,094–0,181. При этом полученный кинетический коэффициент (коэффициент диффузии) изменился при начальном перенасыщении с D = 2,79× 10–7 до конечного D = 9,45х10-5 м2/с, соответствующий размер кристалла варьировался от 1,46 ×10–9до7,47× 10–9 м.
С теоретической позиции концепция трактовки явления кристаллизации, в том числе, и сахарозы как молекулярного диффузионного переноса массы (или, аналогично, явления переноса тепловой энергии в классической теории теплопроводности) скорость распространения возмущения от источника массы или энергии принимается бесконечной, вследствие чего концентрация раствора или температура среды изменяются мгновенно в каждой его точке. Чтобы учесть этот фактор вводят понятие «диффузионного фронта» х =р( t ) (рисунок 1). При этом для раствора на фронте осуществляются условия:
-
1) концентрация с равна концентрации невозмущенной области;
-
2) производная дс/дх на фронте полагается равной нулю, что влечет за собой плавное непрерывное распределение концентрации, а также потока концентрации в возмущенной области и во всей исследуемой области.
Принятые допущения означают, что процесс распространения концентрации осуществляется в две фазы.
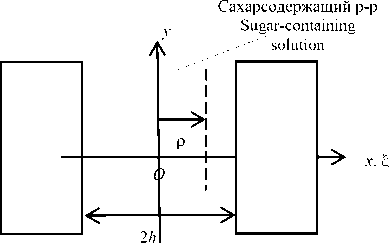
Рисунок 1. Схема к расчету процесса кристаллизации сахарозы в вакуум-аппарате

Кристалл сахарозы | Sucrosecrystal
Ниже, согласно предложенной П.М. Силиным диффузионной модели, с учетом перечисленных особенностей кинетики кристаллообразования в условиях молекулярной конденсации, проводится аналитический и численный анализ процесса кристаллизации сахарозы в вакуум-аппарате.
Постановка задачи
Ставится задача: при заданных геометрических и физико-механических параметрах процесса кристаллообразования получить, с учетом фактора наличия фронта концентрации, количественную оценку по времени эволюции роста размера кристаллов сахарозы, их объемного содержания при обессахаривании межкристального раствора в вакуум-аппарате.
Предварительно, с целью обосновать среднее значение h расстояния между частицами сахарозы исходя из величины объемной концентрации их в растворе принимается, что если V чс и V ут – соответственно, общий объем кристаллов и объем утфеля в вакуум-аппарате, η – объемная концентрация кристаллов в томже объеме, то в соответствии с принятой геометрической моделью жидкостной системы половина расстояния h между двумя соседними частицами составит [6]
h = 5 /(2пт), 0 < П < 1, (1) где η= V чс / V ут , δ – приведенный диаметр частицы сахарозы.
Считают, что массоперенос к частице из жидкой среды осуществляется симметрично и, кроме того, для выбранной расчетной модели с удовлетворительной точностью выполняются все предположения относительно физикомеханических свойств исследуемого объекта.
Поток концентрации q (объем вещества, отводимого с единицы поверхности в единицу времени) целевой субстанции (сахарозы) в направлении оси x в принятой одномерной модели массопереноса рассчитывают по формуле согласно первому закону Фика
∂с q = -D
∂ х
где D – коэффициент диффузии, с – объемная концентрация сахарозы.
При формализации физической модели предполагают, что концентрация сахарозы в исходном растворе одинакова по всему объему, центры кристаллизации распределены равномерно, кристаллы в процессе своего роста имеют форму, близкую прямоугольному параллелепипеду и сохраняют приблизительно схожие размеры. Кроме того, дополнительно считают, что начальный пересыщенный объем раствора включает как центры кристаллизации, достаточно большое количество молекул и частиц этого продукта настолько малым размером, что эти частицы диффундировали к поверхности кристалла и впоследствии встраивались в кристаллическую решетку.
В дальнейшем полагают, что процесс кристаллообразования сахарозы обусловлен ростом кристалла лишь в направлении большей из его граней, то есть, в направлении оси x . Тогда в качестве приближенной геометрической модели кристалла принимается полупространство x > h , ограниченное поверхностью x = h , к которому из области 0 ≤x ≤ h раствора диффундируют молекулы данного вещества (рисунок 1).
Более того, считают, что исследуемый процесс развивается, если концентрация сахарозы превышает растворимость ее или так называемую равновесную концентрацию, т. е. при наличии разницы в концентрации растворенного вещества в пересыщенном растворе.
Тогда с целью количественного анализа задачи о росте кристалла в соответствии с законом сохранения массы приходят к кинетическому уравнению [1]
д с _ д2 c
== г. , д t дx2
uде t – время, D – полагаемый постоянной величиной коэффициент диффузии.
В таком случае, если с п – исходная концентрация сахарозы в пересыщенном растворе, то решение уравнения (3) согласуют с начальным условием
с ( x, 0) = с п =const, 0 < x < h . (4)
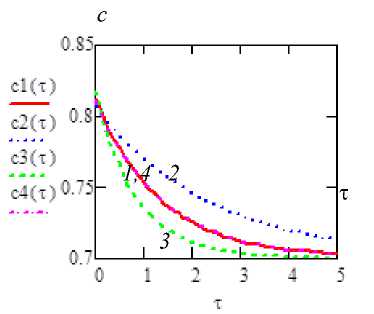
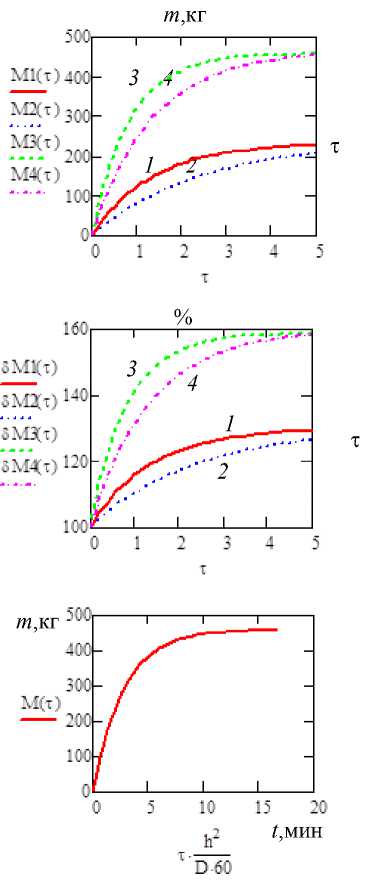
В свою очередь, поскольку посередине расстояния x = 0 между двумя соседними кристаллами концентрация раствора сахарозы достигает максимальное значение, то граничное условие имеет форму дс(0, t) _ „ v , = 0,0 ∂x В соответствии с концепцией Л.П. Хворо-вой и В.А. Коваленко [4, 5] через определенный промежуток времени по мере роста кристалла в растворе в контактирующем с поверхностью кристалла слое раствора скорость осаждения вещества определяется законом (2), что согласуется с представлением о наличии в растворе фронта концентрации. Тогда граничное условие на границе раздела раствор-кристалл x = 0 имеет следующий вид дс(0, t) г .. . —---= Y[c(0,t) - сн] ∂x или(6) дс(0, t) —---= а[c(0,t) - сн] ∂x где a =y/D, Y — так называемый коэффициент кристаллохимической реакции, характеризующий скорость поверхностных процессов, м/с, a - удельный коэффициент диффузии, м-1, сн -концентрация насыщенного раствора сахарозы вблизи кристалла. Решение задачи В дальнейшем, с целью упрощения проводимого исследования вводят безразмерные величины по зависимостям с- с xDt —— = и, 7= 5 , А с hh γh ah = D = Т Аc = сн - сп <10 где т - аналог числа Фурье (диффузионный), о - аналог числа Био(диффузионный). В таком случае задача (3)-(6) примет форму — /и, (8) дт д^^ v ’ и (5,0) = 0, (9) жо = 0>д5 (10) ди (1, t) .. . -------- + сти (1, t) = ст. ∂ξ (11) Прибегая к так называемому методу осреднения, при исследовании задачи с учетом наличия фронта концентрации, решают ее по двум фазам, заменяя левую часть уравнения (8) ее осредненным значением по интервалу (р, 1), а именно, вводят в рассмотрение функцию [7] 1 1 ди 2ф(в)(т)= ----J — d5, 02) 1 - РР дт где в - индекс фазы (в = 1,2);р - безразмерная координата фронта концентрации. Тогда вместо уравнения (8) используют приближенное соотношение д2 и(1) д5 = 2ф(1)(т), удовлетворяющее, согласно (8)-(11) условиям и (1)(р,т) = 0,(14) [диWfeT) дг] р = 0,(15) [ди (1)(^,т) /д£ + о и (1)(^,т)]^ =1 =о,(16) и, кроме того, вытекающему из (12) равенству 2ф(1)(т) = -^j ^Ц- d5.(17) 1 — Рр дт Проводя последовательно интегрирование в (13), имеют ди(1)(^,т) /д^ = 2ф(1)(т)^ +А1,(18) и (1)(^,т) =ф(1)(т^2 +А1^ +В1.(19) Согласуя (15)-(17) с условиями (14)-(16), для определения неизвестных ф(1)(т), А1, В1, с использованием (18), (19), получают систему алгебраических уравнений (о + 2)ф(1) + (о + 1) А1 + оВ1 =о,(20) р2ф(1) + рА1 + В1 = 0,2рф(1) + А1 = 0,(21) решением (20) является ф(1)(т) =о/D1, А1 =-2ор/D1, В1 =ор2/D1, (22) где обозначено D1 =о(1 - р)2 + 2 (1- р).(23) Подставляя (21) в (19), находят и(1)(^,т) =о(^ - р)2/D1. Функция р =р(т) определяется с помощью (17) Поскольку, согласно (23) ^Ц- = - -^2 dp[2D1(5 - Р) + ^51(5 - Р )2], ∂τ D dτ dρ то после подстановки в уравнение (17) значения ф(1)(т) и значения ди(1)/дт, получают D1(1 — P) = = — dP [2 DJ^f—р) df + dD^f—p )2 df], dT p dp)p откуда, после интегрирования 6 D1(1 — p) = —(1 — p )2dP [3 D1 + (1 — p) DA. dT dp Поэтому с учетом (22) имеют dDL = — 2[а(1 — p) + 1], d p Интегрируя, последовательно, по ξ уравнение (28), имеют: 5и^т) /5^ =2ф(2|(т)^+А2(т),(32) и ^т) =ф(2)(т)^2 +А 2^ +В 2.(33) Поскольку из выражений (30), (32) вытекает, что А2(т) = 0, то в таком случае согласно (33) получают и ^т) =ф(2|(т)^2+В 2.(34) 3 D1 + (1 — p) dD = 7(1 — p )2 + 4(1 — p). d р В результаты чего приходят к дифференциальному уравнению относительно р =р(т) 67(1 — Р) + 21 = — (1 — р) ~ 1^(1 — р) + 4], dT или, после разделения переменных к соотношению (1 — р )7(1 — р) + 4] dt =--dp. (24) 67 (1 — р) + 2] 7 Поскольку выполняется начальное условие т = 0 при р = 1, то интегрируя это выражение слева по т от нуля до т, справа - по р от р до единицы, исходя из (24), т. е., выполняя процедуру Удовлетворяя условию (31), имеют 2ф(2)(т) + о[ф(2)(т) + В2] =о, откуда находят В2 = 1 - (о + 2)ф(2)(т)/о. В таком случае (34) принимает вид и^j) = 1 - ф(2)(т) [(о + 2) /о - Й. (35) Функция ф(2)(т) определяется на основе условий (27), (29), с учетом того, что, с одной стороны,5и(2)(1,т) /5т = -5ф(2|(т)/5т•[(о + 2)/о -с2], с другой стороны p (t )=-1 d-Ф2- i< 2 dT 7 + 2 — т 1(1 — p)[7 (1 — p) + 4] J, 6[а(1 — p) + 2] , получают частное решение (1 — p)2 (1 — р) т =--1-- — f2) df = — 1 d^(2)2а + 6 • 3а Ль [1+р1^ 3ст2 I 2 Продолжительность первой фазы находят путем подстановки р =0 в (25) 1 1 Т1 =— + — 12 3о Т2"^ )■ (26) Если (численным путем) разрешить (25) относительно р как неявную функцию, то тем самым определяют Р =р(т). Вторая фаза. по соотношению и фронт концентрации Функцию ф(2)(т) вводят 1 5 (2) 2ф<2|(т) -J u df J от 0 T L Задача ставится таким образом, чтобы по- лучить решение уравнения 52uи , ,,v ' ^Г = W). удовлетворяющее условиям: и(2)(0,Т1) = 0, 5и(2)(0,т) /5^ = 0, 5и(2)(1,т) /5^ + о и(2)(1,т) =о, 6 dT , и поэтому, разделяя далее переменные в этом уравнении и интегрируя полученное в результате соотношение, находят общее решение ф(2)(т) =D2ехр [-3от/(о +3)], где D2 - произвольная постоянная. Тогда в соответствии с (35) и(2)(f, t ) = 1- D2f 7+2 I 7 — f2 Iехр —3s(t-tx) . (s + 3) , (36) где т1определяют по (26). Далее, принимая во внимание (29), находят D2 =о/(о + 2) ехр [3от1 /(о +3)]. После чего, подставляя D2 в (36), окончательно получают и(2) (f, t) = 1- s (s+2) —3 s (t - tx) . (s+ 3) Таким образом, в рамках принятой физикоматематической модели задача об определении поля концентрации сахарозы в области между двумя смежными кристаллами сахарозы в вакуум-аппарате решена полностью. В дальнейшем, возвращаясь согласно (7) к исходному значению с концентрации сахарозы в сахарсодержащем растворе, имеют с (^,т) = сп+ и(2|(^,т)Лс, (38) где и(2)(^,т) определяется по соотношению (37). Для того чтобы рассчитать эффективность процесса кристаллизации сахарозы, предварительно, на базе зависимости (2), (37) определяется поток q концентрации. При этом, поскольку в соответствии с (37), (38) имеют дс дu(2) . 2ос -Ac -3 s (t -t.) — =--Ac = — --ехр — д^ д^ о + 2 [_ (s + 3) или, согласно (7), в размерных переменных — =----, м-1, (40) то в соответствии с (2), (40) дх h 6^ справедлива формула q = D дс/дх. Поэтому поток q концентрации на поверхности x =h(ξ = 1), в явной форме выражается в виде 2оАcD -3s (t -t1) q =------ехр — (o + 2) h (s + 3) В свою очередь, так как за время dт на той же поверхности осаждается объем сахарозы qh2 dt 2оА ch dQ = = ехр D (о + 2) -3о (г - г1) (о + 3) dt то количество А Vсахарозы, оседающей за период времени т получают, интегрируя выражение (41) в пределах от 0 до т. В результате имеют Q (t, A, h) = А V 2оАch г = ехр (о + 2) J р -3о (г - г1) (о + 3) dr = 2(о + 3) h А c = —--------ехр 3 3(о + 2) Р^ или по массе о (г1 - г) (о + 3) _ ог - exp 3 , . L (о + 3) Q(т, D, h) = Q(т, D, h)xpi, кг/м2, где pi - плотность сахарозы. , м3/м2 Пусть в одном кубометре утфеля содержится, в равных объемных долях п, кристаллы сахарозы размером 8 =10-4 м и межкристального раствора коэффициентами, соответственно, пересыщения сп = 0,8 и насыщения сн = 0,7. И пусть, по соглашению, коэффициент кристаллохимической реакции у = 10-6 м2/с [4, 5], коэффициент диффузии раствора De [10-10,5x10-11], м2/с [2]. Требуется на базе выбранных геометрических и физических параметров процесса определить по массе отнесенный к 1 м3утфеля полный молекулярный расход межкристального раствора в зависимости от времени проведения процесса кристаллизации. Предварительно, поскольку, согласно формуле (1) при п = 0,5 половина расстояния между частицами сахарозы составляет h = 6,3 х10-5 м, то в расчетах принимали he[5x10-5; 10-4], м. В свою очередь, так как количество частиц сахарозы равно пх6/(п83), то их общая поверхность S составляет S = 3/8 = 3х104 1/м3. С учетом (38) на рисунок 2 представлены графики зависимости концентрации сахарозы на середине расстояния между двумя смежными частицами (т. е. при x = 0) Как следует из анализа поведения кривых (рисунок 2), к моменту т = 5 концентрация сахарозы посередине между двумя кристаллами в результате конденсации молекул сахарозы на кристаллах примерно выравнивается, приближаясь к значению сн = 1,1 насыщения. Рисунок 2. Зависимости концентрации сахарозы между двумя смежными частицами от безразмерного времени т процесса обработки центров кристаллизации в сахарсодержащем растворе при различных значениях коэффициента D диффузии и половины расстояния h между кристаллами (h = 5х10-5 м: 1 - D = 5х10-11, 2 - D =10-10 м2/с; h = 10-4 м: 3 - D = 5х10-11, 4 – D = 10-10 м2/с) Figure 2. Dependences of the concentration of saccharose between two adjacent particles on the dimensionless time treatments of the processing of crystallization centers in a sugar-containing solution at different values of the diffusion coefficient D and half the distance h between crystals (h = 5х10-5 m: 1 - D = 5х10-11,2 -D = 5х10-10 m2/s; h =10-4 m: 3 - D = 5х10-11,4 - D = 5х10-10 m2/s) Рисунок 3. Зависимости от временит массы m конденсированной на поверхности кристалла сахарозы при различных значениях коэффициента D диффузиии половины расстояния h между кристаллами (h = 5x10-5 м: 1 - D = 5х10-11, 2 - D = 10-10 м2/с; h = 10-4 м: 3 - D = 5х10-11, 4 - D = 10-10 м2/с) Figure 3. Time т dependences of the mass m of sucrose condensed on the surface of the crystal at different values of the coefficient D diffusion and half distance h between crystals (h = 5х10-5 m: 1 - D = 5х10-11 m2/s, 2 - D = 10-10 /с; h = 10-4 м: 3 - D = 5x 10-11,4 - D = 10-10 m2/s) Рисунок 4. Зависимости от времени т относительной массы 5m/mо, % конденсированной на поверхности кристалла сахарозы при различных значениях коэффициента D диффузии и половины расстояния h между кристаллами (h = 5х10-5 м: 1 - D = 5х10-11, 2 - D = 10-10 м2/с; h = 10-4 м: 3 - D = 5х10-11, 4 - D = 10-10 м2/с) Figure 4. Time т dependences of the relative mass 5m/m0, % of sucrose condensed on the surface of the crystal for different values of the diffusion coefficient D and half the distance h between the crystals (h = 5х10-5 m: 1 - D = 5х10-11, 2 - D = 10-10 m2/с; h = 10-4 м: 3 - D = 5х10-11, 4 – D = 10-10 m2/s) Рисунок 5. Зависимость от времени массы осадившейся на поверхности взвеси из кристаллов сахарозы Figure 5. Time dependence of the mass of a suspension of sucrose crystals deposited on the surface Отраженные графиками рисунок 3, 4 результаты вычислений на базе (42) обнаруживают согласованность полученных результатов количественного моделирования исследуемого процесса с физическим смыслом задачи. А именно, с одной стороны, обессахарива-ние раствора по массе в связи с кристаллизацией сахарозы, как по абсолютному (рисунок 3), так и относительному к исходному (рисунок 4) значениям, по прошествии времени экспоненциально возрастает, и тем больше, чем выше значение коэффициента диффузии (например, на рисунок 3, кривая 2 расположена выше кривой 1). С другой стороны, аналогичным образом, графически, например, рисунком 4 отражена зависимость прироста массы от времени: при коэффициенте диффузии D = 5х 10-11 м2/с, с увеличением расстояния h (и, следовательно, с уменьшением счетной концентрация частиц в растворе), интенсивность процесса кристаллизации снижается – кривая 3 ниже кривой 1. Если, при тех же исходных данных по параметрам процесса расчет проводится в реальном временном режиме, то в таком случае, например, при значениях параметров h = 10-4 м и D = 5х10-11 м2/с графическая зависимость от времени t массы m осадившейся на поверхности взвеси из кристаллов сахарозы в вакуум-аппарате имеет показанный на рисунок 5 вид. Как видно по рисунок 5, процесс кристаллизации завершается практически к пятнадцатой минуте и для возобновления его необходимо раствор “раскачивать”, обогащая его пресыщенной сахарсодержащей субстанцией. Однако следует отметить, что отраженные рисунками 2–5 результаты расчетов, из-за того в них не учитывается эффект истощения раствора сахарозой (в частности, коэффициент А = сн - сп полагается постоянной величиной), приводят к завышенным, по сравнению с наблюдаемыми на практике, данными. Семенов Е.В. и др.Вестник ВГУИТ, 2021, Т. 83, №. 1, С. 62-70 Заключение На основе модели диффузионного массо-переноса целевого продукта, такого как сахароза, из пересыщенного межкристального раствора к кристаллу сахарозы, основанного на уравнении нестационарной диффузии (второго закона Фика), обосновывается физико-математическая модель по прогнозированию протекания процесса кристаллизации сахарозы в данном растворе при учете кинетики фронта концентрации. Предлагается аналитический аппарат для расчета зависимости массы целевого продукта от времени в результате процесса кристаллизации. На основе разработанного аналитического аппарата проводится количественное моделирование эффективности данного процесса.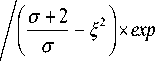
Список литературы Моделирование процесса роста кристаллов сахарозы в сахарсодержащем растворе
- Силин П. М. Технология сахара. Рипол Классик, 2013.
- Магомедов М. Г. Технология получения пасты из сахарной свеклы //Вестник ВГУИТ. 2015. № 3. С. 138-141. doi: 10.20914/2310-1202-2014-3-138-141
- Славянский А.А., Семенов Е., Лебедева Н., Неделькин В. и др. Математическое моделирование кинетики кристаллизации гидратной глюкозы // Сахар. 2014. № 5. С. 45-49.
- Хворова JI.C. Трехпродуктовая технологическая схема получения глюкозы с кристаллизацией двух продуктов в ангидридной форме // Пищевая промышленность. 2017. № 9.
- Хворова JI.C., Баранова JI.B., ГоменюкВ.А. Способ получения кристаллической ангидридной глюкозы. 2018.
- Семенов Е.В., Славянский А.А. Моделирование процесса кристаллизации и центрифугирования. М.: Спутник+, 2015. 217 с.
- Кулинченко В.Р., Мирончук В.Г. Промышленная кристаллизация сахаристых веществ. 2012.
- Berzi К., Suryanarayanan R. Compression-induced crystallization in sucrose-polyvinylpyrrolidone amorphous solid dispersions//Crystal Growth & Design. 2018. V. 18. №2. P. 839-848. doi: 10.1021/acs.cgd.7b01305
- Hubbes S.S., Braun A., Foerst P. Sugar particles and their role in crystallization kinetics and structural properties in fats used for nougat creme production // Journal of Food Engineering. 2020. V. 287. P. 110130. doi: 10.1016/j.jfoodeng.2020.110130
- Velazquez-Camilo O., Bolanos-Reynoso E., Rodriguez E., Alvarez-Ramirez J. Characterization of cane sugar crystallization using image fractal analysis // Journal of Food Engineering. 2010. P. 77-84. doi: 10.1016/j.jfoodeng.2010.03.030
- Khaddour I., Bento L., Ferreira A., Rocha F. Kinetics and thermodynamics of sucrose crystallization from pure solution at different initial supersaturations // Surface Science. 2010. P. 1208-1214. doi: 10.1016/j.susc"2010.04.005
- Frenzel S. Crystallization Schemes in the Sugar Industry// ChemBioEng Rev. 2020. №5. P. 1-9. doi: 10.1002/cben.202000010
- Thakral S., Sonje J., SuryanarayananR. Anomalous behavior of mannitol hemihydrate: Implications on sucrose crystallization in colyophilized systems // International journal of pharmaceutics.2020. V. 587. P. 119629. doi: 10.1016/j.ijpharm.2020.119629
- de Castro B. J. C. et al. Sucrose crystallization: modeling and evaluation of production responses to typical process fluctuations //Brazilian Journal of Chemical Engineering" 2019. V. 36. № 3. P. 1237-1253. doi: 10.1590/0104-6632.20190363s20180240
- SinghK, Gupta S.P., Kumar A., Kumar A. The effect of high intensity ultrasound (HIU) on the kinetics of ciystallizationof sucrose: Elimination of latent period//Ultrasonics sonochemistiy. 2019. V. 52. P. 19-24. doi: 10.1016/j.ultsonch.2018.05.030
- Chakir A., Romane A., Marcazzan G.L., Ferrazzi P. Physicochemical properties of some honeys produced from different plants in Morocco // Arabian Journal of Chemistry. 2016. V. 9. P. S946-S954. doi: 10.1016/j.arabjc.2011.10.013
- Nayik G.A., Dar B.N., Nanda V. Physico-chemical, rheological and sugar profile of different unifloial honeys from Kashmir valley of India// Arabian Journal of Chemistry. 2019. V. 12. № 8. P. 3151-3162. doi: 10.1016/j.arabjc.2015.08.017
- Batal H., Hasib A., Ouatmane A., Dehbi F. et al. Sugar composition and yield of syrup production from the pulp of Moroccan carob pods (Ceratonia siliqua L.) // Arabian Journal of Chemistry. 2016. V. 9. P. S955-S959. doi: 10.1016/j.arabjc.2011.10.012
- Boussaid A., Chouaibi M., Rezig L., Hellal R. et al. Physicochemical and bioactive properties of six honey samples from various floral origins from Tunisia // Arabian journal of chemistry. 2018. V. 11. № 2. P. 265-274. doi: 10.1016/j.arabjc.2014.08.011
- Torr6nen R., Hellstrom J., Mattila P., Kilpi K. Postprandial glycaemic response to berry nectars containing inverted sucrose // Journal of nutritional science. 2017. V. 6. doi: 10.1017/jns.2016.44


