Модифицирующее воздействие слабыми широкополосными электромагнитными полями (ЭМП) на процесс метастазирования меланомы В16 у мышей линии C57BL/6
Автор: Турканов И.Ф., Аистова Л.Г., Флакс Г.А., Болоцкова П.Н., Грязнов В.Г.
Рубрика: Ветеринария
Статья в выпуске: 1 т.265, 2026 года.
Бесплатный доступ
Резистентность меланомы кожи к стандартным схемам лекарственной терапии диктует необходимость поиска новых подходов к лечению. В связи с этим актуальным направлением является изучение влияния физических факторов, в частности, слабых неионизирующих излучений, на процессы опухолевого роста. Целью данной работы стало исследование метастазирования экспериментальной меланомы В16 у мышей линии C57BL/6 под воздействием слабого неионизирующего нетеплового импульсного электромагнитного излучения. Эксперимент проведен на базе Дальневосточного ГАУ. В исследование были включены 120 самцов мышей в возрасте 8 недель, разделенных на две группы (n=60). Животным внутрикожно в правую боковую область инокулировали 1 млн клеток мышиной меланомы В16. Специфическая противоопухолевая терапия в обеих группах не проводилась. Мыши опытной группы с 9-го дня после трансплантации опухоли ежедневно в течение 60 минут подвергались воздействию аппарата «ТОР». Контрольная группа аналогичных процедур не получала. Оценка размеров и локализации метастазов в регионарных лимфатических узлах и отдаленных органах осуществлялась с помощью рентгенологического и ультразвукового исследования. Статистически значимые различия в максимальных линейных размерах метастазов между группами были зафиксированы на 10, 21 и 29 сутки. В контрольной группе метастазирование в легочную ткань регистрировалось уже на 7 сутки. В опытной группе первые признаки поражения легких появились лишь на 22-е сутки, а к 52-м суткам метастазы в легких рентгенологически не определялись. Ультразвуковое исследование на 32-е сутки также не выявило метастазов в периферических лимфатических узлах и внутренних органах у животных, получавших терапию. Таким образом, применение неинвазивной широкополосной электромагнитной терапии способствует существенному замедлению темпов метастазирования меланомы В16 в органы грудной клетки и индуцирует регрессию метастатических очагов во внутренних органах.
Мыши, онкология, опухоль, меланома B16, рак кожи, электромагнитное излучение, ЭМИ, замедление развития опухоли, цитоплазматический кальций, синтаза оксида азота
Короткий адрес: https://sciup.org/142247541
IDR: 142247541 | УДК: 591.29;615.8;616.006 | DOI: 10.31588/2413_4201_1883_1_265_59
Modifying effect of weak broadband electromagnetic fields (EMF) on the process of B16 melanoma metastasis in C57BL/6 mice
The resistance of skin melanoma to standard drug therapy regimens necessitates the search for new treatment approaches. Therefore, studying the influence of physical factors, particularly weak non-ionizing radiation, on tumor growth processes is a relevant direction. The aim of this study was to investigate the metastasis of experimental B16 melanoma in C57BL/6 mice exposed to weak non-ionizing non-thermal pulsed electromagnetic radiation. The experiment was conducted at Far Eastern State Agrarian University. The study included 120 8-week-old male mice, divided into two groups (n=60). The animals were inoculated intradermally in the right lateral region with 1 million B16 murine melanoma cells. No specific antitumor therapy was administered to either group. Mice in the experimental group were exposed to TOR apparatus daily for 60 minutes starting on the 9th day after tumor transplantation. The control group did not receive similar procedures. The size and location of metastases in regional lymph nodes and distant organs were assessed using X-ray and ultrasound. Statistically significant differences in the maximum linear dimensions of metastases between the groups were recorded on days 10, 21 and 29. In the control group, metastasis to lung tissue was recorded as early as day 7. In the experimental group, the first signs of lung damage appeared only on the 22nd day and by the 52nd day, lung metastases were not detectable radiographically. Ultrasound examination on the 32nd day also revealed no metastases in the peripheral lymph nodes or internal organs in the animals receiving the therapy. Thus, the use of noninvasive broadband electromagnetic therapy significantly slows the rate of metastasis of B16 melanoma to the chest organs and induces regression of metastatic lesions in internal organs.
Текст научной статьи Модифицирующее воздействие слабыми широкополосными электромагнитными полями (ЭМП) на процесс метастазирования меланомы В16 у мышей линии C57BL/6
Цитостатические и цитотоксические свойства определяются уровнем продукции различных медиаторов: активных форм кислорода, интерферонов, интерлейкинов, цитокинов, а также лизосомальных ферментов [3]. Данные вещества способны стимулировать клеточную миграцию, принимая участие в управлении процессами альтерации и регенерации тканей. В первой части нашего исследования терапия слабым неионизирующим нетепловым широкополосным импульсным электромагнитным излучением мышей линии C57BL/6, больных меланомой В16, продлевает длительность жизни у 3,3% особей (2 животных из 60). Кроме того, данная терапия у мышей линии C57BL/6, больных меланомой В16, однозначно приводит к уменьшению объема опухоли с 19-22 суток применения. В свете этих данных представляется интересным изучение вопроса метастазирования меланомы В16 у мышей линии C57BL/6.
Клинически значимое уменьшение размеров меланомы B16, наблюдаемое при воздействии импульсного широкополосного электромагнитного излучения (ЭМИ), может быть следствием прямого модулирующего воздействия на внутриклеточные процессы опухолевых клеток [4]. Согласно литературным данным, ключевым первичным звеном этого воздействия является способность ЭМИ вызывать высвобождение ионов кальция (Ca2+) из внутриклеточных депо, выступая универсальным сигнальным триггером [5]. Последующая активация кальций-зависимых путей, таких как синтез оксида азота (NO), может приводить к митохондриальной дисфункции, окислительному стрессу и, в конечном итоге, к гибели клеток [6, 7]. Таким образом, предполагаемый механизм предполагает прямое цитотоксическое действие ЭМИ, не требующее участи интактной иммунной истемы [8].
G. Poste и соавт. (1981) провели анализ метастатических свойств клонов, выделенных из клеточных линий мышиной меланомы B16 (B16-F1 и F10). В результате исследований они демонстрируют значимую клеточную гетерогенность и наличие субпопуляций, обладающих сильно различающимися метастатическими свойствами [9]. Однако, в контексте проведенного исследования по изменению размеров меланомы под воздействием электромагнитного излучения представляется необходимым изучить изменения размеров и количества метастазов этой опухоли.
Цель исследования - изучение процессов метастазирования меланомы В16 у мышей линии C57BL/6 в условиях слабого неионизирующего нетеплового широкополосного электромагнитного излучения.
Условия, материалы и методы. Открытое, нерандомизированное исследование проводилось в условиях вивария факультета ветеринарной медицины, зоотехнии и биотехнологий Дальневосточного ГАУ в период с мая 2025 года по декабрь 2025 г. Объектом исследований явились мыши, имеющие сертификат здоровья и качества, доставленные из НПП «Питомник лабораторных животных» Филиала ФГБУН «Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова» РАН.
В питомнике самцам линии C57BL/6 (n=120), черной масти, выполнялось внутрикожное введение суспензии клеток меланомы B16 на правом боку, в количестве 1 млн клеток/гол. Возраст мышей на начало эксперимента - 8 недель, масса - от 22 до 28 грамм.
Животные были разделены на 2 группы по 60 особей в каждой.
Опытную группу составили особи, получающие с девятого дня болезни, в течение 266 суток, ежедневное аппаратное лечение ТОР в течение 60 минут.
Контрольную группу - особи, которым лечение не проводилось.
Для лечения мышей использовали Аппарат неинвазивной электромагнитной терапии «ТОР» (здесь и далее Аппарат «ТОР»), апробированный в клинике для лечения пациентов с COVID-19 Самарского государственного медицинского университета [10].
Для определения размеров локализации и количества метастазов в брюшной полости УЗИ диагностику на аппарате УЗИ Mindrey ve-tus 7 в условиях ветеринарной клиники «Энимал Сити». Рентгенологические исследования, для выявления наличия метастазов в легких и костных структурах проводили на рентгеновском коллиматоре Ralco R72 в условиях ветеринарной клиники «Энимал Сити». Ультразвуковую и рентгеновскую диагностику проводили на 7, 8, 10, 14, 22, 23, 29, 32, 40, 52, 70 и 184 сутки.
При проведении научных исследований придерживались требований биоэтики согласно Национальным «Общим этическим принципам экспериментов на животных», соответствующим положению «Европейской конвенции о защите позвоночных животных, которые используются для экспериментальных и других научных целей» от 18 марта 1986 г., а также рекомендаций Коллегии Евразийской экономической комиссии № 33 от 14 ноября 2023 г. «О руководстве по работе с лабораторными (экспериментальными) животными при проведении доклинических (неклинических) исследований. Исследования проведены с разрешения локального этического комитета ФГБОУ ВО Дальневосточный ГАУ (протокол № 2 от 28.05.2025 г.).
Статистическую обработку результатов исследования производили по общепринятым методикам с помощью программы Microsoft Excel 2010. Для определения доверительного интервала использовали таблицу Р. Б. Стрелкова. Изменение количественных признаков определяли с помощью непараметрического критерия Манна - Уитни. Сила линейной зависимости между двумя переменными оценивалась с помощью критерия Пирсона.
Результаты и обсуждение. Количество и локализация метастазов в брюшной полости имела самый разнообразный характер. Были поражены как регионарные, так и внутрибрюш-ные лимфоузлы. Хотя количественный параметр метастазирования учесть не представлялось возможным, путем ультразвукового исследования было выявлено обсеменение селезенки, почек, печени, а также общий канцероматоз брюшины и брыжейки тонкой кишки (табл. 1).
Таблица 1 - Метастазирование меланомы В16 во внутренних органах мышей линии С57BL/6 в подопытных группах (n=60 в каждой группе)
|
Поражения внутренних органов/ метастазирование (количество) |
Периоды УЗИ диагностики, сутки |
|||||||
|
7 |
10 |
16 |
20-21 |
29 |
32 |
40 |
||
|
Лимфатические узлы |
Контрольная |
0 |
10 |
10 |
11 |
7 |
2 |
3 |
|
Опытная |
0 |
10 |
7 |
12 |
13 |
1 |
2 |
|
|
Селезенка |
Контрольная |
0 |
3 |
6 |
3 |
5 |
1 |
0 |
|
Опытная |
0 |
7 |
5 |
8 |
7 |
0 |
0 |
|
|
Почки |
Контрольная |
0 |
2 |
3 |
4 |
6 |
2 |
0 |
|
Опытная |
0 |
2 |
0 |
3 |
10 |
0 |
0 |
|
|
Печень |
Контрольная |
0 |
1 |
0 |
4 |
7 |
0 |
0 |
|
Опытная |
0 |
0 |
0 |
3 |
10 |
0 |
0 |
|
|
Канцероматоз брыжейки |
Контрольная |
0 |
1 |
0 |
4 |
6 |
0 |
0 |
|
Опытная |
0 |
0 |
0 |
5 |
10 |
0 |
0 |
|
Необходимо отметить, что повышенная реактивность мышей приводила к уменьшению и элиминации метастазов на 32 сутки исследования. Однако в опытной группе на фоне лечения данный процесс протекал более интенсивно и к 32 суткам метастазиро- вания внутренних органов не было выявлено. Отмечалось лишь поражение лимфатических узлов.
Рентгенологические данные о распространенности метастатического поражения грудной клетки представлены в таблице 2.
Таблица 2 – Метастатическое поражение органов грудной полости и костей тела при меланоме В16 у мышей в динамике
|
Периоды измерений, сутки |
Все го голов |
Патологические изменения/метастазы |
||||||||
|
легкие |
сердце |
деформация костей |
уплотнение ткани в области привития опухолевых клеток |
|||||||
|
n |
% |
n |
% |
n |
% |
n |
% |
|||
|
7 |
Конт. |
7 |
3 |
48,2 |
0 |
0 |
0 |
0 |
4 |
57,1 |
|
Опыт. |
9 |
0 |
0 |
0 |
0 |
0 |
0 |
1 |
11,1 |
|
|
13 |
Конт. |
6 |
2 |
33,3 |
0 |
0 |
0 |
0 |
6 |
100,0 |
|
Опыт. |
9 |
0 |
0 |
0 |
0 |
0 |
0 |
8 |
88,9 |
|
|
14 |
Конт. |
8 |
1 |
12,5 |
1 |
12,5 |
0 |
0 |
7 |
77,8 |
|
Опыт. |
11 |
0 |
0 |
1 |
9,1 |
0 |
0 |
9 |
81,8 |
|
|
22 |
Конт. |
20 |
20 |
100,0 |
0 |
0 |
2 |
10,0 |
20 |
100,0 |
|
Опыт. |
20 |
19 |
95,0 |
1 |
5,0 |
2 |
10,0 |
20 |
100,0 |
|
|
23 |
Конт. |
19 |
9 |
47,4 |
0 |
0 |
2 |
10,5 |
17 |
89,5 |
|
Опыт. |
20 |
10 |
50,0 |
0 |
0 |
1 |
5,0 |
20 |
100 |
|
|
29 |
Конт. |
18 |
7 |
38,9 |
0 |
0 |
4 |
22,2 |
17 |
94,4 |
|
Опыт. |
21 |
11 |
52,4 |
0 |
0 |
3 |
14,3 |
19 |
90,5 |
|
|
40 |
Конт. |
2 |
0 |
0 |
0 |
0 |
1 |
50,0 |
2 |
100,0 |
|
Опыт. |
3 |
1 |
33,3 |
0 |
0 |
0 |
0 |
1 |
33,3 |
|
|
52 |
Конт. |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
1 |
100,0 |
|
Опыт. |
2 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
|
70 |
Конт. |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
Опыт. |
2 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
По данным таблицы 2 видно, что метастазирование в легкие у животных контрольной группы наступало уже на 7 сутки исследования, в опытной группе данный процесс определялся на рентгенограммах с 22 суток. В дальнейшем, с 52 суток метастатическое поражение по результатам рентгенологического исследования грудной клетки полностью исчезает.
Дальнейшее исследование показало, что различия между максимальными линейными размерами метастазов для опытной и контрольной групп являются статистически значимыми на 10, 21 и 29 день. Причем в опытной группе на фоне ЭМИ данные размеры были статистически значимо меньше, что проявилось особенно отчетливо на 29 день (рис.1). При этом необходимо отметить, что количество групп на день измерения отличалась. Кроме того, не представлялось возможным оценить динамику изменения размеров конкретного метастатического узла.
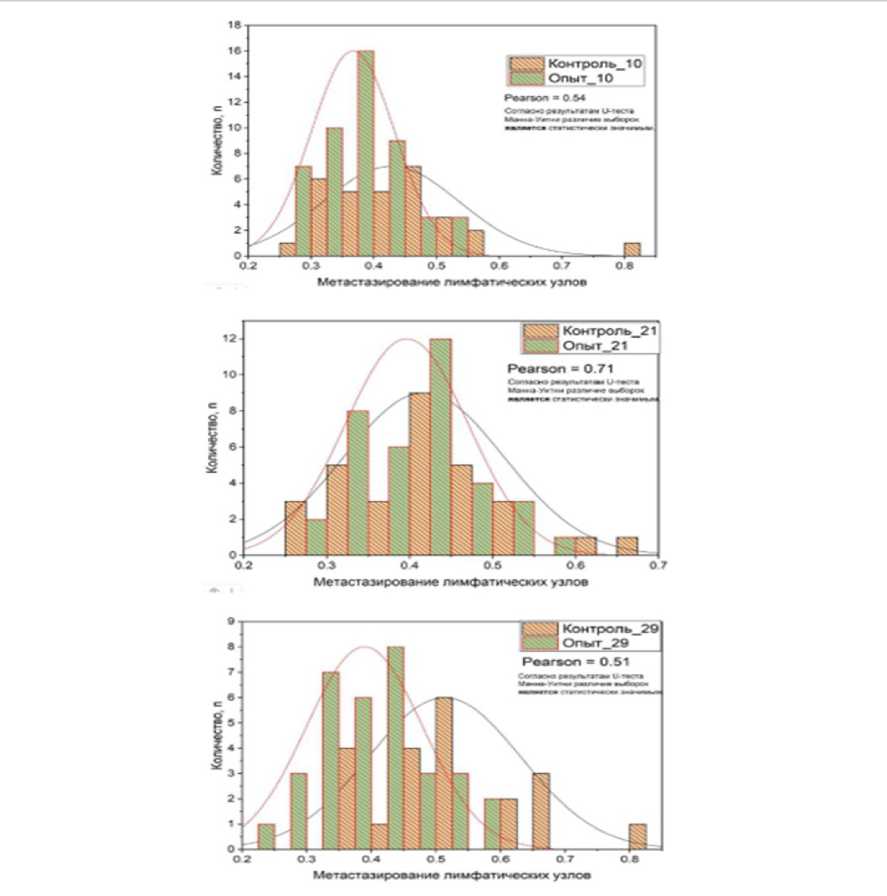
Рисунок 1—Динамика максимальных линейных размеров метастазов в регионарных лимфоузлах у мышей контрольной и опытной групп
Обсуждение. Электромагнитная терапия по результатам нашего исследования в ряде случаев приводила к статистически значимому уменьшению линейного размера метастазов меланомы B16 у мышей линии C57BL/6. Это позволяет предположить реализацию специфического цитотоксического механизма, направленного непосредственно на опухолевые клетки. Полученные данные согласуются с концепцией прямого модулирующего воздействия ЭМИ на внутриклеточный гомеостаз. Кроме этого, воздействие широкополосных электромагнитных полей ускоряло элиминацию метастатического поражения в брюшной полости и грудной клетке. Как показывают литературные данные, фундаментальным триггером биологического действия ЭМИ является его способность влиять на ионный транспорт, в первую очередь вызывая высвобождение ионов кальция (Ca2+) из внутриклеточных депо [11]. Резкий рост концентрации цитоплазматического Ca2+ запускает каскад вторичных факторов. В частности, связываясь с кальмодулином (CaM), Ca2+может активировать конститутивную синтазу оксида азота (cNOS), что приводит к выбросу NO [12]. В условиях опухолевой ткани этот, как правило, регуляторный путь, может приобретать цитотоксические свойства. Известно, что высокие концентрации NO способны подавлять ключевые ферменты митохондриальной дыхательной цепи (например, цитохром с-оксидазу), ингибируя окислительное фосфорилирование и синтез АТФ. Нарушение работы дыхательной цепи является прямым источником резкого увеличения генерации активных форм кислорода (АФК) митохондриального происхождения. Эти АФК, в свою очередь, по принципу положительной обратной связи способны активировать провоспалительные внутриклеточные каскады, такие как инфламмасо-ма NLRP3, что еще более усугубляет повреждение митохондрий и ведет к необратимому падению их мембранного потенциала [13, 14].
Выводы:
-
1. Ежедневное воздействие слабым импульсным широкополосным электромагнитным излучением (ЭМИ) с помощью аппарата «ТОР» в течение 60 минут, начиная с 9-го дня после прививки меланомы B16, приводит к статистически значимому уменьшению размеров метастазов в регионарных лимфатических узлах у мышей линии C57BL/6 по сравнению с контрольной группой по U-критерию Манна-Уитни и t-критерию Стьюдента.
-
2. Полученные данные демонстрируют противоопухолевую эффективность неинвазивной электромагнитной терапии в отношении метастазирования меланомы B16 в условиях, когда не применялись стандартные методы лечения (лучевая и химиотерапия).
-
3. Наблюдаемый терапевтический эффект позволяет рассматривать широкополосное ЭМИ как перспективное физическое воздействие для разработки новых неинвазивных стратегий лечения резистентных опухолей, таких как меланома.


