Мультиплексная ПЦР для индикации и дифференциации возбудителей респираторных вирусных инфекций крупного рогатого скота
Автор: Осянин К.А., Лартон Р.Р., Алимов А.М., Фаизов Т.Х.
Статья в выпуске: 4 т.244, 2020 года.
Бесплатный доступ
В результате проведенной полимеразной цепной реакции установлено, что смесь оли-гонкулеотидных затравок при взаимодействии с одним из ДНК-маркеров не препятствует накоплению специфических продуктов амплификации. Каждому биологическому патогену соответствует индивидуальная флуоресцентная метка. Так, для вирусной диареи крупного рогатого скота это канал R6G, для парагриппа-3 - канал Fam, а для инфекционного ринотра-хеита - Cy5.
Вирусная диарея, геномика, инфекционный ринотрахеит, парагрипп-3, пцр
Короткий адрес: https://sciup.org/142226047
IDR: 142226047 | УДК: 577.113 | DOI: 10.31588/2413-4201-1883-244-4-111-116
Multiplex PCR for indication and differentiation of cables of respiratory viral infections of cattle
Thus, as a result of the conducted polymerase chain reaction, it has been established that the mixture of oligonucleotide primers when interacting with one of the DNA markers does not interfere with accumulation of specific amplification products. Each biological pathogen corresponds an individual fluorescent marker for bovine viral diarrhea channel R6G, for parainfluenza-3-channel Fam, and for infectious rhinotracheitis Cy5.
Текст научной статьи Мультиплексная ПЦР для индикации и дифференциации возбудителей респираторных вирусных инфекций крупного рогатого скота
Ведущее место среди заболеваний телят занимает патология респираторного тракта. Инфекции респираторного тракта ведут к формированию хронической бронхолегочной патологии у крупного рогатого скота (КРС). Поиск причин рецидивирова-ния существенно затрудняет широкий этиологический спектр острых респираторных вирусных инфекций крупного рогатого скота (ОРВИ КРС). В числе вирусов, вызывающих острые респираторные заболевания, отмечают респираторносинцитиальный вирус, вирусы парагриппа, инфекционного ринотрахеита, вирусной диареи-болезни слизистых, бактериальные инфекции [1].
Болезни легких инфекционной этиологии наиболее распространены и являются одной из ведущих причин гибели животных. Они остаются единственным видом патологии, гибель от которого не только не снижается, но и продолжает расти. По прогнозам ветеринарных специалистов, к 2020 году болезни органов дыхания войдут в тройку лидеров по показателям гибели животных [6].
Наиболее значимыми из группы респираторных болезней являются инфекционный ринотрахеит (ИРТ), парагрипп-3 (ПГ-3) и вирусная диарея (ВД). В современном промышленном скотоводстве наиболее эффективным способом профилактики респираторных инфекций крупного рогатого скота считается вакцинация
Ведущую роль в возникновении респираторных болезней играют вирусы инфекционного ринотрахеита крупного рогатого скота (ИРТ КРС), вирусной диареи – болезни слизистых оболочек крупного рогатого скота (ВД-БС КРС). По данным большинства исследователей, респираторные болезни регистрируют в основном у молодняка КРС в возрасте 1-6 месяцев. [7].
Респираторные болезни являются важной причиной экономического ущерба в молочном скотоводстве. Они приводят к падежу животных или снижению скорости их роста, увеличению затрат на лечение, диагностические и профилактические мероприятия [2].
Тяжесть их проявления варьирует от острых клинических форм, приводящих к летальному исходу, до субклинических или бессимптомных, сопровождающихся снижением показателей продуктивности у переболевших животных [8].
Для подтверждения диагноза на эти инфекции используются специфические лабораторно-инструментальные методы исследования: выделение вирусов и токсинов (цитопатическое действие на культуру клеток); серологическая диагностика и полимеразная цепная реакция (ПЦР) или специфическая амплификация.
Недостаток при выделении вирусов на культуре клеток (низкая чувствительность, не всегда можно по цитопатическо- му действию (ЦПД) точно определить вид вируса, ЦПД может и не быть, большие трудности связаны с контаминацией культуры клеток другими биопатогенами и сапрофитными организмами) [5].
Недостаток серологической диагностики (низкая чувствительность (РА, ПР, РСК), низкая специфичность (ИФА с цельным вирусным антигеном), не всегда есть возможность дифференциации вакцинного иммунитета от патологического процесса) [3].
Индикация респираторных заболеваний крупного рогатого скота - долгий и трудоемкий процесс, а на практике зачастую требуется быстрое и точное определение биопатогена циркулирующего в хозяйстве, чтобы своевременно предпринять меры по профилактике и лечению возникшей болезни. Наиболее точным и быстрым методом диагностики является ПЦР, особенно при одновременной амплификации нескольких маркерных областей.
С учетом изложенного целью настоящей работы являлось изыскание олигонуклеотидных праймеров для одновременной индикации и дифференциации геномов возбудителей, наиболее часто регистрируемых респираторных вирусных инфекций мультиплексной полимеразноцепной реакцией.
Материал и методы исследований. Подбор праймеров и зондов для ге-ноиндикации пользовались ресурсами национального центра биологической информатизации (NCBI), BLAST и программой VectorNTI 9.1.0. (Invitrogen Corporation). Выделение ДНК для положительного контроля не требуется, перед ПЦР положительный контроль разбавяли в 100000 раз. С целью применения в мультиплексной ПЦР сконструировали уникальный положительный контроль, содержащую комплиментарную нуклеотидную последовательность ко всем олигонуклиотидным затравкам искомых вирусов.
Результаты исследований. Для оценки генетического полиморфизма и выявления консервативных участков геномов возбудителей инфекционного рино- трахеита, парагриппа-3 и вирусной диареи крупного рогатого скота был создан собственный банк геномов, включающий от 7 до 14 изолятов каждого вида вируса. Путем выравнивания олигонуклеотидных последовательностей геномов каждого из исследуемых вирусов установлены консервативные участки соответствующих геномов. У вируса возбудителя инфекционного ри-нотрахеита в геноме HV тип 1 штамм Cooper консервативный локус находится на участке 4716 - 4846 bp. У вируса парагриппа-3, изолят Egypt2014 консервативный локус находится в зоне 2820-2910 bp. У возбудителя вирусной диареи, изолят Carlito консервативный локус выявлялся на участке 84-204 bp. Установление последовательностей локусов актуальна для варианта «Consensus» при выравнивании нуклеотидных последовательностей. Нуклеотидные последовательности наиболее перспективных в плане специфичности локусов геномов приведены в таблице 1.
С учетом выявленных данных созданы праймеры и зонды для амплификации последовательностей в рамках вышеуказанных консервативных локусов, которые представлены в таблице 2. Одновременно с подбором праймеров был создан и зонд для возможного использования в качестве внутреннего контроля амплификации последовательности гена каппа-казеина.
Опытным путем была установлена оптимальная температура отжига для всех праймеров которая составляла 56 °С, что позволяет реализовывать возможность сочетания тест-систем в мультиплексном формате. Для контроля амплификации (в качестве положительного контроля) был произведен дизайн и синтез кольцевых молекул ДНК (плазмид), включающих в себя амплифицируемые последовательности ДНК. На основе экспериментальных данных разработана реакционная смесь и условия проведения реакции, обеспечивающие эффективное накопление продуктов амплификации для всех исследуемых видов вирусов приведены в таблице 3 и 4 соответственно
Таблица 1 – Маркерные участки геномов вирусов
|
Вирус |
Консервативный локус |
|
Парагрипп-3 |
acaaguaagaaaaacuuaggauuaacgggaauuauccaauccggagac-ggagggacaaauccagaauccacccacgaccaaccaaaccaaagauucaug-gaaaacaaugcuaaagacaaucaaaucauggauucuugggaagagggaucaggaga-caagucaucugacaucucaucggcccucgacauc |
|
Вирусная диарея |
agcgaaggccgaaaagaggcuagccaugcccuuaguaggacuag- caaaacaaggaggguagcaacaguggugaguucguuggauggcugaagcccugagua-caggguagucgucagugguucgacgcuuugugcgacaagccucgagaugccacgug-gacgagggcaugcccacagcacaucuua |
|
Инфекционный ринотрахеит |
ctgtgcccgtgcgtgtagacaggcaagtagcggctcatggcctcggcgacgatgccctt-gagcgtgggg |
Таблица 2 – Нуклеотидная последовательность разработанных праймеров и зондов для генетической идентификации возбудителей вирусных респираторных заболеваний КРС (ИРТ, ПГ-3, ВД-БС).
|
Название |
Последовательность 5` -› 3` |
|
BPG1F |
ttcccaagaatccatgatttgatagt |
|
BPG1R |
aacaaataagaaaaacttaggattaacgga |
|
BPG1P |
Fam-atgtcgagggccgatgagatgtcagatg-BHQ1 |
|
BPG2F |
cagaaagggcgattacattattacaga |
|
BPG2R |
tcttcgatgcagtatccgcatt |
|
BPG2P |
Fam-cattcgccacacacacaactctcttgtcttg-BHQ1 |
|
BVD1F |
cgaaggccgaaaagaggcta |
|
BVD1R |
cgaaccactgacgactaccctg |
|
BVD1P |
R6G-agtggtgagttcgttggatggctgaag-BHQ2 |
|
BVD2F |
agcggcggagcatgtggat |
|
BVD2R |
cacacaggccacaagggaacg |
|
BVD2P |
CY5-cgatgcaacgcgaagaaccttacctggg- BHQ3 |
|
BHV1F |
ctgtgcccgtgcgtgtagac |
|
BHV1R |
cccacgctcaagggcatc |
|
BHV1P |
CY5-tagcggctcatggcctcggcg-BHQ3 |
|
BHV2F |
aggctgtcggcaggacga |
|
BHV2R |
tgcggctgcccgtagc |
|
BHV2P |
CY5-ccaaacacgtagggcgcggcag-BHQ3 |
|
BkapF |
cttggcaggcacagtatttgaca |
|
BkapR |
attactaccaacagaaaccagttgcac |
|
BkapP |
CY5-ttgaagaatttgggcaggtgacctaactg-BHQ3 |
Таблица 3 – Реакционная смесь, в расчёте на одну пробирку
|
Компонент |
Количество, мкл |
|
dNTP |
1,5 |
|
10 Х ПЦР буфер Б |
1,5 |
|
Syn Taq ДНК-полимераза |
0,5 |
|
MgCl 2 |
1,5 |
|
dd H2O |
3,5 |
|
флуоресцентный зонд (типа Taq Man), 10 пкмоль/мкл |
0,5 |
|
смесь праймеров, 10 пкмоль/мкл |
Каждого по 0,5 |
|
MMLV ревертаза |
0,2 |
|
Образец ДНК |
5 |
Таблица 4 – Условия проведения ПЦР состояли из следующих этапов
|
1. |
37°С |
30 мин |
|
2. |
95°С |
5 мин |
|
3. |
95°С |
5 сек |
|
4. |
56°С |
30 сек, детекция, переход на шаг №3 (40 повторов) |
Опытным путем определяли режим и пропорциональный состав ПЦР тест-систем, для индикации каждого из выявляемых биопатогенов методом одиночной ПЦР и в режиме реального времени с одновременной обратной транскрипцией вирусной РНК, в той же реакционной смеси были одинаковы.
Чувствительность тест-систем определялась путем десятикратных разведений препарата плазмидной ДНК для индикации возбудителей вирусной диареи КРС, инфекционного ринотрахеита и парагриппа-3. Стабильная амплификация наблюдалась при разведении 1:10-10, что составило 1 геном-эквивалент на 0,1 мкл плазмидной ДНК.
Основываясь на результате созданных испытаний моно-тест-систем для индикации вирусов ИРТ, ВД, ПГ-3 было выявлено, что максимальной эффективностью амплификации ДНК мишени обеспечивают следующие комплексы олигонук- леотидных затравок: BPG32; BVDV1 и BHV11.
Установленное экспериментом наиболее эффективное соотношение оли-гонуклеотидных затравок для выявления каждого из искомых вирусов, приведено в таблице 6.
В установленную реакционную смесь вводится 5 мкл препарата искомых нуклеиновых кислот. Условия проведения ПЦР были те же, что и для одиночной ПЦР.
В результате проведенных опытов установлена специфическая амплификация целевых праймеров на ДНК-матрице положительного контрольного образца в мультипраймерной реакционной смеси (в качестве ДНК-матрицы выступают нуклеиновые кислоты на каждый из искомых возбудителей).
Результаты амплификации представлены на рисунке 1.
Таблица 6 – Соотношение количества олигонуклеотидных затравок для амплификации
ДНК-матриц респираторных вирусов крупного рогатого скота в мультиплексном варианте
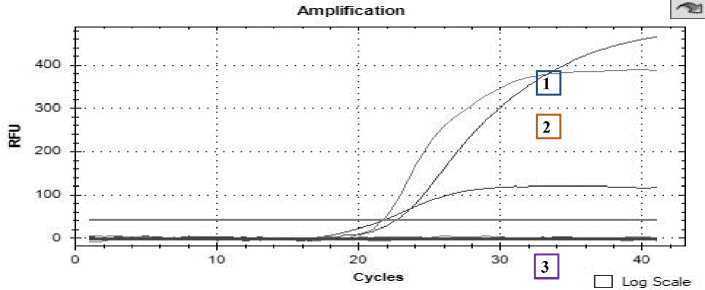
Рисунок 1 – Амплификация ДНК-маркеров легочных вирусов респираторных инфекций крупного рогатого скота в режиме реального времени. Обозначения: 1 –мультиплексная реакционная смесь, содержащая ДНК-матрицы плазмидной ДНК со вставкой специфичного для вируса локуса парагриппа-3; 2- мультиплексная реакционная смесь, в качестве ДНК-
Каждому биологическому патогену соответствовала индивидуальная флуоресцентная метка. В частности, для возбудителя вирусной диареи крупного рогатого скота – канал R6G, для вируса парагриппа-3- канал Fam, и для вируса инфекционного ринотрахеита Cy5. Таким образом разработана технология и режим ПЦР в реальном времени, позволяющие обнаруживать одновременно все 3 генома возбудителя.
Полимеразно-цепная реакция показала, что смесь отобранных олигонуклео-тидных затравок при взаимодействии с одними ДНК-маркерами не препятствует накоплению продуктов амплификации специфических локусов.
Заключение. В результате проведенных исследований определены маркерные локусы генотипов возбудителей ПГ-3, ВД, ИРТ. Изысканы праймеры и зонды, оптимизированы условия и режим мультиплексной ПЦР локусов их геномов. При амплификации исследуемых образцов нуклеиновых кислот в мультиплексной ПЦР в реальном времени доказана возможность одновременной индикации и дифференциации геномов возбудителей ПГ3, ВД, ИРТ.
Список литературы Мультиплексная ПЦР для индикации и дифференциации возбудителей респираторных вирусных инфекций крупного рогатого скота
- Алексеев, А.Д. Петрова О.Г. Дроздова Л.И. Респираторно - синцитиальная инфекция и ее роль в патогенезе острых респираторных заболеваний КРС / А.Д. Алексеев, О.Г. Петрова Л.И. Дроздова // Medicus. - 2016. - № 3. - С. 31-33.
- Котенева С.В., Войтова К.В., Глотова Т.И., Строганова И.Я., Глотов А.Г. Частота выявления генома респираторно-синцитиального вируса у крупного рогатого скота при вспышках бронхопневмоний на молочных комплексах. Российский ветеринарный журнал. Сельскохозяйственные животные. 2016. - № 3. - С. 18
- Кудряшов, А.А. Диагностика инфекционного ринотрахеита и пастереллёза телят в агрохозяйствах / А.А. Кудряшов, B. И. Балабанова, Е.В. Беляева // Международный вестник ветеринарии. - 2017. - № 1. - С. 7-12.
- Магдеева, Э.А. Биологические свойства инактивированной липосомальной вакцины против инфекционного ринотрахеита и парагриппа-3 крупного рогатого скота / Э.А. Магдеева. - Казань. - 2016. - С. 39.
- Нефедченко, А.В. Комплексный подход к определению этиологической структуры респираторных болезней крупного рогатого скота в молочных хозяйствах / А.В. Нефедченко, Т.И. Глотова, А.Г. Глотов // Вестник Красноярского государственного аграрного университета. -2017. - № 1 (124). - С. 65-71.
- Петрова, О.Г. Респираторные заболевания животных и птиц с учетом экологических особенностей территории / О.Г. Петрова, Н.А. Кольберг, С.А. Марковская [и др.]. - Екатеринбург. - 2012. - C. 228.
- Ellis, J.A. Update on viral pathogenesis in BRD / J.A. Ellis // Animal Health Research Reviews. - 2009. - Vol. 10. - P. 151-152.
- Hilton, W.M. BRD in 2014: where have we been, where are we now, and where do we want to go? / W.M. Hilton // Animal Health Research Reviews. - 2014. - Vol. 15 (2). - P. 120.


