Наночастицы селена стабилизированные ТВИН-80 для восполнения дефицита селена в организме животных
Автор: Древко Я.Б., Ларионова О.С., Шелковая А.А., Ларионов С.В.
Рубрика: Ветеринария
Статья в выпуске: 4 т.264, 2025 года.
Бесплатный доступ
Наночастицы находят все большее применение в качестве, как компонентов, так и основных действующих веществ лекарственных средств и кормовых добавок, а особое место занимают наночастицы элементов, которые необходимы для жизнедеятельности живых организмов. Селен — это незаменимый микроэлемент, который участвует в различных процессах живых организмов, что подтверждается, как широким спектром гормонов и ферментов в состав которых он входит, так и научных статей, подтверждающих широкий спектр биологической активности и возможностей применения в повседневной ветеринарной практике. Однако в мире в большинстве используют соли селенистой и селеновой кислоты, в частности селенит натрия, который обладает высокой токсичностью, осложняет его использование и не позволяет часто в полной мере быстро восполнить дефицит данного микроэлемента, что в условиях высокой интенсификации промышленного животноводства повышает издержки и, как следствие, себестоимость. В данной работе рассмотрен новый метод синтеза наночастиц с использованием в качестве поставщика селена дихлордиацетофенонилселенида и в качестве стабилизирующего компонента ТВИН-80, который позволил получать наночастицы селена с низкой себестоимостью размером 3-16 нм, что позволяет предполагать высокую усвояемость данных частиц, а растворимость в воде и высокие показатели дзета потенциала позволяют создавать стабильные коллоидные растворы, которые наиболее удобно применять, как перорально при выпаивании, так и инъекционно. Для впервые синтезированных наночастиц были проведены исследования по определению острой токсичности и местно-раздражающего действия, что позволяет вместе с анализом литературных данных говорить о высокой актуальности дальнейших исследований в области применения их в качестве одного или единственного действующего вещества в ветеринарных препаратах и/или кормовых добавках для животных и птиц.
Селен, наночастица, острая токсичность, ветеринарный препарат, кормовая добавка
Короткий адрес: https://sciup.org/142246741
IDR: 142246741 | УДК: 620.3:619:615:661.155.3 | DOI: 10.31588/2413_4201_1883_4_264_30
TVIN-80 stabilized selenium nanoparticles for replenishing selenium deficiency in animals
Nanoparticles are increasingly used as both components and active ingredients in medications and feed additives, with nanoparticles of elements essential for vital functions of living organisms occupying a special place. Selenium is an essential trace element involved in various processes in living organisms, as evidenced by the wide range of hormones and enzymes it is a component of, as well as scientific articles, confirming its broad range of biological activity and potential applications in everyday veterinary practice. However, worldwide, the majority of selenium salts used are selenous and selenic acids, particularly sodium selenite. Their high toxicity complicates their use and often prevents the rapid and complete replenishment of this micronutrient deficiency. This, in the context of highly intensified industrial livestock farming, increases costs and, consequently, the cost of production. This paper discusses a new method for synthesizing nanoparticles using dichlorodiacetophenonyl selenide as a selenium source and TVIN-80 as a stabilizing component, which made it possible to obtain selenium nanoparticles with a low cost price of 3-16 nm in size, which suggests high digestibility of these particles, and solubility in water and high zeta potential values make it possible to create stable colloidal solutions that are most convenient to use, both orally by drinking and by injection. Acute toxicity and local irritant effects of the newly synthesized nanoparticles were studied. Coupled with literary data analysis it allows us to speak about the high relevance of further research in the field of their use as one or the only active substance in veterinary drugs and/or feed additives for animals and birds.
Текст научной статьи Наночастицы селена стабилизированные ТВИН-80 для восполнения дефицита селена в организме животных
В последние время в мире ведется активный поиск новых методов синтеза наночастиц селена, как с использованием классических химических методов синтеза, так и биотехнологических методов с использованием микроорганизмов [10, 11, 12], основным недостатком данных методов является отсутствие сочетания двух основных факторов: однородность размера частиц и низкая себестоимость [13, 14, 15]. Так многие биотехнологические методы синтеза показывая низкую себестоимость не позволяют получать наночастицы селена одинакового размера, а химические обладают высокой себестоимостью, при этом стоит отметить, что биологическая активность наночастиц сильно меняется в зависимости от их размера, а высокая цена не позволяет использовать их в повседневной ветеринарной практике. На данный момент времени в мире так и не найдена относительно дешевая замена селениту натрия, который и используется в основном при восполнении данного микроэлемента у животных, одним из наиболее распространенных солесодержащих биотехнологических продуктов являются обогащенные селеном дрожжи «Сел-плекс» выпускаемые компанией «Alltech» США [16], однако учитывая низкую концентрацию селена, данная разработка хоть и нашла широкое применение в мире, имеет недостатки связанные с низкой концентрацией селена.
В данной работе нами представлен новый метод синтеза наночастиц селена, который может быть успешно применен в ветеринарии за счет использования отечественных компонентов, и обладающий низкой себестоимостью, при высокой концентрации селена и токсичности, позволяющей успешно включать данные наночастицы, как в рационы кормления, так и в качестве компонента в ветеринарные препараты.
Цель работы - разработать новый метод синтеза наночастиц селена заданного размера стабилизированных фармакопейным поверхностно активным веществом, для дальнейшего применения в ветеринарной практике, как для восполнения дефицита селена в организмах животных и человека, так и для таргет-ной доставки.
Условия, материалы и методы. Исследования проводились на базе ЦКП «Молекулярная биология» и кафедры «Микробиология и биотехнология» ФГБОУ ВО Вавиловского университета.
Для синтеза наночастиц селена использовался дихлордиацетофенонилселенид, который получали в одну стадию из ацетофенона, селенистой кислоты в условиях кислотного катализа.
Для синтеза 1 моля дихлордиацетофено-нилселенида при постоянном перемешивании в плоскодонную колбу, снабженную мешалкой при температуре 20^ к 2,4 моль ацетофенона растворенного в этиловом эфире уксусной кислоты, добавляли 1,1 моль селенистой кислоты, растворенной в воде и 3 моля хлороводорода в виде концентрированной соляной кислоты, через 120 минут полученный осадок отфильтровывали и промывали водой и ацетоном.
Далее полученный дихлордиацетофено-нилселенид растворяли в изопропиловом спирте и добавляли при постоянном перемешивании ТВИН-80 в отношении 10:1 растворенный в воде. В полученный раствор добавляли избыток аммиака и перемешивали на протяжении 5 часов, полученный раствор упаривали на роторном испарителе и получали наночастицы селена с содержанием селена 10%.
Размер частиц определяли методом динамического рассеяния света на приборе Zetasizer Nano ZS.
Для проведения токсичности были использованы белые мыши линии BALB/c, испытания проводили в соответствии с ГОСТ 326442014.
Исследования местно-раздражающего действия проводили на 3 кроликах - самцах возвратом 1 год, породы Советская шиншилла. Для этого за 24 ч до начала проведения исследования выстригали шерсть на участках площадью примерно 10 см по обеим сторонам спины для аппликации и наблюдения. Раствором наночастиц смачивали кусочек марли размером 2×2 см, в объеме 0,5 мл. Прикладывали к переднему краю выстриженного участка спины справа и к заднему - слева. Также смачивали растворителем аналогичные кусочки марли в объеме 0,5 мл, в качестве растворителя использовали дистиллированную воду. Далее покрывали места аппликаций окклюзионной повязкой на 4 ч. Через 4 часа повязку снимали и проводили оценку кожи в месте аппликаций через 1, 24, 48 и 72 ч после удаления образцов.
Изучение гиперчувствительности замедленного типа проводили методом максимального сенсибилизирующего воздействия (GPMT), с использованием 8 голов кроликов породы Советская шиншилла, 5 опытных и 3 контрольных.
Опытной группе кроликов (n=5) в выстриженные участки кожи проводили парные внутрикожные инъекции в объеме 0,1 мл. И вносили следующие растворы: 50% раствор адъюванта Фрейнда, наночастицы селена и наночастицы селена с 50% раствором адъюванта Фрейнда, каждая дозировка составляла 100 мкл.
Контрольной группе животных (n=3) в выстриженные участки кожи проводили парные внутрикожные инъекции в объеме 0,1 мл. И вносили следующие растворы: 50% раствор адъюванта Фрейнда, растворитель наночастиц (дистилированная вода) и дистиллированная вода с 50% раствором адъюванта Фрейнда, каждая дозировка составляла 100 мкл.
Через 7 суток внутрикожной индукционной фазы начинали делать аппликации раствора наночастиц селена.
Для аппликаций пропитывали раствором наночастиц селена фильтровальную бумагу, которые прикладывали на выстриженные участки кожи и фиксировали окклюзионной повязкой вокруг тела животного.
Через 24 ч бумага с раствором удалялась и оценивалось состояние исследуемых участков на наличие эритемы и отека.
При отсутствии реакции на максимальную концентрацию область аппликации 10%-ным раствором натрия додецилсульфата, массировав в кожу за сутки до аппликации. Через 2 недели после завершения местной индукционной фазы, накладывали на свежевыбритые интактные участки кожи кролика, пропитанные исследуемым раствором ватно-марлевые диски, фиксировали окклюзионной повязкой. Удаляли повязку через 24 часа. Все растворы готовили непосредственно перед применением.
После удаления повязки проводили оценку выстриженных участков кожи по Magnusson и Kligman.
Изучение раздражающего и сенсибилизирующего действия выполняли согласно протоколу описанному в ГОСТ Р ИСО 10993-102009, в нашей модификации.
Результаты и обсуждение. Для синтеза однородных по размеру наночастиц необходимо сочетание нескольких факторов, в частности сочетания скорости образования элемента и концентрации поверхностно активного вещества стабилизирующих наночастицы, при этом основная стоимость обычно состоит в стадии очистки полученных частиц от примесей и микрочастиц. В описываем синтезе нами был подобран оптимальный поставщик селена дихлордиацетофенонилселенид, который при приведенных концентрациях ТВИН-80 позволял получать однородные наночастицы, которые в дальнейшем не требовали дорогостоящих методов очистки. Выход наночастиц селена составлял более 90% от теоретического. Анализ методом динамического рассеяния света при 25^ позволил установить, что полученные наночастицы селена имели размер 316 нм (табл. 1, рис. 1), а дзета потенциал составил - 11,3 мВ.
Таблица 1 – Данные динамического рассеяния света наночастиц селена
|
Size d. nm |
Mea n Vol ume % |
Std Dev Volume % |
|
0,4000 |
0,0 |
|
|
0,4632 |
0,0 |
|
|
0,5365 |
0,0 |
|
|
0,6213 |
0,0 |
|
|
0,7195 |
0,0 |
|
|
0,8332 |
0,0 |
|
|
0,9649 |
0,0 |
|
|
1,117 |
0,0 |
|
|
1,294 |
0,0 |
|
|
1,499 |
0,0 |
|
|
1,736 |
0,0 |
|
|
2,010 |
0,0 |
|
|
2,328 |
0,0 |
|
|
2,696 |
0,0 |
|
|
3,122 |
3,6 |
|
|
3,615 |
12,6 |
|
|
4,187 |
19,0 |
|
|
4,849 |
18,1 |
|
Size d. nm |
Mea n Vol ume % |
Std Dev Volume % |
|
5,615 |
14,1 |
|
|
6,503 |
10,3 |
|
|
7,531 |
7,7 |
|
|
8,721 |
5,7 |
|
|
10,10 |
3,9 |
|
|
11,70 |
2,4 |
|
|
13,54 |
1,2 |
|
|
15,69 |
0,5 |
|
|
18,17 |
0,1 |
|
|
21,04 |
0,0 |
|
|
24,36 |
0,0 |
|
|
28,21 |
0,0 |
|
|
32,67 |
0,0 |
|
|
37,84 |
0,0 |
|
|
43,82 |
0,0 |
|
|
50,75 |
0,0 |
|
|
58,77 |
0,1 |
|
|
68,06 |
0,1 |
|
Size d. nm |
Me an Vol ume % |
Std Dev Volume % |
|
78,82 |
0,1 |
|
|
91,28 |
0,1 |
|
|
105,7 |
0,0 |
|
|
122,4 |
0,0 |
|
|
141,8 |
0,0 |
|
|
164,2 |
0,0 |
|
|
190,1 |
0,0 |
|
|
220,2 |
0,0 |
|
|
255,0 |
0,0 |
|
|
295,3 |
0,0 |
|
|
342,0 |
0,0 |
|
|
396,1 |
0,0 |
|
|
458,7 |
0,0 |
|
|
531,2 |
0,0 |
|
|
615,1 |
0,0 |
|
|
712,4 |
0,0 |
|
|
825,0 |
0,0 |
|
|
955,4 |
0,0 |
|
Size d. nm |
Me an Vol um e % |
Std Dev Volume % |
|
1106 |
0,0 |
|
|
1281 |
0,0 |
|
|
1484 |
0,0 |
|
|
1718 |
0,0 |
|
|
1990 |
0,0 |
|
|
2305 |
0,0 |
|
|
2669 |
0,0 |
|
|
3091 |
0,0 |
|
|
3580 |
0,0 |
|
|
4145 |
0,0 |
|
|
4801 |
0,0 |
|
|
5560 |
0,0 |
|
|
6439 |
0,0 |
|
|
7456 |
0,0 |
|
|
8635 |
0,0 |
|
|
1,000 e4 |
0,0 |
|
Statistics Graph (1 measurements)
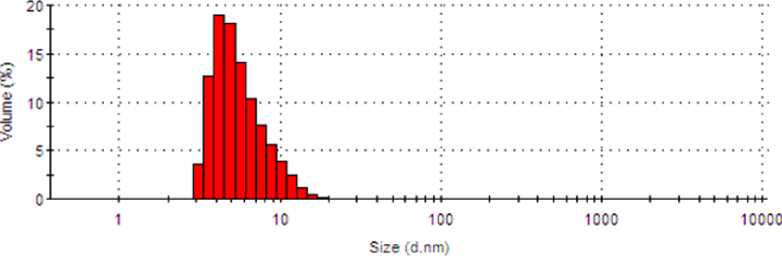
|И Mean with */-1 Standard Deviation error bar|
Рисунок 1 – Данные динамического рассеяния света наночастиц селена
Для определения перспективности полученных наночастиц в качестве кормовой добавки и/или ветеринарного препарата одним из необходимых критериев является проведение доклинических исследований и, в частности, установления острой токсичности и местно-раздражающего действия.
В соответствии с ГОСТ 32644-2014 нами использовались мыши линии BALB/c массой 18-20 г каждой из которой вводили внутрибрюшинно 100 мкл раствора наночастиц селена с дозировкой 5 мг/кг, 50 мг/кг, 300 мг/кг, 2000 мг/кг. В каждой группе животных было по три головы, что позволяло минимизировать в соответствии с требованиями о гуманном обращении с животными, количество задействованного биоматериала, с сохранением необходимой точности. На первом этапе было введено трем животным 100 мкл раствора наночастиц селена в дозировке 5 мг/кг и при наблюдении в течение 14 суток установлено отсутствие смертности, на втором этапе нами трем животным вводились наночастицы селена с дозировкой 50 мг/кг, при этом наблюдение в течение 14 суток выявило смерть одного животного на 11 сутки. Далее еще трем животным были введены наночастицы селена в дозировке 300 мг/кг, на протяжении 14 суток падежа отмечено не было, на следующем этапе трем животным вводили наночастиц селена в дозировке 2000 мг/кг, наблюдение в течение 14 суток показало падеж трех животных на 5, 9 часы и через 2-е суток после введения. Исходя из представленных данных наночастицы селена относятся к 4 классу опасности с LD50= 500 мг/кг.
В результате проведенного эксперимента по оценке местно-раздражающего действия раствора наночастиц селена на кожу кролика при однократном нанесении установлено, что раствор не оказывал раздражающего действия на кожу кроликов. В месте аппликаций кожа имела бледно-розовый цвет, умеренно влажная, эластичная. Патологических изменений кожного покрова в месте нанесения, как раствора наночастиц, так и растворителя выявлено не было.
В ходе изучения сенсибилизирующего действия раствора наночастиц селена, после внутрикожной индукционной фазы отмечали местное покраснение и припухание кожного покрова в местах инъекций. Через 7 дней перед накожной аппликацией исследуемого раствора на места инъекций, осмотром кожного покрова выявлены незначительные остаточные припухлости в месте инъекций растворов с полным альювантом Фрейда, покраснений выявлено не было. В месте введения исследуемого вещества, изменения кожного покрова отсутствовали.
Через 15 дней после удаления окклюзионной повязки с интактных мест аппликации раствора наночастиц селена изменений кожного покрова выявлено не было. Кожа в месте аппликаций была бледно розового цвета, умеренно влажная, эластичная.
Таким образом, можно констатировать, что раствор наночастиц селена не обладает местно-раздражающим действием на кожу и не оказывает сенсибилизирующего действия на кожу кроликов.
Выводы. В результате проведенных исследований был разработан новый метод синтеза наночастиц селена размером 3-16 нм и установлено, LD 50 =500 мг/кг, что соответствует 4 классу опасности. При проведении исследований на местно-раздражающее действие в рамках определения гиперчувствительности замедленного типа, который осуществлялся методом максимального сенсибилизирующего воздействия, установлено, отсутствие аллергизирующего действия препарата на организм опытных животных.


