Немелкоклеточный рак легкого с EGFR мутацией. Терапия афатинибом. Клинический случай
Автор: Бычков Ю.М., Измайлов Т.Р., Большакова С.А.
Журнал: Вестник Российского научного центра рентгенорадиологии Минздрава России @vestnik-rncrr
Рубрика: Клинические наблюдения
Статья в выпуске: 3 т.20, 2020 года.
Бесплатный доступ
У пациентов с немелкоклеточным раком легкого (НМРЛ) в 10-40% случаев могут выявляться соматические мутации в гене рецептора эпидермального фактора роста (EGFR). Назначение EGFR ингибиторов тирозинкиназы у таких пациентов ассоциируется с увеличением эффективности лечения. Препараты первого поколения EGFR ингибиторов тирозинкиназы, гефитиниб и эрлотиниб, увеличивают общую эффективность лечения и выживаемость без прогрессирования по сравнению со стандартной химиотерапией по результатам больших рандомизированных исследований III фазы. Афатиниб являетсянеобратимым ингибитором EGFR. По сравнению с гефитинибом он увеличивает выживаемость без прогрессирования и время до рецидива заболевания Отмечено увеличение общей выживаемости у группы пациентов в мутацией Del19 по сравнению со стандартной химиотерапией. Клинический случай : Мы представляем данные по пациенту 56 лет с распространенной аденокарциномой легкого с мутацией L858R в 21 экзоне, которому в течение 3-х лет проводилась таргетная терапия афатинибом, стандартная химиотерапия, лучевой терапия на метастазы в головной мозг. Интересно, что прием афатиниба успешно возобновлялся за этот период три раза. Заключение : Афатиниб является эффективным препаратом первой линии при EGFR мутированном НМРЛ.
Немелкоклеточный рак легкого, рецептор эпидермального фактора роста, ингибитор тирозинкиназы
Короткий адрес: https://sciup.org/149132146
IDR: 149132146
Management of EGFR-mutant non-small cell lung cancer. Treatment with afatinib: a case report
Approximately 10-40% of patients with newly diagnosed metastatic non-small cell lung cancer (NSCLC) harbor a somatic mutation in epidermal growth factor receptor (EGFR) gene. Tyrosine kinase inhibitors (TKIs) against EGFR have increasingly been associated with improved clinical outcomes in patients with advanced EGFR-mutant NSCLC. First-generation reversible EGFR TKIs, gefitinib and erlotinib, have been proven to improve the objective response rate and to prolong the progression-free survival compared with standard chemotherapy in large phase III trials. Afatinib is an irreversible EGFR inhibitor. Compared with gefitinib in a first-line setting, afatinib prolonged progression-free survival and time to treatment failure. Afatinib has been shown to prolong overall survival in the subset of patients with an EGFR exon 19 deletion compared with chemotherapy. Presentation : We report a case of advanced lung adenocarcinoma in patient 56 years old with activating EGFR mutation (L858R) treated with afatinib, standard chemotherapy, and brain radiation for 3 years. During the treatment period we successfully returned to afatinib therapy three times. Conclusion : Afatinib is an affective EGFR TKIs inhibitor which successfully can be used in a first-line setting in advanced EGFR-mutant NSCLC.
Текст научной статьи Немелкоклеточный рак легкого с EGFR мутацией. Терапия афатинибом. Клинический случай
Вступление
Не менее 50% пациентов с немелкоклеточным раком легкого (НМРЛ) не момент постановки диагноза имеют IV стадию заболевания. У 60-75% пациентов с I-II стадией заболевания после радикального лечения могут появиться отдаленные метастазы. Таким образом, стало понятно, что необходимы новые терапевтические опции [3].
Стандартом 1 линии лечения являются платиносодержащие схемы химиотерапии, что не приводит, однако, к увеличению уровня выживаемости, при том, что переносимость химиотерапии, ее влияние на качество жизни во многих случаях неудовлетворительная [15,17,20,24]. Лечение рака легкого значительно изменилось при появлении информации о драйверных мутациях [13,23]. Дополнительно к уже известным мутациям – EGFR и ALK, добавились ROS-1, BRAF, MET и RET мутации, имеющие конкурентные терапевтические опции [4,11,25].
Соматические мутации гена рецептора эпидермального фактора роста (EGFR), являющегося трансмембранным гликопротеином, встречаются у 40% азиатских пациентов и в 10-15% случаев у пациентов европеоидной расы с аденокарциномой легкого [35]. Cohen и Levi Montalcini [12] открыли EGFR в 1957 году. Через какое-то время, когда взаимосвязь между EGFR и развитием рака стала очевидной, интерес к исследованию EGFR вырос [12]. Рецептор эпидермального фактора относится к семейству ErbB или HER протеиновых киназ, куда входят 4 близких по структуре белка: EGFR (также известный как ErbB1 или HER1), ErbB2 (HER2), ErbB3 (HER3) и ErbB4 (HER4) [12].
В нормальных клетках ErbB протеиновые киназы [12] вовлечены в процессы клеточной пролиферации. Появление мутаций в EGFR сопровождается появлением абберантных, конститутивных сигналов, которые запускают клеточный путь патогенеза, что в конечном итоге приводит к неконтролируемой пролиферации аномальных клеток. Опухолевая гиперэкспрессия EGFR может полностью зависеть от EGFR сигнала, феномен, получивший название «онкогенная зависимость». В этом случае блокада EGFR прекращает процессы пролиферации и индуцирует апоптоз [12].
Онкогенные мутации при НМРЛ, как правило, присутствуют при аденокарциноме [12]. Наиболее часто встречающиеся EGFR мутации – это делеция в 19 экзоне (Del19) и Leu858Arg точечная мутация (L858R) [12]. Таргетное воздействие на EGFR тирозинкиназы при помощи тирозинкиназных ингибиторов продемонстрировало достоверное клинический эффект у пациентов с EGFR активирующими мутациями [30]. На сегодняшний день ингибиторы тирозинкиназы представлены тремя поколениями препаратов:
-
1. Гефитиниб и Эрлотиниб;
-
2. Афатиниб и Дакометиниб;
-
3. Разилетиниб, NM713, Осимертиниб.
Механизм действия последнего поколения ингибиторов тирозинкиназы осуществляется через мутацию Т790М в 20 экзоне гена EGFR, ответственную за 50% случаев резистентности к первой линии терапии ингибиторами тирозинкиназы первого и второго поколений [5,7]. Для применения в первой линии лечения до сегодняшнего дня были одобрены FDA только гефитиниб, эрлотиниб и афатиниб [18]. Осимертиниб был изучен в условиях первой линии терапии в рандомизированном исследовании III фазы FLAURA [5,16,22]. В этом исследовании пациенты с частыми (Del19/L858R) EGFR мутациями были рандомизированы для получения осимертиниба или ингибиторов тирозинкиназы EGFR первого поколения (эрлотиниб или гефитиниб) в качестве единственного препарата для сравнения. Выживаемость без прогрессирования была достоверно выше в группе осимертиниба при сравнении с группой эрлотиниба и гефитиниба (медиана – 18,9 и 10,2 месяцев (p<0,0001), соответственно). Медиана продолжительности ответа составила 17,2 и 8,5 месяцев (р=0,2325), соответственно. [5,16,22] В настоящий момент в первой линии одобрен и осимертиниб (тагриссо). Использование EGFR ингибиторов тирозинкиназы для пациентов с активирующими мутациями EGFR стало стандартом лечения на сегодняшний день [18].
Описание случая.
У пациента 56 лет в феврале 2016 года диагностирован рак правого легкого T2N3M1 с метастатическим поражением легких, мягких тканей спины, левых аксиллярных л/узлов. Гистология: умереннодифференцирвоанная аденокарцинома. При молекулярно- генетическом исследовании выявлена мутация L858R в 21 экзоне. С марта 2016 года начата таргетная терапия препаратом эрлотиниб в дозе 150мг в течение одного месяца. В связи с развитием дерматологической токсичности 3 степени пациент был переведен на лечение препаратом гефитиниб. В мае 2016 года зарегистрировано прогрессирование заболевания в виде продолженного роста первичной опухоли. Проведено 6 курсов химиотерапии по схеме пеметрексед + карбоплатин + бевацизумаб. При контрольном обследовании в августе 2016 года выявлена частичная регрессия первичной опухоли и метастатических очагов. Проведено 3 курса поддерживающей химиотерапии препаратами пеметрексед + бевацизумаб. В ноябре 2016г. по данным КТ органов грудной клетки выявлен рост метастазов в лимфатических узлах. Проведено 4 курса химиотерапии по схеме пеметрексед + цисплатин + бевацизумаб. При контрольном обследовании в марте 2017 года выявлен продолженный рост первичной опухоли, метастазов в легких, метастазов в лимфатических узлах и мягких тканей спины.
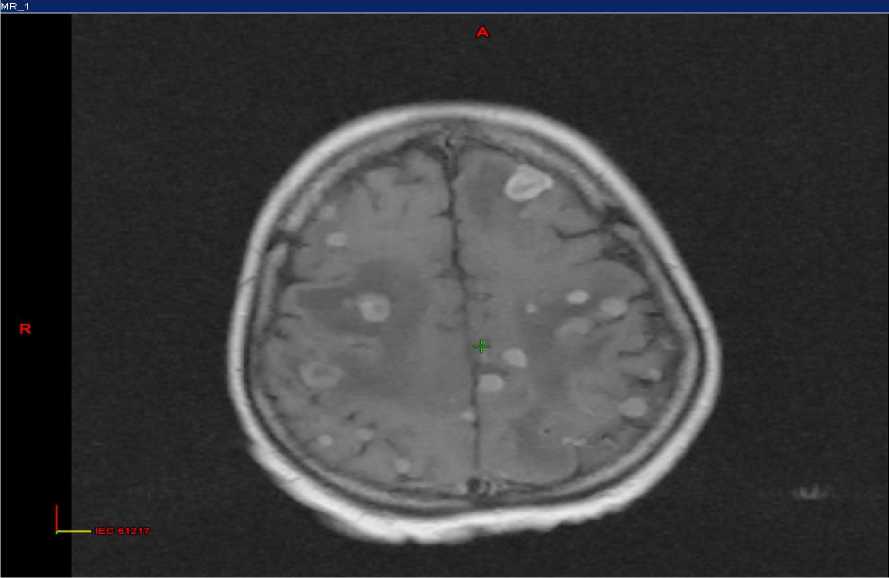
Отмечено появление плеврита справа. Проведено 4 курса химиотерапии по схеме доцетаксел + винорелбин с явлениями нейтропении 3 степени и стоматита 2-3 степени. При обследовании в июне 2017 года по данным КТ органов грудной клетки была отмечена частичная регрессия метастазов в легких и лимфатических узлах. На данном этапе было решено продолжить проведение терапии таргетным препаратом афатиниб. Пациент начал принимать препарат с июня 2017 года. В ноябре 2017 года при контрольном обследовании выявлена частичная регрессия первичной опухоли и метастатических очагов, полная регрессия плеврита справа. Пациент продолжал принимать афатиниб до февраля 2018 года, когда при обследовании было выявлено прогрессирование в виде продолженного роста первичной опухоли в правом легком, метастазов в легких и мягких тканях спины. В марте 2018 года пациент стал отмечать слабость в руках, ногах. При МРТ головного мозга с контрастным усилением диагностировано метастатическое поражение головного мозга.
Больному в РНЦРР в дневном радиотерапевтическом стационаре с 04.04 по 23.04.18 проведен первый этап дистанционной лучевой терапии на весь объем головного мозга на аппарате Рокус РОД 3Гр СОД 34 Гр (42.5 изоГр). Лечение проводилось на фоне сопроводительной терапии, курс перенес удовлетворительно, отрицательных реакций и осложнений не было отмечено. При выписке – неврологический статус без отрицательной динамики.
На втором этапе в РНЦРР с 30.05 по 13.06.2018 больному проведен курс конформной 3D дистанционной лучевой терапии в режиме RapidArc, применялись 2 динамические арки (VMAT)
Средний режим фракционирования на метастазы головного мозга РОД 3Гр по 95% изодозе PTV (планируемый объем облучения) СОД 30Гр (37.5 изоГр) Лечение проводилось на фоне сопроводительной терапии. Проводился курс магнитотерапии (10 сеансов). При выписке отмечена положительная динамика в виде уменьшения очаговой и общемозговой неврологической симптоматики.
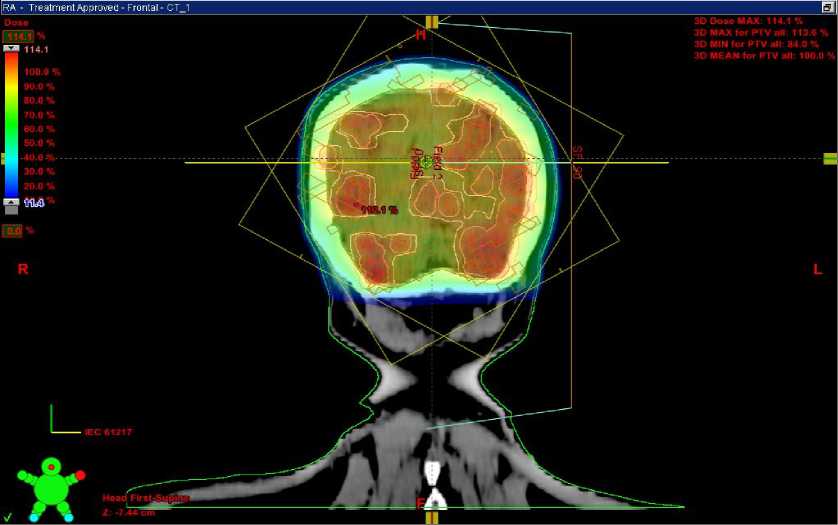
Рис.1. План лучевой терапии c картой дозного распределения в режиме RapidArc.
Аксиальный срез. Программа Eclipse.
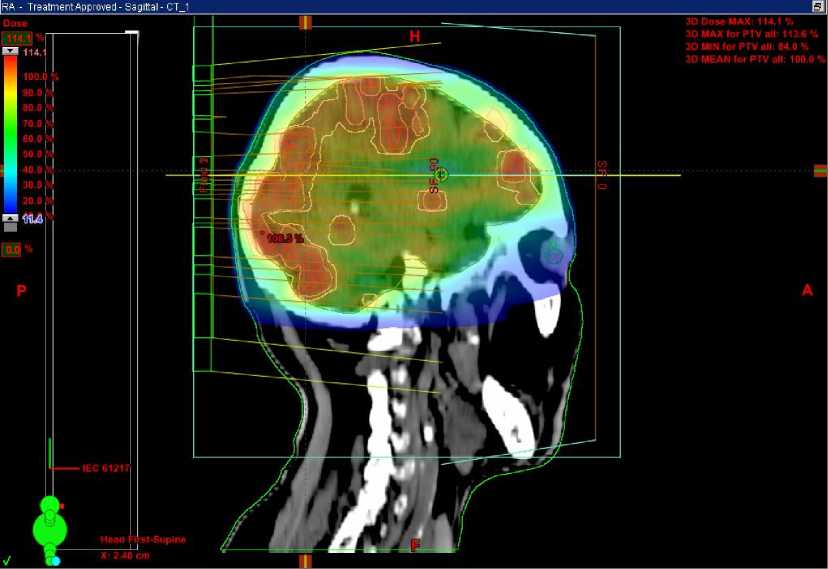
Рис. 2. План лучевой терапии c картой дозного распределения в режиме RapidArc.
Фронтальный срез. Программа Eclipse.
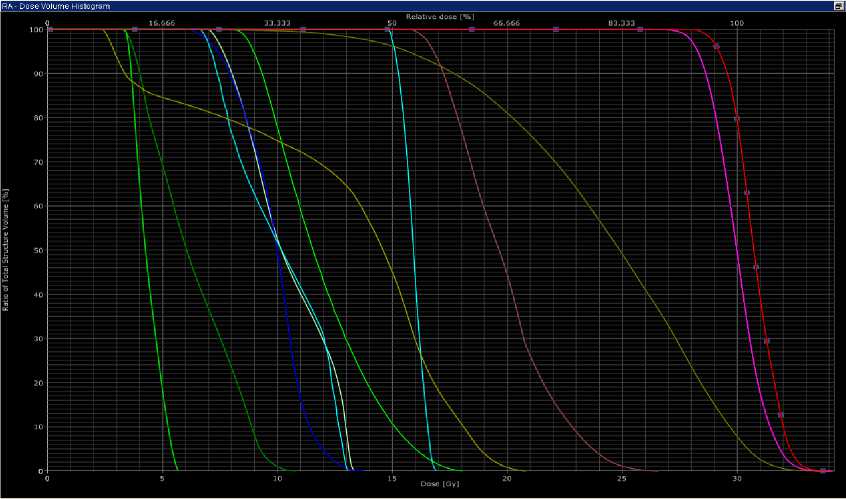
Рис. 3. План лучевой терапии c картой дозного распределения в режиме RapidArc.
Саггитальный срез. Программа Eclipse.
Рис. 4. Гистограмма доза-объем (DVH). PTV (планируемый объем облучения) входит в 95% изодозу. Программа Eclipse.
После окончания облучения пациент продолжил принимать афатиниб по н.в. При контрольном обследовании в августе 2018 года выявлена стабилизация заболевания. Переносимость лечения можно считать удовлетворительной. Отмечены следующие токсические реакции: диарея, выпь, снижение аппетита, повышенная утомляемость. Все реакции были 1-2 степени. При КТ органов грудной клетки в 09/2018 выявлен продолженный рост метастазов в легких. Проведено 2 курса МХТ доцетакселом. При контрольном обследовании в 11/2018 отмечен продолженный рост мтс в легких, диагностировано метастатическое поражение кожи спины. С 01.11.18 по 27.12.18 проведен курс лучевой терапии с паллиативной целью на метастатические очаги кожи лопаточной области (на экзофитный метастаз кожи лопаточной области слева 1 поле 9 Mev РОД3Гр СОД 54Гр (экв 68Гр), на ложе метастазов кожи лопаточной области (все очаги лопаточной области слева) 1поле 6 Mev РОД3Гр СОД 48Гр (экв60Гр), на очаги по срединной 48
подмышечной линии РОД3Гр СОД 42 Гр. С 14.01 по 04.02.2019 проведен курс лучевой терапии с паллиативной целью на метастатические очаги кожи туловища на аппарате ЛУЭ TB - на ложе метастазов кожи подлопаточной области РОД3Гр с СОД45Гр до СОД 54Гр, подмышечной области справа по срединной линии (подкожные узловые образования) РОД3Гр до СОД42Гр, и на надлопаточную область справа РОД 3Гр до СОД 42Гр (экв52Гр). Местно - положительная динамика в виде уменьшения объема образований, лучевая реакция 1 степени. Лучевая терапия проводилась на фоне введения ниволумаба. Смерть пациента зарегистрирована в 03/2019 года от прогрессирования основного заболевания.
Дискуссия.
Механизм действия афатиниба основан на необратимом и ковалентном связывании АТФ – части EGFR тирозинкиназного домена, медиатором реакции является акриламидная группа препарата и цистеиновые радикалы в тирозинкиназном домене рецептора, происходит снижение процессов авто и трансфосфорилирования рецептора и блокада нисходящего трансдукционного сигнального пути патогенеза [3,12]. In vitro афатиниб продемонстрировал свою активность при Del 19 и L858R мутациях EGFR, а также при редко встречающихся мутациях, таких как G719X (экзон 18), L861Q (экзон 21) и S768I (экзон 18) при немелкоклеточном раке легкого (НМРЛ) [12]. Следует отметить, что на доклиническом этапе исследований афатиниб блокировал мутацию Т790М, возникновение которой чаще всего приводит к развитию резистентности к первому поколению EGFR ингибиторов тирозинкиназы. Однако, на клиническом этапе активность афатиниба при наличии мутации Т790М при распространенном НМРЛ оказалась неудовлетворительной из-за различных наномолярных концентраций, требующихся для блокады различных EGFR мутаций [10,19]. В 2013г. FDA одобрил применение афатиниба в первой линии терапии метастатического EGFR мутированного НМРЛ.
Рекомендуемая доза афатиниба составляет 40мг внутрь один раз в день. После приема таблетки максимальная концентрация препарата в плазме крови достигается через 2-5 часов. Афатиниб связывается нековалентно и ковалентно с белками плазмы. Период полувыведения афатиниба составляет 36 часов, преимущественно с калом и 5% препарата выводится с мочой [1,2,3].
Было начато несколько исследований II и III фазы для оценки эффективности афатиниба в качестве I линии терапии у пациентов с распространенным EGFR-мутированным НМРЛ.
Lux Lung 3 (LL3) и Lux Lung 6 (LL6) – два больших рандомизированных исследования III фазы, где проводилось сравнение афатиниба с платиновыми дуплетами. В LL3 рандомизировано 345 пациентов с распространенным EGFR-мутированным распространенным НМРЛ для получения афатиниба (40 мг в день) ежедневно или химиотерапии по схеме пеметрексед + препараты из группы платины в стандартных дозировках, каждые 21 день. Выживаемость без прогрессирования была достоверно выше в группе афатиниба по сравнению с группой химиотерапии - 11,1 vs 6,9 месяцев, соответственно (р=0,001). Медиана выживаемости без прогрессирования при наличии мутаций Del 19 и L858R (n=308) составила 13,6 месяцев в группе афатиниба и 6,9 месяцев в группе химиотерапии (р=0,001) [27].
В исследовании LL6 364 пациента были рандомизированы в группу афатиниба (n=242) или в группу химиотерапии по схеме гемцитабин + цисплатин (n=122). Выявлено, что медиана выживаемости без прогрессирования достоверно больше в группе афатиниба (11,0 vs 5,6 месяцев, соответственно р<0,0001) [32]. На момент публикации результатов исследований окончательные данные по общей выживаемости (ОВ) еще не были доступны. Данные по выживаемости стали доступны после наступления 209 смертей в исследовании LL3 и 237 смертей – в исследовании LL6, достоверных различий по медиане ОВ между группами не выявлено, в группе афатиниба медиана ОВ составила 25,8 месяцев, в группе ХТ - 24,5 месяца (р=0,37) [34]. При анализе ОВ с учетом статуса EGFR мутаций было получено, что терапия афатинибом ассоциируется с достоверным увеличением ОВ при наличии мутаций Del 19 (33,3 vs 18,4 месяцев (р=0,0015)) в исследовании LL3 и 31,4 vs 18,4 месяцев (р=0,0229) в исследовании LL6, что дало основание считать, что эта подгруппа пациентов наиболее хорошо отвечает на терапию афатинибом [34].
С учетом этих результатов было проведено исследование Lux Lung 7 (LL7) по сравнению афатиниба и гефитиниба. В это исследование IIb фазы было набрано 319 нелеченых пациентов с EGFR-мутированным НМРЛ. В одной группе (n=160) проводилась терапия афатинибом, в другой (n=159) – гефитинибом. Медиана продолжительности наблюдения составила 27,3 месяца, медиана выживаемости без прогрессирования – 11,0 месяцев в группе афатиниба и 10,9 месяцев – в группе гефитиниба (р=0,017), медиана времени до развития рецидива заболевания составила 13,7 vs 11,5 месяцев, соответственно (р=0,0073). Общая эффективность (ОЭ) лечения также оказалась выше в группе афатиниба (70% vs 56%, р=0,0083) [21]. В 2017 году были опубликованы результаты по ОВ данного исследования, она составила 27,9 vs 24,5 месяцев в группах афатиниба и гефитиниба, соответственно (р=0,2580). При анализе ОВ в зависимости от наличия мутаций Del 19 и L858R в группах афатиниба и гефитиниба достоверных различий не получено [21].
Эффективность афатиниба подтверждена и в других исследованиях. Недавно получены данные ретроспективного исследования, проведенного в Тайване, где уровень ОЭ составил 77,2%, медиана выживаемости без прогрессирования – 11,8 месяцев у пациентов в EGFR-мутированным распространенным НМРЛ, получивших афатиниб в 1 линии терапии. В этом исследовании не выявлено влияния дозы препарата (40мг vs <40мг) и типа EGFR мутации (Del 19 vs L858R) на эффективность лечения [9]. В другом ретроспективном анализе (n=165) при проведении терапии афатинибом в первой линии лечения медиана выживаемости без прогрессирования составила 19,1 месяц. Получены достоверные различия по медиане выживаемости в зависимости от типа выявленных EGFR мутаций: при De19 – 19,1 месяц, при L858R – 15,8 месяцев, при Т790М – 4,7 месяцев, р=0,01 [31].
Также выявлена эффективность афатиниба при метастатическом поражении ЦНС. Следует отметить, что по сравнению с общей популяцией пациентов с НМРЛ, приблизительно у 1/3 больных с EGFR мутациями выявляются метастазы в ЦНС [29,35]. В исследовании LL3 эффективность афатиниба была изучена в подгруппе пациентов с бессимптомными метастазами в головной мозг, так выживаемость без прогрессирования составила 11,1 месяц в группе афатиниба и 5,4 месяца – в группе ХТ (цисплатин + пеметрексед) [26,33]. В исследовании LL7 данные о большей эффективности афатиниба при сравнении с гефитинибом в подгруппе больных с бессимптомными метастазами в головной мозг (n=26) не подтвердились [21]. В исследовании FLAURA при терапии осимертинибом отмечено увеличение выживаемости без прогрессирования у пациентов с метастазами в головной мозг по сравнению с больными без метастазов в ЦНС. Кроме того, метастазирование в ЦНС в группе осимертиниба отмечалось достоверно реже по сравнению с группой гефитиниба и эрлотиниба – 6% и 15%, соответственно [28]. Внутримозговая активность осимертиниба оценена в сводном анализе данных II фазы исследований AURA и AURA2 . В этих исследованиях ОЭ метастазов в ЦНС составила 54%, в 12% случаев зарегистрирована полная регрессия (ПР), уровень ЦНС контроля за заболеванием составил 92% [6,7,8]. Основываясь на полученных данных осимертиниб должен быть препаратом выбора у пациентов с EGFR (Del19, L858R) мутированным НМРЛ и метастатическим поражение ЦНС.
В настоящее время афатиниб признан стандартом 1 линии терапии наряду с EGFR ингибиторами тирозинкиназы первого поколения у пациентов с EGFR мутированным распространенным НМРЛ. Первоначально для одобрения афатиниба были использованы результаты исследований LL3 и LL6, в которых было показано достоверное увеличение ОЭ и удлинение выживаемости без прогрессирования по сравнению со стандартной химиотерапией [27,32]. Далее в исследовании LL7 было выполнено сравнение афатиниба с первым поколением EGFR ингибиторов тирозинкиназы гефитинибом, здесь также было отмечено увеличение общей выживаемости, медианы выживаемости без прогрессирования и медианы времени до развития рецидива заболевания в пользу афатиниба вне зависимости от типа мутаций, что может отражать потенциальную способность афатиниба в увеличении сроков до развития ожидаемой резистентности [21]. Следует отметить, что афатиниб не увеличивает показателей общей выживаемости при сравнении со стандратной химиотерапией 1 линии и при сравнении с гефитинибом [21]. Имеются данные о том, что афатиниб продемонстрировал достаточную эффективность при нечасто встречающихся мутациях EGFR, как было недавно показано в объединенном анализе данных исследований LL2, LL3 и LL6 [14,33]. Данных об эффективности дакомитиниба и осимертиниба у пациентов с нечасто встречающимися мутациями нет.
Заключение
Афатиниб представляет собой важный препарат для использования в 1 линии терапии при наличии EGFR мутированного распространенного НМРЛ, он способствует увеличению выживаемости без прогрессирования и общей эффективности при сравнении с химиотерапией первой линии и гефитинибом – препаратом первого поколения EGFR ингибиторов тирозинкиназы. Результаты преклинических и клинических исследований указывают на эффективность терапии афатинибом пациентов с нечасто встречающимися EGFR мутациями (особенно G719X, S768I, комплексные мутации). В исследовании ARCHER было показано, что назначение афатиниба в первую линию при EGFR мутированном (Del19, L858R) НМРЛ способствует увеличению выживаемости. В исследовании FLAURA было показано увеличение эффективности лечения при назначении EGFR ингибиторов тирозинкиназы третьего поколения – осимертиниба в первой линии терапии, что несколько пошатнуло позиции афатиниба. Однако в этом исследовании сравнение проводилось только с препаратами первого поколения EGFR ингибиторов тирозинкиназы – гефитинибом и эрлотинибом. И ответа на вопрос, какой препарат использовать в первой линии терапии, пока нет. С одной стороны можно начать лечение с препарата третьего поколения – осимертиниба, с другой стороны – можно начать терапию с препаратов второго поколения (афатиниб, дакомитиниб), а во вторую линию терапии, при прогрессировании заболевания и появлении мутации Т790М, назначить осимертиниб. Окончательные данные по общей выживаемости позволят нам определить оптимальную тактику лечения пациентов.
Список литературы Немелкоклеточный рак легкого с EGFR мутацией. Терапия афатинибом. Клинический случай
- Большакова С.А., Бычков Ю.М. Новое поколение ингибиторов тирозинкиназы: Афатиниб. «Вестник российского научного центра Рентгенорадиологии». 2018. Т. 18.
- Boehringer Ingelheim. Giotrif prescribing information. Ridgefield, CT: Boehringer Ingelheim Pharmaceuticals , Inc., http.//www.giotrf.com/ (accessed 1 July 2018).
- European Medicine Agency. Giotrif: summary of product characteristics, version 24 May 2016. http://www.ema.europa.eu/docs/en GB/document library/EPAR Product Information/hum an/002280/WC500152392.pdf (accessed 1July 2018).
- Facchinetti F., Rossi G., Bria E., et al. Oncogene addiction in non-small cell lung cancer: focus on ROS1 inhibition. Cancer Treat Res. 2017. V. 55. P. 83-95.
- Floc'h N., Martin M.J., Riess J.W., et al. Antitumor activity of osimertinib an irreversible mutant-selective EGFR tyrosine kinase inhibitor, in NSCLC harboring EGFR exon insertion. 2017. Mol Cancer Ther. V. 17. No. 5. P. 885-896.
- Goss G., Tsai C.M., ShepherdF.A., et al. CNS response to osimertinib in patients with T790M-positive advanced NSCLC: pooled data from two phase II trials. Ann Oncol. 2018. V. 29. No. 3. P. 687-693.
- Goss G., Tsai C.M., Shepherd F.A., et al. Osimertinib for pretreated EGFR Thr790Metpositive advanced non-small-cell lung cancer (AURA2): a multicenter, open-label, single-arm, Phase 2 study. Lancet Oncol. 2016. V. 17. No. 12. P. 1643-1652.
- Janne P.A., Yang J.C., Kim D.W., et al. AZD9291 in EGFR inhibitor-resistant non-small-cell lung cancer. N Engl J Med. 2015. V. 372. No 18. P. 1689-1699.
- Kim Y., Sun J., ParkK., et al. P3.01-023 First-line afatinib for non-small cell lung cancer in real world practice. J Thorac Oncol. 2017. V. 12. No. 11. P. S2209.
- Kobayashi Y., Mitsudomi T. Not all epidermal growth factor receptor mutations in lung cancer are created equal: perspectives for individualized treatment strategy. Cancer Sci 2016. V. 107. No. 9. P. 1179-1186.
- Leonetti A., Facchinetti F., Rossi G., et al. BRAF in non-small cell lung cancer (NSCLC): picketing another brick in the wall. Cancer Treat Rev. 2018. V. 66. P. 82-94.
- Dacic S., Flanagan M., Cieply K., et al. Significance of EGFR protein expression and gene amplification in non-small cell lung carcinoma. Am J Clin Pathol. 2005. V. 125. No. 6. P. 860-865.
- Li D., Ambrogio L., Shimamura T., et al. BIBW2992, an irreversible EGFR/HER2 inhibitor highly effective in preclinical lung cancer models. Oncogene. 2008. V. 27. No. 34. P. 47024711.
- Liang S.K., Hsieh M.S., Lee M.R., et al. Real-world experience of afatinib as s first-line therapy for advanced EGFR mutation positive lung adenocarcinoma. Oncotarget. 2017. V. 8. No. 52. P. 90430-90443.
- Mitsudomi T., Morita S., Yatabe Y., et al. Gefitinib versus cisplatin plus docetaxel in patients with non-small-cell lung cancer harbouring mutations of the epidermal growth factor receptor (wjtog3405): an open label, randomized phase 3 trial. Lancet Oncol. 2010. V. 11. No. 2. P. 121-128.
- Mok T.S., Wu Y.L., Ahn M.J., et al. Osimertinib or platinum-pemetrexed in EGFR T790M-positive lung cancer. N Engl J Med. 2016. V. 376. No. 7. P. 629-640.
- Mok T.S., Wu Y.L., Thongprasers S., et al. Gefitinib or carboplarin - paclitaxel in pulmonary adenocarcinoma. N Engl J Med 2009. V. 361. No. 10. P. 947-957.
- National Comprehensive Cancer Network. Clinical practice guidelines in oncology (NCCN Guidelines): non-small cell lung cancer. Version 1.2018. Fort Washington: National Comprehensive Cancer Network. Inc.
- Ninomiya T., Takigawa N., Ichihara E., et al. Afatinib prolongs survival compared with gefitinib in an epidermal growth factor receptor-driven lung cancer model. Nol Cancer Ther. 2013. V. 12. No. 5. P. 589-597.
- Han J.Y., Park K., Kim S.W., et al. First-signal: first-line single-agent Iressa versus gemcitabine and cisplatin trial in never-smokers with adenocarcinoma of the lung. J Clin Oncol. 2012. V. 30. No. 10. P. 1122-1128.
- Park K., Tan E.H., O'Byrne K., et al. Afatinib versus gefitinib as first-line treatment of patients with EGFR mutation-positive non-small-cell lung cancer (LUX-Lung 7): a phase 2B, open-label, randomized controlled trial. Lancet Oncol. 2016. V. 17. No. 5. P. 577-589.
- Piotrowska Z., Fintelmann F.J., Sequist L.V., et al. Response to osimertinib in an EGFR exon 20 insertion-positive lung adenocarcinoma. J Thorac Oncol. 2018. V. 13. No. 10. P. e204-e206.
- Ricciuri B., De Giglio A., Mecca C., et al. Precision medicine against ALK-positive non-small cel lung cancer: beyond crizotonob. Med Oncol. 2018. V. 35. No. 5. P. 72.
- Rosell R., Carcereny E., Gervais R., et al. Erlotinib versus standard chemotherapy as firstline treatment for European patients with advanced EGFR mutation-positive non-small cell lung cancer (eurtac): a multicenter, open-label, randomized phase 3 trial. Lancet Oncol. 2012. V. 13. No. 3. P. 239-246.
- Rucciuti B., Baglivo S., Paglialunga L., et al. Osimertinib in patients with advanced epidermal growth factor receptor T790M mutation-positive non-small cell lung cancer: rationale, evidence and place in therapy. Ther Adv Med Oncol. 2017. V. 9. No. 6. P. 387404.
- Schuler M., Wu Y.I., Hirsh V., et al. First-line afatinib versus chemotherapy in patients with non-small cell lung cancer and common epidermal growth factor receptor gene mutations and brain metastases. J Thorac Oncol. 2016. V. 11. No. 3. P. 380-390.
- Sequist L.V., Yang JC-H, Yamamoto N., et al. Phase III study of afatinib or cisplatin plus pemetrexed in patients with metastatic lung adenocarcinoma with EGFR mutations. J Clin Oncol. 2013. V. 31. No. 27. P. 3327-3334.
- Soria J.C., Ohe Y., Vansteenkiste J., et al. Osimertinib in untreated EGFR-mutated advanced non-small-cell lung cancer. N Engl J Med. 2018. V. 378. No. 2. P. 113-125.
- Sun M., Behrens C., Feng L., et al. HER family receptor abnormalities in lung cancer brain metastases and corresponding primary tumors. Clin Cancer Res. 2009. V. 15. No. 15. P. 4829-4837.
- Tsiambas E., Lefas A.Y., Georgiannos S.N., et al. EGFR gene deregulation mechanisms in lung adenocarcinoma: a molecular review. Pathol Res Pract. 2016. V. 212. No. 8. P. 672677.
- Wu Y., Tu H., Feng J., et al. P3.01-036 A phase IIIb open-label, single -arm study of afatinib in EGFR TKI-naïve patients with EGFRm NSCLC: an interim analysis. J Thorac Oncol. 2017. V. 12. (Suppl. 2). S2214.
- Wu Y-L., Zhou C., Hu C-P, et al. Afatinib versus cisplatin plus gemcitabine for first -line treatment of Asian patients with advanced non-small-cell lung cancer harbouring EGFR mutations (LUX-Lung 6): an openel, randomized phase 3 trial. Lancet Oncol. 2014. V. 15. No. 2. P. 213-222.
- Yang J.C., Sequist L.V., Greater S.L., et al. Clinical activity of afatinib in patients with advanced non-small-cell lung cancer harboring uncommon EGFR mutations: a combined post-hoc analysis of LUX-Lung 2, LUX-Lung 3, and LUX-Lung 6. Lancet Oncol. 2015. V. 16. No. 7. P. 830-838.
- Yang J.C-H, Wu Y.L., Schuler M., et al. Afatinib versus cisplatin based chemotherapy for EGFR mutation-positive lung adenocarcinoma (LUX-Lung 3 and LUX-Lung 6): analysis of overall survival data from two randomized, phase 3 trials. Lancet Oncol. 2015. V. 16. No. 2. P. 141-151.
- SiegelR.L., Miller K.D., JernalA. Cancer statistics. 2018. CA Cancer J Clin. 2018. V. 67. No. 1. P. 7-30.


