Образование и перенос электронных дефектов в твердом электролите RbCu Cl I. 4 3 2
Автор: Остапенко Г.И., Веселова Л.Г.
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Физика твёрдого тела и твердотельная электроника
Статья в выпуске: 2 т.1, 1999 года.
Бесплатный доступ
Проанализированы причины значительного отличия электронной проводимости для образцов твердого электролита RbCu Cl I, приготовленных в различных условиях. Выдвинуто предположение, что величина электронной проводимости зависит от количества электронных дефектов, возникающих при окислении RbCu Cl I в процессе его приготовления. Рассмотрены соответствующие квазихимические реакции. Из экспериментов с ячейкой Вагнера было выяснено, что концентрация электронных дефектов в исследованном образце RbCu Cl I составляет 1,25Ч1018 cm-3. Коэффициент диффузии электронных дефектов равен 1,5Ч10-8 cм2Чс-1 при их проводимости 1,2Ч10-7 СмЧcм-1. Расчетная величина потенциала стеклоуглеродного электрода после электрохимического разложения RbCu Cl I (0,606 В) удовлетворительно совпадает с экспериментальной величиной (0,58 В), что свидетельствует об адекватности рассмотренной моде ли возникновения электронных дефектов при приготовлении RbCu Cl I. 4 3 2
Короткий адрес: https://sciup.org/148197535
IDR: 148197535
Formation and transport of electronic defects in the solid elecrtolyte RbCu Cl I. 4 3 2
This paper analyses the reasons of considerable difference of electronic conductivity for RbCu Cl I 4 3 2 samples, which were prepared under different conditions by various authors. It is assumed that the value of electronic conductivity depends on quantity of electronic defects, which caused by oxidation of RbCu Cl I during its preparation. The relevant quasi-chemical reactions are considered. 4 3 2 During experiments with Wagner's cell it was determined that the concentration of electronic defects in examined RbCu Cl I sample is equal to 1,25*1018 cm-3. The diffusion coefficient of electronic defects is 4 3 2 equal to 1,5*10-8 cm2*s-1; their conductivity is 1,2*10-7 S*cm-1. The estimated value of potential of vitreous-carbon electrode after electrochemical decomposition of RbCu Cl I (0,606V) coincides with the experimental value (0,58V) satisfactorily. This confirms the adequacy 4 3 2 of considered model of electronic defects formation during preparation of RbCu Cl I. 4 3 2
Текст научной статьи Образование и перенос электронных дефектов в твердом электролите RbCu Cl I. 4 3 2
Твердый электролит RbCu4Cl3I2 наряду с высокой ионной проводимостью по ионам Cu+ обладает электронной проводимостью. Если величина ионной проводимости практически одинакова для образцов RbCu4Cl3I2 , исследованных различными авторами, то величины электронной проводимости значительно отличаются (1016...107 См.см-1 [1-3]). Здесь анализируются возможные причины, от которых может зависеть величина электронной проводимости RbCu4Cl3I2.
Твердый электролит RbCu 4 Cl3I 2 имеет широкую запрещенную зону (Е > 3 эВ [1]) , поэтому возникновение в нем ощутимой собственной электронной проводимости маловероятно. Однако J.Schmidt и J.Bazan [4] для стехиометрического CuI, входящего в состав RbCu 4 Cl3I 2 , предлагают следующий механизм образования электронных дефектов (в обозначениях Ф.Крегера и Х.Винка [5]):
Cuх cu = Cuх i + Vх Cu т.е. ион Cu+ из узла (CuхCu) переходит в междоузлие (Cuх .) с образованием нейтральной вакансии VхCu. Затем эта вакансия иони- зируется
VхГ
Cu
= V Г + h • Cu
с образованием отрицательно заряженной вакансии V Cu и дырки h • . Энергия образования дырки составляет 0,29 эВ .
Однако, как было сказано выше, интервал дырочной проводимости RbCu 4 Cl3I 2 составляет несколько порядков величин. Это характерно для примесной проводимости. Поэтому рассмотрим пути появления примесей в RbCu 4 Cl3I2 . Обычно RbCu 4 Cl3I2 готовят плавлением смеси RbCl, CuCl и CuI с последующим длительным отжигом при 130...200 0С [2,6]. При синтезе галогенидов меди и приготовлении RbCu4Cl 3 I2 могут происходить химические реакции, приводящие к появлению примесей в RbCu4Cl 3 [2 . Эти примеси приводят к возникновению атомных и электронных дефектов в решетке RbCu 4 Cl 3 I2 и появлению электронной проводимости.
Рассмотрим некоторые из этих реакций. В основном это реакции окисления галогенидов меди кислородом воздуха, который а небольших количествах присутствует даже при вакуумировании. Для упрощения будем рассматривать RbCu 4 Cl 3 [2 как смесь индивидуальных галогенидов.
Реакция окисления CuCl :
4CuCl + 1/2 O2 = 2 CuCl2 + Cu2O (1)
Здесь два атома меди уходят на поверхность кристалла CuCl и образуют решетку Cu2O . В глубине кристалла CuCl образуются отрицательно заряженные вакансии V'Cu. CuCl и CuCl2 имеют практически одинаковую упаковку ионов Cl- [7] и образуют твердые растворы [8]. Поэтому CuCl2 , по-видимому, не образует индивидуальную решетку. Следовательно, в узлах решетки, обычно занимаемых Cu+- ионами ( Cu х Cu ), образуются Cu2+- ионы ( Cu • Cu ). Тогда реакцию (1) можно записать:
Cu х„
Cu
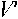
Cu
+ Cu • „
Cu
Cu2 +:
Далее возможна реакция диссоциации
Cu • Cu = Cu х Cu + h • (3)
и захвата дырки отрицательно заряженной вакансией:
V Cu + h ^ = V X Cu (4) с образованием V- центра.
E. Нимон и др . [9] полагают, что имеет место только реакция (2) и в ячейке Вагнера осуществляется перенос ионов Cu2+ терми
чески активированными перескоками электронных носителей между ионами меди различной валентности. Однако C.Schwab и A.Goltzene [7] отмечают, что в монокристаллах CuCl методом ЭПР не обнаружены равновесные ионы Cu2+ и V - центры. Следовательно, в CuCl имеет место реакция (3) и не протекает реакции (4).
Реакция окисления CuI [10]:
2CuI + O2 = 2CuO + Т2-г по-видимому, происходит в две стадии
[11]:
CuI + 1/2O 2 = Cu 2O + I 2 г (5) Cu2O + 1/2O 2 = 2CuO ’г (6)
Вероятно, при протекании реакции (5) на поверхности кристалла CuI строится решетка Cu2O , а внутри кристалла возникают заряженные вакансии меди VCu и иода V • I . Тогда реакцию (5) можно записать:
1/20 2 + 2 Iх I = 12 ОX O +2V Cu + 2V • I +1 2 - , где: Iх I есть I - в решетке CuI, O х O - ион
O2 - в решетке Cu2O . Ассоциация вакансий меди и иода должна привести к разрыхлению кристалла CuI .
При температурах менее 270 0 С закись меди, образовавшаяся на поверхности зерен CuI , содержит избыток кислорода [12] , т.е.
имеет место реакция (6):
1/2O 2 = Oх O ■ 2Vх Cu
Следовательно, при таких температурах CuO не образует индивидуальную решетку, но образует твердые растворы Cu2O - CuO [13], т.е. окислы переменного состава Cu2- x O . При этом часть нейтральных вакансий диссоциирует:
V х Cu = V Cu + h ^ , (7)
что и обеспечивает дырочную проводимость Cu2O .
При повышенных температурах и вакууме из CuI может испаряться иод [14]. Эту реакцию можно записать:
Iх I = Vх I + 1/2I^ (8)
Возникшая нейтральная вакансия иода ( Vх I ) может диссоциировать
Vх I = V • I + e ’ (9)
с образованием избыточного электрона е’.
Практически все приведенные выше реакции создают вакансии в решетке RbCu4Cl 3 I2 и электронные дефекты при его приготовлении. Вакансии теоретически должны привести к увеличению ионной проводимости RbCu4Cl 3 I2 , однако на фоне и без того высокой ионной проводимости по ионам Cu+ этот эффект, по-видимому, незаметен.
Реакции (3), (5) и (9) приводят к образованию дырок и избыточных электронов. Эти электроны, по-видимому, рекомбинируют с дырками. RbCu 403 2 2 имеет дырочную проводимость. Следовательно, реакции (3) и (7) превалируют над реакцией (9). Тем более, что при 200 оС давление паров иода над CuI очень невелико и составляет приблизительно 10 -9 Па [15] и соответственно очень невелико количество образовавшихся по реакциям (8) и (9) избыточных электронов.
Таким образом, можно сделать вывод, что концентрация электронных дефектов зависит от процедуры приготовления RbCu4Cl 3 I2 . Эта концентрация особенно чувствительна к содержанию кислорода в реакционной среде. Следовательно, широкий интервал величин дырочной проводимости в RbCu4Cl 3 I2 можно объяснить различиями условий его приготовления.
Формально, без конкретизации состояния электронных дефектов ( Cu2+ или дырки), с учетом (3) будем записывать электронный
дефект как Cu2+. Так проще записывать химические и электрохимические равновесия в RbCu4Cl 3 I2.
Эксперимент
Исследовали RbCu4Cl 3 I2 , приготовленный по способу, описанному в работе [16].
Ячейки:
Cu /RbCu4Cl 3 I2 / C ( стеклоуглерод) (10) приготавливали в атмосфере сухого воздуха (осушитель Р 2 О 5 ) путем прессования при давлении 2,2 • 10 8 Па порошков RbCu4Cl 3 I2 и меди к плоскому стеклоуглеродному диску диаметром 12 мм. В электролит помещали электрод сравнения из медной проволоки диаметром 0,2 мм. Поджим ячеек составлял примерно 3 • 10 6 Па. Перед измерениями ячейки прокаливали три часа при 140 оС. Измерения проводили с помощью потенциостата П5848 при комнатной температуре.
Результаты и дискуссия
На рис. 1 изображена квазистационарная вольт-амперная характеристика стеклоуглеродного электрода, построенная по результатам потенциостатических измерений. На рис .2 изображена циклическая потенциоди-намическая кривая электрохимического разложения RbCu4Cl 3 I2 на стеклоуглеродном электроде (реверс потенциала при 0,67 Л ).
Рассчитаем равновесную концентрацию ионов Cu2+ в RbCu4Cl 3 I2 . Электроактивны-ми частицами в RbCu4Cl 3 I2 являются ионы Cu+ и Cu2+. Поэтому потенциал медного электрода в RbCu4Cl 3 I 2 :
т о к.Г , [Cu]cu jCu jcu2+/Cu* e [Cu+ ]Cu (11)
о о где: jCu2+/Cu + есть стандартный потенциал пары Cu2+/Cu+ в RbCu4Cl3I2;
[ Cu2 +] Cu - концентрация Cu2+ у медного электрода;
[ Cu +] Cu - концентрация Cu+ у медного электрода;
k - постоянная Больцмана ;
Т - температура;
е - заряд электрона.
Потенциал стеклоуглеродного электрода:
о kT [Cu2+]c jc = jCu 2+,-c ++ T lHKu'L ^
Если предположить, что в RbCu4Cl 3 I2 : [ Cu2 +] << [ Cu +], то [ Cu +] Cu » [ Cu +] C и из (11) и (12) э.д.с. ячейки (10):
kT [Cu 2+ ]C j = jc - jCu = T b—^ (B)
Следовательно, (10) есть концентрационная ячейка и j 0 зависит от соотношения концентраций ионов Cu2+ у электродов.
Величина [ Cu2 +] Cu определяется из равновесия химической реакции:
Cu2+ +Cu0 = 2Cu+.
С использованием j Cu 2 +/ Cu + = 0,624 В [17] при концентрации ионов Cu+ в решетке RbCu4Cl 3 I2 [ Cu +] = 1,585.10 2 см -3 [6] из (11) можно получить:
[Cu2+]Cu = 4,17.1011 cm-3.
Подставляем эту величину в (13) и при j0 = 0,5 В (рис.Р) с учетом “решеточного на сыщения” в RbCu4Cl3I2:
[Cu2+] + [Cu*] = 1,585.102 см -3 получаем:
[Cu2+]C = 1,25.1018 cm-3.
Эта концентрация соответствует содержанию Cu2+ в RbCu4Cl 3 I2 приблизительно 0,8% от всей меди в RbCu4Cl3I2 . С учетом образования твердых растворов CuCl2 в CuCl исследованный RbCu4Cl 3 I2 имеет состав примерно RbCu4-0 03C1 3 L 2 . Эти данные хорошо соответствуют содержанию Cu2+ в RbCu4Cl3I2 около 2% из измерений магнит-
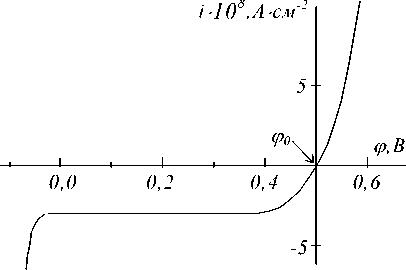
Рис 1. Вольт-амперная характеристика стеклоуглеродного электрода в RbCu4Cl3I2 относительно медного электрода сравнения
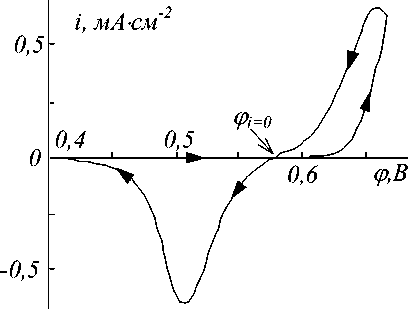
Рис 2. Вольтамперограмма электрохимического разложения RbCu4Cl 3 I 2 на стеклоуглеродном электроде. Скорость развертки потенциала 5 мВЧс1
ной восприимчивости [18].
(При использовании очень чистой СиС1 , при прокаливании под вакуумом 0,1...1 Па с использованием атмосферы сухого аргона получен RbCu4Cl3I2 высокой чистоты [19]. С этим RbCu 4 Cl 3 I2 э.д.с. j 0 в ячейке ( 10 ) равна приблизительно 10 мВ [17], что соответствует [ Си2 +] = 6,2 ■ 1011 см -3 ).
В интервале потенциалов стеклоуглеродного электрода 0... j 0 ионная проводимость по Си + в ячейке ( 10 ) блокирована. Следовательно, горизонтальный участок вольт-амперной характеристики (рис.1) есть предельный диффузионный ток i пр подведения Си2 + к стеклоуглеродному электроду. С учетом реакции (3) проводимость по электронным дефектам исследуемого RbCu4Cl3I2 :
~ _ eLiny sCu '' = sh = kT составляет 1,2.10- См-cм-1, где: L = 1 мм есть толщина слоя КЬСи4С1312 в ячейке (10).
Коэффициент диффузии ионов Си2+ :
_ sCu2 + (kT/e2)
Cu 2 + = [Cu 2 + ]c равен 1,5.10— см2-c-1.
При протекании тока на стеклоуглеродном электроде имеет место электрохимическая реакция:
Cu+ - e = Cu2+ справа налево при j < j0 и слева направо при j > j0. В последнем случае [Си2+] у электрода увеличивается. Как только [Си2+]
превысит предел растворимости Си2 + в RbCu4Cl3I2 , на поверхности электрода пойдет реакция анодного разложения RbCu 4 С1 3 I2 [20]:
RbCu4Cl3I2 = Cu+ + RbCuCl3 + 2CuI (14)
После этой реакции при условии, что продукты реакции полностью покрывают поверхность электрода, одному иону Си2 + из RbCuCl3 соответствуют два иона Си+ из Си1 . Следовательно здесь соотношение [ Си2 +] С / [ Си +] С = 0,5 . При этом соотношении потенциал стеклоуглеродного электрода, вычисленный по (12), должен быть равен 0,606 В . Однако экспериментальный бестоковый потенциал j i= 0 после разложения КЬСи 4 С1 3 12 равен 0,58 В . Различие между расчетным и измеренным бестоковыми потенциалами (26 мВ ) незначительно. Это различие можно объяснить, например, различными коэффициентами активности ионов Си2+ и Си+ в RbCuQ3 и Си1 соответственно, т.е. ошибкой при приравнивании активности и концентрации ионов.
Хорошее соответствие расчетных величин концентрации ионов Си2+ в КЬСи 4 С1 3 12 с экспериментальными э.д.с. ячеек (10) и потенциалом электрохимического разложения электролита свидетельствует об адекватности рассмотренной модели возникновения электронных дефектов при приготовлении RbCu4aзI2 .
Работа выполнена в рамках проекта А 0065 ФЦП “Интеграция”.


