Оценка биологического и радиозащитного действия экспериментальных препаратов
Автор: Фролов А.В., Василевский Н.М., Гурьянова В.А., Майорова Е.Н., Юнусов И.Р., Низамов Р.Н.
Статья в выпуске: 4 т.252, 2022 года.
Бесплатный доступ
Цель проведенных исследований - разработать препарат для коррекции обмена веществ при действии неблагоприятных химических и физических факторов внешней среды. В ходе работы были разработаны 4 варианта препарата- К50-1, К50-2, К80, К100, которые подвергли исследованию на острую токсичность, биологическое действие, способность корректировать обмен веществ при острой лучевой болезни. Результаты исследований показали, что все экспериментальные кормовые добавки относятся к 4 классу опасности (вещества малоопасные); они обладают умеренным стимулирующим эффектом: при длительном поступлении с пищей положительно влияют на рост и развитие организма лабораторных животных; три из них - препараты К50-2, К80, К100 обладают умеренным радиозащитным эффектом: повышают среднюю продолжительность жизни летально облученных белых мышей, соответственно, на 11,4; 15,2 и 7,6 % - при профилактическом и на 21,9; 19,0 и 13,3 % - при лечебно-профилактическом применении.
Кормовые добавки, биологические стимуляторы, адаптогены, острая токсичность, биологическое действие, радиозащитное действие
Короткий адрес: https://sciup.org/142236392
IDR: 142236392 | УДК: 619:616-001.28/.29:579 | DOI: 10.31588/2413_4201_1883_4_252_250
Assessment of biological and radioprotective action of experimental drugs
The purpose of the research is to develop a drug for the correction of metabolism under the influence of adverse chemical and physical environmental factors. In the course of the work, 4 variants of the drug were developed - K50-1, K50-2, K80, K100, which were examined for acute toxicity, biological action, and the ability to correct metabolism in acute radiation sickness. The research results showed that all experimental feed additives belong to the 4th hazard class (substances of low hazard); they have a moderate stimulating effect: with long-term intake with food, they positively affect the growth and development of the body of laboratory animals; three of them - drugs K50-2, K80, K100 have a moderate radioprotective effect: they increase the average life expectancy of lethally irradiated white mice, respectively, by 11.4, 15.2 and 7.6 % -with preventive use and by 21.9, 19.0 and 13.3 % - with treatment and prophylaxis.
Текст научной статьи Оценка биологического и радиозащитного действия экспериментальных препаратов
В условиях современного сельскохозяйственного производства организм животных испытывает воздействие стресс-факторов физической, химической и биологической природы, что приводит к снижению продуктивности [1, 7].
Эффективным способом борьбы со стресс-факторами является использование специальных препаратов – стимуляторов и адаптогенов. Состав таких препаратов различен, в последнее время все больше внимания уделяют средствам, включающим преимущественно вещества природного происхождения [3, 4].
В научной литературе имеется много упоминаний об эффективном использовании биологически активных добавок растительного и животного происхождения в качестве средств защиты животных от действия стресс-факторов различной природы [2, 6, 8].
В связи с вышеизложенным была поставлена цель – разработать препарат для коррекции обмена веществ при действии неблагоприятных химических и физических факторов внешней среды. В ходе исследований отрабатывали четыре варианта препарата в виде кормовых добавок.
Материал и методы исследований. Скрининг компонентов разрабатываемых кормовых добавок проводили на основе приведенных в литературе результатов исследований кормовых добавок аналогичного назначения, акцент делали на использование в рецептуре относительно недорогих легкодоступных компонентов.
Рецептура исследуемых композиций была составлена из веществ растительного и животного происхождения в разных соотношениях. Подготовили четыре состава в твердой форме (однородный порошок с частицами размером до 1 мм), которым присвоили условные наименования: К50-1, К50-2, К80, К100.
Острую токсичность препаратов оценивали в опыте на белых мышах по методике Першина Г.Н. [5]: для оценки каждого препарата сформировали по 10 групп из 5 животных. Препараты вводили в смеси с водой (частицы препарата дополнительно измельчали до размера не более 0,2 мм) внутрижелудочно, доза для первой группы составила 500 мг/кг живой массы, второй – 1000, третьей – 1500, четвертой – 2000, пятой – 2500, шестой – 3000, седьмой – 3500, восьмой – 4000, девятой –4500, десятой – 5000.
Действие препарата при длительном поступлении с кормом определяли в опыте на белых крысах, для чего использовали крысят-отъемышей, из которых сформировали 6 групп, по 10 особей в каждой. Животные первой, второй, третьей, четвертой групп получали обычный корм с добавлением, соответственно, препаратов К50-1, К50-2, К80, К100 в количестве 2 % к массе корма, пятой группы – обычный корм с добавлением препарата К100 в количестве 5 % к массе корма, крысята шестой группы (контрольная) получали только обычный корм. В остальном условия кормления и содержания животных всех групп были одинаковы, соответствовали зоотехническим нормам. Продолжительность опыта составила 30 суток. Учитывали живую массу животных на разных сроках опыта, гематологические показатели, проводили патологоанатомические исследования.
Эффективность разработанных препаратов в качестве радиозащитного средства оценивали в опыте на белых мышах – определяли лечебное, профилактическое и одновременно лечебное и профилактическое действие по интегральному показателю – 30-суточной выживаемости облученных в дозе ЛД100/30 животных, рассчитывали среднюю продолжительность жизни (СПЖ). Острую лучевую болезнь у мышей вызывали путем их облучения на гамма-установке «ПУМА» с источником ионизирующего излучения 137Cs. Опыт поставили на белых мышах живой массой 18-20 г, из которых сформировали 11 групп, по 12 голов в каждой. Препараты задавали в смеси с кормом в количестве 2 % к массе корма. Схема опыта представлена в таблице 1.
Таблица 1 – Схема опыта по оценке радиозащитного действия препаратов
|
Срок опыта |
Группа опыта |
||||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
КО |
К |
|
|
1-30 сутки |
ОР |
ОР |
ОР |
ОР + К502 |
ОР + К80 |
ОР + К10 0 |
ОР + К502 |
ОР + К80 |
ОР + К10 0 |
ОР |
ОР |
|
Облучение в дозе 7,7 Гр (ЛД 100/30 ) |
|||||||||||
|
31-60 сутки |
ОР + К502 |
ОР + К80 |
ОР + К10 0 |
ОР |
ОР |
ОР |
ОР + К502 |
ОР + К80 |
ОР + К10 0 |
ОР |
|
Примечание: ОР – основной рацион; КО – контроль облучения; К – биологический контроль.
Статистическую обработку полученных результатов проводили методом вариационной статистики с применением критерия достоверности Стьюдента.
Результат исследований. В ходе опыта по определению острой токсичности ни в одной из групп после введения препаратов не отмечали гибели. Клинические признаки интоксикации наблюдали при дозах 4000 мг/кг и выше, наиболее ярко выражены они были в группах, где мыши получали препараты К80 и К100 в максимальной дозе – 5000 мг/кг: в течение 4–5 часов после введения препаратов у животных отмечали беспокойство, отказ от корма, разжижение каловых масс.
Далее был поставлен опыт, по оценке биологического действия экспериментальных препаратов. На всем протяжении эксперимента животные имели нормальную пищевую возбудимость, адекватно реагировали на внешние раздражители. Нарушений работы системы пищеварения у них не отмечали.
Результаты измерения живой массы опытных и контрольных животных представлены на рисунке 1.
Как видно из данных, представленных на рисунке, животные разных групп имели различные темпы роста: начиная с 7-10 суток живая масса животных 1, 2, 3, 4 групп заметно превосходила аналогичный показатель в контроле, эта тенденция сохранялась до конца эксперимента; масса животных 5 группы росла параллельно контрольному значению, существенно от него не отличалась. К концу опыта разница с контролем составила 4,0; 4,7; 4,5; 4,9; 0,2 % для 1, 2, 3, 4, 5 групп, соответственно.
Малый прирост живой массы животных 5 группы обусловлен, по нашему мнению, либо существенным отклонением дозы препарата от оптимального значения (5 % к массе рациона против 2 % в 4 группе), либо снижением потребления корма из-за изменения его органолептических показателей, либо сочетанием этих двух факторов.
Для более полного изучения действия препарата на организм белых крыс проводили оценку их гематологических показателей – определяли содержание гемоглобина, количество эритроцитов и лейкоцитов. Результаты этих исследований представлены в таблице 2.
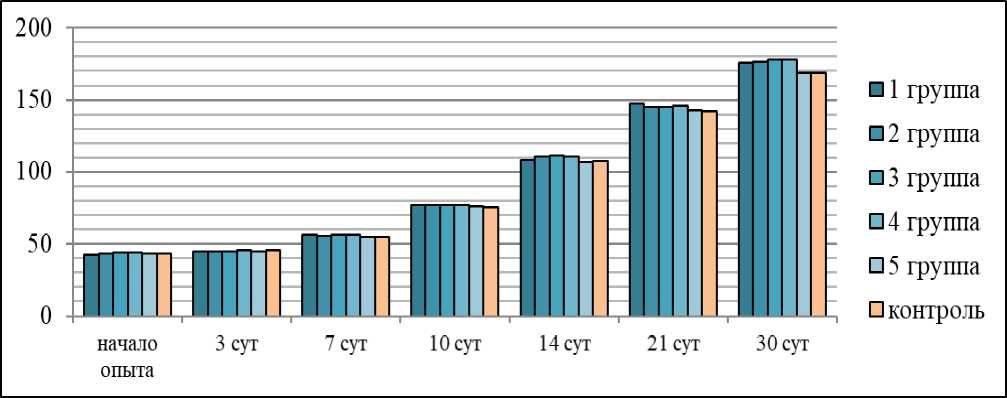
Рисунок 1 – Живая масса подопытных крыс на разных сроках опыта, г
Таблица 2 – Гематологические показатели подопытных крыс (n=5)
|
Группа опыта |
Количество гемоглобина, г/100 мл |
Количество эритроцитов, 1012/л |
Количество лейкоцитов, 109/л |
|
1 |
13,8±0,69 |
6,91±0,58 |
12,9±0,53 |
|
2 |
13,1±0,81* |
6,58±0,60 |
13,3±0,35* |
|
3 |
12,7±0,68 |
6,94±0,51* |
13,1±0,29 |
|
4 |
13,3±0,58* |
6,44±0,49* |
13,3±0,45 |
|
5 |
12,7±0,55 |
6,72±0,61 |
12,6±0,43 |
|
контроль |
12,9±0,70 |
6,56±0,63 |
12,9±0,58 |
*Р<0,05
Как видно из таблицы, значения гематологических показателей всех животных были в пределах нормы, в опыте и контроле различались несущественно.
По окончании опыта для изучения влияния препаратов на состояние и степень развития внутренних органов крыс проводили патологоанатомические исследования, их результаты представлены в таблице 3.
Из данных таблицы видно, что в группах, где животные получали препараты К50-1, К50-2, К80 и К100 в дозе 2 %, масса внутренних органов животных превышала контрольные значения на величину до 3,4; 4,6; 7,1; 14,3 %, соответственно. Препарат К100 в дозе 5 % показал значения близкие к контрольным.
Патологических изменений в органах и тканях подопытных животных не обнаружено. Три композиции, показавшие максимальную биологическую эффективность, – К50-2, К80, К100, подвергли исследованию на наличие у них радиозащитного действия. Результаты этого опыта представлены на рисунках 2 и 3.
Как видно из графиков, включение в рацион мышей кормовых добавок после облучения (оценка лечебного действия) не обеспечило существенного радиозащитного эффекта: повышения выживаемости опытных животных на конец эксперимента не наблюдали, отмечен лишь эффект незначительного увеличения СПЖ опытных животных 1, 2 и 3 групп по сравнению с контрольными – на 5,7; 2,9 и 1,0 %, соответственно.
Таблица 3 – Патологоанатомические показатели подопытных крыс (n=5)
|
Масса органа |
Группа опыта |
|||||
|
1 |
2 |
3 |
4 |
5 |
контроль |
|
|
Тимус, мг |
280,3±3,3* |
279,1±4,0 |
276,5±4,5* |
278,1±5,0* |
276,8±4,5 |
275,3±4,2 |
|
Селезенка, мг |
163,8±5,9* |
162,5±3,7* |
163,2±4,1 |
165,1±3,5* |
158,9±3,2 |
160,3±2,3 |
|
Надпочечники, мг |
49,1±3,1* |
48,6±3,0* |
48,1±3,8 |
47,9±3,1 |
48,1±3,6 |
47,5±2,1 |
|
Печень, г |
4,2±0,04 |
4,5±0,05 |
4,3±0,07 |
4,3±0,04* |
4,2±0,08 |
4,3±0,08 |
|
Почки, г |
1,5±0,02* |
1,4±0,02 |
1,5±0,03* |
1,6±0,05 |
1,5±0,08 |
1,4±0,04 |
*Р<0,05
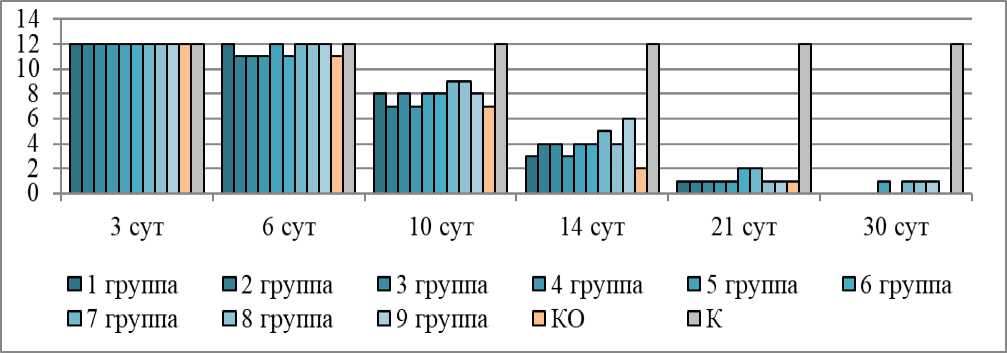
Рисунок 2 – Выживаемость мышей на разных сроках опыта, гол.
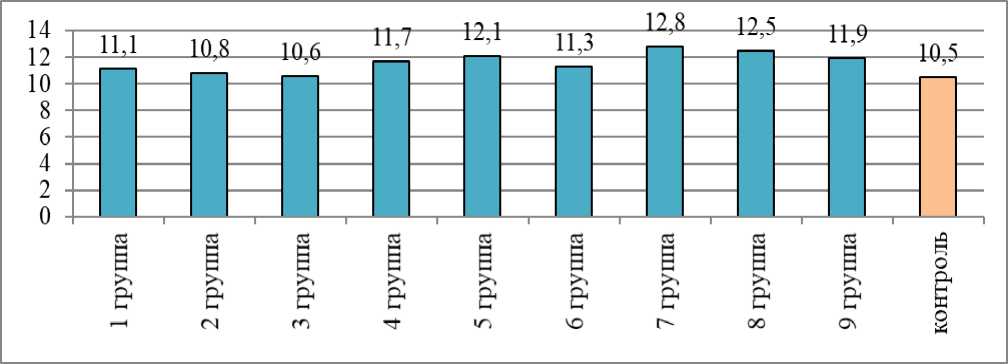
Рисунок 3 – Средняя продолжительность жизни павших мышей, сут.
При скармливании мышам препарата с последующим облучением (оценка профилактического действия) отмечали более выраженный радиозащитный эффект: выживаемость животных 5 группы была выше контрольного значения на 8,3 %, СПЖ в 4, 5 и 6 группах была выше, чем в контроле, соответственно, на 11,4; 15,2 и 7,6 %.
Максимальный эффект был получен при включении препаратов в рацион до и после облучения (оценка лечебного и профилактического действия): выживаемость животных всех групп была на 8,3 % выше контрольного значения, СПЖ – выше на 21,9; 19,0 и 13,3 % в 7, 8 и 9 группах, соответственно.
Заключение. Результаты проведенных исследований позволяют сделать следующие выводы: препараты К50-1, К50-2, К80, К100 относятся к 4 классу опасности (вещества малоопасные); они обладают стимулирующим эффектом: при длительном поступлении в количестве 2 % к массе корма положительно влияют на рост и развитие организма лабораторных животных; препараты К50-2, К80, К100 обладают умеренным радиозащитным эффектом.
растительного происхождения для
Резюме
Цель проведенных исследований – разработать препарат для коррекции обмена веществ при действии неблагоприятных химических и физических факторов внешней среды. В ходе работы были разработаны 4 варианта препарата– К50-1, К50-2, К80, К100, которые подвергли исследованию на острую токсичность, биологическое действие, способность корректировать обмен веществ при острой лучевой болезни.
Результаты исследований показали, что все экспериментальные кормовые добавки относятся к 4 классу опасности (вещества малоопасные); они обладают умеренным стимулирующим эффектом: при длительном поступлении с пищей положительно влияют на рост и развитие организма лабораторных животных; три из них – препараты К50-2, К80, К100 обладают умеренным радиозащитным эффектом: повышают среднюю продолжительность жизни летально облученных белых мышей, соответственно, на 11,4; 15,2 и 7,6 % – при профилактическом и на 21,9; 19,0 и 13,3 % – при лечебно-профилактическом применении.
Список литературы Оценка биологического и радиозащитного действия экспериментальных препаратов
- Жербин, Е. А. Радиационная гематология / Е. А. Жербин, А. В. Чухловин. - М.: Медицина, 1989. -176 с.
- Курило, А. И. Ветеринарногигиенические основы применения биологически активных веществ растительного происхождения для профилактики лучевых поражений: автореф. дис.. доктора ветеринарных наук. - Санкт-Петербург, 1997. - 45 с.
- Низамов, Р. Н. Радиозащитная эффективность натуральной биологически активной кормовой добавки "Вита-Форце М" / Р. Н. Низамов // Вестник Российской военно-медицинской академии. - 2015. -№ 3. - С. 156-158.
- Низамов, Р. Н. Радиозащитные композиции на основе продуктов метаболизма E. Coli / Р. Н. Низамов // Ветеринарный врач. - 2013. - № 4. - С. 2527.
- Першин Г. Н. Методы экспериментальной химиотерапии / Г. Н. Першин. - Москва, 1979. - 541 с.
- Симонова, Л. И. Позитивный радиомодифицирующий эффект новой биологически активной добавки из черноморских моллюсков / Л. И. Симонова // Тезисы докладов 4 съезда по радиационным исследованиям (радиобиология, радиоэкология, радиационная безопасность). - Москва, 2001. - Т. 2. - С. 463-465.
- Тухфатуллов, М. З. Оценка радиозащитных свойств натуральной биологически активной кормовой добавки нового поколения "Вита-Форце М" на лабораторных животных / М. З. Тухфатуллов // Ветеринария, Зоотехния и Биотехнология. - 2018. - № 12. - С. 72-78.
- Muzzarelly R. A. A. Chitin / R. A. A. Muzzarelly. - Oxford: Pergamon Press, 1971. - 309 p.


