Особенности гастроинтестинальных поражений при пищевой аллергии у детей дошкольного возраста
Автор: Сазанова Н.Е., Шабунина Е.И., Галова Е.А., Хохлова Н.М.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 4-1 т.24, 2009 года.
Бесплатный доступ
В статье представлена клинико-функциональная, иммунологическая, морфологическая и иммуногистохимическая характеристика поражений верхнего отдела ЖКТ у детей дошкольного возраста с атопическим дерматитом и кожно-гастроинтестинальными проявлениями пищевой аллергии (ПА). Установлены высокая частота воспалительного процесса в слизистой оболочке (СО) желудка и ДПК, сочетанный характер их поражения, преобладание диффузных форм гастрита и дуоденита, частое вовлечение в воспалительный процесс тонкой кишки с нарушением ее функционального состояния. Доказан аллергический генез воспалительного процесса в СО при гастроинтестинальных поражениях у детей с атопическим дерматитом и кожно-гастроинтестинальной формой ПА с участием преимущественно IgE-опосредуемого механизма. Об этом свидетельствовали выраженная тканевая эозинофилия по всей глубине СО с инфильтрацией эозинофилами эпителия, особенности тучноклеточной популяции, резкое нарастание в СО IgE-плазмоцитов с преобладанием их над IgG-клетками. На органном и тканевом уровнях показано, что аллергический воспалительный процесс в гастродуоденальной СО у детей с ПА протекает на фоне сниженного уровня местной иммунологической и неспецифической защиты
Пищевая аллергия, дети, гастроинтестинальные поражения, морфометрия, аллергическое воспаление, иммуногистохимия
Короткий адрес: https://sciup.org/14919137
IDR: 14919137 | УДК: 616.33-002.2:616.342-002:616-053.4
Features of gastrointestinal disorders in nutritional allergy in preschool children
Clinical, functional, immunological, morphological and immunohistochemical disorders of gastrointestinal tract in preschool children having atopic dermatitis and food allergy are presented in this article.The study performed revealed high frequency of inflammation in the stomach and duodenum with diffuse forms of gastritis and duodenitis and function disorders of intestines. Histologic and immunohistochemical changes of mucous membrane in stomach and duodenum are described. The role of local immunity in pathogenesis of chronic gastroduodenitis in children having nutritional allergy was demonstrated.
Текст научной статьи Особенности гастроинтестинальных поражений при пищевой аллергии у детей дошкольного возраста
E-mail: Galova75@mail.ru
ОСОБЕННОСТИ
ГАСТРОИНТЕСТИНАЛЬНЫХ ПОРАЖЕНИЙ ПРИ ПИЩЕВОЙ АЛЛЕРГИИ
У ДЕТЕЙ ДОШКОЛЬНОГО ВОЗРАСТА
ФГУ «НИИ детской гастроэнтерологии Росмедтехнологий», г. Нижний Новгород
Механизмы формирования этих заболеваний наименее изучены у детей младшего возраста. Имеющиеся в литературе немногочисленные исследования свидетельствуют о ранней их манифестации и хронизации, этиологической многофакторности и патогенетической неоднородности, склонности к ре-цидивированию и прогрессированию, недостаточной эффективности лечения [6, 7, 8, 9, 10].
рованием хронической органной патологии [14, 15, 16, 17].
В свете указанного целью работы явилось изучение клинико-функциональных, иммунологических и морфологических особенностей гастроинтестинальных поражений у детей дошкольного возраста с различными формами ПА.
МАТЕРИАЛ И МЕТОДЫ
Под наблюдением находилось 137 детей 3-6 лет с ПА, представленной у 104 больных атопическим дерматитом (группа АД), у 33 – кожно-гастроинтестинальной формой (группа ПА).
С учетом возможности вовлечения тощей кишки в аллергический воспалительный процесс при ПА у части больных выполнена еюноскопия с биопсией СО тощей кишки. Одновременно оценивалось функциональное состояние тонкой кишки по ее абсорбционной способности (проба с Д-ксилозой) и уровню гидролиза лактозы (стандартный лактозотеларт-ный тест), у ряда пациентов исследовалось содержание в сыворотке крови эссенциального микроэлемента цинка (метод атомно-абсорбционной спектроскопии) как показателя, снижение которого может в определенной мере отражать степень морфофункциональных нарушений в ДПК и тощей кишке, где преимущественно всасывается цинк.
Диагностика ПА включала сбор аллергологического анамнеза, анализ пищевого дневника, проведение элиминационно-провокационных проб, кожное тестирование, определение в сыворотке крови специфических IgE- и IgG-антител к пищевым белкам (ИФА), уровня общего IgE (ИФА).
Оценка иммунологического статуса проводилась по общепринятым показателям гуморального и клеточного иммунитета. Состояние местной защиты определялось по содержанию иммуноглобулинов А, М, G и SIgA в дуоденальном содержимом методом простой радиальной иммунодиффузии по Манчини и по активности лизоцима желудочного и дуоденального соков нефелометрическим методом В.Г. Доро-фейчук (1968).
Обработка цифрового материала результатов исследования проводилась с использованием пакетов компьютерных программ Statistica 6.0 for Windows ХР и «Биостат» в соответствии с общепринятыми современными методами статистического анализа. При сравнении полученных данных пользовались критерием Стъюдента. Проверка нормальности распределения проводилась методом Шапиро-Уилка. Описательная статистика признака включала среднюю арифметическую (M), стандартную ошибку средней (m).
Нулевые гипотезы отвергались при достигнутом уровне значимости соответствующего статистического критерия р<0,05, что принято в биологии и медицине.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Как показали клинические исследования, у детей с атопическим дерматитом аллергический процесс на коже носил характер распространенного, преимущественно (90,4%) среднетяжелого течения, в стадии обострения или неполной ремиссии и проявлялся в виде специфических элементов и очагов эритематозно-сквамозного и лихеноидного характера, приуроченных к типичным местам локализации и сопровождавшихся зудом различной интенсивности. Формирование АД у большинства больных (72%) происходило в первой половине года. Наследственная отягощенность по аллергии имела место у 64,8% обследованных, а частота гастродуоденальной патологии у родственников в семейном анамнезе составила 21%.
По данным скарификационных кожных проб с пищевыми аллергенами, сенсибилизация к различ- ным пищевым белкам выявлена в 90% случаев: к куриному яйцу (64,2%), мясу курицы (58,9%), коровьему молоку (58,9%), рыбе (41,1%), цитрусовым (41,1%). У 71,2% больных определялись повышенные титры специфических IgE-антител, в том числе к яичному белку (58,6%), коровьему молоку (48,6%), рыбе (27,1%), пшенице (27,1%), цитрусовым (25,7%).
Диагностически значимые титры IgG-антител к пищевым белкам также выявлялись у большинства больных (85%), наиболее часто к коровьему молоку и его фракциям (77,1%) и глиадину (47,2%), реже – к сое (37,1%) и овальбумину (34,4%).
Уровень общего IgE (203±30,8 МЕ/мл) значительно превышал возрастную норму (20±3,3 МЕ/мл, Р=0,0001), при этом IgE-гипериммуно-глобулине-мия определялась у 93,2% пациентов и отличалась стойкостью в процессе динамического наблюдения.
Таким образом, результаты аллерготестов свидетельствовали о ведущей роли ПА в генезе аллергодерматоза у больных изучаемой группы и об участии в пищевых аллергических реакциях наряду с IgE-, IgG-опосредуемых механизмов.
В группе больных с кожно-гастроинтестинальной формой ПА ведущими проявлениями аллергии являлись эпизодически возникающие кожные изменения в виде ограниченных очагов эритематозносквамозного поражения, зудящих сыпей, отеков Квинке, аллергической крапивницы. Для больных этой группы было характерно наличие в анамнезе ранних симптомов аллергического поражения кожи: у 72,6% пациентов в первые месяцы жизни имели место проявления младенческой формы АД.
Наряду с этим у большинства пациентов (90%) наблюдались гастроинтестинальные проявления ПА, манифестировавшие также в основном на первом году жизни и, как правило, совпадавшие с периодами обострения кожного аллергического процесса: дис-кинетические расстройства со стороны кишечника (поносы, запоры или их чередование) – 65,5%, тошнота, рвота, метеоризм – 35%, болевой абдоминальный синдром, нередко по типу кишечных колик – 38,2%. Первые проявления ПА, как и у детей с АД, были связаны чаще всего с введением в питание коровьего молока и молочных продуктов, реже – соков, овощных и фруктовых пюре. Семейный анамнез больных данной группы характеризовался высокой частотой не только аллергических (63%), но и заболеваний гастродуоденальной системы (59,4%), а также наличием у трети пациентов наследственной отягощенности одновременно по аллергии и патологии пищеварительного тракта.
По данным кожного тестирования, пищевая сенсибилизация выявлялась в 96,2% случаев, при этом частота положительных проб с отдельными пищевыми аллергенами не отличалась от таковой у детей с АД. Диагностически значимые титры специфических IgG-антител определялись у 84% пациентов, как и при АД, наиболее часто к коровьему молоку 23
и его фракциям (79%) и глиадину (50%). Уровень общего IgE (115,5±13,47 МЕ/мл) в 4 раза превышал возрастную норму (Р=0,0001), при этом повышенные показатели имели место у 100% обследованных.
Наряду с IgE-гипериммуноглобулинемией характерными особенностями иммунного статуса у больных обеих групп являлось умеренное снижение содержания CD3-клеток (53,54±0,56% и 54,26±0,82% против 65,25±0,73% в норме, Р=0,0001 и Р=0,0001) и дисбаланс иммунорегуляторных клеток с дефицитом CD8 (15,09±0,48% и 14,58±0,68% против 25,7±0,54% в норме, Р=0,0001 и Р=0,0001) и повышенным значением ИРИ (2,97±0,11 и 3,02±0,14 при норме 1,54± 0,03, Р=0,0001 и Р=0,0001), что отражало наличие у пациентов атопической гиперчувствительности, лежащей в основе как аллергического поражения кожи, так и ассоциированного с ним воспалительного процесса в гастродуоденальной слизистой.
Изменения гуморального иммунитета у больных обеих групп также были аналогичными: умеренное снижение IgA (0,87±0,11 г/л и 0,88±0,10 г/л против 1,26±0,1 г/л у здоровых, Р=0,014 и Р=0,009), повышение IgM (1,22±0,04 г/л и 1,25±0,05 г/л против 0,87±0,08 г/л, Р=0,0001 и Р=0,0001) при нормальном среднем значении IgG (10,50±0,36 г/л и 11,15± 0,60 г/л). Увеличение концентрации IgE и IgM сопровождалось повышением ЦИК более чем у половины обследованных (163,3±8,2 мкг/мл и 186,6± 12,5 мкг/мл против 115,0±1,7 мкг/мл, Р=0,0001 и Р=0,0001).
Наряду с яркими проявлениями аллергодерматоза для детей с АД при поступлении в клинику была характерна нерезкая выраженность клинических проявлений со стороны ЖКТ: болевой синдром отсутствовал у 33% больных, а диспепсические расстройства и нарушения характера стула, преимущественно в виде запоров, отмечались лишь у трети пациентов (35,5%), нерезкая пальпаторная болезненность живота в пилородуоденальной зоне – менее чем у половины детей. Признаки хронической интоксикации выявлялись в 49% случаев, физиче-
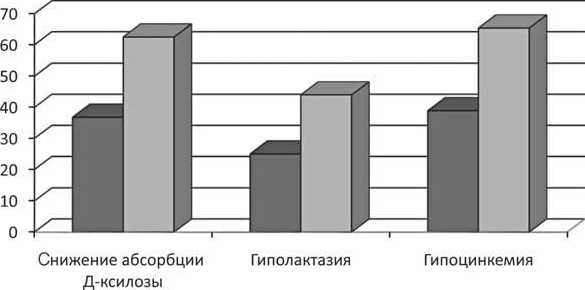
■ АД ОПА
Рис. 1. Частота нарушений функционального состояния тонкой кишки у детей с различными формами ПА (в %).
* – различия между группами статистически значимы (Р=0,029)
ское развитие у большинства детей (84,5%) не нарушалось.
Для больных с ПА была характерна более яркая, чем при АД, клиника гастроинтестинального поражения с высокой частотой и выраженностью болевого (88%) и диспепсического (67%) синдромов, нарушениями стула (70%) с одинаковой частотой разжижения и склонности к запорам, пальпаторной болезненностью в пилородуональной зоне у двух третей пациентов, изменением кислотообразования у 50% больных с преобладанием повышенной продукции.
Установлена более высокая по сравнению с АД частота нарушения функционального состояния тонкой кишки: недостаточность гидролиза лактозы у 44% пациентов, снижение всасывания Д-ксилозы, преимущественно в проксимальном отделе тонкой кишки (62,5%), дефицит цинка в сыворотке крови (65%), что косвенно могло свидетельствовать о более выраженных структурных изменениях СО ДПК и большей частоте вовлечения в воспалительный процесс тощей кишки у детей с кожно-гастроинтестинальными проявлениями ПА по сравнению с АД.
Выполненная у 27 пациентов эндоскопия тощей кишки обнаружила явления еюнита у половины детей с АД, преимущественно эритематозного, и в 95% случаев у пациентов с ПА с одинаковой частотой субатрофических и эритематозных поражений.
Аналогичный характер изменений СО выявлен при гистологии еюнобиоптатов у 27 больных. Гистологическая картина хронического еюнита имела место у всех обследованных. Преобладающей формой поражения был диффузный еюнит (71,4% и 70%), который у трети больных сочетался с субатрофией ворсинок.
Результаты морфометрического исследования биоптатов у 83 больных с АД и 31 ребенка с ПА подтвердили наличие в СО всех отделов гастродуоденальной области выраженного воспалительного процесса, о чем свидетельствовали увеличение в эпителии межэпителиальных лимфоцитов, а в собственной пластинке – повышение клеточной плотности инфильтрата и всех клеточных форм, ответственных за воспаление, особенно незрелых и зрелых плазматических клеток, макрофагов, нейтрофилов, в меньшей степени – лимфоцитов. Характерной особенностью инфильтрата было значительное увеличение эозинофильных гранулоцитов, что сочеталось с постоянным нахождением в эпителии межэпителиальных эозинофилов (МЭЭ), которые в норме не встречаются. Так, в СО ДПК содержание эозинофилов в собственной пластинке ворсинок у больных изучаемых групп составило 520±58 и 489±51 при норме 171±61 клеток на 1 мм2 (Р=0,0001 и Р=0,0001), а в межкриптальном пространстве – 444±47 и 440± 34 клеток на 1 мм2 при норме 102±57, Р=0,0001 и Р=0,0001. Одновременно обнаруживалось накопле- ние МЭЭ в ворсинках (1,89±0,17% и 2,03±0,22%, Р=0,0001 и Р=0,0001) и в криптах (1,53±0,11% и 1,32±0,12%, Р=0,0001 и Р=0,0001). Наличие выраженной тканевой эозинофилии по всей глубине СО ДПК с высоким содержанием МЭЭ отражало участие аллергического (атопического) механизма в ее поражении. Аналогичные результаты были получены при морфометрическом анализе биоптатов СО тощей кишки.
Аллергический генез поражения гастродуоденальной СО подтверждался и результатами исследования у 62 больных АД и 27 детей с ПА тучноклеточной популяции. Общее количество тучных клеток в СО ДПК у больных обеих групп более чем в 2 раза превышало показатели нормы (765±17% и 630±26% против 304±41%, Р=0,0001 и Р=0,0001), при АД это повышение было более существенным (Р=0,0001). Значительно увеличенным оказался и процент дегранулированных форм тучных клеток без статистически значимой разницы в группах (66±1,7% и 64,6±3% против 26,2±3,1%), а постоянной находкой было наличие у больных распадающихся форм клеток. По данным Т.П. Дюбковой (1992), наличие последних в СО является отражением высокой функциональной активности тучных клеток и весьма характерно для хронического гастродуоденита у детей с аллергодерматозами [20].
При иммуногистохимическом исследовании СО ДПК у 53 детей отмечено (табл. 1), что у больных обеих групп имеет место значительное повышение количества плазмоцитов, синтезирующих иммуноглобулины всех классов, что свидетельствовало об активации местной иммунной реакции гуморального типа. Наиболее существенным было увеличение IgE-плазмоцитов, которое наблюдалось у всех пациентов, а среднее содержание этих клеток превышало показатели здоровых при АД в 13 раз, а при ПА – в 10 раз.
Изменялось соотношение клеток: удельный вес плазмоцитов, продуцирующих основной защитный белок – IgA, снижался в 2 раза, несмотря на увеличе-
Таблица 1
Иммуногистохимические показатели СО ДПК у больных изучаемых групп (М ± т)
|
Показатели кл. на 1 мм2 |
Неизмененная СО ДПК (n=9) |
Дети с АД (n=42) |
Дети с ПА (n=11) |
Р 1-2 |
Р 1-3 |
р Р 2-3 |
|
1 |
2 |
3 |
||||
|
Клетки, продуцирующие IgA |
567±53 (58,1%) |
1150±51 (36,5%) |
1098±61 (39,3%) |
0,0001 0,01 |
0,0001 |
– |
|
Клетки, продуцирующие IgM |
293±31 (30,1%) |
777±38 (24,6%) |
781±96 (28,0%) |
0,0001 |
0,0001 |
– |
|
Клетки, продуцирующие IgG |
66±12 (6,8%) |
574±44 (18,2%) |
434±76 (15,5%) |
0,0001 |
0,0001 |
0,011 |
|
Клетки, продуцирующие IgE |
49±15 (5,0%) |
654±31 (20,7%) |
479±66 (17,2%) |
0,0001 |
0,0001 |
0,0001 |
Р – достигнутый уровень значимости критерия различий между группами.
ние абсолютного числа этих клеток; напротив, процентное содержание IgG-плазмоцитов, осуществляющих вторую линию защиты, повышалось в 2,5 раза, а доля IgE-клеток возрастала у больных обследуемых групп в 4 и 3,5 раза. Соотношение среднего числа IgE- и IgG-плазмоцитов было более 1, в то время как в неизмененной СО оно не превышает 0,74; данный факт свидетельствовал о преобладающем местном синтезе иммуноглобулинов класса Е над IgG-антителами.
Значительное повышение абсолютного и относительного числа IgE-плазмоцитов наряду с выраженной тканевой эозинофилией по всей глубине СО, накопление в эпителии МЭЭ, а также особенности тучноклеточной популяции подтверждали аллергический генез воспалительного процесса в гастродуоденальной зоне с участием преимущественно IgE-опосредуемого механизма.
Известно, что непременное условие вовлечения ЖКТ в патологический процесс при аллергии – снижение его барьерной функции. Ведущим фактором местного иммунитета является секреторный IgA, осуществляющий основную защиту СО от пищевых, бактериальных и иных антигенов. Доказано, что SIgA способен блокировать реакции реагинового типа на поверхности эпителия СО ЖКТ.
Проведенное нами у 46 больных изучение содержания SIgA в эпителиальных клетках СО ДПК обнаружило уменьшение его концентрации в эпителии у большинства больных (70%) без статистически значимой разницы в группах, что проявлялось уменьшением яркости специфического свечения. С учетом повышенного абсолютного числа IgA-плазмоцитов в собственной пластинке СО это снижение, очевидно, было обусловлено недостаточным синтезом SC-компонента в эпителиоцитах, что подтверждалось при исследовании SIgA в дуоденальном соке.
Концентрация SIgA в соке ДПК у больных обеих групп была статистически значимо снижена по сравнению со здоровыми (0,153±0,013 г/л и 0,121± 0,016 г/л против 0,195±0,020, Р=0,0001 и Р=0,0001), наиболее значимо в группе детей с ПА (Р=0,012), где отмечалась и большая по сравнению с АД частота сниженных показателей SIgA (88,8% против 58%, Р=0,005).
Одновременно был установлен сниженный уровень неспецифической защиты пищеварительных секретов. Так, лизоцимная активность дуоденального сока в группах больных составила 33,5±1,62% и 37,4±2,83% против 58,5±3,1% у здоровых (Р=0,0001 и Р=0,0001), а активность лизоцима желудочного сока, изученная в динамике секреторного процесса, была снижена во всех порциях сока без статистически значимой разницы в группах. Наиболее низкие показатели лизоцимной активности выявлялись в стимулированной порции желудочного секрета (45±3% и 44,8±3,52% против 72,9±1,1% у здоровых, Р=0,001 и Р=0,001).
Морфометрический анализ клеток, осуществляющих неспецифическую тканевую защиту, также выявил сниженное их содержание в СО ДПК у больных обеих групп. Так, количество клеток Панета составило соответственно 2,32±0,12 и 2,26±0,19 против 3,9±0,2 клеток на крипту в норме (Р=0,0001 и Р=0,0001). Одновременно у больных обеих групп было снижено количество бокаловидных клеток в ворсинках (8,13±0,25% и 8,29±0,49% против 10,23± 1,29% в норме, Р=0,00001 и Р=0,0256) и в криптах (13,66±0,39% и 15,03±0,87% против 18,68±2,03% в норме, Р=0,00001 и Р=0,0115).
Таким образом, проведенные исследования показали, что у детей с ПА аллергический воспалительный процесс в верхних отделах пищеварительного тракта протекает на фоне сниженного уровня местной иммунологической и неспецифической защиты, что доказано на органном и тканевом уровнях.
ВЫВОДЫ
Список литературы Особенности гастроинтестинальных поражений при пищевой аллергии у детей дошкольного возраста
- Заболеваемость органов пищеварения у детей в Ставропольском крае/И.В. Катаев [и др.]//Актуальные проблемы абдоминальной патологии у детей: материалы XIV Конгресса детских гастроэнтерологов России (Москва, 13-15 марта 2007 г.). -Москва, 2007. -С. 25-26.
- Ямолдинов Р.Н. Возрастная структура заболеваний органов пищеварения у детей/Р.Н. Ямолдинов//Актуальные проблемы абдоминальной патологии у детей: материалы XIV Конгресса детских гастроэнтерологов России (Москва, 13-15 марта 2007 г.). -Москва, 2007. -С. 43-44.
- Щербаков П.Л. Вопросы педиатрической гастроэнтерологии./П.Л. Щербаков//Русский медицинский журнал. -2003. -Т. 11, №3. -С. 107-113.
- Гончар Н.В. Взгляд на проблему хронического гастродуоденита у детей спустя 30 лет/Н.В. Гончар, М.И. Соколова//Актуальные проблемы абдоминальной патологии у детей: материалы юбилейного XV Международного конгресса детских гастроэнтерологов России и стран СНГ (Москва, 18-20 марта 2008 г.). -Москва, 2008. -С. 126-127.
- Бурлацкая А.В. Структура заболеваемости верхних отделов желудочнокишечного тракта у детей г. Краснодара по данным детского стационара//А.В. Бурлацкая, Л.В. Карпенко, Н.В. Левицкая/Актуальные проблемы абдоминальной патологии у детей: материалы XIII Конгресса детских гастроэнтерологов России (Москва, 21-23 марта 2006 г.). -Москва, 2006. -С. 104-105.
- Лаврова А.Е. Клиническое значение нарушений содержания цинка и их коррекция у детей с гастродуоденитом при пищевой аллергии: диссертация … канд. мед. наук/Лаврова Алла Евгеньевна. -Н. Новгород, 1998. -167 с.
- Наринская Н.Н. Особенности клиники и течения хронических болезней верхних отделов пищеварительного тракта при пищевой аллергии у детей: автореф. дис....канд. мед. наук: 14.00.09./Наринская Надежда Николаевна. -Москва, 2004. -24 с.
- Этиологическая характеристика основных типов хронического гастрита у детей/Г.В. Волынец [и др.]//Русский медицинский журнал. Детская гастроэнтерология и нутрициология. -2005. -Т. 13. -№18. -С. 1208-1215.
- Состояние гастродуоденальной слизистой у детей раннего и дошкольного возраста/Н.В. Авдеева [и др.]//Актуальные проблемы абдоминальной патологии у детей: материалы XIV Международного конгресса детских гастроэнтерологов России (Москва, 13-15 марта 2007 г.). -Москва, 2007 -С. 166-167.
- Сазанова Н.Е. Механизмы формирования и клинические варианты хронических заболеваний желудка и двенадцатиперстной кишки у детей дошкольного возраста: дис… докт. мед. наук: 14.00.09./Сазанова Наталья Евгеньевна. -Н. Новгород, 2002. -436 с.
- Балаболкин И.И. Атопия и аллергические заболевания у детей/И.И. Балаболкин//Педиатрия. -2003. -№6. -С. 1-6.
- Распространенность пищевой аллергии у детей Молдовы/Л.В. Василос [и др.]//Вопросы детской диетологии. -2005. -Т.3, №1: Актуальные вопросы абдоминальной патологии у детей: материалы XII Конгресса детских гастроэнтерологов России (Москва, 2005 г.). -Москва, 2005. -С. 64-65.
- Ревякина В.А. Пищевая аллергия у детей. Современные аспекты/В.А. Ревякина, Т.Э. Боровик//Российский аллергологический журнал. -2004. -№2. -С. 71-77
- Mucosal pathology of the foregut associated with food allergy and recurrent abdominal pains in children/J Kokkonen [et al.]//Acta Paediatrica. -2001. -January, Vol.90, Issue 1. -P. 16-21.
- Nowak-Wegrzyn A. Food protein-induced enterocolitis syndrome/Nowak-Wegrzyn A, Muraro A.//Curr Opin Allergy Clin Immunol. 2009. -Aug; 9(4):371-7.
- Bonй J. Allergic proctocolitis, food-induced enterocolitis: immune mechanisms, diagnosis and treatment./Bonй J [et al.]//Allergol Immunopathol (Madr). -2009 Jan-Feb. -37(1). -P. 36-42.
- Баранов А.А. Гастроинтестинальная пищевая аллергия у детей/А.А. Баранов, И.И. Балаболкин, О.А. Субботина. -М., 2002.
- Корсунский А.А. Хеликобактериоз и болезни органов пищеварения у детей/А.А. Корсунский, П.Л. Щербаков, В.А. Исаков-М.: ИД Медпрактика, 2002. -168 с.
- Ganza-Zandzou P.S. Natural Outcome of Helicobacter pylori Infection in Asymptomatic Children: A Two-year Follow-up Study/P.S. Ganza-Zandzou [et al.]//Pediatrics. -1999. -V. 104. -№2. -P. 216-221.
- Дюбкова Т.П. Состояние желудка и двенадцатиперстной кишки у детей с аллергическими заболеваниями кожи: Автореферат дис. … к.м.н./Т.П. Дюбкова. -Минск, 1992. -23 с.


