Особенности нуклеофильного присоединения высших линейных и разветвленных аминов к акрилонитрилу
Автор: Казанцев Олег Анатольевич, Ширшин Константин Константинович, Есипович Антон Львович, Жиганов Иван Валентинович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 3 т.8, 2016 года.
Бесплатный доступ
Проведено сравнение нуклеофильного присоединения высших первичных аминов С8-С14 линейного и разветвленного строения к С=С-связи акрилонитрила в метаноле. Для фракций разветвленных аминов определено влияние температуры, соотношения реагентов и их концентрации на выход продуктов цианэтилирования.
Высшие первичные амины, акрилонитрил, метанол, цианэтилирование
Короткий адрес: https://sciup.org/147160363
IDR: 147160363 | УДК: 547.233.1: | DOI: 10.14529/chem160301
Nucleophilic addition of high linear and branched amines to acrylonitrile
Comparison of the nucleophilic addition of high primary amines C8-C14 with linear and branched structure to the C = C bond of acrylonitrile in methanol was conducted. The influence of temperature, ratio of reactants and their concentration on the product yield was defined for fractions of branched amines in reaction of cyanoethylation.
Текст научной статьи Особенности нуклеофильного присоединения высших линейных и разветвленных аминов к акрилонитрилу
Одной из тенденций в современной нефте- и газодобыче является необходимость повышения эффективности мероприятий по борьбе с различными видами коррозии трубопроводов и оборудования. Причиной этого является все более высокое содержание сернистых примесей во многих добываемых нефтях и природных газах. В качестве ингибиторов коррозии в промысловой химии широкое распространение получили различные производных высших линейных аминов [1]. В частности, в работах [2–4] было показано, что высокую эффективность в качестве ингибиторов коррозии на газовых месторождениях, характеризующихся высоким содержанием сероводорода, проявляют алкиламинопропионитрилы, получаемые взаимодействием различных высших линейных аминов (например, диоктиламина) с нитрилом акриловой кислоты (НАК). Одним из важных для промышленного использования преимуществ таких ингибиторов являются мягкие условия их синтеза с высокими выходами по реакции цианэтилирования аминов. В то же время в ряде работ показано, что различные производные высших разветвленных аминов более эффективно ингибируют коррозию в некоторых углеводородных системах по сравнению с производными линейных аминов [5, 6]. Для пропионитрильных производных некоторых разветвленных аминов также показана высокая эффективность в качестве ингибиторов коррозии [7].
Ранее для низших первичных и вторичных аминов было показано [8–11], что скорость реакции их цианэтилирования (уравнение 1) снижается по мере возрастания длины и степени разветвлённости алифатического радикала.
RNH 2 + H 2 C=CHCN → RNHCH 2 CH 2 CN (1)
I
Для высших разветвленных первичных аминов – трет-нониламина, трет-додециламина и трет-пентадециламина – в работах [12, 13] описано их взаимодействие с эквимольными количествами НАК в отсутствие растворителей, а также в присутствии добавок воды или смесей воды с солюбилизатором (диметилформамидом, диметилацетамидом, β-трет-бутиламино- пропионитрилом, β,β|-иминодипропионитрилом) при температуре 78-89 °С. При этом конверсии реагентов по реакции (1) не превышали 66,5 %.
Целью данной работы было сравнение активности в реакции (1) высших разветвленных и линейных аминов в метаноле и определение условий достижения высоких конверсий при использовании промышленных фракций высших первичных разветвленных аминов. В качестве ос- новного растворителя использовался метанол. Это было обусловлено тем, что нуклеофильное присоединение аминогрупп по двойной связи НАК может значительно ускоряться протонодонорными веществами различных классов [8], а метанол является доступным и относительно дешевым протонодонорным растворителем, который широко применяется на нефтяных и газовых промыслах [14]. Проведенные нами предварительные эксперименты подтвердили, что при температуре 25 °С реакция присоединения исследуемых высших первичных разветвленных аминов протекает в 2–3 раза быстрее в метаноле по сравнению с проведением реакции в ацетонитриле, диметилформамиде или в отсутствие растворителя.
Экспериментальная часть
В работе использовались н -октиламин (нОА) и трет -октиламин (тОА) фирмы «Aldrich», НАК марки «Ч» (ГОСТ 11097-73), промышленные фракции разветвленных аминов марок «Тет-
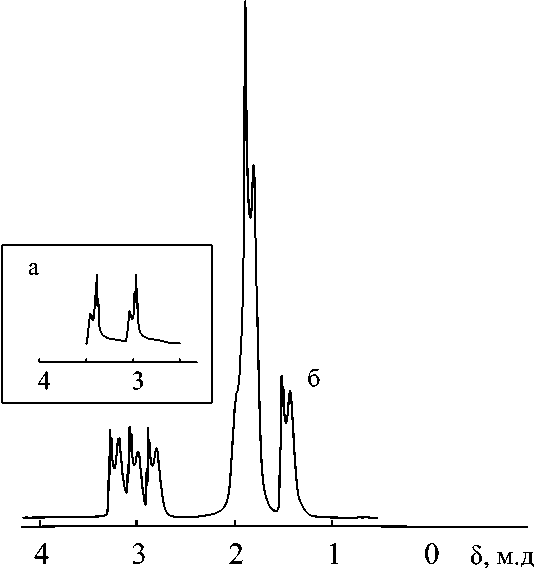
Рис. 1. Фрагменты спектров ЯМР 1Н продуктов взаимодействия НАК с тОА (а) или нОА (б). Т=50 °С. Растворитель CH 3 OD
ракс-03» (РА-9) и «Тетракс-04» (РА-12) производства ОАО «Дзержинское оргстекло» (ТУ ТУ2413-032-55856863-2004). РА-9 содержит набор изомерных разветвленных амины фракции С9 – С12, имеющие по два заместителя при α-углеродном атоме; РА-12 являются аналогичными аминами фракции С12 – С14.
Реакцию присоединения высших аминов к НАК проводили при мольных соотношениях реагентов от 2:1 до 1:2 и температуре 25–82 °С. Протекание реакции цианэтилирования в исследуемых системах было подтверждено методом ЯМР-спектроскопии реакционных смесей при проведении реакции в дейтерометаноле. На рис. 1 в качестве примера показаны фрагменты спектров продуктов взаимодействия НАК с тОА (а) или нОА (б), которые соответствуют сигналам групп C H 3 -C (1,35-1.55 м.д.), C-C H 2 -C (1,65-2,10 м.д.) R-C H 2 -N (2,70-2,90 м.д.), N-C H 2 -CH 2 -CN (2,903,15 м.д.), -C H 2 -CN (3,15-3,50 м.д.). Спектры ЯМР 1H получали при температуре 25 °С на спектрометре «Agilent 400/DDR2» при резонансной частоте 400 MHz.
Анализ количественного состава реакционных смесей проводили методом газовой хроматографии с использованием хроматографа «Хромос ГХ-1000» и капиллярной колонки VertiBond 1701 (длина 60 м, внутренний диаметр 0,25 мм, толщина плёнки – 0,25 мкм) в программируемом режиме: температура термостата колонок в течение 8 мин составляла 70 °С, затем поднималась до 200 °С, температура испарителя – 200 °С, температура детектора – 200 °С; в качестве газа-носителя использовался гелий.
Обсуждение результатов
При цианэтилировании первичных аминов необходимо учитывать, что образующиеся вторичные амины (I) способны присоединяться по С=С-связи не вступившего в реакцию НАК с получением аминодипропионитрила (II) [15]:
RNHCH 2 CH 2 CN + H 2 C=CHCN → RN(CH 2 CH 2 CN) 2 (2) II
Специально проведенный эксперимент показал, что при использовании нОА, двукратного избытка нитрила и температуры 50 °С (5 ч) конверсия исходного амина составила 95,7 %, в то время как конверсия НАК – 76,3 %. Следовательно, кроме эквимольного расхода нитрила и исходного амина по реакции (1), 26 % НАК пошло на образование продукта аминодипропионитрила по реакции (2). Типичная хроматограмма реакционной смеси представлена на рис. 2.
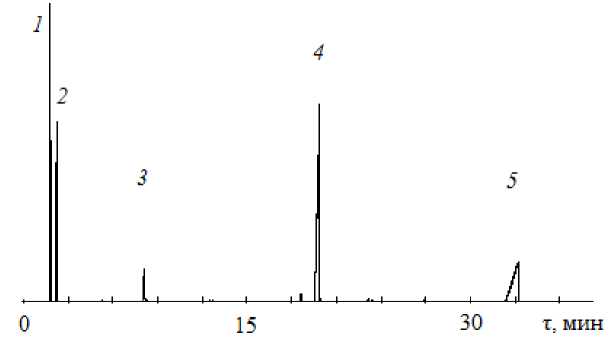
Рис. 2. Хроматограмма реакционной смеси при следующих условиях реакции: [нОА] 0 : [НАК] 0 = 1:2; содержание СН 3 ОН 40 % масс.; 50 °С; 5 ч.
Сигналы: СН 3 ОН (1), НАК (2), нОА (3), продукт I (4), продукт II (5)
При и спол ьзован ии э к ви м ольных количеств нОА и НАК или при замен е н ОА н а и с с ле д уе мы е в раб оте р а зв е тв ле нн ые а ми ны появление продукта диприсоединения н е н а б л ю д а лось. По э тому в д а льн е й ш и х ра с ч е та х у ч итывалось только протекание реакции (1). Для с ра в н е н и я ре ак ц и он н ой с п ос об н ост и в ы с ш и х первичных линейных и разветвленных амин ов были п ров е д е ны сра в н ительн ы е оп ыт ы с ис п ользов а н и е м нОА и тОА (рис. 3). В первом случае уже за 30 мин при температуре 25 °С дос ти гала с ь 95 % -ная конверсия реагентов, в то время как во втором случае за 5 ч она с о с та в и ла 52 % , а п ри пов ы ш е н и и те мперат уры д о 65 °С – 69 %.
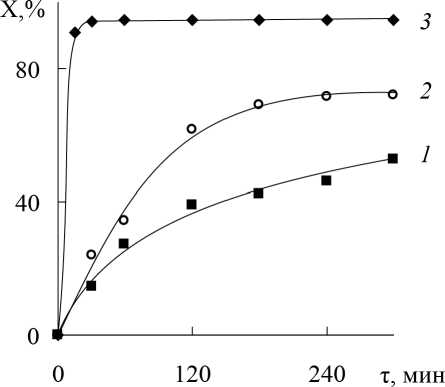
Рис. 3. Зависимость конверсии (X, %) тОА (1, 2) и нОА (3) от времени (t, мин). [Амин] 0 :[НАК] 0 = 1:1; содержание СН 3 ОН 40% масс.; Т= 25 °С (1, 3), 65 °С (2)
Да лее б ыли п ров е де н ы с ери и экспериментов по присоединению фракций а ми н ов Р -9 и Р-12 к АН п ри э к в и мольн ых с оо тн ош е н иях реагентов или избытке амина и варьиров а н и и температуры и к он цен т рац ий ре аген т о в в ме та н ол е . На рис . 4 , а и 5 представлены данные, показывающие в л и я н и е с од е р жа н и я ме тан ола н а кинетику реакции при использовании амин ов Р А -9, на рис. 4, б и в табл. 1 – ан а логи чные э к с п е ри ме н ты с у ча с ти ем а ми н ов Р -12. Для аминов РА-9 при повыше н и и с о д е ржа ни я ме тан ола с 10 до 40 % конверсия за 5 ч возрастает с 40 до 74 %; для амина РА-12 – с 35 д о 69 % . К ром е зн а ч и те льн ого ускорения реакции (1) по мере возрастани я с од е р жа н и я ме та н ол а в ре а к ц и он ных с ме сях, и з п олу че н н ых результатов следует также, что при повышении мо л е к у лярн ой ма с с ы и с п о л ьзу е мых высших разветвленных аминов их активнос ть в ре а к ц и и ц и а н э ти л иров а н и я ( п ри э к в и мольн ом соотношении с НАК) снижается, но незначит е льн о.
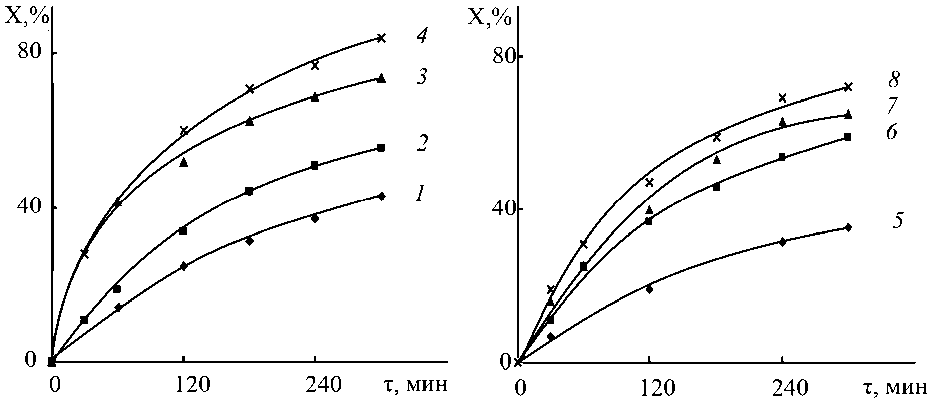
б)
а)
Рис. 4. Зависимость конверсии НАК (X, %) от времени (t, мин) при взаимодействии с РА-9 (а) и РА-12 (б). [Амин] 0 :[НАК] 0 = 1:1; содержание СН 3 ОН, % масс.: 10 (1, 5), 20 (2, 6, 8), 30 (3, 4, 7);
Т, °С: 65 (1, 2, 3, 5, 6, 7), 82 (4, 8)
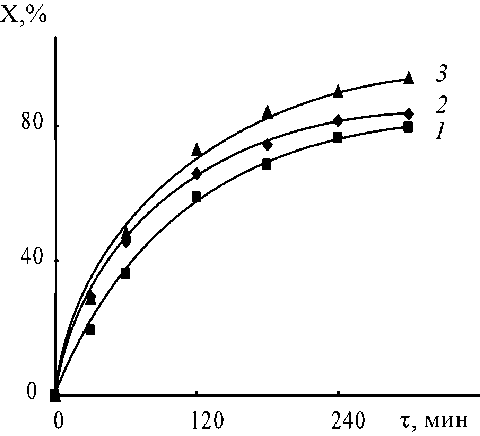
Рис. 5. Зависимость конверсии НАК (X, %) от времени ( τ , мин) при взаимодействии с РА-9 при 65 °С. [Амин] 0 : [НАК] 0 = 1:1 (1, 2), 2:1 (3); содержание СН 3 ОН, % масс.: 40 (1, 3), 50 (2)
Таблица 1
Конверсия НАК в реакции с РА-12 при изменении соотношения реагентов, содержания метанола и температуры
|
№ |
РА-12 НАК |
Т, °С |
Метанол, % масс. |
Конверсия, % |
|||||
|
0,5 ч |
1 ч |
2 ч |
3 ч |
4 ч |
5 ч |
||||
|
1 |
0,5* |
65 |
40 |
39 |
43 |
69 |
82 |
88 |
93 |
|
2 |
1,0 |
65 |
40 |
25 |
34 |
47 |
57 |
62 |
69 |
|
3 |
1,5 |
65 |
40 |
27 |
40 |
57 |
64 |
73 |
78 |
|
4 |
2,0 |
65 |
40 |
27 |
46 |
60 |
72 |
76 |
84 |
|
5 |
2,0 |
65 |
20 |
17 |
26 |
41 |
53 |
63 |
70 |
|
6 |
2,0 |
75 |
20 |
21 |
39 |
59 |
72 |
80 |
83 |
* Дана конверсия аминов.
Добиться роста скорости реакции (1) можно также повышением температуры, хотя влияние этого фактора является менее значительным. Так, при 20%-ной концентрации спирта конверсия РА-9 за 5 ч составила 56 % при температуре 65 °С и 62 % – при температуре 75 °С (соотношение реагентов 1:1). Если температуру поднять еще выше, то можно добиться и более значительного прироста скорости (см., например, рис. 4, кр. 4 и 8). Однако необходимо учитывать, что при повышении температуры при практическом применении исследуемой реакции существенно возрастут энергозатраты на конденсацию паров метанола (температура кипения 64,7 °С) и НАК (77 °С) с последующим их возвратом в реакционную зону.
Еще одним вариантом повышения конверсии является использование начального избытка одного из реагентов. На рис. 5 (кр. 1 и 3) показано, что увеличение начального соотношения РА-9 : НАК с 1,0 до 2,0 повышает конверсию за 5 ч (65 °С) с 74 до 84 %. В случае РА-12 эти показатели составили соответственно 69 и 84 % (табл. 1, № 2 и № 4), а 1,5-кратный избыток амина дал промежуточный результат – 78 % (№ 3). Можно попутно отметить, что при значительном избытке амина разница в реакционной способности двух фракций аминов практически нивелируется. При использовании начального двукратного избытка НАК была достигнута более высокая конверсия по сравнению с вариантом аналогичного избытка РА-12 – 93 % против 84 % (табл. 1, № 1 и № 4).
Сочетание роста температуры и начального избытка амина дает, как и следовало ожидать, более значительное увеличение конверсии по сравнению с действием одного фактора. Так, для цианэтилирования РА-12 при 20%-ном содержании метанола повышение соотношения амин : НАК с 1,0 до 2,0 при одновременном росте температуры с 65 до 75 °С дает прирост конверсии 14 % (табл. 1, № 2 и № 6). Следует отметить, что такого же результата (увеличение конверсии на 14 %) можно добиться, если вместо повышения температуры ввести в реакционную смесь больше метанола (табл. 1, № 5 и № 4). Аналогичные выводы следуют и из анализа других данных, полученных для обеих фракций аминов и представленных на рис. 4, 5 и в табл.1.
Таким образом, полученные данные показали, что при использовании промышленных фракций высших первичных разветвленные аминов можно достигать высоких выходов продуктов в реакции (1), что открывает хорошие перспективы получения эффективных ингибиторов коррозии на основе цианэтилированных производных таких аминов.
Статья подготовлена по результатам НИР, проводимой в рамках выполнения государственного задания №10.1686.2014/К Минобрнауки России.
Список литературы Особенности нуклеофильного присоединения высших линейных и разветвленных аминов к акрилонитрилу
- Kelland, M.A. Production chemicals for the oil and gas industry. Second edition/M.A. Kelland. -CRC Press, Taylor & Francis Group, 2014. -412 p DOI: 10.1201/b16648
- Мельников, В.Г. Защита от коррозии оборудования в газовой промышленности/В.Г. Мельников. -М.: ООО «ИРЦ Газпром», 1999. -66 с.
- Фролова, Л.В. Исследование механизма защитного действия некоторых производных аминов в минерализованных средах, содержащих сероводород/Л.В. Фролова, К.М. Алиева, В.М. Брусникина//Защита металлов. -1985. -Т. 21, № 6. -С. 926-930.
- Аминопроизводные сим-триазина как добавки к турбинным маслам для ингибирования сероводородной коррозии/В.И. Келарев, В.Г. Спиркин, О.Г. Грачёва, И.А. Голубева//Нефтехимия. -1999. -Т. 39, № 3. -С. 221-225.
- Патент 5030385 США. Process of inhibiting corrosion/L. Philip. -09.07.1991.
- Патент 2034932 РФ. Ингибитор сероводородной коррозии/А.В. Болдырев, В.И. Киркач, Н.А. Мизина, Е.С. Хохлова, У.А. Мамедов, А.Г. Базанов. -10.05.1995.
- Патент 3230173 A США. Method and compositions for inhibiting corrosion/J.D. Spivack. -18.01.1966.
- Суминов, С.И. Нуклеофильное присоединение аминогруппы к активированной двойной углерод-углерод связи/С.И. Суминов, А.Н. Кост//Успехи химии. -1969. -Т. 38. -Вып. 11. -С. 1933-1963.
- The catalytic effect of water on cyanoethylation of t-carbinamines/K. Taylor, W. Selcer, P. Montgomery, R. Hughes//J. Am. Chem. Soc. -1959. -V. 81. -P. 5333-5335 DOI: 10.1021/ja01529a023
- t-Carbinamines, RR|R||CNH2 II. Cyanoalylations and related reactions/L. Luskin, M. Culver, G. Gantert, W. Craig//J. Am. Chem. Soc. -1956. -V. 78. -P. 4042-4044 DOI: 10.1021/ja01597a049
- Fulmer, R.W. Cyanoethylation of Fatty Amines Using Acidic Ion Exchange Catalysis/Fulmer//Journal of organic chemistry. -1962. -V. 27. -I. 11. -P. 4115-4116 DOI: 10.1021/jo01058a544
- Патент 2982781 А США. Process for producing beta-aminonitriles and-beta-aminoesters/R.A. Hudges, P.D. Montgomery. -02.05.1961.
- Патент 2982782 A США. Process for producing beta-aminonitriles and beta-aminoesters/W.H. Selcer. -02.05.1961.
- Грунвальд, А.В. Использование метанола в газовой промышленности в качестве ингибитора гидратообразования и прогноз его потребления в период до 2030 г./А.В. Грунвальд//Нефтегазовое дело. -2007. -№ 2. -URL: http://ogbus.ru/authors/Grunvald/Grunvald_1.pdf.
- Буцкус, П.Ф. β-Элиминирование в ряду β-замещенных пропионовых кислот/П.Ф. Буцкус, Г.И. Денис//Успехи химии. -1966. -Т. 35, вып. 11. -С. 1999-2019.


