Патоморфологические исследования внутренних органов лабораторных крыс при изучении хронической токсичности кормовой добавки кобаметин
Автор: Кравченко В.М., Косых А.В., Шантыз А.Х., Еганян Е.С.
Статья в выпуске: 3 т.259, 2024 года.
Бесплатный доступ
Целью исследований стало изучение влияния кормовой добавки кобаметин при длительном применении на органы и ткани лабораторных животных. По результатам исследований можно отметить достоверную разницу в показателях массового коэффициента печени между животными контрольной и опытных групп: в 1-й группе данный показатель был выше, чем в контроле на 15,39 %, во 2-й опытной группе на 25,70 %. Также зафиксирована достоверная разница между контрольной и 2-й опытной группой по разнице массовых коэффициентов селезенки: в опытной группе данный показатель оказался ниже на 16,40 %. Патологоанатомические и гистологические исследования показали, что кормовая добавка кобаметин в дозах 153,0 мг/кг 307,0 мг/кг может вызывать нарушения гемодинамики и в различной степени выраженные дистрофические изменения во внутренних органах подопытных крыс. В контрольной группе животных патоморфологических изменений не установлено. Полученные результаты следует учитывать при составлении полной картины хронического токсического действия добавки с учетом лабораторных данных, общего анализа крови и биохимического профиля сыворотки крови в целях прогнозирования возможных побочных эффектов при выборе доз в клинических исследованиях.
Хроническая токсичность, кобаметин, кормовая добавка, лабораторные животные, внутренние органы, патоморфология, гистоструктура
Короткий адрес: https://sciup.org/142242471
IDR: 142242471 | УДК: 619:574.64:616-091 | DOI: 10.31588/2413_4201_1883_3_259_105
Pathomorphological studies of the internal organs of laboratory rats when studying the chronic toxicity of the feed additive kobamethin
The aim of the research was to study the effect of the feed additive kobamethine on organs and tissues of laboratory animals with prolonged use. According to the research results, there is a significant difference in the liver mass coefficient between the animals of the control and experimental groups: in group 1, this indicator was 15.39 % higher than in the control, and in the 2nd experimental group by 25.7 %. There was also a significant difference between the control and the 2nd experimental group in terms of the difference in the mass coefficients of the spleen: in the experimental group, this indicator was lower by 16.4 %. Pathoanatomical and histological studies have shown that the feed additive kobamethine in doses of 153.0 mg/kg 307.0 mg/kg can cause hemodynamic disorders and to varying degrees pronounced dystrophic changes in the internal organs of experimental rats. No pathomorphological changes were found in the control group of animals. The results obtained should be taken into account when compiling a complete picture of the chronic toxic effect of the supplement, taking into account laboratory data from a general blood test and a biochemical profile of blood serum in order to predict possible side effects when choosing doses in clinical trials.
Текст научной статьи Патоморфологические исследования внутренних органов лабораторных крыс при изучении хронической токсичности кормовой добавки кобаметин
Как известно микроэлементы входят в состав целого ряда ферментов и гормонов поэтому играют значительную роль в питании животных и птицы [9]. По многолетним данным исследований ветеринарных специалистов и ученых одной из главных причин расстройств обмена веществ и, соответственно, здоровья продуктивных животных является хронический комплексный дефицит микроэлементов как кобальт, марганец железо, цинк, медь [1, 2, 4].
Традиционно применяемая минеральная основа компонентного состава корма в виде неорганических солей не является оптимальной для обеспечения жизнедеятельности животных, в виду возможного антагонизма между микроэлементами, их низкой биодоступности, инактивации витаминов [7, 8].
Недостаток кобальта замедляет процесс кроветворения, приводит к эндемическому заболеванию-акобальтозу, ингибированию фермента транскарбоксилазы, фермента оказывающее большое значение в реакциях окисления лейцина [3, 6].
Поэтому включение органических форм микроэлементов в комбикорм позволяет сократить ввод отдельных неорганических кормовых добавок, повысить экономическую эффективность сельскохозяйственного производства за счет улучшения продуктивности животных [8].
А. В. Сорокина с соавторами считает, что «Данные, получаемые в ходе клинико-лабораторных исследований, в частности патоморфологических, представляют особую ценность при составлении полной картины токсического действия препарата при его многократном введении, поскольку позволяют идентифицировать органы-мишени воздействия препарата, оценить степень и обратимость эффектов и, соответственно, спрогнозировать возможные нежелательные явления при клинических исследованиях» [5].
В связи с этим целью данной работы стало определение влияния кормовой добавки кобаметин на органы и ткани лабораторных животных в ходе изучения хронической токсичности.
Материал и методы исследований. Исследования на лабораторных животных проводились на базе научно-испытательного центра токсико-фармакологических исследований и разработки лекарственных средств ветеринарного применения, кормовых добавок и дезинфектантов (НИЦ Ветфармбиоцентр), являющийся структурным подразделением ФГБОУ ВО «Кубанский государственный аграрный университет имени И. Т. Трубилина». Патоморфологические исследования проводили в лаборатории патоморфологии кафедры анатомии, ветеринарного акушерства и хирургии Кубанского ГАУ.
В качестве объекта исследований использовали кормовую добавку кобаметин, которая предоставляет собой комплексное соединение кобальта с 2 амино-метил-тио-(S-оксо-S-амино) масляной кислоты.
Изучение параметров хронической токсичности кормовой добавки проводили на половозрелых крысах разного пола в течение 90 дней. Для исследования было сформировано три группы крыс в возрасте 3-3,5 месяцев, с массой тела, в среднем, 228,33 г (две опытные и одна контрольная) по десять животных в каждой, по пять самок и пять самцов.
В остром опыте величина LD50 была установлена на уровне дозы 1533,4 мг/кг, отправным моментом для выбора доз в первой опытной группе животных явилась 1/10 от LD50, установленной в остром опыте – 153 мг/кг массы тела, второй опытной группе 1/5 или 307 мг/кг массы тела. Третья группа лабораторных крыс служила биологическим контролем. Схема опыта предусматривала однократное ежедневное применение кормовой добавки внутрижелудочно через специальный зонд. Животным контрольной группы аналогичным способом задавали дистиллированную воду.
Патологоанатомические и патогистологические исследования проводили по общепринятой методике, с фиксацией материала в 10 %-ном растворе формалина. Все манипуляции с лабораторными крысами проводили с соблюдением международных рекомендаций с Европейской директивой 2010/63 согласно методике вскрытия и извлечения органов лабораторных животных (крысы).
Результат исследований. В результате анализа полученных результатов при длительном внутрижелудочном введении лабораторным животным кормовой добавки, установлено, что добавка в испытанных дозах оказывает определенное патологическое воздействие на организм лабораторных животных: в 1-й опытной группе был зафиксирован падеж 1-й головы на 14-й день эксперимента), во 2-й опытной группе зафиксирован падеж 1-й крысы на 9-й день эксперимента, в контрольной группе сохранность составила 100 %. У павших животных за 14-38 часов до гибели отмечались учащенное дыхание, снижение двигательной активности, отказ от воды и корма. У выживших животных 1-й опытной группы отмечалось лёгкое угнетение спустя 10 дней после начала хронического опыта, продолжительностью от 2-х до 4-х суток, у животных 2-й опытной группы начиная с 4-х суток эксперимента также отмечалось угнетение и снижение двигательной активности продолжительностью до 7-и суток.
Таблица 1 – Масса внутренних органов и массовые коэффициенты у крыс при изучении хронической токсичности кормовой добавки, г
|
Орган |
Группа |
||
|
контроль |
опыт 1 |
опыт 2 |
|
|
Желудок, г |
2,144±0,121 |
1,919±0,063 |
2,016±0,108 |
|
м.к., % |
0,702±0,037 |
0,640±0,019 |
0,674±0,042 |
|
Селезенка, г |
1,341±0,027 |
1,276±0,026 |
1,133±0,044 |
|
м.к., % |
0,440±0,008 |
0,426±0,009 |
0,378±0,015* |
|
Почки, г |
2,174±0,072 |
2,177±0,046 |
2,284±0,136 |
|
м.к., % |
0,712±0,008 |
0,726±0,008 |
0,760±0,041 |
|
Легкие, г |
3,350±0,214 |
3,231±0,228 |
3,196±0,222 |
|
м.к, % |
1,098±0,067 |
1,076±0,069 |
1,064±0,066 |
|
Сердце, г |
1,325±0,052 |
1,33±0,032 |
1,247±0,035 |
|
м.к., % |
0,434±0,013 |
0,444±0,009 |
0,416±0,009 |
|
Печень, г |
10,31±0,296 |
11,682±0,263 |
12,751±0,563 |
|
м.к., % |
3,378±0,017 |
3,898±0,094* |
4,246±0,133* |
Результаты достоверны по отношении к группе биологического контроля: * - P≤0,05
С целью проведения патологоанатомического исследования внутренних органов и тканей и определения массовых коэффициентов (м.к.) в конце эксперимента была проведена некропсия пяти животных из каждой экспериментальной группы. Результаты определения масс и массовых коэффициентов внутренних органов представлены в таблице 1.
Масса внутренних органов опытных крыс находились в пределах физиологических показателей для данного вида животных. Стоит отметить достоверную разницу в показателях массового коэффициента печени между животными контрольной и опытных групп: в 1-й группе данный показатель был выше, чем в контроле на 15,39 %, во 2-й опытной группе на 25,70 % (при P≤0,05). Также зафиксирована достоверная разница между контрольной и 2-й опытной группой по разнице массовых коэффициентов селезенки: в опытной группе данный показатель оказался ниже на 16,4 % (при P≤0,05).
В целях сравнительного анализа паталогических изменений в органах и тканях относительно павших животных опытных групп была выведена из эксперимента одна крыса контрольной группы на 15 день опыта путем декапитации. Существенных изменений в патологической картине при изучении состояния внутренних органов у крысы контрольной группы не зарегистрировано.
В почках отмечали хроническую венозную гиперемию, которая характеризовалась атрофией канальцев в результате активной диффузной пролиферации молодых клеток соединительной ткани. Большинство эпителиоцитов канальцев находились в состоянии зернистой дистрофии, а часть из них была подвергнута некрозу. При этом повсеместно отмечали отложения пигмента гемосидерина (Рисунок 6).
В миокарде сердца определяли хроническую венозную гиперемию, которая характеризовалась бурой индурацией с атрофией кардиомиоцитов в результате пролиферации молодых клеток соединительной ткани, образованием пигмента гемосидерина и некрозом отдельных кардиомиоцитов (Рисунок 7).
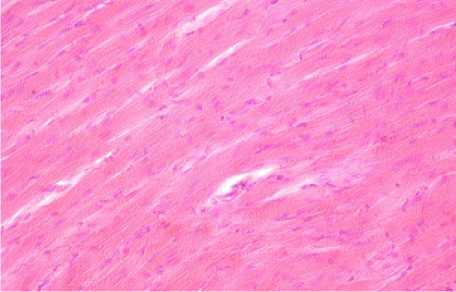
Рисунок 1 - Миокард сердца крысы контрольной группы. Окраска гематоксилином и эозином, ув. 400 (об. 40, ок. 10)
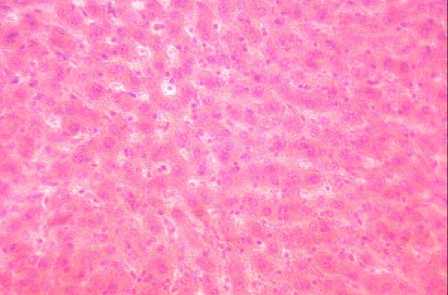
Рисунок 2 – Печень крысы контрольной группы. Окраска гематоксилином и эозином, ув. 400 (об. 40, ок. 10)
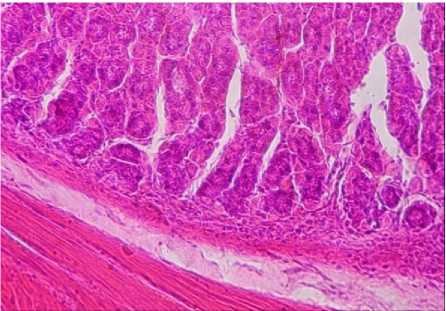
Рисунок 3 – Желудок крысы контрольной группы. Окраска гематоксилином и эозином, ув. 400 (об. 40, ок. 10)
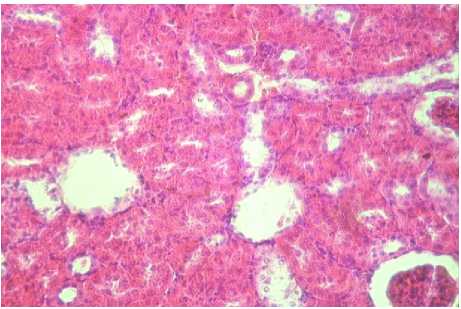
Рисунок 4 – Почка крысы контрольной группы. Окраска гематоксилином и эозином, ув. 400 (об. 40, ок. 10)
В печени отмечали хроническую венозную гиперемию. В результате чего происходила тотальная дискомплексация балок, атрофия, зернистая дистрофия и некроз гепатоцитов, образование пигмента гемосидерина, пролиферация молодых клеток соединительной ткани (Рисунок 8).
В селезенке диагностировали хроническую венозную гиперемию, которая характеризовалось пролиферацией молодых клеток соединительной ткани со стороны капсулы и трабекул, атрофией фолликулов и образование значительного количества гемосидерина в красной пульпе (Рисунок 9).
В желудочных и брыжеечных лимфоузлах отмечали процессы экссудации, которые сопровождались расширением краевых, корковых и мозговых синусов, а также пролиферацию отдельных небольших групп полибластов со стороны капсулы и трабекул.
У крысы первой опытной группы явления нарушения гемодинамики протекали хронически и характеризовались бурой индурацией с накоплением пигмента гемосидерина в легких, печени, почках и увеличением его количества в селезенке. Кроме того, в печени и почках отмечали преобладание процессов острой и хронической альтерации в виде некроза, белковой и жировой дистрофии.
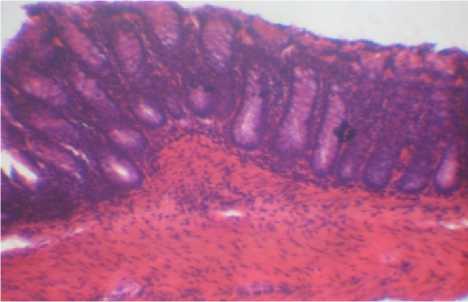
Рисунок 5 – Дуоденум крысы первой опытной группы. Хронический катаральный энтерит. Окраска гематоксилином и эозином, ув. 200 (об. 20, ок. 10)
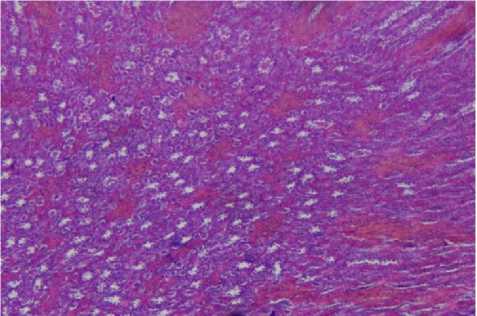
Рисунок 6 – Почка крысы первой опытной группы. Хроническая венозная гиперемия. Окраска гематоксилином и эозином, ув. 200 (об. 20, ок. 10)
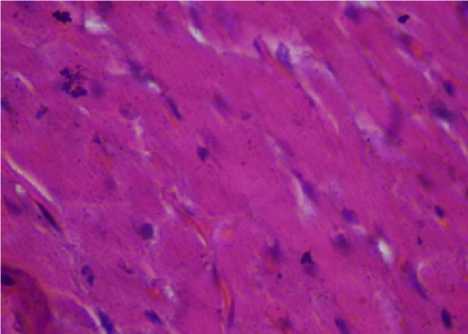
Рисунок 7 – Миокард сердца крысы первой опытной группы. Бурая индурация, кариолизис кардиомиоцитов. Окраска гематоксилином и эозином, ув. 400 (об. 40, ок. 10)
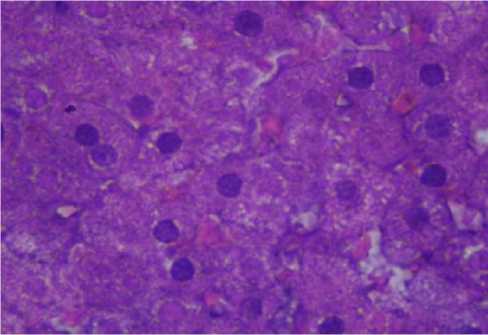
Рисунок 8 – Печень крысы первой опытной группы. Бурая индурация, зернистая дистрофия и кариолизис гепатоцитов.
Окраска гематоксилином и эозином, ув. 600
(об. 40, ок. 15)
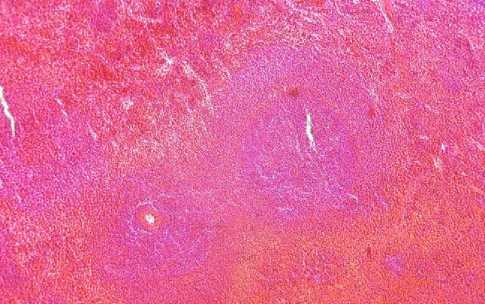
Рисунок 9 – Селезенка крысы первой опытной группы. Бурая индурация.
Окраска гематоксилином и эозином, ув. 200 (об. 20, ок. 10)
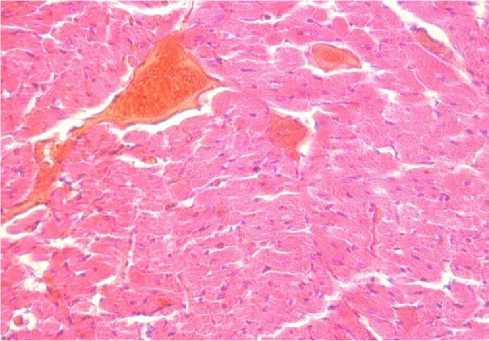
Рисунок 10 – Миокард сердца крысы второй
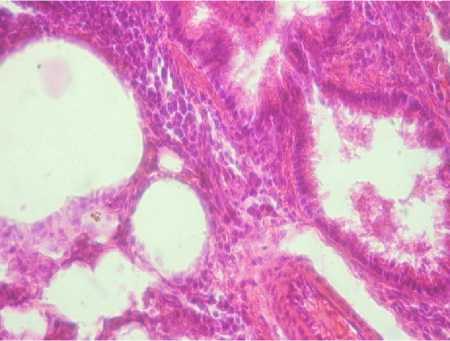
Рисунок 11 – Легкое крысы второй опытной
опытной группы. Острая венозная гиперемия.
Окраска гематоксилином и эозином, ув. 400 (об.
группы. Острая венозная гиперемия и отек.
Окраска гематоксилином и эозином, ув. 400
40, ок. 10)
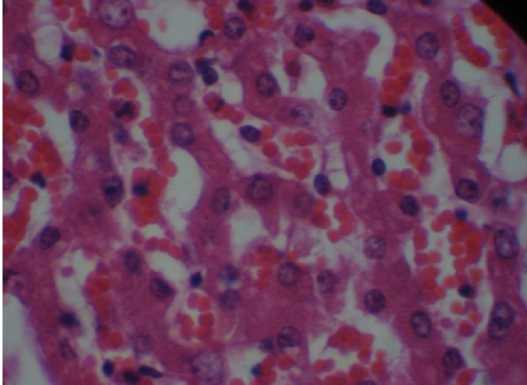
Рисунок 12 – Печень крысы второй опытной группы. Острая венозная гиперемия. Окраска гематоксилином и эозином, ув. 600 (об. 40, ок.
(об. 40, ок. 10)
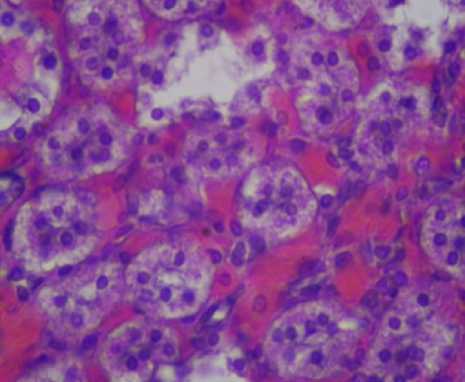
Рисунок 13 – Почка крысы второй опытной группы. Острая венозная гиперемия. Окраска гематоксилином и эозином, ув. 600 (об. 40, ок. 15)
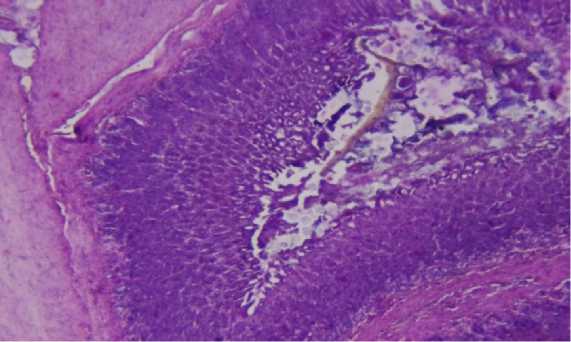
Рисунок 14 – Тонкий отдел кишечника крысы второй опытной группы. Острый катаральный энтерит. Окраска гематоксилином и эозином, ув. 200 (об. 20, ок. 10)
В миокарде сердца отмечали острое венозное полнокровие, которое характеризовалось расширением кровеносных сосудов, вследствие чего эндотелиальные клетки приобретали уплощенную и вытянутую форму (Рисунок 10).
В легких определяли острое венозное полнокровие сосудов, преимущественно капилляров, выпот отечной жидкости в бронхи, бронхиолы в альвеолы, в результате этого часть бронхов, бронхиол и альвеол была расширена, а альвеолярный эпителий десквамирован (Рисунок 11).
В печени выявляли острую венозную гиперемию междольковых капилляров, что обуславливало раздвигание и искривление печеночных балок. Некоторые балки находились в состоянии дискомплексации (Рисунок 12).
В почках выявляли острую венозную гиперемию, которая характеризовалась переполнением капилляров, расположенных между канальцами и их сдавливанием, в результате чего просветы канальцев ссужались (Рисунок 13).
В селезенке из-за острой венозной гиперемии в красной пульпе отмечается тотальное расширение синусов, в результате чего эндотелиальные клетки приобретали вытянутую форму и располагались на значительном расстоянии друг от друга.
В дуоденуме определяли острое катаральное воспаление, которое характеризовалось гиперсекрецией эпителиоцитов слизистой оболочки, в результате чего они увеличивались в размере, а затем разрывались и весь экссудат, состоящий из секрета и остатков эпителиоцитов, поступал в просвет кишечника и полностью его заполнял (Рисунок 14).
В бронхиальных и средостенных лимфоузлах отмечали острое венозное полнокровие, которое характеризовалось переполнением и расширением кровеносных сосудов, переполнением и расширением краевых, корковых и мозговых синусов, содержащих в себе элементы крови.
В желудочных и брыжеечных лимфоузлах отмечали экссудативное воспаление, которое характеризовалось переполнением и расширением краевых, корковых и мозговых синусов в результате экссудации серозного экссудата, содержащего в своем составе незначительное количество лимфатических клеток.
Заключение.
Патологоанатомические и гистологические исследования показали, что кормовая добавка кобаметин в дозах 153,0 мг/кг 307,0 мг/кг может вызывать нарушения гемодинамики и в различной степени выраженные альтеративные изменения во внутренних органах подопытных крыс. В контрольной группе животных патоморфологических изменений не установлено.
Полученные результаты следует учитывать при составлении полной картины хронического токсического действия добавки с учетом лабораторных данных общего анализа крови и биохимического профиля сыворотки крови в целях прогнозирования возможных побочных эффектов при выборе доз в клинических исследованиях.
Список литературы Патоморфологические исследования внутренних органов лабораторных крыс при изучении хронической токсичности кормовой добавки кобаметин
- Бабаев, Ш. Б. Применение меди, марганца и кобальта при лечении гипо- и гиперхромных форм анемии / Ш. Б. Бабаев [и др.] // Микроэлементы в сельском хозяйстве и медицине. – Киев, 2009. – С. 127.
- Ветеринарная токсикология / Д. Д. Хайруллин, Ф. А. Медетханов, А. П. Овсянников, Л. А. Муллакаева. – Казань: Казанская государственная академия ветеринарной медицины имени Н.Э. Баумана, 2019. – 150 с.
- Еганян, Е. С. Изучение острой и хронической токсичности кормовой добавки абиопептид-плюс на лабораторных животных / Е. С. Еганян, А. Х. Шантыз, Е. Ю. Марченко // Международный научно-исследовательский журнал. – 2020. – № 12- 2(102). – С. 91-94.
- Жолобова, И. С. Изучение острой токсичности нового хелатного соединения на основе кобальта / И. С. Жолобова, А. В. Косых // Точки научного роста: на старте десятилетия науки и технологии. Материалы ежегодной научно-практической конференции преподавателей по итогам НИР за 2022 г., Краснодар, 12 мая 2023 года. – Краснодар: Кубанский государственный аграрный университет имени И.Т. Трубилина, 2023. – С. 211–213.
- Опыт проведения клинико-лабораторных исследований в доклинической оценке безопасности лекарств (Часть 2: биохимические и патоморфологические исследования) / А. В. Сорокина, С. В. Алексеева, Н. В. Еремина, А. Д. Дурнев // Ведомости научного центра экспертизы средств медицинского применения. Регуляторные исследования и экспертиза лекарственных средств. – 2019. – Т. 9. – № 4. – С. 272-279.
- Иванов, И. С. Влияние микроэлементов Cu, Co, Zn и Mn в органической форме на организм животных / И.С. Иванов, В. А. Руденок, Е. И. Трошин, А. Н. Куликов // Вопросы нормативно-правового регулирования в ветеринарии. – 2016. – № 4. – С. 246-249.
- Куликов, А. Н. Влияние хелатных комплексов Cu и Zn с глицином и сульфатов данных металлов на мясную продуктивность ягнят / А. Н. Куликов, И. С. Иванов, А. В. Шишкин, Ю. Г. Крысенко // Инновационные технологии для реализации программы 20 научно-технического развития сельского хозяйства: материалы Международной научно-практической конференции. В 3 т. – Ижевск: ФГБОУ ВО Ижевская ГСХА. – 2018. – Т. 2. – С. 66-68.
- Фоминова, И. О. Профилактика смешанных заболеваний животных микроэлементами / И. О. Фоминова // Инновации в производстве, хранении и переработке сельскохозяйственной продукции: науч.- практ. конф. студентов, аспирантов и молодых ученых. – Ставрополь. – 2015. – С. 240-243.
- Шантыз, А. Х. Хроническая токсичность кормовой добавки абиотоник / А. Х. Шантыз, Е. Ю. Марченко // Политематический сетевой электронный научный журнал Кубанского государственного аграрного университета. – 2020. – № 161. – С. 52-60.


