Персонализированные аспекты развития идиопатического коксартроза
Автор: Мироманов Александр Михайлович, Забелло Трофим Васильевич, Доржеев Владимир Владимирович, Мироманова Наталья Анатольевна, Емельянов Артур Сергоевич
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 3, 2017 года.
Бесплатный доступ
Цель. Выявить персонализированные прогностические критерии развития идиопатического остеоартроза тазобедренного сустава. Материалы и методы. В исследование включено 100 неродственных пациентов с идиопатическим остеоартрозом тазобедренного сустава III-IV стадии в возрасте 61,3 ± 8,5 лет, русской национальности, проживающих на территории Забайкальского края. Контрольную группу составили 100 пациентов без патологии суставов аналогичного возраста (60 ± 8,3 года), национальности и ареала проживания. Критерии исключения - другие виды остеоартрозов (посттравматические, ревматоидные и пр.), острые и хронические воспалительные заболевания в стадии обострения, остеопороз. В работе использован клинический, лабораторный (полиморфизм генов - TLR2-753Arg > Gln, TLR6-249Ser > Pro, FCGR2A-166His > Arg, DEFB1-52G > A, DEFB1-20G > A, TGFb1-25Arg > Pro, TNFα-308G > А, IL4-589C > Т) и инструментальный (рентгенография) методы исследования. Результаты. Статистическая значимость различий между группой пациентов с идиопатическим коксартрозом и группой контроля отмечена в случаях носительства генотипа -166Arg/Arg гена FCGR2A (χ2 - 99,2, p
Идиопатический коксартроз, прогноз, гены, полиморфизм
Короткий адрес: https://sciup.org/142201022
IDR: 142201022 | УДК: 616.728.2-007.248-021.3:575.174.015.3-047.72 | DOI: 10.18019/1028-4427-2017-23-3-331-335
Personalized aspects of idiopathic osteoarthrosis of the hip joint
Objective To reveal personalized predictive criteria of idiopathic osteoarthrosis of the hip joint. Material and methods The study included 100 unrelated patients with grade III-IV idiopathic osteoarthritis of the hip joint, aged 61.3 ± 8.5 years, Russian citizens of Zabaykalsky Krai. Control group consisted of 100 patients of matching age (60 ± 8.3 years), ethnic background and geographic range. Exclusion criteria for the patients were other types of osteoarthritis (post-traumatic, rheumatoid, etc.), acute inflammatory diseases and exacerbations of chronic conditions, and osteoporosis. Clinical, laboratory (polymorphism of genes determined for TLR2-753Arg > Gln, TLR6-249Ser > Pro, FCGR2A-166His > Arg, DEFB1-52G > A, DEFB1-20G > A, TGFb1-25Arg > Pro, TNFα-308G > А, IL4-589C > Т) and radiological methods were employed in the study. Results Statistically significant differences between patients with idiopathic coxarthrosis and control group were observed in carriers of -166Arg genotype / Arg FCGR2A gene (χ2 - 99.2, p
Текст научной статьи Персонализированные аспекты развития идиопатического коксартроза
Коксартроз является наиболее распространенным заболеванием суставов [1, 2] и в 60 % случаев приводит к снижению работоспособности, в 11,5 % – к инвалидности и почти в 80 % – к необходимости проведения первичной артропластики сустава, что свидетельствует о высокой медицинской и социальной значимости данного заболевания, которое не только значительно ухудшает качество жизни больного, но и приводит к большим социально-экономическим затратам [3, 4].
Предвидение возможного развития данного заболевания и при необходимости проведение превентивных профилактических мер является важным аспектом современной медицины [5].
К настоящему времени многими исследователями ведутся поиски маркеров развития остеоартроза [6, 7, 8, 9, 10, 11], однако, к сожалению, «идеального» диа- гностического показателя до сих пор не выявлено.
Согласно исследованиям последних лет, ведущая роль в развитии заболеваний отводится наследственным факторам. Генетически обусловленная продукция белков оказывает значимое влияние на развитие целого ряда патологических состояний, в том числе и развитие остеоартрозов [11]. Вследствие вышесказанного, выявление ассоциации той или иной патологии с определенным генотипом, в конечном итоге, позволит создать базу данных (генетический паспорт) и своевременно осуществлять необходимые профилактические мероприятия, тем самым предотвращать развитие заболеваний и/или осложнений [12].
Цель исследования – выявить персонализированные прогностические критерии развития идиопатического остеоартроза тазобедренного сустава.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проводилось согласно этическим принципам, предъявляемым Хельсинкской Декларацией Всемирной Медицинской Ассоциации (World Medical Association Declaration of Helsinki (1964, 2011 – поправки) и «Правилами клинической практики в Российской Федерации», утвержденными Приказом Минздрава РФ 19.06.2003 г. № 266.
В качестве объекта исследования использованы образцы периферической крови 100 неродственных пациентов в возрасте 61,3 ± 8,5 лет с идиопатическим остеоартрозом тазобедренного сустава III–IV стадии, русской национальности, проживающих на территории Забайкальского края и получивших высокотехнологичную медицинскую помощь (тотальное эндопротезирование тазобедренного сустава) в травматологическом отделении НУЗ «Дорожная клиническая больница на ст. Чита-2». Контрольная группа была представлена 100 пациентами без патологии суставов аналогичного возраста (60 ± 8,3 года), национальности и ареала проживания. Критерии исключения – другие виды остеоартрозов (посттравматические, ревматоидные, подагрические и пр.), острые и хронические воспалительные заболевания в стадии обострения, остеопороз.
Для генетических исследований выбирали точко-вую мутацию TLR2 в позиции 753 (Arg > Gln), мутацию TLR6 в позиции 249 (Ser > Pro), мутацию FCGR2A в позиции 166 (His > Arg), мутацию DEFB1 в позиции 52 (G > A), мутацию DEFB1 в позиции 20 (G > A), мутацию TGFb1 в позиции 25 (Arg > Pro), мутацию TNFα в позиции 308 (G > А) и мутацию IL4 в позиции 589 (C > T). Амплификацию фрагмента исследуемых генов проводили в термоцикле (модель Ре «Бис» – М111 (ООО «Бис-Н», г. Новосибирск). В работе использовали стандартные наборы праймеров научно-производственной фирмы «Литех»-«SNP» (Москва). Визуализацию продуктов амплификации выполняли с помощью электрофореза в 3 % агарозном геле с добавлением бромистого этидия в проходящем ультрафиолетовом свете [12].
Исследования осуществляли при поступлении пациентов в стационар. Полученные данные обработаны с помощью пакета программ «Microsoft Office Exel 2010» и «BIOSTAT». Для описания характера распределения количественных признаков определялись средние величины (М), стандартные отклонения (SD). Для анализа групп по качественному бинарному признаку применялся критерий χ2. Для сравнения количественных показателей использовали критерий Манна-Уитни. Степень риска развития событий оценивали по величине отношения шансов (odd ratio (OR)) с расчетом для него 95 % доверительного интервала (CI). Различия считались статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ И ДИСКУССИЯ
Распределение носительства генотипов исследуемых полиморфизмов представлено в таблице.
Зафиксировано, что не все исследуемые мутантные генотипы имели статистическую значимость различий между группой пациентов с идиопатическими коксар-трозами и группой контроля: генотип -166Arg/Arg гена FCGR2A (χ2 – 99,2, p<0,0001, OR – 255,2); генотип -52А/ А гена DEFB1 (χ2 – 58,7, p < 0,0001, OR – 11,2); генотип -20А/А гена DEFB1 (χ2 – 42,2, p < 0,0001, OR – 8,3); генотип -589Т/Т гена IL4 (χ2 – 49,7, p < 0,0001, OR – 25,2) (таблица).
При детальном персонифицированном анализе состава выявленных полиморфизмов в группе с коксартро-зами отмечено, что при одновременном носительстве 3 и 4 мутантных гомозигот исследуемых полиморфизмов отмечается более раннее развитие заболевания (до 40 лет) и его быстрое прогрессирование, в то время как у лиц контрольной группы носительство 2 и более мутантных гомозигот изучаемых SNP генов не выявлено.
Обнаружено, что FCGR2A (CD32) входит в группу рецепторов для Fc – конца иммуноглобулинов класса G. Данный рецептор локализован на моноцитах, гранулоцитах, эозинофилах, макрофагах и В-лимфоцитах и способствует взаимодействию с иммуноглобулинами и, как следствие, приводит к развитию ответной реакции в виде активации макрофагов, сопровождаемой синтезом цитокинов и других биологически активных молекул. Работ по изучению влияния полиморфизма гена FCGR2A(His166Arg) на развитие остеоартрозов нами не выявлено, однако отмечено, что сочетанное носительство генотипа -166Arg/Arg гена FCGR2A с генотипом -159С/С гена СD14 у пациентов с гриппом AH1N1 приводило к молниеносному течению и летальному исходу [13].
В последнее время большое внимание уделяется изучению факторов врожденного иммунитета, в частности противомикробным пептидам, к которым относятся дефенсины. β-дефенсины обладают широким спектром противобактериальной, противовирусной и противогрибковой активности, участвуют в хемотаксисе, в индукции адаптивного иммунитета, в созревании дендритных клеток и пр. β-дефенсин 1 кодируется геном DEFB1, который локализуется на коротком плече хромосомы 8 в локусе 8p22-23 в кластере β-дефенсинов. Полиморфизм гена DEFB1 может быть ассоциирован с выраженностью продукции ß-дефенсина 1 на уровне слизистых оболочек, поэтому данным полиморфизмом можно объяснить различную восприимчивость к заболеваниям инфекционного генеза [14].
Установлено, что полиморфные маркеры DEFB1 (-20G/A, -44C/G, -52G/A) ассоциированы с широким спектром заболеваний (ВИЧ-1-инфекцией, сепсисом, инфекцией, вызванной C. albicans, P. aeruginosa и др.). Таким образом, можно сделать предположение, что полиморфные маркеры могут быть связаны со сниженными (неполноценными) реакциями врожденного иммунитета за счет дефектов в генах, что приводит к снижению экспрессии дефенсинов и, тем самым, способствует уменьшению защиты на уровне слизистых оболочек и развитию патологии [15].
Показано, что наличие гомозиготного генотипа -589Т/Т гена IL4 сопровождается сниженной продукцией цитокина IL-4, что, в свою очередь, способствует длительному сохранению повышенного содержания провоспалительных цитокинов, и соответственно, прогрессированию воспаления, что неумолимо приводит к деструктивным процессам в тканях [16].
Таблица
Значения SNP исследуемых генов в развитии идиопатического коксартроза (χ2)
|
Генотип |
Группа контроля (n = 100) |
Группа c идиопатическим коксартрозом (n = 100) |
OR [95 % CI] |
Исход |
|
SNP гена TLR2(Arg753Gln) |
||||
|
Arg/Arg |
65 (65 %) |
84 (84 %)* |
2,83 [1,44–5,55] |
Благоприятный |
|
Arg/Gln |
35 (35 %) |
16 (16 %)* |
0,35 [0,18–0,69] |
Благоприятный |
|
Gln/Gln |
– |
– |
1,0 [0,02–50,89] |
Неблагоприятный |
|
SNP гена TLR6 (Ser249Pro) |
||||
|
Ser/Ser |
4 (4 %) |
9 (9 %) |
2,37 [0,71–7,98] |
Благоприятный |
|
Ser/Pro |
54 (54 %) |
38 (38 %) |
0,52 [0,3–0,92] |
Благоприятный |
|
Pro/Pro |
42 (42 %) |
53 (53 %) |
1,56 [0,89–2,72] |
Неблагоприятный |
|
SNP гена FCGR2A(His166Arg) |
||||
|
His/His |
68 (68 %) |
10 (10 %)* |
0,05 [0,02–0,11] |
Благоприятный |
|
His/Arg |
32 (32 %) |
34 (34 %)* |
1,09 [0,61–1,97] |
Благоприятный |
|
Arg/Arg |
– |
56 (56 %)* |
255,2 [15,4–4223] |
Неблагоприятный |
|
SNP гена DEFB1(G52A) |
||||
|
G/G |
54 (54 %) |
12 (12 %)* |
0,12 [0,06–0,24] |
Благоприятный |
|
G/A |
35 (35 %) |
30 (30 %)* |
0,8 [0,44–1,44] |
Благоприятный |
|
A/A |
11 (11 %) |
58 (58 %)* |
11,2 [5,32–23,5] |
Неблагоприятный |
|
SNP гена DEFB1(G20A) |
||||
|
G/G |
52 (52 %) |
19 (19 %)* |
0,22 [0,11–0,41] |
Благоприятный |
|
G/A |
36 (36 %) |
28 (28 %)* |
0,69 [0,38–1,26] |
Благоприятный |
|
A/A |
12 (12 %) |
53 (53 %)* |
8,3 [4,0–17] |
Неблагоприятный |
|
SNP гена TGFb1(Arg25Pro) |
||||
|
Arg/Arg |
60 (60 %) |
67 (67 %) |
1,35 [0,76–2,41] |
Благоприятный |
|
Arg/Pro |
28 (28 %) |
25 (25 %) |
0,86 [0,46–1,61] |
Благоприятный |
|
Pro/Pro |
12 (12 %) |
8 (8 %) |
0,64 [0,25–1,63] |
Неблагоприятный |
|
SNP гена TNFα(G308А) |
||||
|
G/G |
73 (73 %) |
73 (73 %) |
1,0 [0,54–1,87] |
Благоприятный |
|
G/A |
27 (27 %) |
26 (26 %) |
0,95 [0,51–1,78] |
Благоприятный |
|
A/A |
– |
1 (1 %) |
3,0 [0,12–75,3] |
Неблагоприятный |
|
SNP гена IL4(C589T) |
||||
|
C/C |
73 (73 %) |
29 (29 %)* |
0,15 [0,08–0,28] |
Благоприятный |
|
C/T |
25 (25 %) |
37 (37 %)* |
1,76 [0,96–3,24] |
Благоприятный |
|
T/T |
2 (2 %) |
34 (34 %)* |
25,2 [5,86–108,7] |
Неблагоприятный |
Примечание: * – статистическая значимость различий по сравнению с группой контроля (при р < 0,05).
Прогнозирование идиопатического коксартроза иллюстрируется следующими клиническими наблюдениями.
Клиническое наблюдение № 1 . Пациент И., 58 лет, госпитализирован на плановое оперативное лечение с диагнозом: идиопатический коксартроз справа III-IV ст., слева I-II ст. НФС I-II ст. Коксалгия справа (МКБ-10 – М16.1) (рис. 1). Сопутствующая патология: атеросклероз аорты, мозговых артерий, симптоматическая гипертензия. При поступлении пациенту произведено исследование SNP гена FCGR2A(His166Arg), SNP гена DEFB1(G52A), SNP гена DEFB1(G20A) и SNP гена IL4(C589T). Установлено, что пациент является носителем генотипа -166Arg/Arg гена FCGR2A, генотипа -52G/А гена DEFB1, генотипа -20G/G гена DEFB1 и генотипа -589Т/Т гена IL4, что подтверждает наши доводы о влиянии сочетания исследуемых мутантных гомозигот на развитие коксартроза.
Клиническое наблюдение № 2. Пациент Д., 38 лет, госпитализирован на плановое оперативное лечение с диагнозом: идиопатический двусторонний коксартроз IV ст., НФС III ст. Коксалгия больше слева (МКБ-10 – М16.1) (рис. 2). В первые сутки пациенту произведено исследование SNP гена FCGR2A(His166Arg), SNP гена DEFB1(G52A), SNP гена DEFB1(G20A) и SNP гена IL4(C589T). Установлено, что пациент является носителем 4 мутантных гомозигот исследуемых генов: генотипа -166Arg/Arg гена FCGR2A, генотипа -52А/А гена DEFB1, генотипа -20А/А гена DEFB1 и генотипа -589Т/Т гена IL4, что может свидетельствовать о влиянии носительства трех и более мутантных гомозигот на более раннее и быстро прогрессирующее течение данного заболевания.
Клиническое наблюдение № 3 . Резидент из группы контроля В., 50 лет, имеющийся диагноз: ЖКБ. Хронический калькулезный холецистит, ремиссия. Атеросклероз аорты, мозговых артерий. Симптоматическая гипертензия. Каких-либо симптомов и синдромов поражения суставов не выявлено (рис. 3). При исследовании у данного человека SNP гена FCGR2A(His166Arg), SNP гена DEFB1(G52A), SNP гена DEFB1(G20A) и SNP гена IL4(C589T) зафиксировано носительство только 1 мутантной гомозиготы исследуемых генов – генотип -20А/А гена DEFB1. Данный факт свидетельствует о низкой предрасположенности к развитию коксартроза.
К линическое наблюдение № 4 . Резидент из группы контроля М., 60 лет, имеющийся диа-гноз: ИБС. Прогрессирующая стенокардия напряжения II ф. кл. Н2А. Атеросклероз аорты, мозговых артерий. Симптоматическая гипертензия. Каких-либо симптомов и синдромов поражения суставов не зарегистрировано (рис. 4). При исследовании у данного пациента SNP гена FCGR2A(His166Arg), SNP гена DEFB1(G52A), SNP гена DEFB1(G20A) и SNP гена IL4(C589T) носительства мутантных гомозигот изучаемых генов не выявлено.
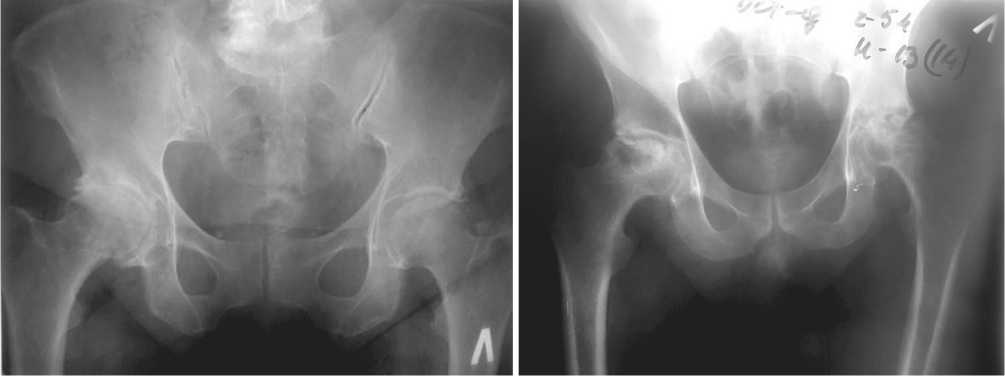
Рис. 1. Рентгенограмма таза в прямой проекции. Идиопатический коксартроз III-IV ст. справа, II ст. слева
Рис. 2. Рентгенограмма таза в прямой проекции. Идиопатический двусторонний коксартроз IV ст.
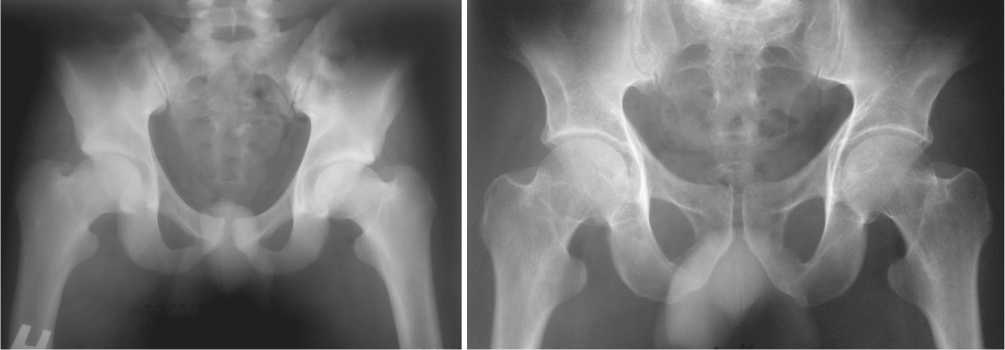
Рис. 3. Рентгенограмма таза в прямой проекции у пациента В. без патологии тазобедренных суставов
Рис. 4. Рентгенограмма таза в прямой проекции пациента М. без патологии тазобедренных суставов
Таким образом, выявление генотипа -166Arg/Arg гена FCGR2A, генотипа -52А/А гена DEFB1, генотипа -20А/А гена DEFB1 и генотипа -589Т/Т гена IL4 у резидентов позволяет прогнозировать развитие идиопатического коксартроза, что санкционирует возможность проведения превентивных профилактических мероприятий и предотвращения развития данного социально значимого заболевания.
ВЫВОДЫ
-
1. Определение SNP генов – FCGR2A (His166A), DEFB1 (G52A), DEFB1(G 20A) и IL-4 (C589 T) позволяет предвидеть развитие коксартроза при наличии сочетания носительства как минимум 2 их мутантных гомозигот.
-
2. При выявлении носительства 3 и более мутантных гомозигот SNP генов – FCGR2A (His166A), DEFB1 (G52A), DEFB1(G 20A) и IL-4 (C589 T) отмечается раннее и быстро прогрессирующее течение идиопатического коксартроза.
Список литературы Персонализированные аспекты развития идиопатического коксартроза
- Травматизм, ортопедическая заболеваемость, состояние травматолого-ортопедической помощи населению России в 2015 году: сборник/под ред. С.П. Миронова. М.: Телер, 2016. 145 с.
- Adatia A., Rainsford K.D., Kean W.F. Osteoarthritis of the knee and hip. Part I: aetiology and pathogenesis as a basis for pharmacotherapy//J. Pharm. Pharmacol. 2012. Vol. 64, N 5. P. 617-625. Doi: 10.1111/j.2042-7158.2012.01458.x.
- Buchanan W.W., Kean W.F. Osteoarthritis I: Epidemiological risk factors and historical considerations//InflammoPharmacology. 2002. Vol. 10, N 1-2. P. -21 DOI: 10.1163/156856002320751982
- Hunter D.J., McDougall J.J., Keefe F.J. The symptoms of osteoarthritis and the genesis of pain//Med. Clin. North Am. 2009. Vol. 93, N 1. P. 83-100 DOI: 10.1016/j.mcna.2008.08.008
- Об утверждении стратегии развития медицинской науки в Российской Федерации на период до 2025 года: распоряжение Правительства РФ № 2580-р от 28.12.2012//КонсультантПлюс, 2012. URL: www.consultant.ru (дата обращения: 11 апреля 2017).
- Способ прогнозирования предрасположенности к развитию и тяжести течения деформирующего артроза коленного сустава у взрослых: пат. 2249210 Рос. Федерация. № 2003104858/15; заявл. 17.02.2003; опубл. 20.08.2004, Бюл. № 9. 6 с.
- Способ ультразвуковой диагностики ранних стадий остеоартроза тазобедренного сустава: пат. 2321350 Рос. Федерация. № 2006137731/14; заявл. 25.10.2006; опубл. 10.04.2008, Бюл. № 10. 8 с.
- Способ прогнозирования риска возникновения остеоартроза у лиц с гипермобильностью суставов: пат. 2558990 Рос. Федерация. № 2014132991; заявл. 11.08.2014; опубл. 10.08.2015, Бюл. № 22. 9 с.
- Способ прогнозирования предрасположенности к развитию посттравматического остеоартроза коленного сустава: пат. 2600860 Рос. Федерация. № 2014153254/15; заявл. 25.12.2014; опубл. 27.10.2016, Бюл. № 30. 11 с.
- Chapman K., Valdes A.M. Genetic factors in OA pathogenesis//Bone. 2012. Vol. 51, N 2. P. 258-264 DOI: 10.1016/j.bone.2011.11.026
- Забелло Т.В., Мироманов А.М., Мироманова Н.А. Генетические аспекты развития остеоартроза//Фундам. исслед. 2015. № 1-9. С. 1970-1976.
- Полиморфизм гена TNF-α (G-308А) у больных с гнойно-воспалительными осложнениями при переломах длинных костей конечностей в Забайкальском крае/А.М. Мироманов, О.Б. Миронова, М.В. Трубицын, Ю.А. Витковский//Забайкал. мед. вестн. 2013. № 1. С. 41-45. URL: http://chitgma.ru/zmv2 (дата обращения: 11 апреля 2017).
- Генетический полиморфизм CD14, TNFα и FCGR2A у больных гриппом AH1N1 в Забайкальском крае/Н.Н. Страмбовская, А.В. Говорин, Ю.А. Витковский, А.А. Петров//Мед. иммунология. 2011. № 1. С. 83-86.
- The complexity of selection at the major primate beta-defensin locus/C.A Semple, A. Maxwell, P. Gautier, F.M. Kilanowski, H. Eastwood, P.E. Barran, J.R. Dorin//BMC Evol. Biol. 2005. Vol. 5. P. 32 DOI: 10.1186/1471-2148-5-32
- Ассоциация полиморфных маркеров, локализованных в 5'-нетранслируемой области гена β-дефенсина DEFB1, с гипертрофией аденоидных вегетаций/О.А. Свитич, Л.В. Ганковская, И.В. Рахманова, И.А. Зайцева, В.А. Ганковский//Вестн. РГМУ. 2012. № 3. С. 59-62.
- Миронова О.Б. Некоторые патогенетические механизмы развития хронического травматического остеомиелита при переломах длинных трубчатых костей: автореф. дис. … канд. мед. наук: 14.03.03. Чита, 2014. 22 с.


