Получение и исследование алюмосиликатного сорбента
Автор: Кузнецова И.В., Гетманская М.В., Черненко С.С.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Химическая технология
Статья в выпуске: 1 (87), 2021 года.
Бесплатный доступ
Разработана технологическая схема синтеза алюмосиликатного сорбента в лабораторных условиях с использованием глины Семилукского месторождения. При нагревании образца сорбента в интервале 30-225оС происходит потеря свободной влаги, в интервале температур 405-550 оС начинает испаряться связанная вода и происходит разложение органических веществ. Исследована сорбция сульфида натрия поверхностью сорбента. Определены постоянные ? и n в уравнение Фрейндлиха A=1,38?C1.19. Формируемая площадь удельной поверхности S=12,8 м2/г. Проведено сравнительное исследование кислотно-основных свойств поверхности синтезируемого алюмосиликатного сорбента и диатомита Celite 545 60/80 MESH индикаторным методом. Адсорбция на кислотно-основных центрах поверхности синтезируемого алюмосиликатного сорбента выше адсорбции на поверхности диатомита. На поверхности синтезируемого алюмосиликатного сорбента находятся как кислотные (рК=1,7; 3,46), так и основные (рК=18,8; 9,2) центры Бренстеда. Объем пор синтезируемого алюмосиликатного сорбента равен 0,25 см3/г. Это значение меньше, чем объем пор диатомита 1,86 см3/г.
Алюмосиликатный сорбент, кислотно-основные центры, объем пор, удельная поверхность, получение сорбента
Короткий адрес: https://sciup.org/140257340
IDR: 140257340 | УДК: 64 | DOI: 10.20914/2310-1202-2021-1-309-315
Obtaining and research of aluminosilicate sorbent
A technological scheme for the synthesis of an aluminosilicate sorbent in laboratory conditions using clay from the Semilukskoye deposit has been developed. When the sorbent sample is heated in the range of 30-225 ° C, a loss of free moisture occurs, in the temperature range of 405-550 ° C, bound water begins to evaporate and decomposition of organic substances occurs. The sorption of sodium sulfide by the sorbent surface has been studied. The constants ? and n are determined in the Freundlich equation A = 1.38 ? C1.19. Formed specific surface area S = 12.8 m2 / g. A comparative study of the acid-base properties of the surface of the synthesized aluminosilicate sorbent and diatomite Celite 545 60/80 MESH by the indicator method has been carried out. The adsorption on the acid-base centers of the synthesized aluminosilicate sorbent surface is higher than the adsorption on the diatomite surface. On the surface of the synthesized aluminosilicate sorbent, there are both acidic (pK = 1.7; 3.46) and basic (pK = 18.8; 9.2) Bronsted centers The pore volume of the synthesized aluminosilicate sorbent corresponds to 0.25 cm3 / g. This value is less than the pore volume of diatomite 1.86 cm3 / g.
Текст научной статьи Получение и исследование алюмосиликатного сорбента
Актуальность применения алюмосиликатных сорбентов на сегодняшний день велика: крекинг нефти, получение чистого кислорода, увеличение прочности строительных материалов [1]. Кислотостойкие природные алюмосиликатные сорбентов используются для защиты окружающей среды от ряда промышленных выбросов, очистки сточных вод, морской воды от нефти [2, 3].
Этот материал обладает поистине уникальными физико-химическими свойствами. Кристалличность обеспечивает механическую и химическую стабильность, одинаковый и контролируемый размер пор, каналов, полостей [4].
Ключевую роль в протекании сорбционных и каталитических явлений играют дефекты структуры, представляющие собой для алюмосиликатов кислотно-основные центры различной природы (силанольные группы, ненасыщенные атомы алюминия, подвижные протоны, являющиеся противоионами тетраэдров [AlO 4 ]–, или центры, образующиеся при смещении отрицательного заряда в [AlO 4 ]–). Информация о количестве поверхностных кислотно-основных центров алюмосиликатов позволяет дать прогнозную оценку их физико-химических свойств [5].
Анализ литературных и патентных источников показывает, что широко варьируемый химический состав алюмосиликатного сорбента позволяет модифицировать физико-химические свойства материалов. Нано размеры полостей,
This is an open access article distributed under the terms of the Creative Commons Attribution 4.0 International License возможность упорядоченного расположения активных центров, селективность и направленность воздействия на химические группы молекул делают алюмосиликатные сорбенты не только инструментом нано технологий, но и их объектом [6]. База данных о синтезированных алюмосиликатных сорбентах регулярно обновляется и публикуется под названием «Atlas of Zeolite Structures».
Цель работы – получение алюмосиликатного сорбента с использованием глины ПГБ (г. Семилуки), исследование его физикохимических свойств. А также сравнительное исследование кислотно-основных свойств алюмосиликатного сорбента и диатомита.
Материалы и методы
Материалами данного исследования являлись: сухой диатомит Celite 545 60/80 MESH и синтезируемый алюмосиликатный сорбент.
Диатомит (кизельгур. инфузорная земля. горная мука. цеолит) – осадочная горная порода белого цвета, состоящая преимущественно из останков диатомовых водорослей, их скелетов. Химически диатомит на 80% состоит из водного кремнезёма. Диатомит обладает большой пористостью, способностью к адсорбции, кислотостойкостью [7]. Плотность природных диатомитов колеблется от 0,960 до 1,250 г/см3, и зависит, главным образом, от количества глинистых примесей. Содержание примесей не велико, но они значительно влияют на температуру плавления жидкой фазы в диатомитовом материале при нагревании.
Результаты химического анализа диатомита Celite 545 60/80 MESH показали, что в нем содержится: SiO 2 91,4%; Al 2 O 3 4,7%; Fe 2 O 3 1,9%, СаО 0,5%. Суммарное содержание TiO 2 , Na 2 О, К 2 О, Р 2 О 5 – 1,5%.
Для получения алюмосиликатного сорбента смешивали 25 г. глинозема из боксита с 3,125 мл 56% HNO 3 и 75 мл воды. Полученный материал сушили при температуре 150 Т в течении часа. 3 г высушенного продукта перемешивали с 51 г. глины ПГБ (Семилуки) и водой. Полученную смесь пластичной консистенции с содержанием влаги 55% формовали в виде гранул 5 мм, сушили при температуре 120-140 Т в течении 6 часов и прокаливали при 500-600 Т в течении 2-х часов с постепенным повышением температуры до 750 Т в течении 4-х часов (рисунок 2). Получили вещество белого цвета с размерами гранул 5 мм. Температуру термообработки определяли по данным термического анализа (рисунок 3).


Рисунок 2. Образец синтезируемого алюмосиликатного сорбента
Figure 2. Sample of synthesized aluminosilicate sorbent
Рисунок 1. Диатомит Celite 545 60/80 MESH
Figure 1. Diatomite Celite 545 60/80 MESH
Изучение процесса дегидратации синтезируемого алюмосиликатного сорбента проводили методом термогравиметрического анализа. Термогравиметрия является ценным методом количественного анализа. По кривой ТГ можно определить потерю массы образца при нагревании (∆m). Каждый пик на дифференциальной кривой (кривая ДТГ) соответствует максимальной скорости изменения массы, то есть истинной температуре химической реакции [8]. Исследования проводились на приборе модели Netzsch STA 449 F3 Jupiter при нагревании образцов в платиновых тиглях от 30 до 1000 °C со скоростью 10 K/мин в атмосфере азота. По результатам синхронного термического анализа определяли температурные интервалы процессов, происходящих при нагревании синтезированного алюмосиликатного сорбента.
Для определения сорбционных свойств синтезированного алюмосиликатного сорбента были приготовлены семь растворов различных концентраций сульфида натрия (по 100 см3), смешивая указанные в таблица 1 объёмы 0,05 М раствора сульфида натрия с дистиллированной водой [9, 10].
Таблица 1.
Объёмы сульфида натрия и дистиллированной воды
Table 1.
Volumes of sodium sulfide and distilled water
|
Образец Sample |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
Кислота, см 3 Acid, cm 3 |
100 |
75 |
50 |
25 |
15 |
7 |
5 |
|
Вода, см 3 Water, cm 3 |
0 |
25 |
50 |
75 |
85 |
93 |
95 |
Каждый раствор делили на две равных части по 50 см3. Одну часть используют для определения концентрации растворов до адсорбции.
Во вторую часть растворов добавляли по 3 г адсорбента и выдерживали при периодическом встряхивании в течение 40 мин. Затем алюмосиликатный сорбент из растворов отфильтровывали через бумажные складчатые фильтры и определяли концентрации растворов после адсорбции. Концентрации исследуемых растворов до и после адсорбции (С) определяли титрованием аликвотной части раствора (10 см3) 0,05М раствором сульфида натрия в присутствии крахмала до устойчивой синей окраски.
Сорбционную емкость (А, ммоль/г) вычисляли по формуле:
А = ( С - Ср ) * V
m где C, Ср – исходная и равновесная концентрация ионов исследуемых металлов в растворе соответственно, ммоль/дм3; V – объем раствора, дм3; m – масса сорбента, г.
Экспериментальные методы оценки кислотно-основных свойств поверхности твердого тела многочисленны и разнообразны: ИК-, УФ-и видимая спектроскопия, ЭПР, адсорбционно- химические (адсорбция на границе раздела фаз), индикаторный метод, ЯМР – спектроскопия [11, 12]. Индикаторный метод основан на селективной адсорбции кислотно-основных индикаторов с заданными значениями рКа кислотно-основного перехода и спектрофотометрическом определении изменения оптической плотности их растворов. При этом силу кислотно-основных центров поверхности характеризуют рКа индикатора, адсорбирующегося в сопряженной форме, а количество адсорбированного индикатора определяет количество центров данной силы.
Вещества и реактивы, которые использовались для приготовления растворов индикаторов, а также массы индикаторов представлены в таблице 2.
Для каждого индикатора готовились пять проб.
Таблица 2.
Основные характеристики использованных индикаторов
Table 2.
The main characteristics of the indicators used
|
Название индикатора Name indicator |
Молярная масса, г моль Molar mass, g mol |
Формула Formula |
Масса навески Hinge weight |
Растворитель Solvent |
pKa |
Длина волны максимального поглощения, λ , нм Maximum absorption wavelength, λ, nm / |
|
Метиловый фиолетовый Methyl violet |
393,94 |
C 23 H 28 N 3 Cl |
0,1 |
60% этанол ethanol |
1,7 |
540 |
|
Фуксин основной Fuchsin basic |
323,83 |
C 20 H 20 N 3 Cl |
0,1 |
50% этанол ethanol |
2,1 |
540 |
|
Метиловый оранжевый Methyl orange |
327,32 |
C 14 H 14 N 3 O 3 SNa |
0,1 |
Вода Water |
3,46 |
464 |
|
Тимоловый синий Thymol blue |
466,59 |
C 27 H 30 O 5 S |
0,1 |
20% этанол ethanol |
8,8 |
440 |
|
Нейтральный красный Neutral red |
288,78 |
C 15 H 17 ClN 4 |
0,1 |
60% этанол ethanol |
9,2 |
490 |
Три параллельных пробы (0,1 г порошка анализируемого оксида + 3 мл индикатора), холостая проба (0,1 г порошка анализируемого оксида + 2 мл воды дистиллированной), раствор чистого индикатора объемом 3 мл.
Пробы хорошо перемешивались и выдерживались в течение суток при температуре 20 °С. Затем перед измерением в три параллельные пробы и пробы чистого индикатора добавлялось по 2 мл воды и пробы перемешивались, а в холостую пробу добавлялось 3 мл индикатора и проба также перемешивалась. Полученные растворы, содержащие навеску синтезированного алюмосиликатного сорбента, центрифугировались в течение 3 минут при 9000 об / мин. Исследуемые растворы изучались с помощью метода фотоколориметрии (колориметр КФК-2МП)
в кюветах толщиной 1 мм относительно дистиллированной воды при длине волны, соответствующей максимуму поглощения каждого индикатора (таблица 2).
По полученным данным проводился расчет удельной адсорбции и строилась ее зависимость от pKa.
Расчет удельной адсорбции g, моль / г:
cV D o - D D o - D 2
--------±------
D 0 a 1 a 2
где с – концентрация индикатора, моль/дм3; V – объем пробы, дм3; D 0 – оптическая плотность исходного индикатора; D 1 – оптическая плотность индикатора после сорбции образцом; D 2 – оптическая плотность холостой пробы (растворитель + образец материала); ɑ 1 , ɑ 2 – навески образца, г.
Данная методика позволяет проводить оценку общих кислотно-основных свойств поверхности синтезируемого алюмосиликатного сорбента с дифференциацией реакционных центров по силе в зависимости от рКа используемых индикаторов.
Плотность твердых образцов определяется путем погружения их в жидкость с известным значением плотности р 0 . В качестве вспомогательной жидкости обычно используют воду или этанол, а для пород, содержащих водорастворимые соли и набухаемые в воде глины, а также карбонаты, в качестве рабочей жидкости используется очищенный керосин или ацетон. Удаление воздуха из образца производится путем вакуумирования.
Для работы с синтезируемым алюмосиликатным сорбентом, диатомитом и рабочей жидкостью (ацетон) использовали пикнометр (колба Рейшауэра). Определение пористости по ацетону проводили в соответствии с ГОСТ 6217–52 [13].
Результаты и обсуждение
В процессе нагревания предварительно высушенного сорбента от 30 до 1000 С происходит уменьшение массы (кривая ТГ). Наибольшая потеря массы происходит до 550 °C На кривой ДТГ (рисунок 3) присутствуют два тепловых эффекта: первый в области температур 30-225 С с минимумом при 91 °С второй - в зоне температур 405-550 С с минимумом при 409 С.
При нагревании образца в интервале 30-225 С происходит потеря свободной влаги 2,65%. В интервале температур 405– 550 С - потеря массы 6,72%, испаряется связанная вода из алюмосиликата zAl 2 O 3 nSiO 2 mH 2 O и происходит разложение органических веществ из глины, присутствующей в сорбенте. Общая потеря массы составляет 9,37% (кривая ТГ). Значит термообработку синтезированного алюмосиликата надо вести при температуре свыше 550 С
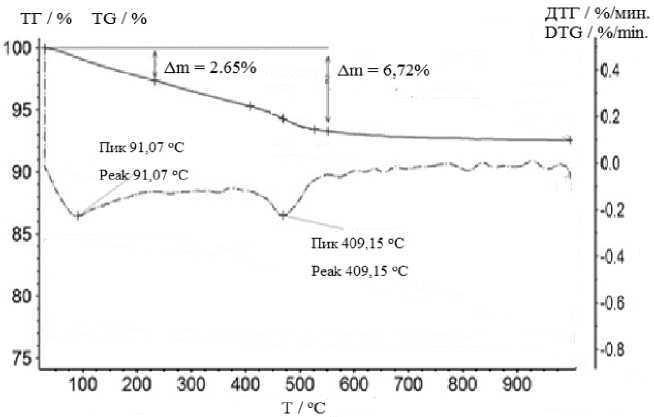
Рисунок 3. Термограмма нагревания образца от 30 до 1000 С
Figure 3. Thermogram of heating the sample from 30 to 1000 С
По результатам исследования сорбционных свойств синтезируемого алюмосиликатного сорбента по поглощению сульфида натрия была построена изотерма адсорбции (рисунок 4). Ее вид соответствует кривой сорбции на пористом твердом теле [9, 10].
Определили постоянные ß и n в уравнение Фрейндлиха из графика, построенного в координатах lgA= f(1/C) (рисунок 5). Уравнение Фрейндлиха для данного процесса выглядит так: A=1,38×C1.19.
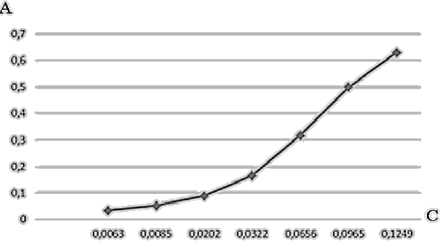
Рисунок 4. Изотерма адсорбции
Figure 4. Isotherm of adsorption
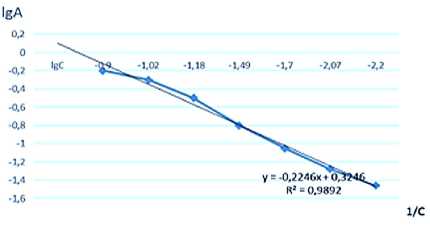
Рисунок 5. Зависимость lg A от 1/C
Figure 5. Dependence of lg A on 1/C
Определили значение предельной адсорбции A max = 0.085 моль/кг. Вычислили удельную активную поверхность сорбента по формуле S уд =A max ×Na×S 0 , где S 0 =2,51×10-19 м2 - площадь занимаемой одной молекулой адсорбата Na 2 S в насыщенном адсорбционном слое. Площадь удельной поверхности синтезируемого сорбента S уд =12,8 м2/г.
Было проведено сравнительное исследование кислотно-основных свойств поверхности синтезируемого алюмосиликатного сорбента и диатомита (рисунок 6,7). На поверхности синтезируемого алюмосиликатного сорбента находятся как кислотные, так и основные центры Бренстеда, которые играют определяющую роль в сорбционных процессах и гетерогенном катализе для реакций полимеризации олефинов, диспропорционирования и изомеризации. Адсорбция на кислотно-основных центрах поверхности полученного сорбента (рК= 1,7; 3,46; 8,8; 9,2) выше адсорбции диатомита. Сорбция на кислотном центре с рК =3,5 диатомита выше, чем на таком же центре алюмосиликатного сорбента. Авторами [5] также было доказано присутствие как кислотных, так и основных центров на поверхности природного алюмосиликата титриметрическим методом.
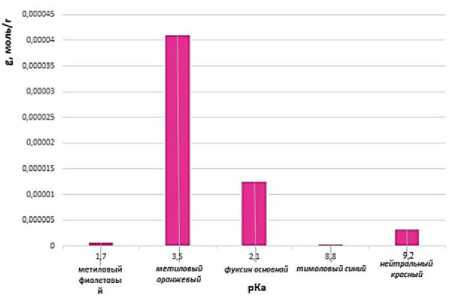
Рисунок 6. Зависимость удельной адсорбции диатомита от значения pKa индикатора
Figure 6. Dependence of the specific adsorption of diatomaceous earth on the pKa value of the indicator
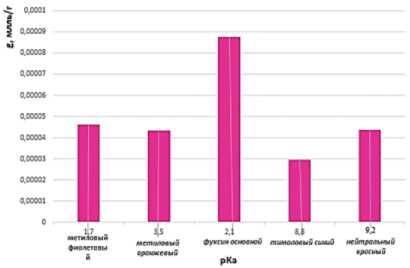
Рисунок 7. Зависимость удельной адсорбции синтезируемого алюмосиликатного сорбента от значения pKa индикатора
Figure 7. Dependence of the specific adsorption of the synthesized aluminosilicate sorbent on the pKa value of the indicator
Общий объем пор для синтезируемого алюмосиликатного сорбента 0,25 см3/г, а диатомита – 1,86 см3/г. Объем пор синтезируемого алюмосиликатного сорбента меньше, чем диатомита. Известно, что диатомит в связи с присутствием в его структуре кремниевых панцирей одноклеточных водорослей обладает большой внутренней поверхностью, содержит до 80–90% пустот. Этот материал имеет в основном макропористую структуру, поры с радиусом 4–40 мкм составляют около 15% суммарного объема пор [1]. То есть диатомит обладает высоким значением объема пор, но низкой кислотно-основной активностью, а синтезируемый алюмосиликат, напротив, показал высокие кислотно-основные свойства и среднее значение объема пор. Как известно [12], для увеличения кислотно-основной активности поверхности сорбента дополнительно необходима ее модификация химическим способом в зависимости от поставленных задач. В процессе синтеза алюмосиликата параллельно происходит и химическая модификация его поверхности.
Заключение
Предложена технологическая схема синтеза алюмосиликатного сорбента в лабораторных условиях с использованием глины (г. Семилуки). Методом синхронного термического анализа определены температурные интервалы процессов дегидратации и разложения органических веществ синтезируемого алюмосиликатного сорбента. По результатам исследования сорбционных свойств синтезируемого алюмосиликатного сорбента по отношению к сульфиду натрия была построена изотерма адсорбции. Определили постоянные ß и n в уравнение Фрейндлиха. Показано, что адсорбция на поверхности кислотно-основных центров синтезируемого алюмосиликатного сорбента выше адсорбции диатомита. Объем пор синтезируемого алюмосиликатного сорбента меньше, чем диатомита.
Список литературы Получение и исследование алюмосиликатного сорбента
- Шуктомова И.И., Рачкова Н.Г. Свойства цеолитов и их применение // Журн. Вестник института биологии Коми научного центра Уральского отделения РАН. 2Q1Q. № 8. С. 9-11
- Bandura L., Woszuk A., Kolodynska D., Franus W. Application of Mineral Sorbentsfor Removal of Petroleum Substances //A ReviewMnerals. 2017. V."7. P. 37. doi: 10.3390/mm7030037
- Abdugaffarova K.K. et al. New Sorption Materials on the Basis of Aluminosilicates for Wasterwater Treatment // Nano Hybrids and Composites. 2017. V. 13. P. 190-196. doi: 10.4028/www.scientific.net/nhc.l3.190
- Treto-Suarez M.A., Prieto-Garcia .Т.О., Mollineda-Trujillo A. et al. Kinetic study of removal heavy metal from aqueous solution using the synthetic aluminum silicate // Sci Rep 2020. № 10. P. 10836. doi: 10.1038/s41598-020-67720-0
- Грибанов E.H., Оскотская Э.Р., Кузьменко А.П. Особенности строения, морфологии и кислотно-основных свойств поверхности алюмосиликата Хотынецкого месторождения. Конденсированные среды и межфазные границы // 2018. Т.20. № 1. С. 42-49. doi: 10.17308/kcmf.2018.20/475
- Agliullin MR, Talzi V.P., Filippova N.A. et al. Two-step sol-gel synthesis of mesoporous aluminosilicates: highly efficient catalysts for the preparation of 3,5 - dialkylpyndines//Appl Petrochem Res. 2018. V. 8. P. 141-151. doi: 10.1007/sl3203-018-0202-0
- Косарев A.B., Атаманова O.B., Тихомирова Е.И., Истрашкина М.В. Моделирование структуры композиционных адсорбентов "алюмосиликат-неионное ПАВ" в решении задач повышения эффективности водоочистки // Вестник Кыргызско-Российского Славянского университета. 2Q17. Т. 17. №. 8. С. 116-12Q.
- Нифталиев С.И., Кузнецова И.В., Лыгина Л.В., Саранов И.А. Термический анализ (теория и практика). Воронеж: ВГУИТ. 2018. 56 с."
- Комендантова Е.А., Кваша Д.Ю. Адсорбция в водоочистке. Возможности природных адсорбентов // Синергия Наук. 2017. №. 11. С. 913-930.
- Шилина А.С., Милинчук В.К. Сорбционная очистка природных и промышленных вод от катионов тяжелых металлов и радионуклидов новым типом высокотемпературного алюмосиликатного адсорбента // Журн. Сорбционные и хроматографические процессы. 2Q1Q. № 2. C. 24Q-241
- Федосеева В. И., Миронова А. А. Влияние активации бентонита на его адсорбционные свойства // Вестник Северо-Восточного федерального университета им. МК Аммосова. 2Q17. №. 4 (6Q).
- Бельчинская Л.И., Ходосова Н.А., Новикова Л.А., Стрельникова О.Ю., Ресснер Ф., Петухова А.В., Жабин А.В. Определение соотношения активных центров // Физикохимия поверхности и защита материалов. 2Q16. № 4. С. 363-37Q.
- Евсина Е.М. ГОСТ 6217-52 Пористость по ацетону// Журн. Научный потенциал регионов на службу модернизации. 2Q12. № 2. С. 15Q-151.
- Белецкая М. Г., Богданович Н. И. Формирование адсорбционных свойств нанопористых материалов методом термохимической активации // Химия растительного сырья. 2Q13. №. 3.
- Belchinskaya Г., Novikova Г., Khokhlov V., Гу Tkhi J. Contribution of ion-exchange and non-ion-exchange reactions to sorption of ammonium ions by natural and activated aluminosilicate sorbent // J. Appl. Chem. 2Q13. V. 9. doi: 1Q.1155/2Q13/78941Q
- Akpomie K.G., Onyeabor C.F., Ezeofor C.C., Ani J.U. et al. Natural aluminosilicate clay obtained from south-eastern Nigeria as potential sorbent for oil spill remediation // Journal of African Earth Sciences. 2Q19. V. 155. P. 118-123. doi: 10.1016/j.jafrearsci.2019.04.013
- Semenyutina A.V., Semenyutina V.A., Khuzhakhmetova A.S., Svintsov I.P. The Decrease in the Concentration of formaldehyde in the environment of Aluminosilicate Sorbents // Key Engineering materials. Trans Tech Publications Ltd, 2Q19. V. 802. P. 57-68. doi: 10.4028/www.scientific.net/KEM.802.57
- Caliskan N, Kul A.R., Alkan S., Sogut E.G., Alacabey I. Adsorption of Zinc (II) on diatomite and manganese-oxide-modified diatomite: A kinetic and equilibrium study // Journal of hazardous materials. 2Q11. V. 193. P. 27-36. doi: 10.1016/j,jhazmat.2011.06.058
- Sheng G., Dong H, Li Y. Characterization of diatomite and its application for the retention of radiocobalt: role of environmental parameters // Journal of environmental radioactivity. 2Q12. V. 113. P. 1Q8-115. doi: 1Q.1Q16/j.jenvrad.2Q12.Q5.Q11
- Ibrahim S.S., Selim A.Q. Heat treatment of natural diatomite // Physicochem. Probl. Mner. Process. 2012. V. 48. №. 2. P. 413-424.


