Получение рекомбинантного антигена для серологической диагностики бруцеллеза
Бесплатный доступ
Бруцеллез сельскохозяйственных животных представляет собой одну из наиболее значимых проблем в сфере практической ветеринарии. Своевременное выявление и изоляция инфицированных животных являются критически важными для предотвращения распространения данной инфекции и обеспечения эпизоотического благополучия хозяйства. Диагностические исследования при бруцеллезе в большинстве своем основаны на серологических методах, таких как реакция связывания комплемента и иммуноферментный анализ (ИФА). Целью исследования являлось получение рекомбинантного антигена возбудителей бруцеллеза и изучение его серологической активности в непрямом твердофазном ИФА. В результате анализа иммуногенных эпитопов белков возбудителя бруцеллеза выполнен дизайн антигена, нуклеотидная последовательность которого была клонирована в составе экспрессирующей конструкции на основе вектора pET28а(+). Сконструированный рекомбинантный антиген бруцеллеза был успешно синтезирован в культурах бактериального штамма-продуцента и очищен с применением метода аффинной хроматографии. Полученный препарат использовали в разведении 10 мкг/мл в качестве антигена при проведении непрямого твердофазного ИФА для выявления антител против бруцеллеза. По результатам ИФА установлено, что рекомбинантный антиген проявлял серологическую активность в отношении противобуцеллёзных А-, Sи М-антител. Коэффициент специфичности рассчитывали относительно данных ИФА с сывороткой крови в разведении 1:128. Так, для рекомбинантного антигена при реакции с сывороткой крови крупного рогатого скота против Brucella abortus коэффициент специфичности составил 3,5, B. melitensis – 5,5, S антигена бруцелл – 14,25, R антигена – 0,75. Таким образом, разработанный антиген показал большой потенциал для применения в серологических реакциях для индикации антител против возбудителей бруцеллёза, для которых характерен рост в S-форме бактериальных колоний.
Бруцеллез, ИФА, диагностика, крупный рогатый скот, эпитоп, антиген
Короткий адрес: https://sciup.org/142246298
IDR: 142246298 | УДК: 579.841.93:616-07:61-097 | DOI: 10.31588/2413_4201_1883_3_263_100
Obtaining a recombinant antigen for serological diagnostics of brucellosis
Brucellosis of farm animals is one of the most significant problems in the field of practical veterinary science. Timely detection and isolation of infected animals are critically important for preventing the spread of this infection and ensuring the epizootic well-being of the farm. Diagnostic studies for brucellosis are mostly based on serological methods, such as complement fixation reaction and enzyme immunoassay (ELISA). The aim of the study was to obtain a recombinant antigen of brucellosis pathogens and study its serological activity in an indirect solid-phase ELISA. Based on the analysis of immunogenic epitopes of brucellosis pathogen proteins, an antigen was designed, the nucleotide sequence of which was cloned as part of an expression construct based on the pET28a(+) vector. The designed recombinant brucellosis antigen was successfully synthesized in cultures of the producer bacterial strain and purified using affinity chromatography. The resulting preparation was used in a dilution of 10 micrograms/ml as an antigen in an indirect solid-phase ELISA to detect antibodies against brucellosis. According to the ELISA results, it was found that the recombinant antigen exhibited serological activity against anticellular A-, S-, and M-antibodies. The specificity coefficient was calculated relative to the ELISA data with blood serum in a dilution of 1:128. Thus, for the recombinant antigen in the reaction with cattle blood serum against Brucella abortus, the specificity coefficient was 3.5, B. melitensis - 5.5, Brucella S antigen - 14.25, R antigen - 0.75. Thus, the developed antigen showed great potential for use in serological reactions for the indication of antibodies against brucellosis pathogens, which are characterized by growth in the S-form of bacterial colonies.
Текст научной статьи Получение рекомбинантного антигена для серологической диагностики бруцеллеза
Несвоевременное выявление инфицированных животных приводит к заражению здорового поголовья и обуславливает стойкое неблагополучие хозяйства по бруцеллезу [2]. Эпизоотическая ситуация по бруцеллезу в Российской Федерации остается напряженной, особенно в Северо-Кавказском, Южном, Сибирском и Приволжском федеральных округах [3].
Одними из основных методов диагностики бруцеллеза являются серологические – реакция связывания комплемента (РСК), иммуно-ферментный анализ (ИФА), Роз-Бенгал проба (РПБ) [4]. Во многих серологических тест-системах в качестве антигена используются липополисахариды (ЛПС) клеточной стенки, однако, при использовании ЛПС-антигена встречаются перекрёстные реакции с антигенами других грамотрицательных бактерий [5]. Также на практике часто бывает необходимость дифференциации иммунизированных животных от естественно инфицированных особей. Применение современных серологических тестов, позволяющих различать поствакцинальные антитела от антител, возникающих в результате инфекции, в сочетании с регулярной профилактической иммунизацией, обеспечит возможность контроля и ликвидации бруцеллеза [6].
В последние годы в серологической диагностике инфекционных болезней животных с успехом применяются рекомбинантные антигены (искусственно созданные аминокислотные последовательности участков различных белковых молекул исследуемого возбудителя), которые имеют следующие преимущества: отсутствие необходимости культивирования вирулентного патогена; стандартизация анализа [7]; дифференциация поствакцинальных антител от антител естественно инфицированных животных [8], физико-химическая стабильность, возможность использования большего разнообразия потенциальных мишеней [9]. Таким образом, можно предположить, что применение рекомбинантных антигенов в серологических тестах повысит качество диагностики бруцеллёза и специфичность метода.
Целью исследования являлось получение рекомбинантного антигена возбудителей бруцеллеза и изучение его серологической активности в непрямом твердофазном ИФА.
Для наработки антигена разработанным плазмидным вектором трансформировали компетентные клетки Escherichia coli штамма DH5α с применением хлористого кальция, методом теплового шока, согласно протоколу F.M. Ausubel (2003) [10]. Культуру трансформированных клеток, содержащих модифицированную плазмиду с интегрированным геном, культивировали в 100 мл жидкой питательной среде LB (Lysogeny broth) с добавлением канамицина (20 мкг/мл). Выделение плазмидной ДНК из клеток E. coli осуществляли набором MiniPrep (ЗАО «Евроген», Россия), в соответствии с инструкцией производителя. Концентрацию выделенной плазмиды измеряли с помощью спектрофотометра UV5Nano (Mettler Toledo, США). Трансформацию компетентных клеток E. coli штамма BL21(DE3) осуществляли по аналогии с клетками штамма E. coli DH5α, следуя протоколу F.M. Ausubel (2003) [10]. После получения продуктов экспрессии и трансляции была проведена металл-аффинная хроматография антигена с применением сорбента на основе Ni2+-сефарозы. Концентрацию белка в препарате антигена бруцеллеза определяли с использованием спектрофотометра UV5Nano (Mettler Toledo, США).
В работе использовали сыворотку крови крупного рогатого скота против B. abortus, B. melitensis , а также S и R антигены бруцелл, входящие в состав набора для дифференциальной серологической диагностики бруцеллеза и контроля иммунного ответа крупного рогатого скота, иммунизированного вакциной из штамма B. abortus 82. В качестве отрицательного контрольного образца (ОКО) применяли сыворотку крови не инфицированного бруцел-лами крупного рогатого скота (из того же диагностического набора).
В качестве конъюгата антивидовых антител использовали коммерческий препарат ан-тивидового иммунопероксидазного конъюгата против IgG крупного рогатого скота в разведении 1:20000 («Sigma», США). Постановку способа ИФА на основе сконструированного антигена проводили по методике, опубликованной ранее [11]. Для определения минимального титра антител сыворотки вносили в объеме 4 мкл в первые лунки планшета в разведении 1:25 на ФБР и титровали методом последовательных двукратных разведений (последнее разведение 1:256). В процессе тестирования сывороток в одном разведении в качестве рабочего использовали разведение 1:25. Коэффициент специфичности определяли, как отношение значения оптической плотности, полученного в реакции с каждым наименованием сыворотки (отдельно, с A, S, M, R антителами) к значению оптической плотности полученного в реакции с отрицательным контролем.
Результаты и обсуждение . По результатам запроса информации в базе данных было выявлено девять иммуногенных эпитопов бруцелл. Детальный BLAST-анализ каждого иммуногенного эпитопа позволил для дальнейшей работы отобрать лишь три – qwallpylf (126905), avnaatynr (IEDB ID 92377) антиген Leucine-binding protein domain-containing protein (UniProt:A9MD94) и etvwpffy (92626). Анализ наличия сигнальных пептидов в полных аминокислотных последовательностях для отобранных антигенов показал, что в последовательности антигена «Leucine-binding protein domain-containing protein» на позициях 27-28 а.а. обнаружен сигнальный пептид, действующий по механизму Sec/SPI, что теоретически увеличивает его иммунный потенциал.
В линейном выражении аминокислотная последовательность трех применяющихся иммуногенных эпитопов была следующей qwall-pylfavnaatynretvwpffya, и характеризовалась соответствующими физическими свойствами: число аминокислот 27, молекулярная масса 3252.67 г/М, коэффициент экстинкции 15220 М-1см-1, изоэлектрическая точка возникает при pH = 6.53, суммарный заряд при нейтральном pH = 0, пептид плохо растворим в воде. Для повышения физико-химических свойств антигена была проведена его модификация. В структуру антигена было добавлено девять гидрофильных аминокислот из последовательности нитрат редуктазы, последовательность mkktaiaiavalagfatvaqa сигнального пептида Sec E. coli, а также комбинация нейтральных и гидрофильных аминокислот и гистидиновый тэг, к С-концу молекулы, что позволит обеспечить удобную и эффективную очистку. В результате изменения антиген приобрёл следующую аминокислотную последовательность: mkktaiaiavalagfatvaqahwkesqwallpylfadlkerierav naatynreraereygsetvwpffyagtqrdsihhhhhh. По результатам анализа разработанного антигена проведенном на пептидном калькуляторе установлено, что молекулярный вес аминокислотной последовательности, состоящий из 84 аминокислот, равен 9718.82 г/М, коэффициент экстинкции — 22190 М-1см-, изоэлектрическая точка достигается при pH = 9,11, суммарный заряд при нейтральном pH = 1,7, пептид плохо растворим в воде.
Следует отметить, что в полученной аминокислотной последовательности нет цистеинов, что свидетельствует об отсутствии формирования дисульфидных мостиков, негативно влияющих на конформацию и растворимость белка.
Для получения желаемой аминокислотной последовательности на прокариотическом продуценте была проведена кодонная оптимизация и перевод её из аминокислотной последовательности в нуклеотидную с учётом вида продуцента и добавлением кодона, останавливающего синтез белка. В результате была получена следующая последовательность: «atgaagaagactgccatcgccatcgccgtagcgttggcaggctttg caacggtcgcacaagcccactggaaggagagtcaatgggctttgtt accatatttgttcgctgacctgaaagagcgtattgagcgtgcagtgaa cgcagcaacttacaaccgtgaacgtgcagaacgtgagtacggtagc gagacagtctggccattcttctatgcaggtacccagcgtgattctattc atcaccatcatcaccattga». Длина данной последовательности составила 255 п.н. Затем она была вставлена в плазмидный вектор pET28a(+).
Далее осуществляли наработку разработанной плазмиды следующим образом. В начале провели трансформацию плазмиды в клетки E. coli . Затем выполнили селекцию трансформированных бактериальных клеток по гену устойчивости к ка-намицину. Визуально результат продуцента рекомбинантного антигена представлен на рисунке.
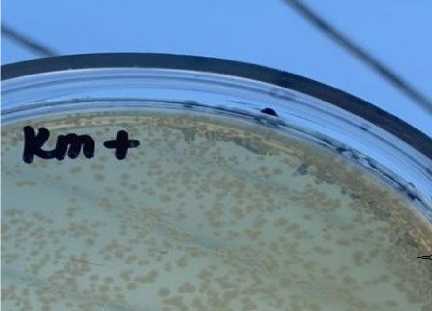
а)
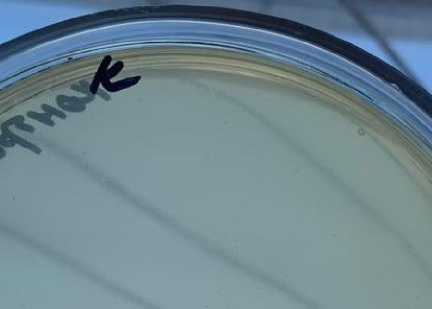
б)
Рисунок – Рекомбинантный антиген, сконструированный для выявления антител против бруцеллёза: а – рост бактериальных клеток, продуцентов рекомбинантного антигена на среде с селективным антибиотиком; б – отсутствие роста нетрансформированных бактериальных клеток на среде с селективным антибиотиком
К числу важнейших требований, предъявляемых к диагностическим антигенам, относится высокое качество применяемого антигенного материала. После получения продуктов экспрессии и трансляции проводили атмосферную аффинную хроматографическую очистку антигенов. Концентрация белка в препаратах антигена бруцеллеза составила 5,0 мг/мл. Полученный препарат был использован в разведении 10 мкг/мл в качестве антигена при проведении непрямого твердофазного ИФА для выявления антител против бруцеллеза. Результаты серологических реакций рекомбинантного антигена с сыворотками крупного рогатого скота, содержащими / не содержащими антитела против возбудителя бруцеллёза представлены в таблице.
Из представленных в таблице данных видно, что рекомбинантный антиген проявлял серологическую активность в отношении про-тивобуцеллёзных А-, S- и М-антител, в отношении R-антител такой активности не наблюдалось. Коэффициент специфичности рассчитывали относительно данных ИФА с сывороткой крови в разведении 1:128. Так для рекомбинантного антигена при реакции с сывороткой крови крупного рогатого скота против B. abortus коэффициент специфичности составил 3,5, B. melitensis – 5,5, S антигена бруцелл – 14,25, R антигена – 0,75.
Таблица - Результаты серологических реакций рекомбинантного антигена с сыворотками крупного рогатого скота
|
Разведение |
ОП сывороток крови μ± sd |
||||
|
A |
S |
M |
R |
ОКО |
|
|
1 |
2 |
3 |
4 |
5 |
6 |
|
1:2 |
0,63±0,16 |
1,19±0,15 |
0,70±0,16 |
0,05±0,13 |
0,066±0,07 |
|
1:4 |
0,52±0,11 |
1,16±0,12 |
0,72±0,16 |
0,05±0,11 |
0,046±0,13 |
|
1:8 |
0,50±0,13 |
0,94±0,07 |
0,46±0,07 |
0,07±0,12 |
0,06±0,13 |
|
1:16 |
0,35±0,10 |
1,00±0,05 |
0,44±0,12 |
0,07±0,09 |
0,04±0,05 |
|
1:32 |
0,29±0,08 |
0,93±0,10 |
0,38±0,11 |
0,05±0,15 |
0,04±0,14 |
|
1:64 |
0,27±0,15 |
0,77±0,15 |
0,32±0,13 |
0,06±0,18 |
0,04±0,12 |
Продолжение Таблицы
|
1 |
2 |
3 |
4 |
5 |
6 |
|
1:128 |
0,14±0,12 |
0,57±0,09 |
0,22±0,08 |
0,03±0,14 |
0,04±0,17 |
|
1:256 |
0,10±0,09 |
0,32±0,03 |
0,14±0,05 |
0,05±0,03 |
0,05±0,06 |
Примечание: A – сыворотка крови крупного рогатого скота против B. abortus; S – сыворотка крови крупного рогатого скота против S антигена бруцелл; М – сыворотка крови крупного рогатого скота против B. melitensis; R – сыворотка крови крупного рогатого скота против R антигена бруцелл .
Таким образом, разработанный антиген показал большой потенциал для применения в серологических реакциях для индикации антител против возбудителей бруцеллёза, для которых характерен рост в S-форме бактериальных колоний.
Выводы. В результате анализа иммуногенных эпитопов белков возбудителя бруцеллеза выполнен дизайн антигена со следующей аминокислотной последовательностью «mkktaiaia valagfatvaqаhwkesqwallpylfadlkerieravnaatynre-raereygsetvwpffyagtqrdsihhhhhh». Сконструированный антиген характеризовался оптимальными физико-химическими показателями, такими как растворимость, коэффициент экстинкции, а также расчётными значениями рН и изоэлектрической точки молекулы. Созданная аминокислотная последовательность была переведена в нуклеотидную и клонирована в состав экспрессирующей конструкции на основе вектора pET28а(+). Установлено, что рекомбинантный антиген бруцеллеза может быть успешно произведен в культурах бактериального штамма-продуцента и очищен с использованием метода аффинной хроматографии. Полученный препарат был использован в разведении 10 мкг/мл в качестве антигена при проведении непрямого твердофазного ИФА для выявления антител против бруцеллеза. По результатам ИФА установлено, что коэффициент специфичности антигена при реакции с сывороткой крови крупного рогатого скота против B. abortus составил 3,5, B. melitensis - 5,5, S и R антигенов - 14,25 и 0,75 соответственно. Разработанный антиген показал большой потенциал для применения в серологических реакциях для индикации антител против возбудителей бруцеллёза, для которых характерен рост в S-форме бактериальных колоний.


