Прогноз отдалённых медицинских радиологических последствий аварии на Чернобыльской АЭС для граждан России и Республики Беларусь по основным радиационно-обусловленным заболеваниям
Автор: Чекин С.Ю., Максютов М.А., Кащеев В.В., Меняйло А.Н., Власов О.К., Щукина Н.В., Корело А.М., Туманов К.А.
Рубрика: Научные статьи
Статья в выпуске: 4 т.25, 2016 года.
Бесплатный доступ
В соответствии с требованиями Международного агентства по атомной энергии (МАГАТЭ) меры контроля после радиационной аварии должны определяться с надлежащим учётом остаточных радиационных рисков, а облучённое население должно быть проинформировано о потенциальных рисках для здоровья. В данной работе на основе рекомендованных международными организациями моделей риска получен прогноз пожизненных радиационных рисков для населения загрязнённых районов Брянской и Гомельской областей, зарегистрированного в Едином чернобыльском регистре России и Беларуси. За период 1986-2016 гг. ожидаемый пожизненный радиационный ущерб от аварии на Чернобыльской АЭС для этого населения реализовался в среднем на 42% по лейкозам и раку щитовидной железы (как по числу случаев, так и по потерянным годам жизни), на 22% - по смертности от рака молочной железы и на 28% - по заболеваемости раком молочной железы. Ожидаемое после 2016 г. число радиационно-индуцированных случаев заболеваний и смертей, а также радиационно-индуцированные потери человеко-лет жизни, связанные с лейкозами и раком щитовидной железы, в 1,4 раза будет превышать аналогичные показатели 1986-2016 гг. Для рака молочной железы ожидаемое превышение над ущербом за период 1986-2016 гг. может составить около 2,5 раз по заболеваемости и около 3,5 раз по смертности. Полученные оценки пожизненных радиационных рисков свидетельствуют о необходимости мер послевосстановительного контроля на загрязнённых территориях в виде долговременного наблюдения за состоянием здоровья населения.
Существующее облучение, чернобыльская аэс, Россия, республика беларусь, загрязнённая радионуклидами территория, население, лейкозы, рак молочной железы, рак щитовидной железы, пожизненный радиационный риск, радиационно-обусловленные потери лет жизни
Короткий адрес: https://sciup.org/170170273
IDR: 170170273 | DOI: 10.21870/0131-3878-2016-25-4-07-19
The forecast of the long-term medical radiological consequences of the Chernobyl accident for population of Russia and Republic of Belarus on the main radiation-caused diseases
According to requirements of the International Atomic Energy Agency (IAEA), controlling measures after radiation accident should be planned with due consideration of possible radiation risks, and the exposed population has to be informed on potential health risks. Lifetime radiation risks for the population of the contaminated regions of Bryansk and Gomel areas registered in the Joint Russian-Belarus Chernobyl registry was calculated with the models recommended by the international organizations. During 1986-2016 possible lifetime adverse radiation effects on health condition were manifested as leukemia and thyroid cancer (both as the number of cases, and potential years of life lost) in 42% of expected cases; breast cancer - in 28%, radiation associated mortality from breast cancer - in 22%. After 2016 the expected number of radiation-related leukemia and thyroid cancer cases, as well as deaths from the diseases and potential years of life lost will exceed the numbers of 1986-2016 by 1.4 times. Radiation related breast cancer incidence will increase by 3.5 times as compared with 1986-2016, mortality from breast cancer will increase by 2.5 times. Obtained estimates of lifetime radiation risks clearly show the need for long-term radioecological surveillance of the affected areas and health monitoring of affected population.
Текст научной статьи Прогноз отдалённых медицинских радиологических последствий аварии на Чернобыльской АЭС для граждан России и Республики Беларусь по основным радиационно-обусловленным заболеваниям
В соответствии с основополагающим принципом оптимизации защиты Международного агентства по атомной энергии (МАГАТЭ) [1] все радиационные риски должны проходить оценку как априори, так и впоследствии, с использованием дифференцированного подхода к различным категориям облучённых лиц и с учётом неопределённости знаний.
После выполнения мероприятий по ликвидации последствий радиационной аварии и осуществления поставарийных мер защиты должна быть проведена оценка эффективности осуществлённых действий. В соответствии с требованиями Международных основных норм безопасности МАГАТЭ [2] меры послевосстановительного контроля должны быть определены «с над-
Чекин С.Ю.* – зав. лаб.; Максютов М.А. – зав. лаб., к.т.н.; Кащеев В.В. – зав. лаб., к.б.н.; Меняйло А.Н. – ст. научн. сотр., к.б.н.; Власов О.К. – зав. лаб., д.т.н.; Щукина Н.В. – ст. научн. сотр.; Корело А.М. – ст. научн. сотр.; Туманов К.А. – зав. лаб., к.б.н. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИРЦ» Минздрава России.
лежащим учётом остаточных радиационных рисков», а для населения, подвергающегося облучению, должно быть обеспечено наличие информации о потенциальных рисках для здоровья.
В частности, Требование 47 «Ответственность правительства в отношении ситуаций существующего облучения» гласит: «5.5. Регулирующий орган или другой соответствующий компетентный орган осуществляет стратегию защиты, включая… b) обеспечение для лиц, подвергающихся облучению, наличия информации о потенциальных рисках для здоровья…» [2], а Требование 49 – «5.15. После завершения восстановительных мероприятий регулирующий орган или другой соответствующий компетентный орган: a) рассматривает, вносит по мере необходимости изменения и официально устанавливает тип, масштабы и продолжительность любых мер послевосстановительного контроля, ранее определённых в плане восстановительных мер, с надлежащим учётом остаточных радиационных рисков».
По определению Международной комиссии по радиологической защите (МКРЗ) [3] радиационный риск человека является многокомпонентной характеристикой: «Его основными компонентами являются величины стохастического характера: вероятность развития смертельного радиационно-индуцированного онкологического заболевания, взвешенная вероятность развития наследственных радиационных эффектов и число лет жизни, потерянных в результате нанесения радиационного вреда».
Для оценки потенциальных рисков для здоровья использования номинальных коэффициентов риска МКРЗ [3] недостаточно. Номинальные коэффициенты риска были вычислены для несуществующей композитной, так называемой референсной, популяции. Эти коэффициенты неприменимы для количественного прогноза радиологических последствий в какой-либо конкретной реальной популяции. Согласно Рекомендациям МКРЗ [3] (параграф 242), должны приниматься во внимание национальные и региональные особенности облучённых контингентов.
Наиболее развитые страны имеют опыт количественного расчёта радиационных рисков с учётом эпидемиологических показателей и демографии своего населения. В частности, для населения США коэффициенты радиационных рисков в пересчёте на уровни загрязнения окружающей среды различными радионуклидами приводятся в отчёте Агентства защиты окружающей среды (EPA) [4]. В России методика учёта национальных особенностей эпидемиологии и демографии при расчёте радиационных рисков от внешнего облучения изложена в действующих МУ 2.1.10.3014-12 [5]. Важное значение также имеют выводы проведенных постчернобыльских эпидемиологических исследований [6-8].
Материалы и методы
Прогноз пожизненных радиационных рисков в данной работе выполнен для лиц из населения загрязнённых районов Брянской и Гомельской областей, зарегистрированных в Едином чернобыльском регистре России и Беларуси (Едином регистре) [9] и доживших до 2016 г. Загрязнёнными районами в Брянской области в настоящее время считаются: Гордеевский, Злын-ковский, Климовский, Клинцовский, Красногорский, Новозыбковский; в Гомельской области: Брагинский, Буда-Кошелевский, Ветковский, Добрушский, Ельский, Кормянский, Наровлянский, Хойникский, Чечерский.
Общая численность населения загрязнённых районов, зарегистрированного в Едином регистре и дожившего до 2016 г., представлена в табл. 1.
Таблица 1
Численность населения загрязнённых районов Брянской и Гомельской областей в 2016 г.
|
Пол |
Население загрязнённых районов Брянской области, человек |
Население загрязнённых районов Гомельской области, человек |
|
Мужской |
57718 |
30653 |
|
Женский |
75253 |
39864 |
|
Всего |
132971 |
70517 |
Показатели радиационных рисков, использованные для прогнозирования
Рекомендованные Научным комитетом по действию атомной радиации Организации Объединённых Наций (НКДАР ООН) модели годовых радиационных рисков (для годовых показателей заболеваемости и смертности) представлены в докладе 2008 г. [10]. В докладе НКДАР ООН 2013 г. [11] представлен анализ опубликованных в научной печати данных о радиационных рисках населения, облучённого в молодом возрасте, до 20 лет, условно называемого в докладе «детским» населением. В частности, проанализированы как собственные модели риска НКДАР ООН [10], так и модели риска Всемирной организации здравоохранения (ВОЗ) 2013 г. [12].
В докладе 2013 г. НКДАР ООН [11] приходит к выводу, что для населения, облучённого в молодом возрасте, оценки радиационных рисков по совокупности всех злокачественных новообразований (ЗНО) должны получаться путём суммирования радиационных рисков по каждой локализации ЗНО в отдельности. Этот вывод основан, в частности, на том, что для некоторых локализаций, таких как рак молочной железы, рак щитовидной железы, лейкозы, радиационные риски при облучении в молодом возрасте существенно превышают риски при облучении в старших возрастах.
В данной работе рассматриваются радиационные риски заболеваемости и смертности по основным локализациям ЗНО, на которые обращается внимание в докладах 2013 г. НКДАР ООН [11] и ВОЗ [12]: все солидные ЗНО (солидные раки), ЗНО (рак) щитовидной железы, ЗНО (рак) молочной железы и лейкозы (исключая хронический лимфолейкоз).
Учитывая, что максимальные дозы, накопленные населением за счёт проживания на загрязнённых территориях России и Республики Беларусь, характерны для лиц, родившихся в 1986 г., рекомендации НКДАР ООН [10] и модели радиационных рисков по локализациям ЗНО [10, 12] особенно актуальны для текущих (в 2016 г.) возрастов населения 30-50 лет.
Для вычисления различных величин пожизненного радиационного риска для населения Брянской и Гомельской областей была рассмотрена фактическая динамика по календарным годам доз по населённым пунктам Брянской и Гомельской областей по данным Единого регистра [9]. Радиационные риски рассчитаны по методике многократного облучения (за исключением рисков для рака щитовидной железы, где принималось однократное облучение в 1986 г.).
Модели радиационных рисков, рекомендованные НКДАР ООН [10] и ВОЗ [12], записываются через интенсивные показатели радиационно-обусловленной заболеваемости (или смертности).
Воздействие радиации на здоровье человека проявляется, в частности, как увеличение риска заболевания или смерти по причине ЗНО. Обозначим λ0 как величину показателя фоновой заболеваемости ЗНО или смертности по причине ЗНО, зависящую от возраста a, пола s и локализации ЗНО. Воздействие радиации приводит к увеличению X0 на дополнительную величину, называемую избыточным абсолютным риском (EAR). Наблюдаемый показатель X заболеваемости (или смертности) представляется в виде суммы фонового и радиационно-обусловленного показателей:
X = Xo + EAR , (1)
где EAR – избыточный абсолютный риск (Excess Absolute Risk), обусловленный облучением. Модель вида (1) называется аддитивной моделью радиационного риска.
Наблюдаемый показатель X заболеваемости (или смертности) также может быть представлен в виде мультипликативной модели радиационного риска:
X = X o - ( 1 + ERR ) , (2)
где ERR – избыточный относительный риск (Excess Relative Risk), обусловленный облучением.
В мультипликативной модели (2) избыточный абсолютный риск зависит от фонового показателя, учитывая тем самым взаимодействие фоновых факторов риска ЗНО с радиационным фактором риска:
EAR = ERR ■ Xo . (3)
При вычислении радиационных рисков по моделям ВОЗ [12] использовали соответствующие рекомендации ВОЗ по усреднению мультипликативной и аддитивной моделей с весами, зависящими от локализации опухоли. Доля мультипликативной модели: лейкозы – 0,5, щитовидная железа – 0,5, молочная железа – 0. Модели рисков заболеваемости лейкозами и смертности по причине лейкозов для НКДАР ООН [10] и ВОЗ [12] одинаковы.
Зная избыточный абсолютный риск EAR для каждого года жизни, можно вычислить пожизненный атрибутивный риск (lifetime attributable risk – LAR) заболеваемости или смертности от ЗНО заданной локализации. LAR – это показатель риска в когорте, характеризующий радиационные последствия с учётом вероятности различных возрастов дожития в этой когорте (с учётом функции дожития S или функции здорового дожития S’ ).
Показатель риска LAR для заболеваемости или смертности вычисляется по формулам (4) или (5) соответственно.
за б .
LAR ( s,c,e,g,.....
g n , d 1 ,...,
a max Г s '( s,c,e,a ) ■ 1
d n ) = Z i___заб ., , a = e [_■ EAR (s , c , a , g ..... g n , d ..... d n )J
LAR смерт . ( s,c,e,g 1 ,..., gn,d1,...,
a max Г S ( s,e,a ) ■ 1
)= Z i J a = e [■ EAR р ■ (s,c,a,g,,.., g„,d,,, dn )J
Здесь s - пол, с - индекс локализации ЗНО, e - достигнутый возраст, g, < e - возрасты при облучении за прошедшие календарные годы (1 – n), d ,..., d – соответствующие эквивалентные годовые дозы облучения в органе или ткани c, S – функция дожития, S′ – функция здорового дожития, amax – максимальный возраст дожития (89 лет).
Функция дожития s ( s,e,a ) характеризует вероятность для группы лиц пола s и возраста e дожить до возраста a . Формула для вычисления S представлена ниже.
Г
S ( s, e, a ) = exp | -
L
a — 1 .
общ . смерт
Z Xo k = e
4 1 1
( s,k ) l
J .
a > e
Здесь ло6щ ' смерт '(s,k) - показатель общей фоновой смертности от всех причин для лиц пола s в возрасте k.
Функция здорового дожития s ' ( s,c,e,a ) характеризует вероятность для человека пола s и возраста e дожить до возраста a и не заболеть при этом ЗНО локализации c .
a - 1
\ iv 1 общ ' смерт , \ забб , х смерт .( . х1
S ' ( s,c,e,a ) = exp | - £ x 0 ( s-k ) + л о ( s,k,c ) - ^ 0 ( s,k,c ) |
L k = e J . (7)
a > e
Зная пожизненный атрибутивный риск, можно определить среднюю пожизненную атрибу- тивную долю (lifetime attributable risk fraction – LARF) радиации в наблюдаемом эффекте (в %).
LARF
( s,c,e,g , ,'„, 9n,d1,..., d n ) =
________ LAR ( s, c, e, g ...... 9 n,d 1..... d n ) ________
LAR ( s,c,e,g , ,'„, 9n,d1,..., d n ) + LBR ( e,c )
■ 100 % ’
где LBR – величина пожизненного фонового риска заболеваемости (или смертности), рассчитанного от возраста дожития e .
a max
LBR 366' ( ee,c ) = ^ Я 3б6' ( s,a,c ) ■ S '( e,c,a,l ) , (9)
a = e a max
LBR смерт ' ( e,c ) = ^ ^ 0мерт ( s,a,c ) ■ S ( e,a,l ) . (10)
a = e
Методика вычисления радиационно-обусловленных потерь лет жизни YLL (years of life lost) приведена в докладе НКДАР ООН [10]. Величина YLL в докладе [10] приводится на единицу дозы, и в таком виде не имеет широкого применения, так как зависимость YLL от дозы не является линейной. В данной работе при вычислении функций дожития использовали средние дозы облучения населения по населённым пунктам, и YLL вычисляли без нормировки на дозу. Таким образом, использовалась следующая формула:
YLL ( s,c,e,g 1 ,..',
gn,d1,...,
d ) amax Г S ( s,e,a ) - 1
a = e L- S d ( s, c, e, a , g 1 ,''', g n ,d l ,''', d n ) J
Здесь S d – функция дожития, учитывающая увеличение смертности за счёт облучения. Она вычисляется аналогично функции дожития, но к показателю общей смертности добавляется избыточный абсолютный риск (EAR) смертности:
S dose ( s ,c,e,a,g i ,’", 9 n , d 1 ,’", d n ) = exp I - E I ^ 0Щ P ( s,k ) + EAR смерт ■( s,c,a,9 1 ,..., 9 n ,d 1 ,..., d n ) | | . (12)
L k=e L JJ a > e
Результаты и обсуждение
На рис. 1а-3б приведены примеры построенных прогнозов пожизненных атрибутивных рисков (LAR), усреднённых по населению загрязнённых районов Брянской и Гомельской областей, в зависимости от достигнутого в 2016 г. возраста, для радиационного риска заболеваемости лейкозами, раком молочной железы и раком щитовидной железы.
Максимальный пожизненный риск в основном имеют лица 1986 г. рождения (достигнутый возраст 30 лет в 2016 г.), так как они имеют максимальную накопленную дозу за время проживания на загрязнённых территориях и минимальный возраст при облучении щитовидной железы радиоизотопами йода.
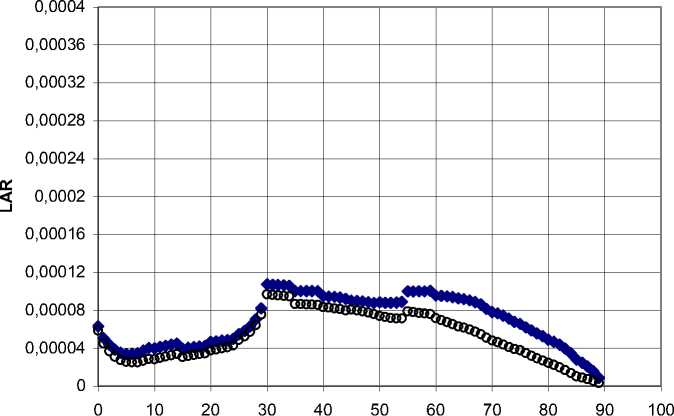
♦ Муж. о Жен.
Возраст в 2016 г.,лет
Рис. 1а. Пожизненные атрибутивные риски (LAR), усреднённые по демографическому составу населения загрязнённых районов Брянской области, в зависимости от достигнутого в 2016 г. возраста, для радиационного риска заболеваемости лейкозами.
Модели НКДАР ООН [10] и ВОЗ [12] (совпадают).
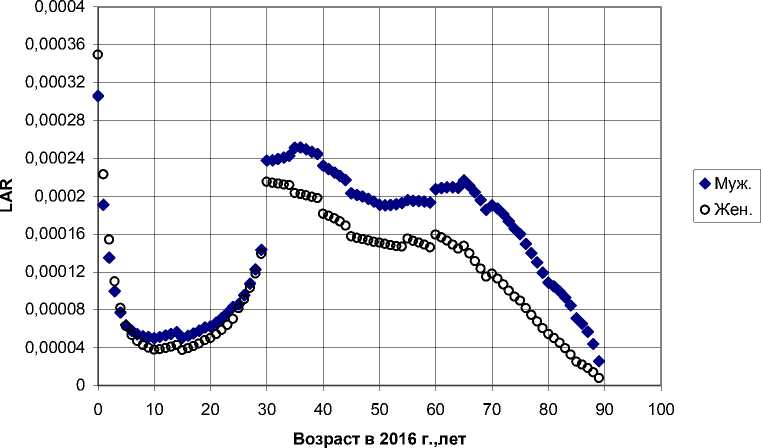
Рис. 1б. Пожизненные атрибутивные риски (LAR), усреднённые по демографическому составу населения загрязнённых районов Гомельской области, в зависимости от достигнутого в 2016 г. возраста, для радиационного риска заболеваемости лейкозами.
Модели НКДАР ООН [10] и ВОЗ [12] (совпадают).
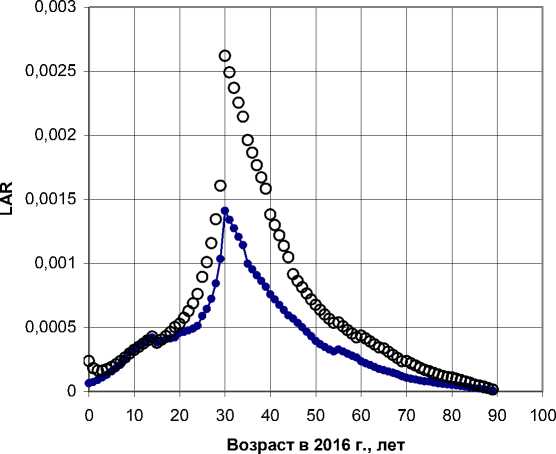
Брянская обл.
о Гомельская обл.
Рис. 2. Пожизненные атрибутивные риски (LAR), усреднённые по демографическому составу населения загрязнённых районов Брянской и Гомельской областей, в зависимости от достигнутого в 2016 г. возраста, для радиационного риска заболеваемости раком молочной железы. Модель ВОЗ [12].
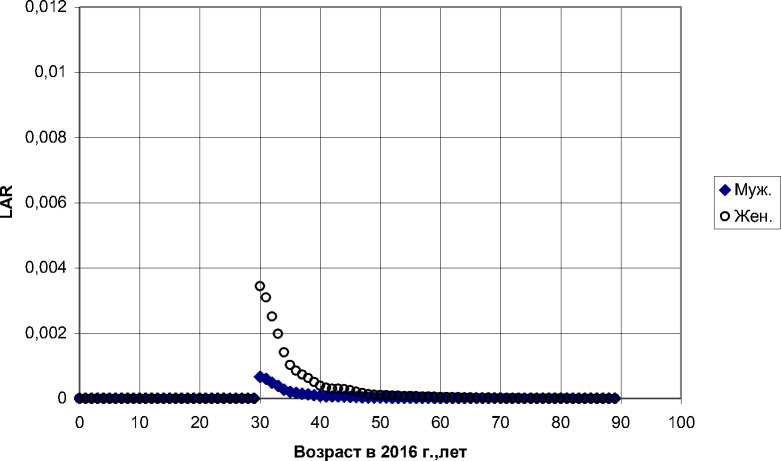
Рис. 3а. Пожизненные атрибутивные риски (LAR), усреднённые по демографическому составу населения загрязнённых районов Брянской области, в зависимости от достигнутого в 2016 г. возраста, для радиационного риска заболеваемости раком щитовидной железы. Модель ВОЗ [12].
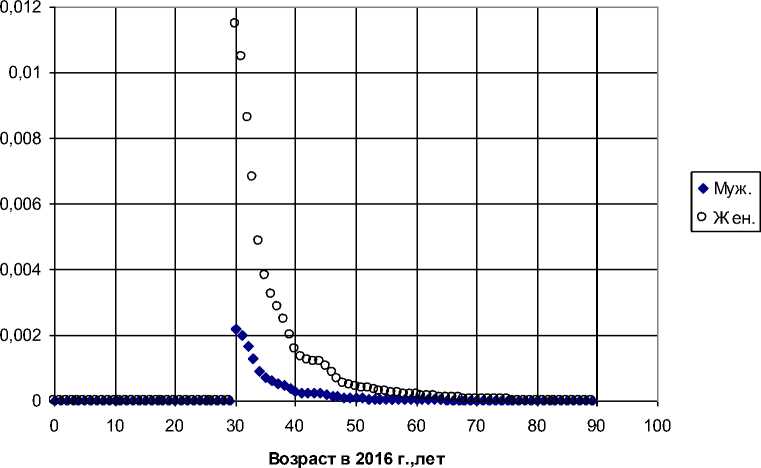
Рис. 3б. Пожизненные атрибутивные риски (LAR), усреднённые по демографическому составу населения загрязнённых районов Гомельской области, в зависимости от достигнутого в 2016 г. возраста, для радиационного риска заболеваемости раком щитовидной железы.
Модель ВОЗ [12].
Обобщающие данные по текущим и прогнозируемым медицинским радиологическим последствиям аварии на ЧАЭС для населения загрязнённых районов Брянской и Гомельской областей приведены в табл. 2-4 для лейкозов, рака молочной железы (РМЖ) и рака щитовидной железы (РЩЖ). В этих таблицах максимальный пожизненный атрибутивный риск заболеваемости и смертности относится к лицам в возрасте 30-35 лет в 2016 г., проживающим в наиболее загрязнённых населённых пунктах Брянской и Гомельской областей.
Таблица 2
Основные показатели текущих и прогнозируемых медицинских радиологических последствий аварии на ЧАЭС для населения загрязнённых районов Брянской и Гомельской областей, связанные с радиационно-индуцированной заболеваемостью
|
Радиационно-индуцированные случаи заболеваний за 1986-2016 гг. |
Радиационно-индуцированные случаи заболеваний после 2016 г. |
Максимальный пожизненный атрибутивный риск заболеваемости (LAR) |
|
|
Брянская область |
|||
|
Лейкозы |
65 |
85 |
0,00070 |
|
РМЖ |
126 |
326 |
0,00883 |
|
РЩЖ |
169 |
246 |
0,01857 |
|
Гомельская область |
|||
|
Лейкозы |
149 |
196 |
0,00184 |
|
РМЖ |
243 |
591 |
0,01992 |
|
РЩЖ |
433 |
592 |
0,02591 |
Таблица 3
Основные показатели текущих и прогнозируемых медицинских радиологических последствий аварии на ЧАЭС для населения загрязнённых районов Брянской и Гомельской областей, связанные с радиационно-индуцированной смертностью
|
Радиационно-индуцированные случаи смерти за 1986-2016 гг. |
Радиационно-индуцированные случаи смерти после 2016 г. |
Максимальный пожизненный атрибутивный риск смертности (LAR) |
|
|
Брянская область |
|||
|
Лейкозы |
43 |
61 |
0,0005 |
|
РМЖ |
36 |
133 |
0,0035 |
|
РЩЖ |
0 |
0 |
0,0000 |
|
Гомельская область |
|||
|
Лейкозы |
100 |
139 |
0,0013 |
|
РМЖ |
71 |
243 |
0,0078 |
|
РЩЖ |
0 |
0 |
0,0000 |
Таблица 4
Произошедшие и прогнозируемые радиационно-обусловленные потери человеко-лет жизни среди населения загрязнённых районов Брянской и Гомельской областей, связанные с радиационно-индуцированной смертностью
|
Радиационно-индуцированные потери человеко-лет жизни за 1986-2016 гг. |
Радиационно-индуцированные потери человеко-лет жизни после 2016 г. |
Максимальный пожизненный атрибутивный риск смертности (LAR) |
|
|
Брянская область |
|||
|
Лейкозы |
562 |
773 |
0,0005 |
|
РМЖ |
494 |
1746 |
0,0035 |
|
РЩЖ |
0 |
0 |
0,0000 |
|
Гомельская область |
|||
|
Лейкозы |
1217 |
1673 |
0,0013 |
|
РМЖ |
934 |
3153 |
0,0078 |
|
РЩЖ |
0 |
0 |
0,0000 |
Проведённым вычислениям присущи неопределённости, обусловленные объективным отсутствием статистических данных о заболеваемости и смертности российского населения и населения Республики Беларусь за текущий 2016 г. Поэтому в расчётах использовали последние по времени доступные статистические данные, за 2014 г. Фоновые показатели заболеваемости и смертности для населения России использовали по данным справочника [13].
Для Республики Беларусь источником данных о половозрастных показателях заболеваемости ЗНО и смертности от ЗНО являлся справочник [14], выпущенный Национальным статистическим комитетом Республики Беларусь. Этот справочник содержит общее число случаев заболеваний ЗНО по некоторым отдельным локализациям. В данном справочнике отсутствуют данные по ЗНО лимфатической и кроветворной ткани (включая лейкозы). Кроме того, нет данных о возрастной структуре заболеваемости по отдельным локализациям и отсутствуют данные о смертности по причине ЗНО. Для получения фоновых показателей заболеваемости в Республике Беларусь из числа заболевших необходимо использовать половозрастную численность населения в Республике Беларусь. Эти данные были получены из электронного статистического справочника [15]. Чтобы восполнить недостающие данные о фоновых показателях заболе- ваемости и смертности по лейкозам в Республике Беларусь, вместо них использовали российские показатели [13]. Дополнительно принимали допущения, что летальность лейкозов и доля лейкозов в общем числе ЗНО лимфатической и кроветворной ткани в Республике Беларусь и России совпадают.
Выводы
Как показывают данные табл. 2-4, за период 1986-2016 гг. ожидаемый пожизненный радиационный ущерб от аварии на ЧАЭС для населения загрязнённых районов Брянской и Гомельской областей реализовался в среднем на 42% по лейкозам и раку щитовидной железы (как по числу случаев, так и по потерянным годам жизни), на 22% - по смертности от рака молочной железы и на 28% - по заболеваемости раком молочной железы. Ожидаемое после 2016 г. число радиационно-индуцированных случаев заболеваний и смертей, а также радиационно-индуцированные потери человеко-лет жизни, связанные с лейкозами и раком щитовидной железы, среди облучённого населения в 1,4 раза будет превышать аналогичные показатели за предыдущие 30 лет (1986-2016 гг.), прошедшие после аварии на ЧАЭС. Для рака молочной железы ожидаемое превышение над ущербом за период 1986-2016 гг. может составить около 2,5 раз по заболеваемости и около 3,5 раз по смертности. Это связано с тем, что лица в возрасте до 20 лет на начало облучения (в 1986 г.), имеющие максимальные годовые атрибутивные риски (EAR), с течением времени будут вносить увеличивающийся вклад в заболеваемость и смертность популяции в целом.
Следует также отметить, что максимальный пожизненный атрибутивный риск смертности (LAR) (для населения в возрасте 30 лет в 2016 г.) по причине РМЖ для загрязнённых районов Гомельской области (LARмакс=7,8 х 10 ■ 3) существенно превышает ограничение индивидуального пожизненного риска для населения в нормальных условиях облучения, установленное действующими российскими нормами радиационной безопасности (НРБ-99/2009) [16] на уровне (70 лет х 5 х 10- 5 /год)=3,5 х 10-3. Сам по себе этот факт не является нарушением НРБ-99/2009, так как ограничение норм безопасности не распространяется на ситуации существующего облучения в поставарийный период, однако свидетельствует о необходимости мер послевосстанови-тельного контроля в виде наблюдения за состоянием здоровья населения загрязнённых территорий.
Работа выполнена в рамках Программы совместной деятельности по преодолению последствий чернобыльской катастрофы в рамках Союзного государства на период до 2016 г. в 2016 г. по теме «Формирование групп повышенного радиационного риска на основе комплексного анализа данных Единого чернобыльского регистра России и Беларуси, включающего уточненные оценки радиационных рисков и прогноз отдалённых медицинских радиологических последствий аварии на Чернобыльской атомной электростанции для граждан России и Беларуси, подвергшихся радиационному воздействию вследствие чернобыльской катастрофы».
Список литературы Прогноз отдалённых медицинских радиологических последствий аварии на Чернобыльской АЭС для граждан России и Республики Беларусь по основным радиационно-обусловленным заболеваниям
- Основополагающие принципы безопасности. Серия норм МАГАТЭ по безопасности, № SF-1. Вена: МАГАТЭ, 2007. 23 с.
- Радиационная защита и безопасность источников излучения: Международные основные нормы безопасности. Общие требования безопасности, часть 3. Вена: МАГАТЭ, 2015. 518 с.
- Рекомендации 2007 года Международной комиссии по радиологической защите. Публикация 103 МКРЗ: пер. с англ. под ред. М.Ф. Киселева и Н.К. Шандалы. М.: Изд. ООО ПКФ «Алана», 2009. 344 с.
- Cancer risk coefficients for environmental exposure to radionuclides. EPA-402-R-99-001, FGR 13. Oak Ridge National Laboratory, U.S. Environmental Protection Agency Office of Radiation and Indoor Air 1200 Pennsylvania Ave., NW, Washington, DC 20460, 1999. 186 p.
- Оценка радиационного риска у населения за счёт длительного равномерного техногенного облучения в малых дозах. МУ 2.1.10.3014-12. М.: Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека, 2012.
- Ivanov V.K., Gorski A.I., Tsyb A.F., Maksioutov M.A., Tumanov K.A., Vlasov O.K. Radiation-epidemiological studies of thyroid cancer incidence among children and adolescents in the Bryansk oblast of Russia after the Chernobyl accident (1991-2001 follow-up period)//Radiat. Environ. Biophys. 2006. V. 45, N 1. P. 9-16.
- Ivanov V.K., Tsyb A.F., Konogorov A.P., Rastopchin E.M., Khait S.E. Case-control analysis of leukaemia among Chernobyl accident emergency workers residing in the Russian Federation, 1986-1993//J. Radiol. Prot. 1997. V. 17, N 3. P. 137-157.
- Ivanov V.K., Tsyb A.F., Petrov A.V., Maksioutov M.A., Shilyaeva T.P., Kochergina E.V. Thyroid cancer incidence among liquidators of the Chernobyl accident: absence of dependence of radiation risks on external radiation dose//Radiat. Environ. Biophys. 2002. V. 41, N 3. P. 195-198.
- Максютов М.А., Корело А.М., Туманов К.А., Иванов В.К. Банк радиологических данных Единого чернобыльского регистра России и Беларуси//Медицинские радиологические последствия Чернобыля: прогноз и фактические данные спустя 30 лет: сборник тезисов международной научно-практической конференции. Обнинск, 17-19 мая 2016 г. 90 с. . URL: http://www.radiation-and-risk.com/abstracts.pdf (дата обращения 2.09.2016 г.).
- United Nations Scientific Committee on the Effects of Atomic Radiation (UNSCEAR). Sources and effects of ionizing radiation. UNSCEAR 2006 Report. Vol. I, Annex A: Epidemiological studies of radiation and cancer. New York: United Nation, 2008.
- United Nations Scientific Committee on the Effects of Atomic Radiation (UNSCEAR). Sources, effects and risks of ionizing radiation. UNSCEAR 2013 Report. Vol. II, Scientific Annex B: Effects of radiation exposure of children. New York: United Nations, 2013.
- Health risk assessment from the nuclear accident after the 2011 Great East Japan Earthquake and Tsunami based on a preliminary dose estimation. World Health Organization, 2013.
- Злокачественные новообразования в России в 2014 году (заболеваемость и смертность)/Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: МНИОИ им. П.А. Герцена -филиал ФГБУ «НМИРЦ» Минздрава России, 2016. 250 с.
- Женщины и мужчины Республики Беларусь. Статистический сборник. Минск: Национальный статистический комитет Республики Беларусь, 2016.
- Официальный сайт. URL: http://demdata.belstat.gov.by/Search.html (дата обращения: 29.08.2016 г.).
- Нормы радиационной безопасности (НРБ-99/2009). СанПин 2.6.1.2523-09. М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2009. 100 с.


