Прогноз выживаемости и результаты таргетной терапии хронического миелолейкоза
Автор: Шуваев В. А., Мартынкевич И. С., Фоминых М. С., Потихонова Н. А., Зотова И. И., Удальева В. Ю., Зенина М. Н., Тиранова С. А., Кудряшова С. А., Мартыненко Л. С., Бакай М. П., Цыбакова Н. Ю., Мотыко Е. В., Полушкина Л. Б., Клеина Е. В., Руженкова Ю. С., Павленко Н. Б., Волошин С. В., Бессмельцев С. С.
Журнал: Вестник гематологии @bulletin-of-hematology
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.14, 2018 года.
Бесплатный доступ
Хронический миелолейкоз (ХМЛ) -злокачественное новообразование кроветворной ткани, ассоциированное с характерной хромосомной аномалией (филадельфийской хромосомой). Для лечения хронического миелолейкоза впервые была разработана высокоточная таргетная терапия отдельным классом препаратов - ингибиторов тирозинкиназ (ИТК),позволившая изменить прогноз заболевания. Цель современной терапии ХМЛ - максимальное подавление Ph-положительного опухолевого клона, снижение риска прогрессии заболевания, достижение продолжительностижизни больных, сравнимой с общей популяцией. Достижение полного цитогенетического ответа (ПЦО) и большого молекулярногоответа (БМО) - это ранние благоприятные прогностические признаки длительной выживаемости без прогрессирования при условии постоянной терапии. В настоящее время ИТК являются основным средством терапии ХМЛ и имеют доказанное преимущество над другими методами лечения Терапия ИТК первой и второй линии должнабыть выбрана с учетом наибольшей эффективности и наименьшего риска побочных явлений.Ранняя оценка ответа на лечение, предупреждение развития резистентности и быстроепереключение на максимально эффективную терапию при отсутствии оптимального ответадолжны быть основными принципами современной терапии ХМЛ. Целью данной работы было изучить прогнози эффективность таргетной терапии хронического миелолейкоза и её смены по данным молекулярно-генетического мониторинга.
Хронический миелолейкоз, таргетная терапия, ингибиторы тирозинкиназ, иматиниб, нилотиниб, дазатиниб, бозутиниб, клиническая практика
Короткий адрес: https://sciup.org/170172522
IDR: 170172522
Syurvival prognosis and target therapy results in chronic myeloid leukemia patients
Chronic myeloid leukemia (CML) is amalignant neoplasm of hematopoietic tissue associated with a characteristic chromosomal (Philadelphia chromosome) abnormality. For the treatmentof chronic myeloid leukemia was first developedhigh-precision targeted therapy with a special classof drugs - tyrosine kinase inhibitors (TKI), whichhad changed the CML prognosis. At present the aimof CML therapy is maximum suppression of tumorclone, reducing the risk of disease progression,achieving life expectancy of patients comparableto the General population. Achieving a completecytogenetic response (CCyR) and a major molecularresponse (MMR) are early favorable prognosticsigns of longterm progression-free survival withcontinued therapy. Currently, TKI is the primarytreatment for CML and has a proven advantageover other treatments modalities. Therapy of the first and second line TKI shouldbe chosen taking into account the highest efficiencyand the lowest risk of side effects. Early evaluationof treatment response, prevention of resistance development and rapid switching to the most effectivetherapy in the absence of optimal response shouldbe the basic principles of modern cMl therapy. The aim of this work was to study the prognosisand effectiveness of targeted therapy of chronicmyeloid leukemia and its change according to molecular genetic monitoring. To conduct the study were analyzed the resultsof diagnosis and treatment of 307 patients withCML observed at our institution in the period 2005- 2018. A comparison of prognostic scales for predicting overall (OS) and progression-free survival.
Текст научной статьи Прогноз выживаемости и результаты таргетной терапии хронического миелолейкоза
Введение . Хронический миелолейкоз (ХМЛ) — злокачественное новообразование кроветворной ткани, обусловленное злокачественным перерождением плюрипотентной стволовой клетки, характеризующееся усилением пролиферации гранулоцитарного ростка без потери способности к диффе-
(PFS) showed a better sensitivity of the ELTS scale compared to the Sokal risk group. In the imatinib treatment — 57 % of patients have achieved CCyR and 46 % of patients — MMR. The switch of therapy to second-generation TIC was performed in 40 % of patients. The target levels of response in second-line TKI treatment were achieved as follows: CCyR in 57 % of patients, MMR in 43 %. The results of treatment differed signi^icantly depending on the term of previous treatment with imatinib: more or less than 24 months. Third-line TKI therapy was administered to 41 % of patients who had been treated with second-line treatment.As a result of the third line of therapy: CCyR was reached in 42 % patients, MMR during third-line treatment was achieved in 25 % of patients. At the same time, differences in the total duration of previous therapy of TKI were important for survival results: more or less than 48 months.
As a result of our study, we would like to conclude that the treatment of patients with chronic myeloid leukemia with tyrosine kinase inhibitors can lead to successful suppression of the tumor and prevent progression in most patients. With the ineffectiveness or intolerance of imatinib, therapy with tyrosine kinase inhibitors of the second and even third lines can be effective in a large proportion of patients. One of the most important factors in preventing the development of tumor resistance is early switching to the next treatment lines in the presence of signs of resistance and/or intolerance.
ренцировке, ассоциированное с характерной хромосомной аномалией (филадельфийской хромосомой) [1, 2]. Продукт специфической для ХМЛ генетической транслокации — белок BCR-ABL был впервые выделен в 1986 г. [3]. Иммунотерапия в виде интерферона начала использоваться в 1980-х годах и по- зволила впервые у небольшой части больных получить цитогенетические ответы и восстановить нормальный гемопоэз [4]. В 1996 г. N. Lydon и B. Druker опубликовали первые экспериментальные данные о препарате STI-571, который после опубликования первых результатов клинических исследований в 2001 г. был зарегистрирован как иматиниб и явился первым препаратом из класса ингибиторов тирозинкиназ (ИТК), который совершил переворот в лечении ХМЛ [5].
Цель современной терапии ХМЛ — максимальное подавление Ph-положительного опухолевого клона,снижение риска прогрессии заболевания, достижение продолжительности жизни больных, сравнимой с общей популяцией. Достижение полного цитогенетического ответа (ПЦО) и большого молекулярного ответа (БМО) — это ранние благоприятные прогностические признаки длительной выживаемости без прогрессирования при условии постоянной терапии [6, 7].
В настоящее время ИТК являются основным средством терапии ХМЛ и имеют доказанное преимущество перед другими методами лечения. Механизм действия ИТК обусловлен блокадой АТФ-связывающего кармана молекулы BCR-ABL, что лишает белок BCR-ABL тирозинкиназной активности, дающей опухолевым клеткам пролиферативное преимущество. При постоянном воздействии ИТК происходит редукция опухолевого клона и восстановление нормального гемопоэза.
Терапия ИТК первой и второй линии должна быть выбрана с учетом наибольшей эффективности и наименьшего риска побочных явлений. Ранняя оценка ответа на лечение, предупреждение развития резистентности и быстрое переключение на максимально эффективную терапию при отсутствии оптимального ответа должны быть основными принципами современной терапии ХМЛ [7].
В Российской Федерации в настоящее время зарегистрированы четыре лекарственных препарата из группы ИТК для лечения ХМЛ: иматиниб, нилотиниб, дазатиниб и бозутиниб.
Иматиниб — ингибитор тирозинкиназ,ко-торый способен значительно подавлять активность BCR-ABL тирозинкиназы, а также ингибировать C-KIT, PDGFR — киназную активность. Начальная доза не зависит от пола, массы тела, роста, расы пациента и составляет 400 мг в сутки для хронической фазы (ХФ) и 600 мг в сутки для фазы акселерации (ФА) и бластного криза (БК) у взрослых [8].
Нилотиниб — мощный, высокоселективный ингибитор BCR-ABL-тирозинкиназы. Синтезирован на основе молекулы иматиниба и обладает бόльшим сродством к BCR-ABL -тирозинки-назе по сравнению с иматинибом [9]. Активен в отношении мутантных форм BCR-ABL тиро-зинкиназы (за исключением мутаций Y253H, E255K/V, F359V, T315I) [10]. Выпускается в виде капсул по 150 и 200 мг. В первой линии терапии показан больным с ХФ ХМЛ в начальной дозе 600 мг/сут и в ФА ХМЛ в дозе 800 мг/сут. Во второй линии терапии нилотиниб назначается в дозе 800 мг/сут в ХФ и ФА [11].
Дазатиниб — многоцелевой препарат, взаимодействующий со многими тирозинкиназными и нетирозинкиназными белками.Дазатиниб ингибирует тирозинкиназу BCR-ABL и тиро-зинкиназы семейства Src (SRC, LCK, YES, FYN), C-KIT, EPHA2, PDGFRβ, PDGFRα. Активен в отношении большинства мутантных форм BCR-ABL за исключением мутаций T315I, T315A, V299L, F317L/V/I/C [10]. Способен in vitro ингибировать рост клеточных линий с гиперэкспрессией BCR-ABL , активацией альтернативных онкогенных путей, включающих киназы семейства SRC (LYN, HCK). Показана возможность дазатиниба проникать через гематоэнцефалический барьер. Рекомендуемая доза дазатиниба для ХФ составляет 100 мг/сут, а для ФА и БК 140 мг/сут [12].
Бозутиниб является также многоцелевым препаратом, блокирующим тирозинкиназы BCR-ABL и семейства Src (SRC, LCK, YES, FYN), C-KIT, EPHA2, PDGFRβ, PDGFRα. Плохо чувствительны к применению бозутиниба мутантные формы BCR-ABL T315I, V299L, G250E, E255K/V [10]. Препарат зарегистрирован в России в настоящее время для лечения хронического миелолейкоза в хронической фазе,фазе акселерации или бластного криза при непереносимости или неэффективности предшествующей терапии иматинибом,нилотинибом и дазатинибом. Рекомендуемая доза бозутиниба составляет 500 мг/сут, прием один раз в день во время еды.
Необходимо отметить,что абсолютных противопоказаний для использования любого препарата ингибиторов тирозинкиназ нет. Вместе с тем при выборе конкретного препарата для назначения больному ХМЛ необходимо учитывать фазу заболевания, сопутствующую патологию и риск развития побочных эффектов в процессе терапии,а также спектр мутаций гена BCR-ABL.
Для оценки эффективности терапии необходимо проводить своевременный мониторинг гематологических, цитогенетических и молекулярно-генетических показателей [7]. Результаты терапии у больных ХМЛ оцениваются по данным гематологического, цитогенетического и молекулярного методов исследования. В зависимости от вида исследования и степени подавления опухолевого клона выделяют различные виды ответа: гематологический, цитогенетический и молекулярный.
Эффект терапии первой линии может быть расценен как оптимальный, предупреждение или неудача терапии . Оптимальный ответ свидетельствует о благоприятном прогнозе и ожидаемой длительной безрецидивной выживаемости пациентов.При оптимальном ответе лечение ИТК продолжают в прежней дозе.
Для оптимального ответа необходимо достижение:
-
— полного гематологического ответа в течение первых 3 месяцев терапии ИТК;
-
— полного цитогенетического ответа в течение первых 6 месяцев терапии ИТК;
-
— большого молекулярного ответа в течение первых 12 месяцев терапии ИТК.
Предупреждение указывает на необходимость тщательного мониторинга и готовность к смене терапии.
Неудача терапии предполагает низкую вероятность длительной безрецидивной выживаемости и является показанием к смене терапии.Потеря достигнутой ранее ремиссии, появление новых мутаций, дополнительные хромосомные аберрации (ДХА) в Ph + клетках при проведении терапии ИТК также являются свидетельством неудачи лечения.
Факторы предостережения — биологические признаки более агрессивного течения заболевания, требующие более тщательного наблюдения за больным.К таким факторам относятся: группа высокого риска ХМЛ на момент установления диагноза; клинические значимые ДХА в Ph + клетках на момент установления диагноза (трисомия 8, трисомия/до-полнительная Ph-хромосома ( + der(22) t(9;22) (q34; q11)), —Y — если выявлены в ФА и БК изохромосома 17 (i(17)(q10)), трисомия 19, изодериват (22)(q10) t(9; 22)(q34; q11) в ХФ) в ходе лечения ИТК: выявление –7/del(7q), 3(q26.2), комплексных ДХА, мутаций BCR-ABL , сочетание ДХА и мутаций, ДХА80
При недостаточной эффективности или непереносимости терапии первой линии при выборе ИТК для смены терапии необходимо учитывать анамнез лечения, в том числе наблюдавшиеся побочные эффекты, сопутствующую патологию, результаты определения мутационного статуса BCR–ABL. При неудаче терапии иматинибом необходима смена терапии на другие ИТК. Повышение дозы иматини-ба до 600–800 мг/сут может являться только временной мерой в условиях ограниченного доступа к ИТК второго поколения.
При неудаче лечения первой и второй линии четких рекомендаций по ведению больных, получающих третью линию терапии, нет. Возможности терапии при неудаче первой и второй линии лечения,а также при прогрессии ХМЛ до продвинутых фаз ограничены. Отсутствие резерва нормального кроветворения, длительные цитопении,даже без формальных признаков прогрессии заболевания до продвинутых фаз, делают трудно выполнимым длительное применение ИТК в постоянном режиме и в полных дозах, что снижает эффективность воздействия на лейкозный клон и увеличивает вероятность прогрессии заболевания. Учитывая биологически обусловленную сниженную эффективность терапии третьей линии,максимально полно должны быть использованы алгоритмы индукции ремиссии на предыдущих этапах лечения.
Вместе с тем,раннее активное переключение при неудаче первой линии терапии может дать больше шансов преодолеть потенциальную резистентность к ИТК и обеспечить достижение целевых ответов и длительную безреци-дивную выживаемость большему количеству больных ХМЛ.
Таким образом, целью данной работы было изучить прогноз и эффективность таргетной терапии хронического миелолейкоза и её смены по данным молекулярно-генетического мониторинга.
Материалы и методы. Для проведения исследования создана база данных, в которую включена информация о больных хроническим миелолейкозом, наблюдавшихся в РосНИИГТ в период с 2005по 2018 годы.
Собраны и проанализированы следующие показатели:
-
— клинико-демографические показатели общей выборки больных, распределение пациентов по группам риска и их влияние на общую и беспрогрессивную выживаемость;
— эффективность терапии ИТК первой линии с оценкой частоты достижения целевых ответов, соответствующих срокам лечения;
-
— эффективность терапии ИТК второй линии с оценкой частоты достижения целевых ответов, соответствующих периодам лечения в зависимости от сроков переключения (длительности предшествующей терапии первой линии);
-
— эффективность терапии ИТК третьей линии с оценкой частоты достижения целевых ответов, соответствующих периодам лечения в зависимости от сроков переключения (длительности предшествующей терапии ИТК (первой и второй линии).
Для анализа использовались методы описательной статистики, оценка выживаемости проводилась с помощью кривых Каплана-Мейера и логарифмического рангового критерия.Об-работка данных проводилась на персональном компьютере с помощью пакетов прикладных программ Microsoft Office 2013 и Statistica 9.0 for Windows.
Результаты. Всего в базу данных была включена информация о 307 больных ХМЛ: 136 мужчинах и 171 женщине.Медиана возраста на момент установления диагноза составила 51 год (5–85 лет). Продолжительность наблюдения от момента установления диагноза составила: медиана 6,1 лет, интервал от 0,1 до 21 года. У 92 % пациентов диагноз ХМЛ был установлен в хронической фазе заболевания, 7 % больных на момент диагностики имели ФА и 1 % находились в БК.В соответствии с группой риска Sokal пациенты распределились следующим образом: низкая группа риска — 51 %, промежуточная — 4 % и высокая у 20 % больных, в 25 % случаев достаточной информации для определения группы риска не имелось.При стратификации пациентов по группам риска по шкале ELTS у 44 % определялся низкий риск, у 21 % — промежуточный и 9 % больных имели высокую группу риска, у 25 % информации для определения группы риска также было недостаточно.На момент проведения анализа 211 (69 %) пациентов были живы. Оценочная медиана выживаемости составила 12,3 года, при этом 5-летняя и 10-летняя общая выживаемости (ОВ) были: 83 % и 63 % соответствен-но.Прогрессирование в продвинутые фазы заболевания (ФА и БК) наблюдалось у 14 % пациентов.Медиана времени от момента установления диагноза до прогрессирования составила 7,4 года (0,2–18,5). Общая выживаемость статистически значимо не различалась по группам риска шкалы Sokal, тогда как при оценке различий ОВ по шкале ELTS была получена статистическая значимость (p = 0,12) выживаемости между группами пациентов низкого (медиана 16,6 лет) и промежуточного с высоким степенями рисков (медиана 9,5 лет), рисунок 1.
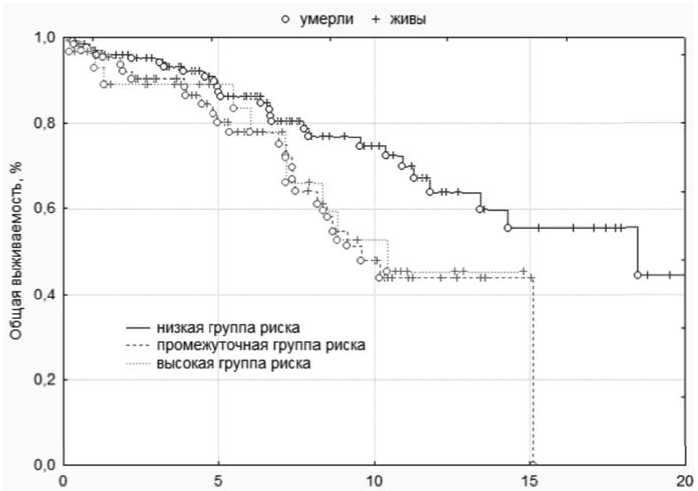
Время от установления диагноза, лет
Рисунок 1. Общая выживаемость больных хроническим миелолейкозом в соответствии с группой риска по шкале ELTS.
При анализе беспрогрессивной выживаемости в группах риска по шкале Sokal были получены отличия порогового уровня статистической значимости (p = 0,49), тогда как шкала ELTS позволила получить более высоко значимые
(p = 0,003) различия между всеми группами. Пятилетняя БПВ в соответствии с группами риска по шкале ELTS составила: 97,2 % для низкого риска, 92,4 % для промежуточного и 83,8 % для высокого риска ( рисунок 2 ).
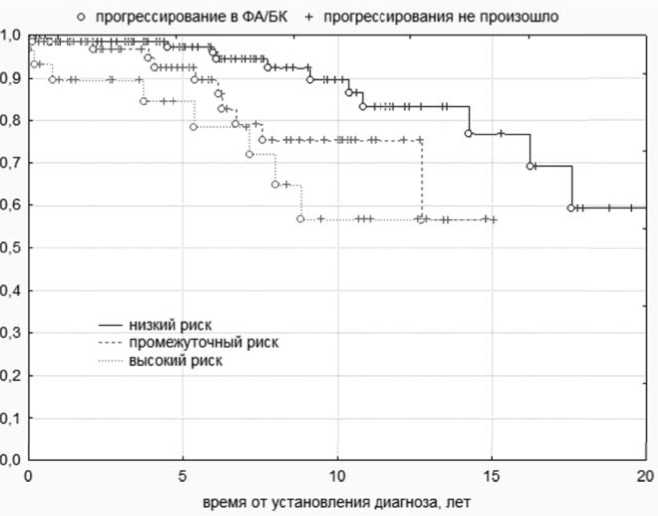
Рисунок 2. Беспрогрессивная выживаемость больных хроническим миелолейкозом в соответствии с группой риска по шкале ELTS.
Таргетная терапия в первой линии проводилась у 300 пациентов.У подавляющего большинства больных использовался имати-ниб (n = 287; 95,7 %), незначительная часть в качестве первой линии ИТК получала ни-лотиниб (n = 9; 3,0 %), дазатиниб (n = 3; 1,0 %) и бозутиниб (n = 1; 0,3 %). С учетом небольшого количества ИТК2, применявшегося в качестве первой линии терапии, для корректной оценки результатов анализ эффективности терапии первой линии проводился только в группе пациентов, получавших иматиниб.
Терапия в начальной дозе 400 мг была начата у 264 (92 %) пациентов, дозировку в 600 мг получали 17 (6 %) больных, 800 мг — 3 (1 %) и у 1 (0,3 %) пациентки лечение было начато в дозе 300 мг в сутки.Медиана времени от момента установления диагноза до начала терапии составила 1,3 месяца (0–219,8 месяцев). Целевых уровней ответа при терапии иматини-бом достигли следующие категории пациентов:
-
— полного гематологического ответа
(ПГО) — 93 % пациентов, медиана времени достижения составила 0,9 месяца, в течение первых 3 месяцев ПГО был до- стигнут у 72 % пациентов;
-
— полного цитогенетического ответа (ПЦО) — 57 % пациентов, медиана продолжительности терапии до достижения ПЦО составила 7,5 месяцев, при этом в течение первых 6 месяцев терапии ПЦО был достигнут у 46 % пациентов;
-
— большого молекулярного ответа (БМО) — 46 % пациентов, медиана продолжительности приема иматиниба до достижения БМО составила 24,6 ме-сяцев,при этом в течение первого года терапии БМО был достигнут у 14 % пациентов.
Смена терапии на ИТК второго поколения была проведена у 40 % пациентов, у 30 % в связи с резистентностью и у 8 % больных по причине выраженных побочных явлений (непереносимости), в остальных (2 %) случаев смена терапии проводилась по другим причинам. Медиана продолжительности терапии иматинибом перед сменой на вторую линию составила 23,8 месяцев (0,7–145,4 месяцев).
В рамках второй линии терапии 67 % пациентов получали нилотиниб, в 31 % случаях при- менялся дазатиниб, бозутиниб использовался у оставшихся 2 %. Целевых уровней ответа при терапии второй линии достигли следующие категории пациентов:
— ПГО на момент начала терапии второй линии отсутствовал у 35 пациентов и был достигнут в ходе терапии у 27 (77 %) из них, медиана времени достижения составила 2,3 месяца, в течение первых 3 месяцев ПГО был достигнут у 49 % пациентов;
— ПЦО на момент начала второй линии терапии отсутствовал у 89 больных, в ходе лечения он был достигнут у 51 (57 %) пациентов, медиана продолжительности терапии до достижения ПЦО составила 4,0 месяцев, при этом в течение первых 12 месяцев терапии ПЦО был достигнут у 42 (47 %) больных;
— БМО на момент начала терапии второй линии отсутствовал у 99 пациентов и был достигнут в ходе лечения у 43 (43 %) из них, медиана продолжительности приема ИТК второй линии до достижения БМО составила 6,7 месяцев.
Для оценки влияния скорости переключения на вторую линию терапии ИТК пациенты были разделены на следующие группы по продолжительности предшествующего лечения иматинибом: 24 месяцев и менее (≤24) — 59 пациентов и более 24 месяцев терапии (>24) — 57 человек. Результаты оценки эффективности в выделенных группах пациентов представлены в таблице 1 .
Таблица 1
Эффективность терапии второй линии терапии ИТК в группах пациентов в зависимости от продолжительности предшествующей терапии иматинибом
|
Группа пациентов |
ПЦО в общей группе, % |
Достижение ПЦО при его отсутствии перед началом терапии, % |
Медиана продолжительности терапии до достижения ПЦО, мес. |
БМО в общей группе, % |
Достижение БМО при его отсутствии перед началом терапии, % |
Медиана продолжительности терапии до достижения БМО, мес. |
|
≤24 месяцев |
66 % |
63 % |
3,7 |
51 % |
48 % |
6,5 |
|
>24 месяцев |
65 % |
50 % |
4,9 |
49 % |
39 % |
8,8 |
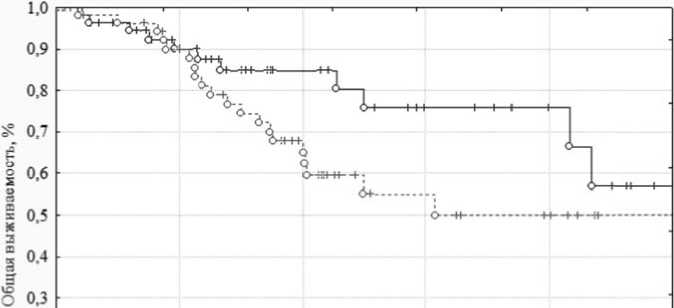
Значительных различий по частоте и по скорости достижения ПЦО и БМО между группами получено не было,однако при анализе ОВ наблюдалась статистическая тенденция (p = 0,1) значимости различий,при этом медиана ОВ для группы с ранним переключением (менее 24 месяцев предшествующей терапии иматини-бом) была не достигнута при сроке наблюдения 11,9 лет, тогда как при позднем переключении медиана ОВ составила 5,3 года ( рисунок 3 ). Медиана ОВ в общей группе больных была 8,7 лет с момента начала второй линии лечения ИТК, при этом 5-летняя ОВ составила 64 %.
Прогрессирование в ФА/БК произошло у 11 % пациентов,при этом в группе с ранним переключением частота составила только 3,6 %, тогда как в группе с поздним переключением 18,4 %, различия были статистически значимы (p = 0,036), 5-летняя БПВ для группы с ранним переключением составила 93 %, тогда как для группы позднего переключения только 75%, рисунок 4 . Полученные результаты соответствуют данным многоцентровых исследований нилотиниба и дазатиниба во второй линии терапии ХМЛ [13, 14].
о умерли + живы
менее 24 месяцев предшествующей терагош иматинибом более 24 месяцев предшествующей терапии иматинибом
О 2 4 6 8 10
Время от начала терапии второй линии, лет
Рисунок 3. Общая выживаемость больных хроническим миелолейкозом при второй линии терапии ИТК в зависимости от продолжительности предшествующей терапии иматинибом.
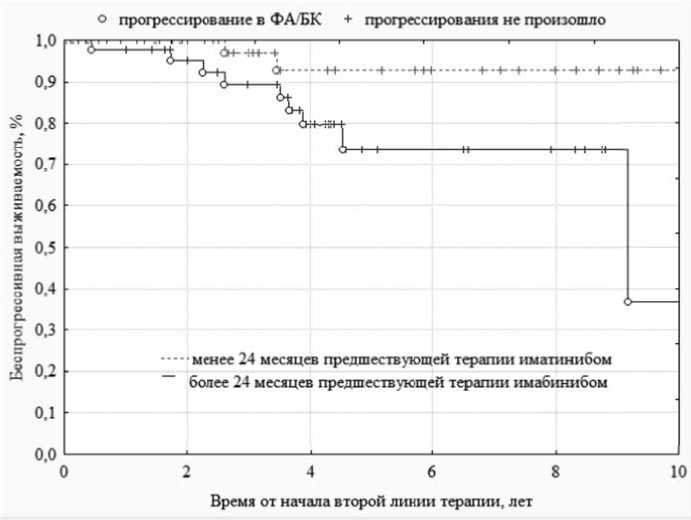
Рисунок 4. Беспрогрессивная выживаемость больных хроническим миелолейкозом при второй линии терапии ИТК в зависимости от продолжительности предшествующей терапии иматинибом.
Терапия ИТК третьей линии была назначена 47 (41 %) пациентам из 116, получавших вторую линию.Смена терапии была проведена у 26 (22 %) пациентов в связи с резистентностью и у 21 (18 %) пациентов по причине непереносимости. Медиана продолжительности терапии второй линии перед сменой составила 14,4 месяцев (0,1–67,5 месяцев).
В рамках третьей линии терапии дазатиниб был назначен 34 (72 %) пациентам, нилотиниб получали 5 (11 %) пациентов, в оставшихся случаях использовался бозутиниб — 3 (6 %) и понатиниб — 3 (6 %). Целевых уровней ответа при терапии третьей линии достигли следующие категории:
-
— ПГО на момент начала терапии третьей линии отсутствовал у 10 пациентов, у 8 (80 %) из них он был достигнут в ходе терапии, медиана времени достижения составила 1,2 месяца, в течение первых 3 месяцев ПГО был достигнут у 7 из 8 пациентов;
-
— ПЦО на момент начала терапии третьей линии отсутствовал у 31 больного, в ходе терапии ПЦО достигли 13 (42 %) из них, медиана продолжительности терапии до достижения ПЦО составила 6,9 месяцев, при этом в течение первых 12 месяцев терапии ПЦО был достигнут у 8 (26 %) больных;
-
— БМО перед началом третьей линии терапии отсутствовал у 36 больных, в ходе
лечения был достигнут у 9 (25 %) пациентов, медиана продолжительности приема ИТК в третьей линии терапии до достижения БМО составила 8,6 месяцев.
Для оценки влияния длительности предшествующего лечения на эффективность третьей линии терапии ИТК пациенты были разделены на следующие группы по продолжительности предшествующего лечения ИТК первой и второй линии: 48 месяцев и менее (≤48) — 29 пациентов и более 48 месяцев терапии (>48) — 18 человек. Результаты оценки эффективности в выделенных группах пациентов представлены в таблице 2 .
Таблица 2
Эффективность терапии третьей линии терапии ИТК в группах пациентов в зависимости от продолжительности предшествующей терапии первой и второй линии
|
Группа пациентов |
ПЦО в общей группе, % |
Достижение ПЦО при его отсутствии перед началом терапии, % |
Медиана продолжительности терапии до достижения ПЦО, мес. |
БМО в общей группе, % |
Достижение БМО при его отсутствии перед началом терапии, % |
Медиана продолжительности терапии до достижения БМО, мес. |
|
≤48 месяцев |
69% |
50% |
2,9 |
41% |
27% |
6,2 |
|
>48 месяцев |
50% |
33% |
14,0 |
28% |
21% |
8,6 |
Частота и скорость достижения ПЦО и БМО в группе с большей длительностью предшествующей терапии были ниже.При анализе ОВ различия между группами находились на пороге (p = 0,6) статистической значимости различий, при этом медиана ОВ для группы с ранним переключением (менее 48 месяцев предшествующей терапии первой и второй линии)была не достигнута при сроке наблюдения 9,3 лет, тогда как при позднем переключении медиана ОВ составила 3,1 года ( рисунок 5 ). Медиана ОВ в общей группе больных была 4,1 года с момента начала третьей линии терапии ИТК, при этом
5-летняя ОВ составила 49 %. Прогрессирование в ФА/БК произошло у 6 (15 %) пациентов, при этом в группе с меньшим сроком предшествующей терапии (≤ 48) частота прогрессирования составила только 8 % (n = 2), тогда как в группе с большей предлеченностью (> 48) — 31 % (n = 4), различия были статистически значимы (p = 0,03), 5-летняя БПВ для группы с меньшим сроком предшествующей терапии (≤ 48) составила 95 %, тогда как для группы с большей предлеченностью (>48) только 50 %, рисунок 6 .
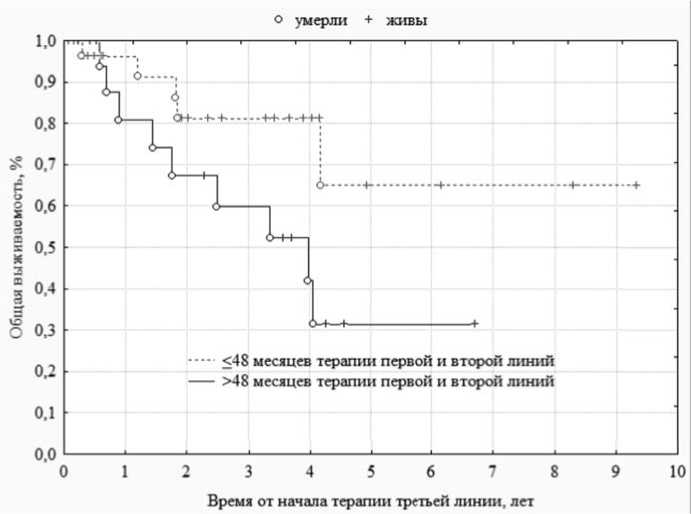
Рисунок 5. Общая выживаемость больных хроническим миелолейкозом при третьей линии терапии ИТК в зависимости от продолжительности предшествующей терапии первой и второй линий.
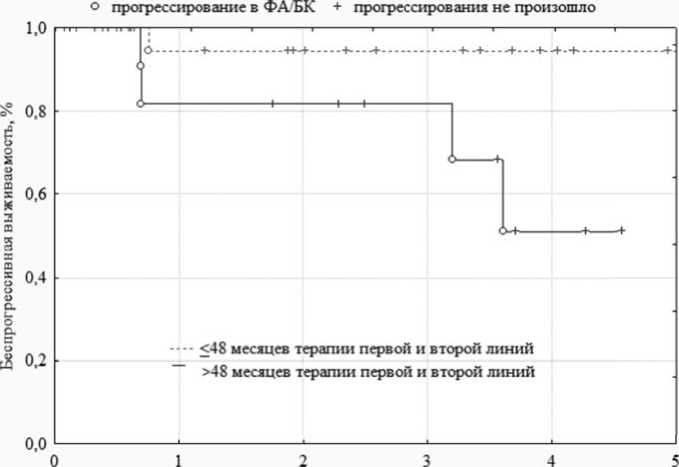
Время от начала третьей линии терапии, лет
Рисунок 6. Беспрогрессивная выживаемость больных хроническим миелолейкозом при третьей линии терапии ИТК в зависимости от продолжительности предшествующей терапии первой и второй линий.
Выводы. Несмотря на то,что этиология ХМЛ до настоящего времени не выяснена патогенез заболевания достаточно хорошо расшифрован,что позволило создать высокоточный метод лечения заболевания,избира-тельно воздействующий на опухолевый клон. Внедрение нового класса препаратов — тар- 28
гетной терапии,направленных на устранение молекулярно-генетических основ патогенеза, коренным образом изменило прогноз,превра-тив ХМЛ из фатальной опухоли крови в хроническое заболевание, не ограничивающее продолжительность жизни у большинства больных.
Исходя из собственного опыта таргетной терапии можно заключить,что лечение больных хроническим миелолейкозом ингибиторами тирозинкиназ может приводить к успешному подавлению опухоли и предотвращению прогрессирования у большинства пациентов. При неэффективности или непереносимости иматиниба терапия ингибиторами тирозинки-наз второй и даже третьей линии может быть эффективной у значительной части больных. Одним из важнейших факторов предотвраще- ния развития устойчивости опухоли является раннее переключение на следующие линии лечения при наличии признаков резистентности и/или непереносимости.
Благодаря стремительным прорывным успехам в области фундаментальной и прикладной гематологии хронический миелолейкоз в настоящее время превращается из тяжелого, фатального опухолевого заболевания в обратимый, хорошо поддающийся правильному терапевтическому воздействию процесс.
Список литературы Прогноз выживаемости и результаты таргетной терапии хронического миелолейкоза
- Абдулкадыров К. М., Бессмельцев С. С., Рукавицын О. А. Хронический миелолейкоз.— СПб.: СпецЛит., 1998.— 464 с.
- Абдулкадыров К. М., Шуваев В. А., Мартынкевич И. С. Миелопролиферативные новообразования — М.: Littera, 2016.— 304 с.
- The chronic myelogenous leukemia-specific P210 protein is the product of the bcr/abl hybrid gene / D. G. Ben-Neriah, A. M. Mes-Masson, O. N. Witte et al. // Science.— 1986.— Vol. 233, № 4760.— P. 212-214.
- Leukocyte interferon-induced myeloid cytoreduction in chronic myelogenous leukemia / M. Talpaz, K. B. McCredie, G. M. Mavligit et al. // Blood.— 1983.— Vol. 62, № 3.— P. 689-692.
- Effects of a selective inhibitor of the Abl tyrosine kinase on the growth of Bcr-Abl positive cells / B. J. Druker, S. Tamura, E. Buchdunger et al. // Nat Med.— 1996.— Vol. 2, № 5.— P. 561-566.
- Long Term Follow up of Patients with CML in Chronic Phase Treated with First-Line Imatinib Suggests That Earlier Achievement of a Major Molecular Response Leads to Greater Stability of Response / S. Branford, R. Lawrence, A. Grigg et al. // Blood.— 2008.— Vol. 112, № 11.— P. 2113.
- Клинические рекомендации по диагностике и лечению хронического миелолейкоза / А. Г. Туркина, А. Ю. Зарицкий, В. А. Шуваев и др. // Клиническая онкогематология. Фундаментальные исследования и клиническая практика.— 2017.— Т. 10, № 3.— С. 4294-316.
- Иматиниб (Imatinib): инструкция, применение и формула. Регистр лекарственных средств россии.— 2014.— [Электронный ресурс]. Дата обновления 18.05.2014 г.— URL: www. rlsnet. ru/mnn_index_id_3041. htm (дата обращения 15.04.2015 г.).
- Drug evaluation: Nilotinib — a novel Bcr-Abl tyrosine kinase inhibitor for the treatment of chronic myelocytic leukemia and beyond / E. Jabbour, J. Cortes, F. Giles et al. // IDrugs.— 2007.— Vol. 10, №7.— P. 468-479.
- Activity of Bosutinib, Dasatinib, and Nilotinib Against 18 Imatinib-Resistant BCR/ABL Mutants / S. Redaelli, R. Piazza, R. Rostagno et al. // Journal of Clinical Oncology.— 2009.— Vol. 27, № 3.— P. 469-471.
- Тасигна® (Tasigna). Инструкция по применению, противопоказания, состав и цена. Регистр лекарственных средств россии.— 2014.— [Электронный ресурс].— URL: www. rlsnet. ru/ tn_index_id_39736. htm (дата обращения 15.04.2015 г.).
- Спрайсел® (Sprycel®) Инструкция по применению, противопоказания, состав и цена. Регистр лекарственных средств россии.— 2015.— [Электронный ресурс].— URL: http://www. rlsnet. ru/tn_index_id_38851. htm#pokazaniya-preparata-sprajsel® (дата обращения 01.01.2015 г.).
- Expanding Nilotinib Access in Clinical Trials (ENACT) / F. E. Nicolini, A. Turkina, Z.-X. Shen et al. // Cancer.— 2012.— Vol. 118, № 1.— P. 118-126.
- Long-term outcome with dasatinib after imatinib failure in chronic-phase chronic myeloid leukemia: follow-up of a phase 3 study / N. P. Shah, F. Guilhot, J. Cortes et al. // Blood.— 2014.— Vol. 123, №15.— P. 2317-2324.


