Прогнозирование появления высокотрансмиссивных штаммов вируса Sars-Cov-2 на территории Санкт-Петербурга с использованием рекуррентной нейронной сети
Автор: Кустова Д.В., Кириенко А.Н., Мартынкевич И.С.
Журнал: Вестник гематологии @bulletin-of-hematology
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.18, 2022 года.
Бесплатный доступ
В 2020 году Всемирная организация здравоохранения (ВОЗ) объявила тяжелый острый респираторный синдром, вызванный вирусом SARS-CoV-2, пандемией. Трансмиссивность SARS-CoV-2 связывают с аффинностью связывания спайкового S-белка вируса с рецептором ангиотензинпревращающего фермента 2 (АПФ2), что является ключевым событием при проникновении вируса в клетку. Не случайно большинство вакцин нацелено на блокирование S-белка для невозможности связывания с АПФ2. Предсказание возникновения штаммов с мутациями, приводящих к повышению аффинности комплекса S-белок/ АПФ2, является важной задачей для предотвращения новых вспышек эпидемии и быстрого реагирования на появление высококонтагиозных штаммов. Предсказание появления высоко-трансмиссивных штаммов является важной медико-биологической задачей, в том числе и онкогематологии, поскольку именно пациенты с иммунодефицитом и находящиеся на иммуносупрессивной терапии подвержены наибольшему риску заражения и тяжелого течения COVID-19. В нашей статье был проведен анализ вариабельности аминокислотных последовательностей S-белка SARS-CoV-2, полученных из клинических образцов на территории Санкт-Петербурга с 15 марта 2020 года по 16 июня 2021 года. На основе проанализированных последовательностей с помощью рекуррентной нейронной сети было предсказано появление новых мутаций в рецептор-связывающем мотиве и проведена оценка их влияния на связывание с АПФ2 рецептором. Было предсказано появление мутаций в позициях L455, R457, N481, T500 и G504 и показано, что данные мутации усиливают аффинность связывания с АПФ2 увеличивая трансмиссивность.
Sars-cov-2, s-белок, ангиотензинпревращающий фермент 2, мутации, молекулярный докинг, нейронные сети
Короткий адрес: https://sciup.org/170194034
IDR: 170194034
Prediction of the highly transmissible strains of Sars-Cov-2 virus appearance on the territory of Saint- Petersburg using a recurrent neural network
In 2020, the World Health Organization (WHO) declared severe acute respiratory syndrome, caused by the SARSCoV- 2 virus, a pandemic. The transmissivity of SARS-CoV-2 is associated with the binding affinity of the virus spike S-protein to the angiotensin converting enzyme receptor 2 (ACE2), which is a key event in the penetration of the virus into the cell. It is no coincidence that most vaccines are aimed at blocking binding the S-protein to ACE2. Predicting the occurrence of strains with mutations leading to an increase of the S-protein/ACE2 complex affinity is an important task for preventing new outbreaks of the epidemic and responding quickly to the appearance of highly contagious strains. Predicting the appearance of highly transmissive strains is an important biomedical task, including hematology, since it is patients with immunodeficiency and those on immunosuppressive therapy who are at the greatest risk of infection and severe COVID-19. In our article, the variability of amino acid sequences of SARS-CoV-2 S-protein obtained from clinical samples in St. Petersburg from March 15, 2020 to June 16, 2021 was analyzed. Based on the analyzed sequences, the emergence of new mutations in the receptor-binding motif was predicted using a recurrent neural network model and their effect on binding to the ACE2 receptor was evaluated. The appearance of mutations in positions L455, R457, N481, T500 and G504 was predicted and it was shown that these mutations enhance the affinity of binding to ACE2 by increasing transmissivity.
Текст научной статьи Прогнозирование появления высокотрансмиссивных штаммов вируса Sars-Cov-2 на территории Санкт-Петербурга с использованием рекуррентной нейронной сети
Введение. Первые случаи нового заболевания, приводящего к развитию тяжёлого острого респираторного синдрома, были зарегистрированы в конце 2019 года в китайском городе Ухань. Вскоре стало известно, что болезнь вызвана новым одноцепочечным РНК(+)-вирусом SARS-CoV-2, относящимся к семейству β-коронавирусов. В настоящее время болезнь, получившая название COVID-19 (аббревиатура от англ. COronaVIrus Disease 2019 — коронавирусная инфекция 2019 года), распространилась по всему миру и приняла характер пандемии [1,2].
Проникновение вирусных частиц внутрь клетки-хозяина происходит за счет связывания гликозилированных S-белков, которые находятся на поверхности вируса, с рецептором ангио-тензинпревращающего фермента 2 (АПФ2). Внутри клетки происходит репликация вирусной РНК, синтез структурных белков и сборка вирусных частиц, после чего упакованные вирусные частицы высвобождаются через лизосомы [3,4].
Вирус SARS-CoV-2 вызывает развитие респираторной инфекции, оказывающей также значительное влияние на систему кроветворения и гемостаз. Среди наиболее распространенных гематологических изменений отмечают лимфопению, нейтрофилию, эозинопению, тромбоцитопению и тромбоцитоз [5]. Кроме того, у пациентов с тяжелым течением заболевания отмечалось аномальное присутствие предшественников эритроцитов в периферической крови [6,7].
Значительным открытием стало обнаружение рецептора АПФ2 на поверхности гемопоэтических стволовых клеток и клеток-предшественников [8,9]. Важной особенностью является тот факт, что клетки-предшественники эритроцитов - ERP-S2 (CD71+ CD235A-) и ERP-S3 (CD71+ CD235a+) способны инфицироваться SARS-CoV-2, который успешно амплифици-ровал свой геном внутри этих клеток [9]. Именно связывание S-белка с рецептором АПФ2 является ключевым этапом инфицирования. При изучении этого процесса было показано, что S-белок, находящийся на поверхности вириона в тримерном состоянии, связывается с АПФ2 и расщепляется на субъединицы S1 и S2 [10–12]. Субъединица S1 содержит домен связыва- ния рецептора (RBD, 319-541 а.к.), который непосредственно связывается с доменом пептидазы (PD) рецептора АПФ2, в то время как S2 отвечает за слияние мембран. В структуре RBD особо выделяют рецептор-связывающий мотив RBM (437-508 а.к.) – участок, содержащий большинство контактирующих аминокислотных остатков S-белка, которые связываются с АПФ2 рецептором. В составе S1 субъединицы важным является также N-терминальный домен (NTD), который хоть и является менее иммуногенным, чем RBD, однако, недавние исследования показали способность анти-NTD антител нейтрализовать SARS-CoV-2 [12,13].
Важно отметить, что RBD является наиболее изменчивым у родов Coronavirinae и рассматривается как ответственный за вирусную трансмиссивность и адаптацию [1,14]. Шесть аминокислот SARS-CoV-2 являются критическими для связывания с АПФ2 рецептором и определения видоспецифичности – L455, F486, Q493, S494, N501 и Y505. Интересным является тот факт, что 5 из шести данных аминокислот не соответствуют вирусу SARS-CoV, который также проникает в клетки за счет связывания с АПФ2 рецептором [15]. Кроме того, для SARS-CoV-2 были получены доказательства существования положительного отбора, направленного на закрепление определенных мутаций в S-гене [16]. Поэтому, совершенно неудивительно, что внимание многих ученых направлено на изучение механизмов формирования комплекса S-белок - АПФ2, отслеживание мутаций, появляющихся в S гене, создание лекарств и вакцин, блокирующих именно S-белок SARS-CoV-2 [17–19].
В решении таких задач большую роль играют методы математической биологии. Так, компьютерное моделирование белков нашло широкое применение при анализе формирования комплекса S-белок – АПФ2-рецептор [10,20–23]. Моделирование позволяет оценить влияние мутаций в S-белке на связывание с АПФ2 рецептором, что определяет патогенность и вирулентность новых штаммов [24]. Неслучайно, наиболее быстрое распространение в популяции имеют штаммы, мутации в которых повышают связывающую способность S-белка с АПФ2 рецептором [25,26].
Эпидемиологические и биохимические исследования показывают, что трансмиссивность различных штаммов SARS-CoV-2 пропорциональна аффинности связывания [11,27]. Следовательно, трансмиссовность SARS-CoV-2 может быть теоретически оценена по аффинности связывания RBM-АПФ2. Соответственно, следует отслеживать появление мутаций, повышающих аффинность данного комплекса, поскольку именно таким мутациям благоприятствует естественный отбор [28].
Алгоритмы машинного обучения активно используются в вычислительной биологии и биоинформатике для прогнозирования мутаций. Например, нейронные сети успешно применяются для прогнозирования мутаций в вирусах гриппа [29], точечных мутаций, возникающих при выравнивании последовательностей РНК [30] и мутаций в определенных сайтах [31]. Несмотря на разнообразие алгоритмов, возникает проблема с динамическим моделированием последовательных данных. Так, появление рекуррентных нейронных сетей (RNN) c долговременной и кратковременной памятью (LSTM) нашло применение для решения проблемы управления нелинейной динамикой в исследованиях временных рядов [32]. Было показано, что модели, основанные на RNN превосходят модели на основе логистической регрессии (LR) и методе опорных векторов (SVM) [33]. Это связано с тем, что модели на основе RNN в отличие от LR и SVM могут использовать свою внутреннюю память для обработки последовательностей произвольной длины. Модель на основе RNN-LSTM использовалась для предсказания возникновения мутаций в геномной последовательности SARS-CoV-2 и показала увеличение количества замен C>T в будущем времени [34], а также легла в основу конвейера «Tempel», предсказывающего вероятность появления мутаций вируса гриппа в следующем сезоне, опираясь на временные данные о последовательностях гемагглютинина [33].
Помимо выбора модели и обучающего алгоритма необхо- димо правильно представить входные данные. Применение нейронных сетей к численно преобразованным последовательностям аминокислот или нуклеиновых кислот демонстрирует неоднозначные результаты [30]. Поэтому одним из решений проблемы подготовки входных данных является применение методов обработки естественного языка (NLP) [33,35,36]. NLP позволяет представить аминокислотную последовательность в виде многомерных векторов. В частности, ProtVec преобразует аминокислотную последовательность в виде перекрывающихся «биологических» слов, состоящих из 3 аминокислот, представленных в векторе 1*100 [32]. Предсказание возникновения новых штаммов с новыми свойствами, в частности, повышенной трансмиссивностью за счет более эффективного связывания вирусных частиц с рецепторами на поверхности клеток, позволяет заранее решить ряд эпидемиологических задач в период пандемии – оценить эффективность уже существующих вакцин против возможных штаммов, дает время на создание новых вакцин и на подготовку системы здравоохранения к новым «волнам» эпидемии. Разработка механизмов оценки появления новых трансмиссивных штаммов найдет свое значение и в фундаментальной науке, позволив, например, объяснить влияние SARS-CoV-2 на гематологический статус пациента. Именно поэтому целью нашей работы стало предсказание возникновения мутантных штаммов с повышенной трансмиссивностью SARS-CoV-2 на территории Санкт-Петербурга. Для этого нами была изучена вариабельность S-белка у штаммов SARS-CoV-2, выделенных на территории Санкт-Петербурга с 15 марта 2020 года по 16 июня 2021 года. На основе проанализированных последовательностей методами машинного обучения нами было предсказано появление новых мутаций и проведена оценка их влияния на связывание S-белка с АПФ2 рецептором, т.е. транс-миссивность штаммов.
Материалы и методы. Для проведения анализа использовались данные, представленные на сайте GISAID (https://www. [37]. В анализ брали аминокислотные последовательности S-белка SARS-CoV-2, полученные из образцов клинического материала в период с середины марта 2020 года по середину июня 2021 года. По состоянию на 16 июня 2021 года в этой базе содержалось 852 полных последовательности S-белка SARS-CoV-2, полученных на территории Санкт-Петербурга. В качестве референсной последовательности использовали Wuhan-Hu-1 (EPI_ISL_402124) [38].
Филогенетический анализ проводили с использованием пакета BioPython [39] для Python и свободного программного обеспечения UGENE v.39.0 ru/) [40]. Множественное выравнивание последовательностей проводили c помощью алгоритма MUSCLE [41]. Для построения филогенетического дерева использовали метод максимального правдоподобия (ML).
Для предсказания мутаций использовали конвейер, основанный RNN, представленный в работах Rui Yin, а также Shashata Sawmya с соавторами [31,33].
Для предварительной подготовки входных данных следовали протоколу, представленному в работе Rui Yin [33]. Выровненные последовательности были разделены на три волны заболеваемости в соответствии с данными Роспотребнадзора. Первая волна – с марта 2020 по сентябрь 2020, вторая волна – с октября 2020 по март 2021 и третья волна – с апреля 2021 по июнь 2021. Входные данные представлены в виде 1254*100-мерного векторного пространства на основе ProtVec [36]. Прогнозирование мутаций проводили на фрагменте RBM мотива (437-507 а.к.).
Для прогнозирования мутировавшей аминокислоты в предсказанной позиции использовали таблицу вероятности мутаций аминокислот, представленную в работе Shaomin Yan и Guang Wu [42].
Для моделирования по гомологии фрагмента S-белка SARS-CoV-2 (331-524 а.к.), содержащей предсказанные мутации в RBM мотиве, использовали сервер SWISS-MODEL (https://swissmodel. [43–47]. В качестве шаблона использовали структуру S-белка SARS-CoV-2 (7ddn) из базы данных PDB (http://www.
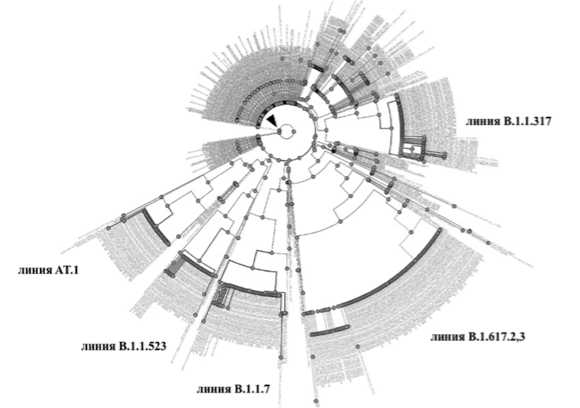
Рис. 1. Филогенетическое дерево вариантов S-белка, распространенных на территории Санкт-Петербурга. Стрелкой отмечена референсная последовательность S-белка Wuhan-Hu-1 (EPI_ISL_402124).
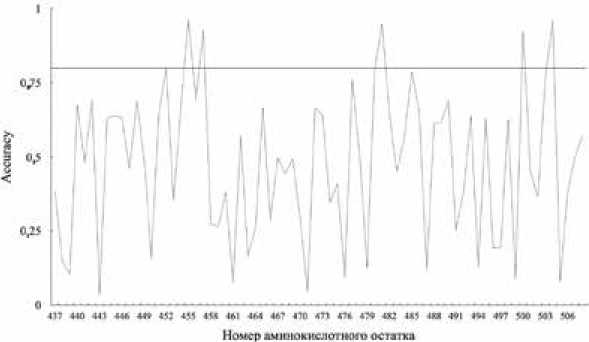
Рис. 2. Точность прогноза мутаций аминокислотных остатков. Черная линия обозначает базовую линию.
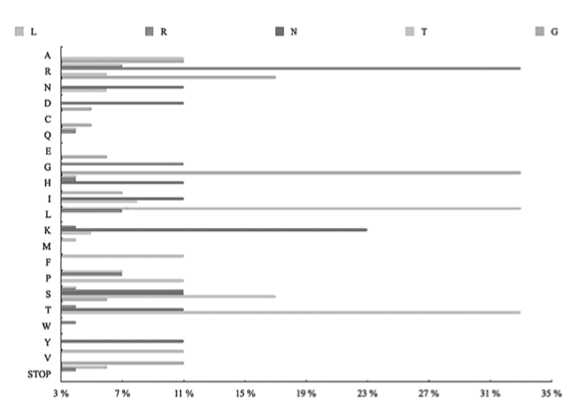
Рис. 3. Прогноз потенциальных мутаций аминокислот по позициям L455,
R457, N481, T500, G504 на основе вероятности трансляции между кодо-
нами РНК и мутированными аминокислотами. Аланин; R, Аргинин; N, Аспарагин; D, Аспарагиновая кислота; V, Валин; H, Гистидин; G, Глицин; Q, Глутамин; E, Глутаминовая кислота; I, Изолейцин; L, Лейцин; K, Лизин; M, Метионин; P, Пролин; S, Серин; Y, Тирозин; T, Треонин; W, Триптофан; F, Фенилаланин; C, Цистеин; STOP, стоп-кодон
Для моделирования взаимодействия между фрагментами, содержащими предсказанные мутации в RBM мотиве S-белка (331-524 а.к.) и АПФ2 рецептором (6M17) использовался сервер ClusPro [49–52]. Скоринг функция для отбора наиболее правдоподобных моделей:
E=0,4E_rep+(-0,4E_att )+600E_elec+1,00E_DARS, где E_rep и E_att- вклады в межмолекулярные силы Ван-дер-ваальса, E_elec-электростатическая энергия, E_DARS-потенциал, основанный на парной структуре [49–52].
Для прогнозирования аффинности в белок-белковых комплексах использовали сервер PRODIGY [53,54]. Полученные данные визуализировали с помощью программы PyMol [55].
Результаты. Анализ множественного выравнивания последовательностей, показал, что NTD область (139-168 а.к.) и RBD домен (319-541 а.к.) являются наиболее вариабельными. Филогенетический анализ вариантов S-белка показал, что на территории Санкт-Петербурга преобладают линии AT.1, B.1.1.523, B.1.1.7, B.1.617.2,3, B.1.1.317 (Рисунок 1). Далее работу вели только с фрагментом RBD домена (331–524 а.к.), поскольку именно он является ключевым в связывании S-белка с АПФ2 рецептором [12,13].
Конвейер, основанный на рекуррентной нейронной сети, предсказал 5 ключевых аминокислот, в которых может произойти мутация в ходе эволюции. Лейцин (L) в 455 положении, аргинин (R) в 457, аспарагин (N) в 481, треонин (T) в 500 и глицин (G) в 504. Результат точности (Accuracy) прогнозирования мутаций аминокислотных остатков представлен на рисунке 2. На рисунке 3 показана вероятность мутации аминокислот в предсказанных положениях в другую аминокислоту.
Для дальнейшего анализа были выбраны преобладающие замены: L455F, L455V, R457G, R457S, N481K, T500S, G504R.
С помощью сервера SWISS-MODEL были получены третичные структуры фрагментов (331–524 а.к.) S-белка SARS-CoV-2 линии B.1.617.2 и SARS-CoV-2 линии B.1.617.2 с внесенной мутацией в 455 положении, а также, референсного S-белка SARS-CoV-2 с мутациями в положении 455, 457, 481, 500, 504. С помощью сервера ClusPro было проведено молекулярное моделирование взаимодействия полученных фрагментов с АПФ2 рецептором. Визуализация моделей взаимодействия фрагментов S-белка линии B.1.617.2 и референсного S-белка SARS-CoV-2 с мутацией в ключевой аминокислоте L455 с АПФ2 рецептором представлена на рисунке 4.
Для всех построенных моделей была проведена оценка энергии и аффинности связывания. Средняя и низшая энергия связывания фрагментов (331–524 а.к.) S-белка SARS-CoV-2 с АПФ2 рецептором, полученная с помощью сервера ClusPro, представлена на рисунке 5А. Предсказание аффинности связывания моделей белок-белкового комплекса представлено на рисунке 5Б.
Обсуждение. Анализ геномных изменений вирусов, в частности SARS-CoV-2, является одним из ключевых этапов реагирования и борьбы с распространением заболеваний. Секвенирование решает широкий спектр задач, направленных на идентификацию и характеризацию вируса (в частности, разработку диагностических тест-систем), изучение передачи и географического распространения и оценку эволюции вируса (WHO). Совместно с методами компьютерного моделирования секвенирование позволяет оценить влияние мутаций на трансмиссивность. Подключение к таким исследованиям машинного обучения даёт возможность предсказать появление новых опасных мутаций, что позволяет заранее принимать меры для предотвращения распространения новых штаммов и дает время на разработку новых лекарств и вакцин, что особенно актуально для пациентов с злокачественными опухолями системы крови, характеризующихся иммунодефицитом и находящихся на иммуносупрессивной терапии.
В нашей работе мы провели филогенетический анализ аминокислотных последовательностей штаммов, выделенных в Петербурге с марта 2020 по июнь 2021 гг., и оценили их генетическое разнообразие, обращая особое внимание на линии, которые имеют мутации в S-гене. Штаммы с мутациями в S гене, которые приводят к замене аминокислот в RBD домене и усиливают связывание с АПФ2, привлекают особое внимание из-за высокой скорости распространения, такие штаммы ВОЗ обозначает как «вызывающие опасения».
Так, среди линий, выявленных в Санкт-Петербурге с марта 2020 по июнь 2021, долю в 14,41% занимает линия B.1.1.317, имеющая мутации в S-белке Q675R, D138Y, S477N, A845S (Рисунок 1). Данная линия была впервые выявлена в марте 2020 во Вьетнаме и характеризуется, кроме того, мутацией в нуклеокап-сиде A211V. Варианты с такой мутацией мало распространились в мире, однако в России в феврале – марте 2020 года занимали 26,9% [56]. Данный набор мутаций обеспечивает штамму эффективное связывание с АПФ2 рецептором и ускользание от иммунного ответа [56].
Линия B.1.1.523, имеющая долю в 4,28% в Санкт-Петербурге (Рисунок 1), несет в себе мутацию E484K, характерную и для других штаммов, например, B.1.351 (Южная Африка) и B.1.1.28 (Бразилия) и вызывает особый интерес, поскольку способна снижать нейтрализацию антителами [57]. Штаммы с мутацией E484K, которая влияет на формирование комплекса с АПФ2, быстро вытеснили другие варианты вируса и распространились на другие страны [58]. Варианты SARS-CoV-2. Новости о вспышках болезней 31 декабря 2020 г. – ВОЗ; Nelson et al., 2021) [59].
Важно отметить значительную долю (5,64%) линии АТ-1 (B.1.1.370.1) [60] в анализируемых нами последовательностях (Рисунок 1). Данная линия впервые была выявлена в Северо-Западном федеральном округе и характеризуется вставкой N679delinsKGIAL и делецией по позициям C136_Y144del, находящимися в S-белке. Данные мутации могут оказывать влияние на эффективность разрезания S-белка фурином и на эффективность проникновения вируса в клетку [61]. Данный штамм распространился не только на Северо-Западе России, но и в таких странах как Финляндия, Германия, Британия .
На июнь 2021 года 22,87% секвенированных штаммов относятся к линии B.1.617 (Рисунок 1). Филогенетический анализ показывает наличие в Санкт-Петербурге линий B.1.617.2 и B.1.617.3. Данные линии были выделены в октябре-феврале 2020-2021 гг в Индии и несут важные замены в RBD домене – L452R и T478K. Линия B.1.617.2 характеризуется большей трансмиссивностью, а антитела и сыворотки вакцинированных людей хоть и способны нейтрализовывать данный штамм, но с гораздо более низкой эффективностью [62–64]. Большая доля данных штаммов от всех секвенированных образцов связана, как с доминированием данного штамма в мире на июнь 2021, так и с увеличением количества секвенируемых образцов в Санкт-Петербурге.
При сравнении филогенетических данных штаммов из Санкт-Петербурга с данными, полученными в других регионах, выявляется ряд общих черт распространения SARS-Cov-2 в России. Так, ни в одном регионе не был выявлен исходный штамм Wuhan-Hu-1, подавляющее большинство штаммов, циркулировавших на ранних этапах пандемии, относились к линиям B.1, B.1.1 и B.1.* (кладам G, GR, и GH), также обнаруживаются штаммы с мутациями, с которым ряд исследователей связывают уклонение от иммунного ответа (Водопьянов и др., 2020, Осина и др., 2020) [65]. Особенность филогении SARS-CoV-2 в Санкт-Петербурге является появление штамма AT-1, получившего название «северо-западный» [61].
Аминокислотные последовательности S-белка штаммов, получивших распространение на территории Санкт-Петербурга, использовались как входные данные для нейронной сети. В нашей работе мы показали возможное появление мутаций в позициях – L455, R457, N481, T500 и G504. В дальнейший анализ брали варианты S-белка с аминокислотными заменами, имеющими наибольшую вероятность (Рисунок 3) – L455F, L455V, R457S, R457G, N481K, T500S, G504R.
На основе предсказанных мутаций были построены модели взаимодействия фрагментов S-белка (331-524 а.к.) с измененными аминокислотами с АПФ2 (Рисунок 4). Оценку влияния
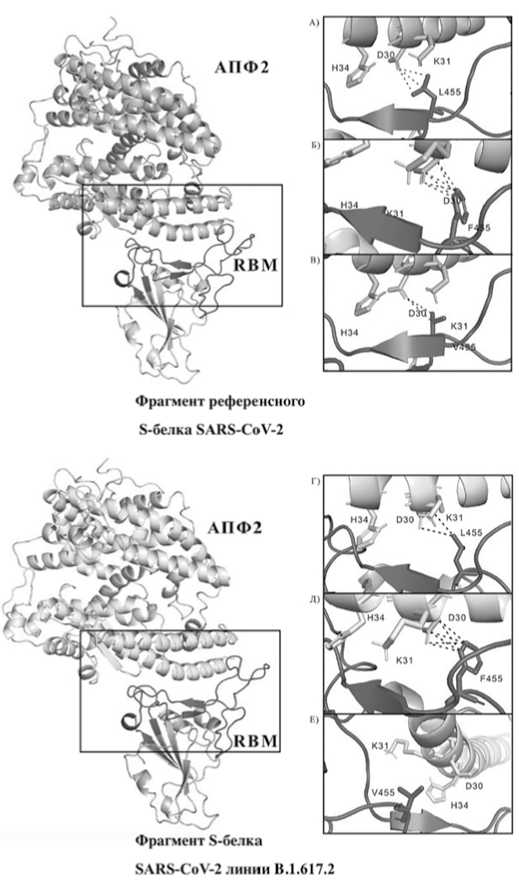
Рис 4. Визуализация моделей взаимодействия фрагмента S-белка SARS-CoV-2 линии B.1.617.2 и референсного S-белка SARS-CoV-2 c АПФ2 рецептором. Черным прямоугольником выделена область, в которой происходит взаимодействие с АПФ2. Пунктирные линии – длина связи меньше 4 Å. А) Фрагмент референсного S-белка SARS-CoV-2. Б) Фрагмент референсного S-белка SARS-CoV-2 с мутацией в L455F. В) Фрагмент референсного S-белка SARS-CoV-2 с мутацией в L455V. Г) Фрагмент S-белка SARS-CoV-2 линии B.1.617.2. Д) Фрагмент S-белка SARS-CoV-2 линии B.1.617.2 с мутацией в L455F. Е) Фрагмент S-белка SARS-CoV-2 линии B.1.617.2 с мутацией в L455V.
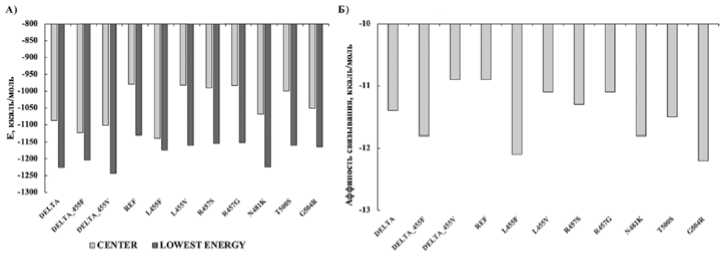
Рис. 5. А) Средняя и низшая энергия связывания фрагментов (331–524 а.к.) S-белка SARS-CoV-2 с АПФ2 рецептором. Б) Предсказанная аффинность моделей белок-белкового комплекса. DELTA - Фрагмент S-белка SARS-CoV-2 линии B.1.617.2, REF - Фрагмент S-белка SARS-CoV2 Wuhan-Hu-1.
таких мутаций проводили в сравнении с соответствующим участком S-белка исходного штамма Wuhan-Hu-1. Мы показали, что данные мутации увеличивают аффинность связывания, что свидетельствует о формировании более стабильных комплексов (Рисунок 5Б).
Мутация в позиции L455 представляет особый интерес, поскольку данная аминокислота напрямую взаимодействует с АПФ2 рецептором в позициях D30, K31 и H34 [10,66]. Наши данные говорят о возможности возникновения замен L455V и L455F, причем мутация L455F предпочтительнее исходя из значений энергии связывания (-11,1 ккал/моль-1 и -12,1 ккал/ моль-1 соответственно) (Рисунок 5A). Штаммы с заменой L455F уже были идентифицированы в США [28]. Такая замена хоть и встречается с низкой частотой на территории США, однако, имеет наиболее высокие абсолютные изменения свободной энергии связывания из изученных авторами [28]. Примечательно предположение о том, что замена Tyr442→Leu455 повысила способность SARS-CoV-2-RBD связываться с рецептором АПФ2 по сравнению с SARS-CoV-RBD [22].
Исходя из ключевой роли данной аминокислоты в формировании комплекса S-белок – АПФ2 и полученных нами данных о более стабильных комплексах с мутациями L455V и L455F, был проведен анализ вариантов S-белка штамма B.1.617.2 (22,87% от всех проанализированных нами последовательностей) с АПФ2 рецептором (Рисунок 4Г-4Е). Аффинность комплекса S-белок (B.1.617.2) – АПФ2 составляет –11,4 ккал/моль-1, с мутацией L455F –11,8 ккал/моль-1, с мутацией - L455V –10,9 ккал/ моль-1 , что говорит о том, что данные мутации не оказывают существенного влияния на формирование комплекса (Рисунок 5). Однако данные, полученные нами на основе прогнозирования мутаций, а также тот факт, что мутация L455F уже выявлялась в популяции, говорят о том, что вероятность появления новых штаммов с такой мутацией достаточно высока. Так, на- пример, штаммы с мутацией D614G появились независимо в разных странах и закрепились в популяции, заменив исходный штамм Wuhan-Hu-1[67].Таким образом, проанализировав вариабельность S-белка у штаммов, выявленных на территории Санкт-Петербурга в период с 15 марта 2020 г. по 16 июня 2021 г., мы определили возможные сайты возникновения мутаций, предсказали преобладающие аминокислотные замены в данных сайтах и показали, что все предсказанные нами мутации оказывают влияние на связывание RBD домена S-белка с АПФ2 рецептором, увеличивая аффинность связывания. Это свидетельствует о формировании более стабильных комплексов S-белок/АПФ2-рецептор, а значит такие штаммы могут обладать большей трансмиссивностью. Полученные нами данные, а также опыт использования нейронных сетей для предсказания высококонтагиозных штаммов позволит в следующих работах оценить появление таких штаммов у когорты онкогематологи-ческих больных.
Конфликты интересов
Источник финансирования
Вклад авторов
Концепция и дизайн: Кустова Д.В., Кириенко А.Н.
Сбор и обработка данных: Кустова Д.В., Кириенко А.Н.
Представление материалов исследования: Кустова Д.В., Кириенко А.Н.
Анализ и интерпретация: Кустова Д.В., Кириенко А.Н.
Подготовка рукописи: Кустова Д.В., Кириенко А.Н., Мартын-кевич И.С.
Окончательное одобрение рукописи: Мартынкевич И.С.
Список литературы Прогнозирование появления высокотрансмиссивных штаммов вируса Sars-Cov-2 на территории Санкт-Петербурга с использованием рекуррентной нейронной сети
- Zhou P., Yang X. Lou, Wang X.G., et al. A pneumonia outbreak associated with a new Coronavirus of probable bat origin // Nature.-2020.- Vol. 579, P.270-273.
- Huang Y., Yang C., Xu X., et al. Structural and functional properties of SARS-CoV-2 spike protein: potential antivirus drug development for COVID-19 // Acta Pharmacologica Sinica.-2020.- Vol. 41, No. 9.- P.1141-1149.
- Fehr A.R., Perlman S. Coronaviruses: An Overview of Their Replication and Pathogenesis // Coronaviruses: Methods and Protocols-2015.- Vol. 1282, No. 1.- P. 1-23.
- Ghosh S., Dellibovi-Ragheb T.A., Pak E., et al. ß-Coronaviruses use lysosomal organelles for cellular egress // Cell.-2020.- Vol. 183, No. 6.- P. 1520-1535.
- Leticia de Oliveira Toledo S., Sousa Nogueira L., das Graças Carvalho M., et al. COVID-19: Review and hematologic impact // Clinica Chimica Acta.-2020.- Vol. 510.- P. 170-176.
- Bernardes J.P., Mishra N., Tran F., et al. Longitudinal Multi-omics Analyses Identify Responses of Megakaryocytes, Erythroid Cells, and Plasmablasts as Hallmarks of Severe COVID-19 // Immunity.-2020.- Vol. 53, No. 6.- P.1296-1314.
- Shahbaz S., Xu L., Osman M., et al. Erythroid precursors and progenitors suppress adaptive immunity and get invaded by SARS-CoV-2 // Stem Cell Reports.-2021.- Vol. 16, No. 5.- P.1165-1181.
- Ropa J., Cooper S., Capitano M.L., et al. Human Hematopoietic Stem, Progenitor, and Immune Cells Respond Ex Vivo to SARS-CoV-2 Spike Protein // Stem Cell Reviews and Reports.-2021.- Vol. 17, No. 1.- P.253-265.
- Huerga Encabo H., Grey W., Garcia-Albornoz M., et al. Human Erythroid Progenitors Are Directly Infected by SARS-CoV-2: Implications for Emerging Erythropoiesis in Severe COVID-19 Patients // Stem Cell Reports.-2021.- Vol. 16, No. 3.- P.428-436.
- Lan J., Ge J., Yu J., et al. Structure of the SARS-CoV-2 spike receptor-binding domain bound to the ACE2 receptor // Nature.-2020.- Vol. 581.- P.215-220.
- Hoffmann M., Kleine-Weber H., Schroeder S., et al. SARS-CoV-2 Cell Entry Depends on ACE2 and TMPRSS2 and Is Blocked by a Clinically Proven Protease Inhibitor // Cell.-2020.- Vol. 181, No. 2.- P.271-280.
- Chi X., Yan R., Zhang J., et al. A neutralizing human antibody binds to the N-terminal domain of the Spike protein of SARS-CoV-2 // Science.-2020.- Vol. 369.- P. 650-655.
- Liu L., Wang P., Nair M.S., et al. Potent neutralizing antibodies against multiple epitopes on SARS-CoV-2 spike // Nature.-2020.- Vol. 584.- P.450-456.
- Wu F., Zhao S., Yu B., et al. A new coronavirus associated with human respiratory disease in China // Nature.-2020.- Vol. 579.- P.265-269.
- Wan Y., Shang J., Graham R., et al. Receptor Recognition by the Novel Coronavirus from Wuhan: an Analysis Based on Decade-Long Structural Studies of SARS Coronavirus // Journal of Virology.-2020.- Vol. 94, No. 7.
- Zhan X.Y., Zhang Y., Zhou X., et al. Molecular evolution of SARS-CoV-2 structural genes: Evidence of positive selection in spike glycoprotein // bioRxiv.-2020.- No. 628.- P.0-3.
- Komissarov A.B., Safina K.R., Garushyants S.K., et al. Genomic epidemiology of the early stages of the SARS-CoV-2 outbreak in Russia // Nature Communications.-2021.- Vol. 12, No. 1.- P.1-13.
- Li Q., Wu J., Nie J., et al. The Impact of Mutations in SARS-CoV-2 Spike on Viral Infectivity and Antigenicity // Cell.-2020.- Vol. 182, No. 5.- P.1284-1294.
- Min L., Sun Q. Antibodies and Vaccines Target RBD of SARS-CoV-2 // Frontiers in Molecular Biosciences.-2021.- Vol. 8.- P.1-9.
- Xiantian X., Ping C., Jingfang W., et al. Evolution of the novel coronavirus from the ongoing Wuhan outbreak and modeling of its spike protein for risk of human transmission // SCIENCE CHINA Life Sciences.-2020.- Vol. 63, No. 3.- P. 457-460.
- Wrapp D., Wang N., Corbett K.S., et al. Cryo-EM structure of the 2019-nCoV spike in the prefusion conformation // Science.-2020.- Vol. 367.- P.1260-1263.
- Renhong Y., Yuanyuan Z., Yaning L., et al. Structural basis for the recognition of SARS-CoV-2 by full-length human ACE2 // Science.-2020.- Vol. 367.- P.1444-1448.
- Zhou T., Tsybovsky Y., Gorman J., et al. Cryo-EM Structures of SARS-CoV-2 Spike without and with ACE2 Reveal a pH-Dependent Switch to Mediate Endosomal Positioning of Receptor-Binding Domains // Cell Host and Microbe.-2020.- Vol. 28, No. 6.- P.867-879.
- Arul Murugan N., Javali y P.S., Jeyaraj Pandian C., et al. Computational Investigation of Increased Virulence and Pathogenesis of SARS-CoV-2 Lineage B.1.1.7 // bioRxiv.-2021.-Vol. 449.
- Khateeb J., Li Y., Zhang H. Emerging SARS-CoV-2 variants of concern and potential intervention approaches // Critical Care.-2021.- Vol. 25, No. 1.- P.1-8.
- Harvey W.T., Carabelli A.M., Jackson B., et al. SARS-CoV-2 variants, spike mutations and immune escape // Nature Reviews Microbiology.-2021.- Vol. 19, No. 7.- P.409-424.
- Walls A.C., Park Y.J., Tortorici M.A., et al. Structure, Function, and Antigenicity of the SARS-CoV-2 Spike Glycoprotein // Cell.-2020.- Vol. 181, No. 2.- P.281-292.
- Wang R., Chen J., Gao K., et al. Analysis of SARS-CoV-2 mutations in the United States suggests presence of four substrains and novel variants // Communications Biology.-2021.- Vol. 4, No. 1.- P.1-14.
- Yan S., Wu G. Application of neural network to predict mutations in proteins from influenza A viruses - A review of our approaches with implication for predicting mutations in coronaviruses // Journal of Physics: Conference Series.-2020.- Vol. 1682, No. 1.
- Salama M.A., Hassanien A.E., Mostafa A. The prediction of virus mutation using neural networks and rough set techniques // Eurasip Journal on Bioinformatics and Systems Biology.-2016.- Vol. 2016, No. 1.- P.1-11.
- Sawmya S., Haisam A., Rafid M. Analyzing hCov Genome Sequences : Predicting Virulence and Mutation // bioRxiv. -2021.- P.1-14.
- Hochreiter S., Schmidhuber J. Long Short-Term Memory // Neural Computation.-1997.- Vol. 9, No. 8.- P.1735-1780.
- Yin R., Luusua E., Dabrowski J., et al. Tempel: Time-series mutation prediction of influenza A viruses via attention-based recurrent neural networks // Bioinformatics.-2020.-Vol. 36, No. 9.- P.2697-2704.
- Hossain M.S., Pathan A.Q.M.S.U., Islam M.N., et al. Genome-wide identification and prediction of SARS-CoV-2 mutations show an abundance of variants: Integrated study of bioinformatics and deep neural learning. // bioRxiv.-2021.
- Hie B., Zhong E.D., Berger B., et al. Learning the language of viral evolution and escape // Science.-2021.- Vol. 371.- P.284-288.
- Asgari E., Mofrad M.R.K. Continuous distributed representation of biological sequences for deep proteomics and genomics // PLoS 0NE.-2015.- Vol. 10, No. 11.- P.1-15.
- Elbe S., Buckland-Merrett G. Data, disease and diplomacy: GISAID's innovative contribution to global health // Global Challenges.-2017.- Vol. 1, No. 1.- P.33-46.
- Okada P., Buathong R., Phuygun S., et al. Early transmission patterns of coronavirus disease 2019 (COVID-19) in travellers from Wuhan to Thailand, January 2020 // Eurosurveillance.-2020.- Vol. 25, No. 8.
- Cock P.J.A., Antao T., Chang J.T., et al. Biopython: Freely available Python tools for computational molecular biology and bioinformatics // Bioinformatics.-2009.- Vol. 25, No. 11.- P.1422-1423.
- Okonechnikov K., Golosova O., Fursov M., et al. Unipro UGENE: A unified bioinformatics toolkit // Bioinformatics.-2012.- Vol. 28, No. 8.- P.1166-1167.
- Edgar R.C. MUSCLE: Multiple sequence alignment with high accuracy and high throughput // Nucleic Acids Research.-2004.- Vol. 32, No. 5.- P.1792-1797.
- Yan S., Wu G. Prediction of Mutation Positions in H5N1 Neuraminidases From Influenza A Virus by Means of Neural Network // Annals of Biomedical Engineering.-2010.- Vol. 38, No. 3.- P.984-992.
- Waterhouse A., Bertoni M., Bienert S., et al. SWISS-MODEL: Homology modelling of protein structures and complexes // Nucleic Acids Research.-2018.- Vol. 46, No. 1.-P.296-303.
- Bienert S., Waterhouse A., De Beer T.A.P., et al. The SWISS-MODEL Repository-new features and functionality // Nucleic Acids Research.-2017.- Vol. 45, No. 1.- P.313-319.
- Guex N., Peitsch M.C., Schwede T. Automated comparative protein structure modeling with SWISS-MODEL and Swiss-PdbViewer: A historical perspective // Electrophoresis.-2009.- Vol. 30, No.1.- P.162-173.
- Studer G., Rempfer C., Waterhouse A.M., et al. QMEANDisCo—distance constraints applied on model quality estimation // Bioinformatics.-2020.- Vol. 36, No. 6.- P.1765-1771.
- Bertoni M., Kiefer F., Biasini M., et al. Modeling protein quaternary structure of homo- and hetero-oligomers beyond binary interactions by homology // Scientific Reports.-2017.- Vol. 7, No. 1.- P.1-15.
- Berman H.M. The Protein Data Bank // Nucleic Acids Research.-2000.- Vol. 28, No. 1.- P.235-242.
- Desta I.T., Porter K.A., Xia B., et al. Performance and Its Limits in Rigid Body Protein-Protein Docking // Structure.-2020.- Vol. 28, No. 9.- P.1071-1081.
- Vajda S., Yueh C., Beglov D., et al. New additions to the ClusPro server motivated by CAPRI // Proteins: Structure, Function and Bioinformatics.-2017.- Vol. 85, No. 3.-P.435-444.
- Kozakov D., Hall D.R., Xia B., et al. The ClusPro web server for protein-protein docking // Nature Protocols.-2017.- Vol. 12, No. 2.- P.255-278.
- Kozakov D., Beglov D., Bohnuud T., et al. How good is automated protein docking? // Proteins: Structure, Function, and Bioinformatics.-2013.- Vol. 81, No. 12.- P.2159-2166.
- Vangone A., Bonvin A.M.J.J. Contacts-based prediction of binding affinity in protein-protein complexes // eLife.-2015.- Vol. 4.- P.1-15.
- Xue L.C., Rodrigues J.P., Kastritis P.L., et al. PRODIGY: A web server for predicting the binding affinity of protein-protein complexes // Bioinformatics.-2016.- Vol. 32, No. 23.-P.3676-3678.
- Schrödinger, LLC The {PyMol} Molecular Graphics System, Version~1.8 // -2015.-.
- Klink G. V, Safina K.R., Garushyants S.K., et al. Spread of endemic SARS-CoV-2 lineages in Russia // medRxiv.-2021.
- Jangra S., Ye C., Rathnasinghe R., et al. SARS-CoV-2 spike E484K mutation reduces antibody neutralisation // The Lancet Microbe.-2021.- Vol. 2, No. 7.- P.283-284.
- Akkiz H. Implications of the Novel Mutations in the SARS-CoV-2 Genome for Transmission, Disease Severity, and the Vaccine Development. // Frontiers in medicine.-2021.-Vol. 8.
- Nelson T.L., Fosdick B.K., Biela L.M., et al. Association Between COVID-19 Exposure and Self-reported Compliance With Public Health Guidelines Among Essential Employees at an Institution of Higher Education in the US // JAMA Network Open.-2021.- Vol. 4, No. 7.
- O'Toole Â., Scher E., Underwood A., et al. Assignment of epidemiological lineages in an emerging pandemic using the pangolin tool // Virus Evolution.-2021.-Vol. 7, No. 2.
- Gladkikh A., Dolgova A., Dedkov V., et al. Characterization of a Novel SARS-CoV-2 Genetic Variant with Distinct Spike Protein Mutations // Viruses -2021.- Vol. 13, No. 6.
- Planas D., Veyer D., Baidaliuk A., et al. Reduced sensitivity of SARS-CoV-2 variant Delta to antibody neutralization // Nature.-2021.- Vol. 596, No.- P.276-280.
- Wall E.C., Wu M., Harvey R., et al. Neutralising antibody activity against SARS-CoV-2 VOCs B.1.617.2 and B.1.351 by BNT162b2 vaccination // The Lancet.-2021.- Vol. 397.-P.2331-2333.
- Winger A., Caspari T. The Spike of Concern—The Novel Variants of SARS-CoV-2 // Viruses.-2021.- Vol. 13, No. 6.
- Osina N.A., Krasnov Y.M., Guseva N.P., et al. Molecular-genetic monitoring of sARs-CoV-2 genovariants in the territory of the volga federal district of the Russian Federation. Communication // Problemy Osobo Opasnykh Infektsii.-2021.- Vol. 2, No. 1.- P.122-127.
- Yi Y., Lagniton P.N.P., Ye S., et al. COVID-19: what has been learned and to be learned about the novel coronavirus disease // International journal of biological sciences.-2020.-Vol. 16, No. 10.- P. 1753-1766.
- Korber B., Fischer W.M., Gnanakaran S., et al. Tracking Changes in SARS-CoV-2 Spike: Evidence that D614G Increases Infectivity of the COVID-19 Virus // Cell.-2020.- Vol. 182, No. 4.- P.812-827.


