Рандомизированное плацебо-контролируемое исследование эффективности применения севитина у больных алкоголизмом на этапе формирования ремиссии
Автор: Ярыгина Е.Г., Прокопьева В.Д., Аржаник М.Б., Молькина Л.Г., Бохан Н.А.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 4-1 т.25, 2010 года.
Бесплатный доступ
В плацебо-контролируемом исследовании продемонстрировано, что прием севитина (препарата, основным действующим веществом которого является антиоксидант карнозин) больными алкоголизмом в течение 1 месяца на этапе формирования ремиссии ускоряет нормализацию активности аминотрансфераз сыворотки крови, эффективно снижает содержание продуктов окислительной модификации белков и липидов в плазме крови пациентов. Сделано заключение, что севитин может служить важным дополнением к стандартной схеме лечения в наркологической практике в комплексной реабилитации больных алкоголизмом на этапе формирования ремиссии.
Алкоголизм, окислительный стресс, севитин
Короткий адрес: https://sciup.org/14919295
IDR: 14919295 | УДК: 613.
Randomized placebo-controlled investigation of efficacy of application of sevitine in alcoholic patients at the stage of formation of remission
The placebo-controlled investigation has demonstrated that intake of sevitine (preparation which basic acting substance is anti-oxidant carnosine) by alcoholic patients during 1 month at the stage of formation of remission accelerates normalization of activity of aminotransferases of blood serum, effectively reduces content of products of oxidative modification of proteins and lipids in blood plasma of patients. It has been concluded that sevitine may serve as an important addition to standard scheme of the therapy in addiction psychiatry practice in complex rehabilitation of alcoholic patients at the stage of formation of remission.
Текст научной статьи Рандомизированное плацебо-контролируемое исследование эффективности применения севитина у больных алкоголизмом на этапе формирования ремиссии
Успешность реабилитации больных алкоголизмом в значительной степени зависит от поддерживающей терапии на этапе формирования ремиссии [1]. Биологические исследования алкогольной зависимости (АЗ) показывают, что нарушения метаболических процессов во многом определяются активацией свободнорадикальных процессов, накоплением активных форм кислорода (АФК), формированием в организме состояния окислительного стресса (ОС), которое поддерживается в силу многих причин, в том числе, вследствие токсического действия этанола и его метаболита ацетальдегида [2, 3].
В связи с этим представляет интерес использование в качестве дополнительной антиоксидантной терапии больных алкоголизмом средств, обладающих антиоксидантными свойствами: регулирующих антиоксидантную систему защиты организма и инактивирующих АФК, снижая тем самым выраженность ОС в условиях патологии [4, 5]. Одним из перспективных препаратов такого рода является севитин. Севитин – препарат, основным действующим веществом которого является природный гидрофильный гистидин-содержащий дипептид карнозин, который, по литературным данным, является антиоксидантом, антирадикальным агентом, мембраностабилизато-ром [6], нейропротектором, регулятором гомеостаза, общеукрепляющим средством [7], способен улучшать когнитивные функции мозга при нарушениях мозгового кровообращения [8]. Ранее нами было показано, что карнозин способен in vitro повышать устойчивость эритроцитов больных алкоголизмом к гемолизирующему действию кислоты, предохранять клетки от структурных повреждений [9]. В настоящее время препараты на основе карнозина используются в клинической практике. Так, для лечения катаракты применяют глазные капли с карнозином [10], севитин успешно используют в качестве дополнительного препарата при лечении пациентов с дисциркуляторной энцефалопатией [8]. Использование севитина оказалось весьма перспективным в плане фармакологической коррекции утомления, ускорения восстановления и повышения физической работоспособности у спортсменов [11]. В настоящей работе мы использовали севитин в качестве антиоксидантной терапии у больных с АЗ на этапе формирования ремиссии.
Цель работы: плацебо-контролируемое исследование эффективности приема севитина больными алкоголизмом вне стационара на этапе формирования ремиссии для купирования окислительного стресса.
Материал и методы
Работа проводилась в рамках рандомизированного, простого слепого, контролируемого плацебо исследования и была одобрена этическим комитетом при НИИ психического здоровья СО РАМН (г. Томск).
Всего в исследовании участвовало 107 мужчин. Из них 77 человек – больные алкоголизмом II стадии (диагноз по МКБ-10 соответствует коду F10.2.), которые прошли стационарный курс стандартной дезинтоксикационной терапии и восстановительного лечения на базе отделения аддиктивных состояний НИИ психического здоровья СО РАМН. При формировании групп пациентов были использованы следующие критерии включения: возраст от 25 до 60 лет, диагностированная алкогольная зависимость II стадии, стаж алкоголизма – 10–15 лет, подписание информированного согласия на участие в исследовании, прохождение стандартного курса антиалкогольного лечения, установка на трезвость. Критерии исключения: возраст старше 60 лет, психические заболевания в анамнезе (шизофрения, маниакально-депрессивный психоз), алкогольные психозы в анамнезе, зависимость от других психоактивных веществ, судорожные припадки любой этиологии, выраженные соматические нарушения.
Больные алкоголизмом в случайном порядке были распределены в 3 группы. В основную группу вошли 32 пациента, которые на этапе формирования ремиссии (вне стационара) принимали препарат севитин в дозе 1,2 г/сут в течение 1 мес. В группу плацебо были включены 20 больных, которые на этапе формирования ремиссии принимали препарат плацебо севитин в течение 1 мес. В группу сравнения вошли 25 пациентов, которые в течение первого месяца после стационарного лечения на этапе формирования ремиссии не принимали никаких фармакологических препаратов. Пациенты с алкогольной зависимостью проходили обследование дважды: первый раз – после традиционного алкогольного лечения в стационаре (1-я точка) и второй раз – через 1 мес. (2-я точка). В контрольную группу вошли 30 практически здоровых мужчин, которые не состояли на учете у психиатра или нарколога, не имели хронических соматических заболеваний в стадии обострения и не употребляли алкоголь, по крайней мере, 10 дней перед исследованием.
Группы всех участников исследования не различались между собой по возрасту и длительности заболевания (табл. 1).
Таблица 1
Характеристика групп обследуемых лиц
|
Доноры |
Группы |
Количество доноров |
Возраст (лет) |
Продолжительность употребления алкоголя (лет) |
|
Здоровые |
Контрольная |
30 |
40,2±1,8 |
– |
|
Больные |
Основная |
32 |
38,6±1,9 |
10,7±2,1 |
|
алкоголизмом |
Плацебо |
20 |
43,9±2,0 |
11,0±3,0 |
|
Сравнения |
25 |
42,7±2,0 |
11,4±3,4 |
Биологически активная добавка к пище (БАД) севи-тин (активное вещество L-карнозин, таблетки по 0,150 г) и препарат плацебо севитин (идентичный по внешнему виду таблеткам БАД севитин, но не содержащий активного вещества L-карнозина) были безвозмездно предоставлены производственно-торговым предприятием ООО “Медтехника”, г. Казань. Для изготовления БАД севитин производителем использована субстанция L-карнозин, изготовленная фирмой “Yonezawa Haman Chemicals, Ltd” (4300-18. 2-Chome, Hachimanpara, Yonezawa City, Yamagata, Япония).
Определение таких лабораторных показателей крови, как скорость оседания эритроцитов (СОЭ), количество эритроцитов и лейкоцитов, концентрация гемоглобина и глюкозы, активность аспартаттрансаминазы (АСТ) и аланинтрансаминазы (АЛТ)) проводили методами, которые общеприняты в клинической и биохимической лабораториях НИИ психического здоровья СО РАМН. Концентрацию продуктов перекисного окисления липидов в плазме крови определяли колориметрически по реакции с тиобарбитуровой кислотой (ТБК-реактивные продукты, ТБК-РП) [12], карбонилированные производные белков (карбонилы белков) – спектрофотометрически по реакции с 2,4-динитрофенилгидразином [13].
Статистическую обработку данных осуществляли с помощью пакета прикладных программ Statistica 8.0. Проверка согласия распределения исследуемых показателей с нормальным законом проводилась по критериям Колмогорова–Смирнова и Шапиро–Уилка. Для сравнения показателей в 1-й и 2-й точках использовался непараметрический критерий Вилкоксона. Для сравнения независимых выборок использовали критерии Манна–Уитни и Kрускела–Уоллиса.
Результаты и обсуждение
Основные лабораторные показатели крови участников исследования представлены в таблице 2.
Оказалось, что лабораторные показатели крови во всех группах пациентов не превышали нормальных значений как в 1-й, так и во 2-й точках. При этом в основной группе после 1 месяца приема севитина статистически значимо снизился показатель СОЭ (р<0,05), а в группе плацебо после приема плацебо севитина наблюдалось статистически значимое снижение лейкоцитов (р<0,05). В условиях патологии повышение СОЭ и лейкоцитов происходит, как правило, при воспалительных и инфекционных процессах. В нашем исследовании у пациентов не выявлялось выраженного воспалительного процесса, однако статистически значимое снижение СОЭ в основной группе и тенденция к снижению данного показателя в группах плацебо и сравнения, а также статистически значимое снижение лейкоцитов в группе плацебо позволяют сделать заключение, что во всех группах пациентов за 1 мес., в течение которого формировалась ремиссия, происходит постепенная нормализация метаболических процессов, которая не связана с действием севитина, а обусловлена тем, что пациенты в этот период воздерживались от употребления алкоголя.
Как видно из таблицы 2, за 1 мес. формирования ремиссии у пациентов произошли также изменения в ак-
Таблица 2
Основные лабораторные показатели крови участников исследования
|
Показатели |
Группа контроля* |
Основная группа |
Группа плацебо |
Группа сравнения |
|||
|
n=30 |
До приема севитина (1-я точка), n=32 |
После 1 мес. приема се-витина (2-я точка),n=27 |
До приема плацебо севитина (1-я точка), n=20 |
После 1 мес. приема плацебо севи-тина (2-я точка), n=15 |
После стационарного лечения (1-я точка), n=24 |
Через 1 мес. после стационарного лечения (2-я точка), n=21 |
|
|
Эритроциты(х1012/л) |
4,73 + 0,16 |
4,64±0,06 |
4,72±0,06 |
4,56±0,07 |
4,58±0,08 |
4,80±0,08 |
4,89±0,09 |
|
Гемоглобин, г/л |
150,0 + 6,3 |
141,4±2,2 |
145,3±1,9 |
148,7±3,43 |
147,8±2,00 |
143,8±2,35 |
144,5±2,0 |
|
СОЭ, мм/ч |
1–10* |
9,2±1,1 |
7,1±0,6# |
9,4±1,5 |
7,4±1,4 |
8,6±1,05 |
6,7±0,8 |
|
Лейкоциты(х109/л) |
4–9* |
6,9±0,4 |
6,7±0,3 |
8,3±0,5 |
7,2±0,4# |
6,5±0,4 |
6,6±0,3 |
|
Глюкоза, ммоль/л |
4,5–6* |
4,92±0,13 |
4,76±0,15 |
5,07±0,12 |
5,02±0,21 |
4,92±0,15 |
4,77±0,11 |
|
АСТ, Е/л |
до37** |
26,6±2,27 |
20,7±1,94# |
28,5±2,33 |
22,8±3,22 |
32,5±2,69 |
24,6±2,00## |
|
АЛТ, Е/л |
до 42** |
38,7±4,80 |
22,3±3,21## |
33,0±2,93 |
25,8±4,87# |
28,8±3,71 |
26,0±2,83 |
Примечание: * – показатели нормы взяты из справочника Камышников В.С. О чем говорят медицинские анализы. Минск: Беларусская наука, 2001. изд. 3; ** показатели нормы взяты из диагностического набора для определения активности аминотрансфераз, производитель P.Z. Cormay, 2005. # – р<0,05, ## – р<0,01 – статистически значимые различия по сравнению с показателями в той же группе в 1-й точке.
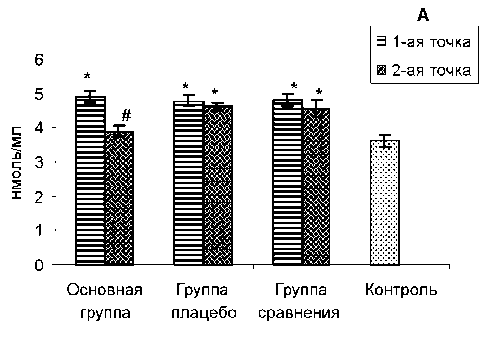
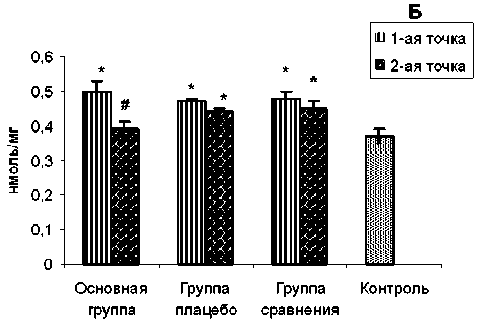
Рис. 1. Содержание продуктов ПОЛ (А) и карбонильных производных белков (Б) в плазме крови доноров исследуемых групп. Примечание: * – статистически значимые различия по сравнению с контролем (p<0,01); # – статистически значимые различия по сравнению с 1-й точкой (p<0,01)
тивности аминотрансфераз сыворотки крови. В основной группе активность как АСТ, так и АЛТ статистически значимо снизилась (р<0,05 и р<0,01 соответственно). В группе плацебо статистически значимо снизилась только активность АЛТ (р<0,05), а активность АСТ значимо не изменилась. В группе сравнения, напротив, статистически значимо снизилась АСТ (р<0,01), а АЛТ имела лишь тенденцию к снижению.
Известно, что аминотрансферазы сыворотки крови (АСТ и АЛТ) являются маркерными ферментами повреждения клеток. По данным Волковой З.И. и соавт. [14], повышенная активность аминотрансфераз сыворотки крови у больных алкоголизмом отражает тяжесть алкогольной интоксикации и может быть использована для контроля за проводимым лечением. Полученные нами результаты показывают, что во всех группах пациентов происходит нормализация активности аминотрансфераз сыворотки крови, однако в основной группе этот процесс происходит заметно быстрее. Более быстрая нормализация аминотрансфераз пациентов при приеме севитина свидетельствует о способности данного препарата снижать тяжесть алкогольной интоксикации и позволяет предполагать, что механизм такого эффекта севитина связан с его антиоксидантными и мембраностабилизирующими свойствами.
Для изучения влияния приема севитина больными алкоголизмом на их оксидативный статус мы провели оценку содержания продуктов ПОЛ и карбонилов белков в плазме крови пациентов всех групп в 1-й и 2-й точках. Результаты представлены на рисунке 1.
Видно, что во всех трех группах больных в 1-й точке содержание как продуктов ПОЛ (рис. 1, А), так и карбонильных производных белков (рис. 1, Б) в плазме крови статистически значимо повышено по сравнению с контролем (р<0,01). Эти данные свидетельствуют о том, что организм пациентов всех групп в начале периода формирования ремиссии находится в состоянии окислительного стресса, несмотря на то, что все больные прошли курс стационарного антиалкогольного лечения.
Через 1 месяц (2-я точка) в основной группе больных, принимавших севитин, содержание продуктов ПОЛ в плазме крови, как и карбонилов белков, статистически значимо снизилось (р<0,01) и перестало отличаться от контрольных значений (рис. 1, А, Б).
В то же время в группах плацебо и сравнения во 2-й точке содержание продуктов ПОЛ, как и карбонилов белков, практически не отличалось от уровня этих показателей в 1-й точке, при этом они оставались статистически значимо выше соответствующих показателей в контрольной группе (рис. 1, А, Б).
Таким образом, прием севитина больными алкоголизмом на стадии формирования ремиссии существенно ускоряет нормализацию уровня продуктов ПОЛ и карбонильных производных белков в плазме крови, снижает выраженность окислительного стресса в организме пациентов. Плацебо севитин таким действием не обладает.
Выводы
-
1. Севитин способствует нормализации активности аминотрансфераз сыворотки крови больных с АЗ, что свидетельствует о стабилизирующем действии севитина на мембраны клеток (в частности, на мембраны гепатоцитов).
-
2. Севитин эффективно снижает выраженность ОС в организме пациентов с АЗ, о чем свидетельствует статистически значимое снижение продуктов ПОЛ и карбонилов белков в плазме крови больных, принимавших севитин.
-
3. Севитин может служить важным дополнением к стандартной схеме лечения в наркологической практике в комплексной реабилитации больных алкоголизмом на этапе формирования ремиссии.
Список литературы Рандомизированное плацебо-контролируемое исследование эффективности применения севитина у больных алкоголизмом на этапе формирования ремиссии
- Дудко Т.Н. Реабилитация наркологических больных (реабилитология и реабилитационные концепции)//Вопросы наркологии. -2006. -№ 1. -С. 31-41.
- Nordmann R., Ribiere C., Rouach H. Implication of free radical mechanisms in ethanol-induced cellular injury//Free Radic. Biol. Med. -1992. -№ 12. -Р. 219-240.
- Бохан Н.А., Прокопьева В.Д. Молекулярные механизмы влияния этанола и его метаболитов на эритроциты in vitro и in vivo. -Томск: Изд-во Том. ун-та, 2004. -115 с.
- Пирожков С.В., Панченко Л.Ф. Использование антиоксидантов для лечения абстинентных и постабстинентных расстройств у больных алкоголизмом//Наркология. -2006.-№ 4. -C. 54-59.
- Зиновьева О.Е. Антиоксидантная терапия в лечении диабетической и алкогольной полиневропатии//Consilium Medicum. -2006. -Т. 8, № 8. -C. 120-124.
- Стволинский С.Л. Защита организма от окислительного стресса карнозином: эколого-биохимический подход: дис. … д-ра. биол. наук. -М., 2006. -86 с.
- Болдырева. А.А. Карнозин и защита тканей от окислительного стресса. -М.: Изд-во МГУ -Диалог, 1999. -362 с.
- Беляев М.С. Карнозин как фактор эндоэкологической защиты организма от повреждений, вызванных окислительным стрессом: автореф. дис. … канд. биол. наук. -М., 2008. -24 с.
- Prokopieva V.D., Bohan N.A., Johnson P., Аbe H., Boldyrev A.A. Effects of carnosine and related compounds on the stability and morphology of erythrocytes from alcoholics//Alcohol & Alcoholism. -2000. Vol. 35. -№ 1. -Р. 44-48.
- Волков О.А. Биологическая роль карнозина и его использование в офтальмологии//Клиническая офтальмология. -2005. -Т. 6, № 3. -С. 128-130.
- Рожкова Е.А., Орджоникидзе З.Г., Дружинин А.Е., Сейфулла Н.Р., Панюшкин В.В., Кузнецов Ю.М. Карнозин и антиоксиданты природного происхождения как средства профилактики острого посленагрузочного окислительного стресса//Экспериментальная и клиническая фармакология. -2007. -Т. 70, № 5. -С. 44-46.
- Коробейникова Э.Н. Модификация определения продуктов перекисного окисления липидов в реакции с тиобарбитуровой кислотой//Лабораторное дело. -1989. -№ 7. -С. 8-9.
- Levine R.L. Determination of carbonyl content in oxidatively modified proteins//Meth. Enzymol. -1990. -Vol. 186. -P. 464-478.
- Волкова З.И., Маркова М.Н., Савченко Л.М., Лукьянова Н.А. Клиническое значение определения некоторых ферментов в сыворотке крови у больных хроническим алкоголизмом//Проблемы алкоголизма (клиника, патогенез, терапия): сб. научных трудов. -М., 1986. -С. 82-93.


