Редактирование генома сельскохозяйственных животных с помощью технологии CRISPR/CAS9
Автор: Ларкина Татьяна Александровна, Крутикова Анна Алексеевна, Козикова Лариса Васильевна
Журнал: Молочнохозяйственный вестник @vestnik-molochnoe
Рубрика: Биологические и сельскохозяйственные науки
Статья в выпуске: 3 (31), 2018 года.
Бесплатный доступ
Одной из самых обсуждаемых тем в современной генетике стало появление технологии редактирования геномов биологических объектов CRISPR/ Cas9, которая оказала огромное влияние на молекулярную биологию, эта технология позволяет добавлять, удалять и вносить изменения в геном различных организмов, в том числе и высших млекопитающих. Это инновационный и мощный инструмент получения животных с заданными признаками. Стало возможным за относительно короткий срок создать животное с измененным геномом, что позволит повысить качество и эффективность производства продукции животноводства. В статье приводится обзор успешных экспериментов в мировой практике по редактированию сельскохозяйственных животных с помощью технологии CRISPR/Cas9.
Редактирование генома, мрнк, ген, мутация
Короткий адрес: https://sciup.org/149126672
IDR: 149126672 | УДК: 575.162
Editing the genome of farm animals using CRISPR / CAS9 technology
One of the most discussed topics in modern genetics is the technology emergence for editing of biological objects genomes CRISPR / Cas9, which has a huge impact on molecular biology, this technology allows adding, removing and making changes to the genome of various organisms, including higher mammals. It is an innovative and powerful tool for obtaining animals with specified characteristics. It has become possible in a relatively short time to create an animal with the modified genome, which improves the quality and efficiency of livestock production. The article gives an successful experiments overview in the world practice of editing agricultural animals using CRISPR / Cas9 technology.
Текст научной статьи Редактирование генома сельскохозяйственных животных с помощью технологии CRISPR/CAS9
Введение . Благодаря своей простоте в использовании технология CRISPR/Cas9 занимает на сегодняшний день лидирующее положение в практике молекулярной генетики. Всего пару лет назад технология редактирования с помощью CRISPR/ Cas9 стремительно пересекла границу из фантастики в реальность и была принята на вооружение в десятках лабораторий по всему миру. Большое количество статей говорят о получении положительных результатов в этой области.
CRISPR это иммунная система бактерий, защищающая их от чужеродных вирусов. Впервые она была обнаружена у Escherichia coli в конце 1980-х годов. Японские учёные заметили, что в геноме бактерии присутствуют повторяющиеся последовательности, разделенные спейсерами – уникальными участками ДНК. Но какую роль они играют, исследовали объяснить на тот момент не смогли. И только в 1992 году Франциско Мохика назвал их CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats ‒ сгруппированные короткие палиндромные повторы, разделенные промежутками). Далее генетики выяснили, что CRISPR связаны с выработкой комплекса белков, названных Cas, которые узнают проникший в клетку бактерии вирус и вырезают кусок чужеродной ДНК и вставляют его в кассету CRISPR (рис. 1) . Если клетка вновь встречается с идентичным вирусом, система CRISPR/ Cas9 с легкостью помогает побороть инфекцию (рис. 2) [1].
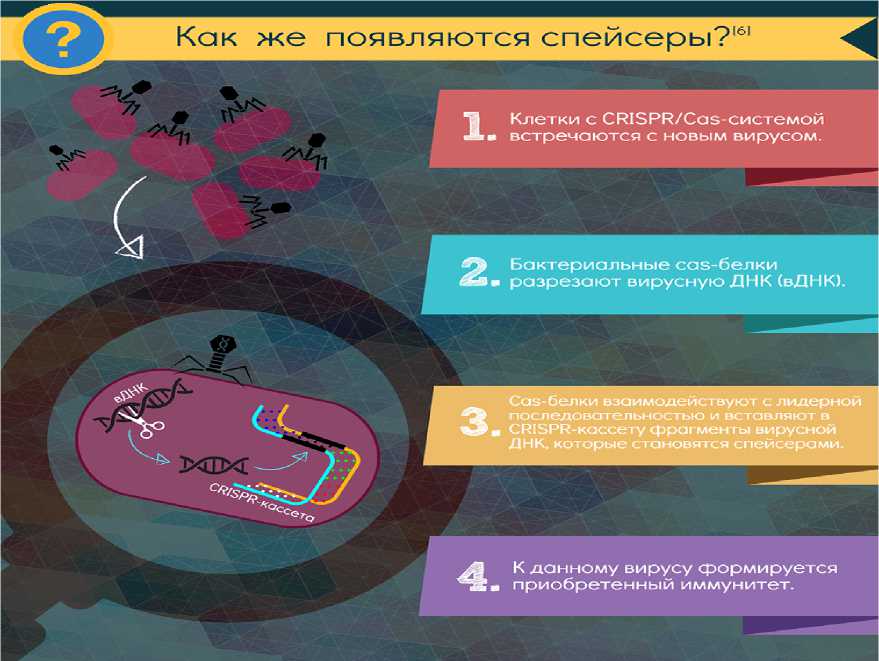
Рисунок 1. Формирование CRISPR-опосредованного иммунитета у бактерий [2]
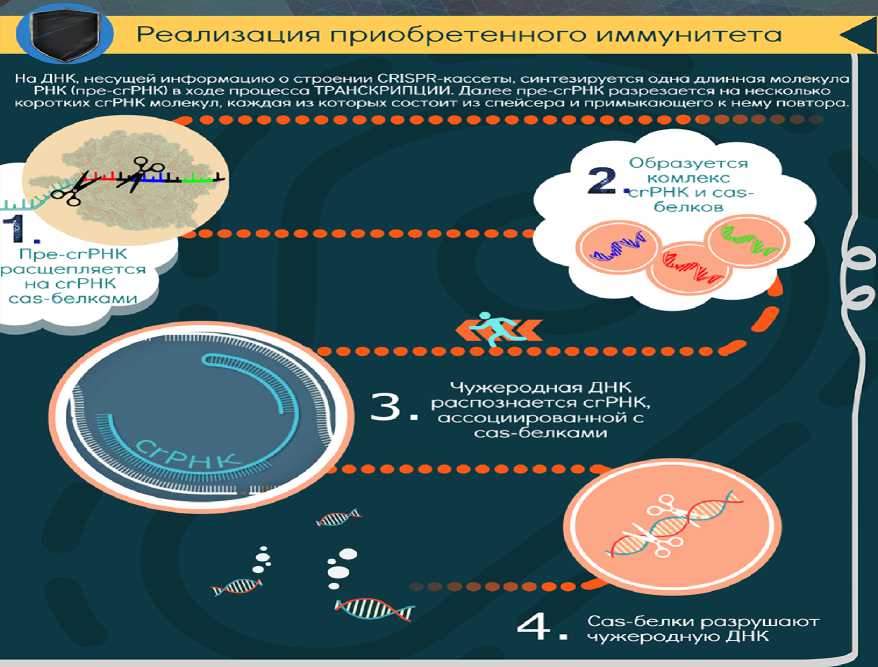
Рисунок 2. Реализация приобретенного иммунитета у бактерий [2]
Основная часть. Изменение генома животных на молекулярном уровне осуществлялось преимущественно методами трансгенеза, но эффективность была близка к нулю. Специалисты в области генной инженерии с большим азартом переняли технологию CRISPR/Cas9 для внесения изменений в геном сельскохозяйственных животных, что позволило более точно в облегченной форме модифицировать гены, участвующие в формировании хозяйственно полезных признаков у животных.
Объект исследований ‒ свиньи.
Свиньи ‒ животные неприхотливые и плодовитые, поэтому за короткий срок можно получить большое поголовье поросят, также свиноводство является важной отраслью животноводства для обеспечения продовольствием населения. К тому же, свинья это идеальная модель для исследования различных заболеваний человека. Китайский учёный Tang Hai c соавторами продемонстрировал применение CRISPR/Cas9 технологии для нокаута гена vWF (гликопротеин плазмы крови), мутация которого у человека вызывает серьезную болезнь Виллебранда (спонтанные кровотечения, болезнь схожа с гемофилией). В процессе производства мяса важным фактором является активное кровотечение после убоя, так как оставшаяся кровь является идеальной средой для роста бактерий, а это в свою очередь опасно для жизни человека. Таким образом, нокаут гена vWF позволит снизить сворачива-емость крови, что будет способствовать активному ее оттоку после убоя животного. Показано, что введение генетических конструкций методом цитоплазматической инъекции мРНК/Cas9 и мРНК/sgRNA в зиготы не оказывает существенного влияния на развитие эмбрионов свиней. В общей сложности 76 инъецированных эмбрионов были трансплантированы в 5 суррогатных матерей, 10 из 16 родившихся поросят содержали целевую делецию на участке гена vWF, эффективность мутации в этом случае составила около 63%. Эти результаты показывают, что с помощью технологии CRISPR/Cas9 группа исследователей смогла получить как одноаллельных, так и биаллельных мутантных жизнеспособных свиней за один шаг путем прямой инъекцией в зиготу [3].
Двойной эксперимент провел Whitworth K. с коллегами, они получили свиней с отредактированным геномом с нокаутом генов CD163 и CD1D (антигенные маркёры клеток иммунной системы) двумя методами: путём переноса ядер соматических клеток (Somatic cell nuclear transfer ‒ SCNT) в ооциты-реципиенты, а также методом цитоплазматической инъекции генетических конструкций в зиготу. Когда система CRISPR/Cas9 была введена методом инъекции в зиготу, почти 100% эмбрионов свиней содержали INDEL-мутацию в целевом гене и оказались жизнеспособны. У поросят, полученных путем SCNT, были проблемы со здоровьем, и они подверглись эвтаназии [4]. Модификация генома на уровне зигот имеет свои плюсы, например получение гипоморфных мутаций (потеря функции гена), не способных передаваться потомству, или в результате получаются гетерозиготные животные, несущие аллель дикого типа, что требует дополнительных шагов для получения гомозиготных особей. Метод SCNT позволяет выделить мутантные клетки перед началом эксперимента и гарантирует получение животных с запланированными модификациями генов [5].
Свиньи могут выступать продуцентами важных человеческих белков. Одним из таких белков является сывороточный альбумин. Этот белок участвует во многих жизненно важных процессах в организме, в том числе в регуляции кровяного давления в системе циркуляции, а также в транспортировке жирных кислот, аминокислот, желчных пигментов и различных компонентов сыворотки крови. При различных травмах, ожогах, в ходе хирургических операций сывороточный альбумин вводят в качестве заменителя плазмы. Так Peng с соавторами, используя преимущества системы CRISPR/Cas9, создал плазмидный вектор, нацеленный на локус альбумина свиней, который содержал в себе кДНК человеческого сывороточного альбумина и sgRNA (направляющую РНК) для нокаута гена альбумина свиней, чтобы блокировать экспрессию эндогенного альбумина. В результате эксперимента, в крови 16 поросят присутствовал человеческий альбумин [6]. X. Wang с коллегами наблюдали низкую частоту целевой встройки ДНК-фрагментов (ssODN) при ПЦР-анализе бластоцист свиней (13 %), а эффективность внедрения мутаций в ген Mitf с помощью инъекции CRISPR/Cas9 в зиготы свиней составила 100 % [7].
При всех достоинствах использования технологии CRISPR/Cas9 для генетической модификации одноклеточных эмбрионов у этого метода есть существенный недостаток – это мозаицизм развивающегося организма, возникающий в том случае, когда целенаправленные изменения генетической информации происходят не во всех бластомерах эмбриона. Если CRISPR/Cas9 модифицирует геном не на одноклеточной, а на двуклеточной стадии, то есть вероятность, что мутирует лишь часть генома, то есть лишь половина клеток родившегося животного будут нести целевую мутацию. Кроме того, если репарация по механизму NHEJ (негомологичная, когда концы ДНК сшиваются лигазой напрямую, без гомологичного шаблона) протекает с изменением целевого локуса, то модификации, произошедшие в разных клетках, могут приводить к различающимся мутациям. Таким образом, животное будет состоять из клеток с разными мутациями в целевом локусе генома. Если мозаицизм наблюдается в половых клетках, то проведение скрещиваний затянется на длительный срок, чтобы получить гомозиготных носителей мутации [8].
В 2015 году X. Zhou методом SCNT получил колонию мутированных фибробластов свиней с нокаутом по гену TYR (тирозиназа) и двойным нокаутом по генам PINK1 (киназа) и PARK2 (ген паркина). В результате получили 15 тирозиназных (TYR) и 20 (PARK2 и PINK1) биаллельных мутантных свиней. Все они были гомозиготными, свиньи с выключенной тирозиназой показали типичный альбинизм, а свиньи с двойным нокаутом по генам PARK2 и PINK1 были сильно истощены [9]. Положительные работы по INDEL-мутациям (делеции в геноме) с использованием CRISPR/Cas9 системы были опубликованы у К. Whitworth [10], L. Huang [11], K. Wang [12] и многих других исследователей. Еще одну успешную работу по введению гена мыши UCP1 (адипонектина) в эндогенный локус UCP1 свиньи провел Q. Zheng с коллегами. В результате семейство свиней Ariodactyl Suidae, которые до этого не имели функционального гена UCP1, отвественного за терморегуляцию организма, показало улучшенную способность поддерживать температуру тела во время холодового воздействия. Таким образом, свиньи семейства Ariodactyl Suidae адаптировались к холоду, это снижает неонатальную смертность поросят и уменьшает экономические затраты на обогрев помещений для содержания животных [13].
О бъект исследований – крупный рогатый скот.
В настоящее время разведение крупного рогатого скота с целью получения продукции ведется в трех направлениях – молочное, мясное и молочно-мясное. Скотоводство занимает одно из ведущих мест в обеспечении населения полноценными продуктами питания. Применение технологии редактирования генома у крупного рогатого скота позволит существенно повысить продуктивность животных, сократить технологические потери, а также получить животных с заданными качествами.
Японский учёный M. Ikeda изучает местную породу крупного рогатого скота Вагю (японская черная), которая известна своей мраморностью и высоким содержанием ненасыщенных жиров. Более 60 лет велась селекция на мраморность, но это привело к накоплению рецессивных мутаций, которые вызывают генетические заболевания. Одним из таких заболеваний является синдром недостатка изолейцил-тРНК-синтетазы (IARS). Замещение в гене IARS (235G>C) приводит к замене аминокислотного состава белка (Val79Leu) вызывая тем самым снижение синтеза белка. У гомозиготных мутантных телят наблюдается задержка внутриутробного развития, они или умирают в утробе или рождаются нежизнеспособными. Для восстановления мутантного гена IARS учёные использовали вектор, который включал в себя систему CRISPR/Cas9 для создания двухцепочечного разрыва вблизи места мутации, ДНК, которая содержала синонимичный кодон для правильной аминокислоты, а также зеленый флуоресцентный белок (AcGFP) для идентификации включения ДНК в геном мутантного эмбриона. Отредактированные бластоцисты подсаживали суррогатным коровам. Получили пять жизнеспособных плодов. Анализ геномной ДНК плода показал, что мутантный аллель был исправлен [14].
Болезни животных также активно исследуются мировым сообществом учёных. Туберкулез причиняет животноводству большой экономический ущерб, что связано с преждевременной выбраковкой, снижением продуктивности и сдачей молодых животных на убой, продолжительными и дорогостоящими противоэпизоотическими мероприятиями. Группа учёных во главе с Y. Gao ввели ген NRAMP1, экспрессирующийся в макрофагах мыши и контролирующий чувствительность к М. bovis в культуру фибробластов эмбрионов крупного рогатого скота. В результате секвени- рования генома учёные продемонстрировали, что ген NRAMP1 встроился в целевой участок и правильно экспрессируется. Путём переноса ядер из культуры фибробластов (Somatic cell nuclear transfer ‒ SCNT) в ооциты-реципиенты, получили 11 жизнеспособных телят с повышенной устойчивостью к туберкулезу [15].
Объект исследований ‒ козы и овцы.
Разведение коз и овец было самым популярным животноводческим направлением с древних времен. Человек приручил этих животных не одно тысячелетие тому назад, по некоторым сведениям это произошло 6–8 тысяч лет назад. С тех пор они верно служат человеку, обеспечивая его молоком, шерстью, пухом, шкурами и мясом.
В 2014 году W. Ni показал успешную индукцию в первичных фибробластах коз прецизионных мутаций с эффективностью от 9 до 70%. Котрансфекция c использованием объединения из двух или четырех различных систем Cas9/gRNAs позволила получать линии клеток, несущих разрывы одновременно в двух или четырех генах с эффективностью 20 и 2% соответственно [16]. Трансгенные козы, несущие мутации, могут быть получены в течение 5 месяцев (продолжительность беременности 150‒155 дней). Козы ‒ удобный объект для исследований, у них достаточно короткий период откармливания и размножения. Козье молоко имеет высокую питательную ценность. Однако козье молоко, как и коровье, содержит различные аллергены, преимущественно β-лактоглобулин (BLG). В прошлом году W. Zhou путем коинъекции мРНК (Cas9) и направляющих РНК (sgRNAs) в зиготу козы нокаутировал 29-bp регион 1 экзона β-лактоглобулина. Уровень экспрессии BLG резко снизился (p <0,01) у мутантных коз. Кроме того, результат вестерн-блот анализа подтвердил отсутствие белка BLG в козьем молоке [17].
Большое значение уделяется совершенствованию продуктивности животных, которые относятся к шерстной группе. В Китае продемонстрировали увеличение подшерстка кашемировых коз за счет частичной потери функции гена FGF5 (ген длины шерсти) в результате редактирования генома животных с помощью инъекции системы Cas9/gRNA в зиготу [18].
Использование мелкого рогатого скота в качестве доноров тканей и органов для лечения заболеваний человека становится все более актуальным. Поскольку диабет является распространенным заболеванием, которое можно лечить с помощью тканей, полученных из стволовых клеток, Vilarino М. с коллегами сосредоточил свое внимание на гене PDX1. PDX1 (панкреатический и дуоденальный гомеобокс-белок 1) представляет собой транскрипционный фактор, который участвует в развитии поджелудочной железы в эмбриональном периоде и не только. В этом исследовании они оценили, может ли нарушение PDX1 остановить развитие поджелудочной железы у овец. В результате микроинъекции CRISPR/Cas9 в зиготу получились двуаллельные мутанты с отсутствием поджелудочной железы. Для уменьшения мозаики животного систему CRISPR/Cas9 вводят перед репликацией ДНК в зиготе или даже до оплодотворения [19].
Для увеличения мясной продуктивности животных необходимо нокаутировать ген MSTN (миостатин), который участвует в ингибировании дифференцировки и роста мышц. M. Crispo с коллегами выделил 53 бластоцисты, полученные после микроинъекции зиготы CRISPR/Cas9, они были перенесены в 29 суррогатных матерей, что привело к 65,5% (19/29) беременности овец и 41,5% (22/53) новорожденным ягнятам. Из 22 рожденных ягнят, проанализированных секвенированием, десять показали мутации indel в гене MSTN. Вестерн-блот анализ гомозиготных носителей подтвердил отсутствие миостатина, а у ягнят рост мышечной массы проявлялся активнее, чем у аналогов дикого типа [20]. Успеха достигли Wang X. с коллегами после точного нокаута системой Cas9/gRNA трех генов (MSTN, ASIP и BCO2). Эффективность таргетинга в этих трех генах у родившихся ягнят составляла 27‒33%, что подтвердило эффективность метода микроинъекции в зиготу для создания генетически модифицированных овец [21].
Объект исследований ‒ куры.
Наряду с созданием генетически измененных сельскохозяйственных животных ‒ млекопитающих (свиней, коров, коз, овец, кроликов), не меньший интерес представляет создание кур с отредактированным геномом. Однако классический метод микроинъекции генетической конструкции Cas9/gRNA в зиготу связан с проблемами в точности определения овуляции, большом количестве желтка в яйцеклетке, труднодоступностью яйцеклетки, сильным уплотнением цитоплазмы около пронуклеусов [22]. Эффективным способом создания кур с измененным геномом является трансформация бластодермальных клеток с использованием лентивирус-ных и ретровирусных векторов. Прорывом в области редактирования генома курицы стали успешные исследования китайских ученых. Они нокаутировали два гена яичного белка (OVA) и овомукоид (OVM) с использованием вирусной инфекции у раннего эмбриона в первичных зародышевых клетках, которые можно культивировать и генетически модифицировать in vitro. Таким образом можно получить яйца без белков овальбумина и овомукоида, тем самым снизив аллергенность яиц [23].
Для производства вакцин для борьбы с птичьим гриппом группа американских исследователей провела серию экспериментов по выключению тяжелой цепи иммуноглобулина В, что привело к отсутствию выработки антител и блокированию развития В-клеток [24].
Заключение.
Сельскохозяйственные животные с успешно отредактированным геномом технологией CRISPR/Cas9 представляют собой усовершенствованные организмы-модели, применяемые для доказательства новых концепций крупномасштабного производства продуктов питания и их производных, которые представляют существенный интерес для биомедицины, биофармацевтики и хозяйственной отрасли. В ближайшем будущем совершенствование технологий редактирования генома позволит расширить технические возможности методов трансгенеза, способствующих процветанию науки, развитию молекулярной биологии, а также станет научной базой для улучшения отечественных пород сельскохозяйственных животных с целью обеспечения населения полноценными и качественными продуктами питания.
Список литературы Редактирование генома сельскохозяйственных животных с помощью технологии CRISPR/CAS9
- Barrangou R., Fremaux C., Deveau H., Richards M., Boyaval P., Moineau S., Romero D.A., Horvath P. CRISPR provides collected resistance against viruses in prokaryotes. Science (N.Y.), 2007, vol. 315, pp. 1709-1712.
- Волкова, О. Просто о сложном: CRISPR/Cas/О. Волкова, А. Коротаев//Биомолекула -2016 . URL: https://biomolecula.ru/articles/prostoo-slozhnom-crispr-cas. Дата обращения: 23.07.2018 г.
- Hai T., Teng F., Guo R. One-step generation of knockout pigs by zygote injection of CRISPR/Cas system. Cell Res., 2014, vol.24, pp. 372-375. DOI: 10.1038/cr.2014.11
- Whitworth K.M., Lee K., Benne J.A. Use of the CRISPR/Cas9 System to Produce Genetically Engineered Pigs from In Vitro-Derived Oocytes and Embryos. Biology of Reproduction, 2014, vol. 91, no.3, pp. 78-90.
- Трансгенные сельскохозяйственные животные: современное состояние исследований и перспективы/Н. А. Зиновьева, Н. А. Волкова, В. А. Багиров, Г. Брем//Экологическая генетика. -2015. -Т. 13. -№ 2. -С. 58-76.
- Peng J., Wang Y., Jiang J., Zhou X., Song L., Wang L., Ding C., Qin J., Liu L., Wang W., Liu J., Huang X., Wei H. Production of human albumin in pigs through CRISPR/Cas9mediated knockin of human cDNA into swine albumin locus in the zygotes. Zhang Sci. Reports, 2015.
- DOI: 10.1038/srep16705
- Wang X., Zhou J., Cao C., Huang J., Hai T., Wang Y., Zheng Q., Zhang H., Qin G., Miao X., Wang H., Cao S., Zhou Q., Zhao J. Efficient CRISPR/Cas9-mediated biallelic gene disruption and sitespecificknockin after rapid selection of highly active sgRNAs in pigs. Sci. Reports, 2015.
- DOI: 10.1038/srep13348
- Система CRISPR/Cas9 -универсальный инструмент геномной инженерии/А.В. Смирнов, А.М. Юнусова, В.А. Лукьянчикова, Н.Р. Баттулин//Вавиловский журнал генетики и селекции. -2016. -Т. 20. -№4. -С. 493-510. -.
- DOI: 10.18699/VJ16.175
- Zhou X., Xin J., Fan N., Zou Q., Huang J., Ouyang Z., Zhao Y., Zhao B., Liu Z., Lai S., Yi X., Guo L., Esteban M.A, Zeng Y., Yang H., Lai L. Generation of CRISPR/Cas9mediated gene-targeted pigs via somatic cell nuclear transfer. Cell Mol Life Sci, 2015, vol. 72, pp. 1175-1184.
- DOI: 10.1007/s00018-014-1744-7
- Whitworth K.M., Benne J.A., Spate L.D., Murphy S.L., Samuel M.S., Murphy C.N., Richt J.A., Walters E., Prather R.S., Wells K.D. Zygote injection of CRISPR/Cas9 RNA successfully modifies the target gene without delaying blastocyst development or altering the sex ratio in pigs. Transgenic Res., 2017, vol. 26, no.1, pp. 97-107.
- DOI: 10.1007/s11248-016-9989-6
- Huang L., Hua Z., Xiao H., Cheng Y., Xu K., Gao Q., Xia Y., Liu Y., Zhang X., Zheng X., Mu Y., Li K. CRISPR/Cas9-mediated ApoE-/-and LDLR-/-double gene knockout in pigs elevates serum LDL-C and TC levels. Oncotarget, 2017, vol. 8, no.23, pp. 37751-37760.
- DOI: 10.18632/oncotarget.17154
- Wang K., Ouyang H., Xie Z., Yao C., Guo N., Li M., Jiao H., Pang D. Efficient Generation of Myostatin Mutations in Pigs Using the CRISPR/Cas9 System. Sci Rep., 2015.
- DOI: 10.1038/srep16623
- Zheng Q., Lin J., Huang J., Zhang H., Zhang R., Zhang X., Cao C., Hambly C., Qin G., Yao J., Song R., Jia Q., Wang X., Li Y., Zhang N., Piao Z., Ye R., Speakman J.R., Wang H., Zhou Q., Wang Y., Jin W., Zhaoa J. Reconstitution of UCP1 using CRISPR/Cas9 in the white adipose tissue of pigs decreases fat deposition and improves thermogenic capacity. Proc Natl AcadSci U S A, 2017, vol.114, no. 45, pp. 9474-9482.
- DOI: 10.1073/pnas.1707853114
- Ikeda M., Matsuyama S., Akagi S., Ohkoshi K., Nakamura S., Minabe S., Kimura K., Hosoe M. Correction of a Disease Mutation using CRISPR/Cas9-assisted Genome Editing in Japanese Black Cattle. Sci Rep., 2017. -w
- DOI: 10.1038/s41598-017-17968
- Gao Y., Wu H., Wang Y., Liu X., Chen L., Li Q., Cui C., Liu X., Zhang J., Zhang Y. Single Cas9 nickase induced generation of NRAMP1 knockin cattle with reduced offtarget effects. Genome Biol., 2017.
- DOI: 10.1186/s13059-016-1144-4
- Ni W., Qiao J., Hu S., Zhao X., Regouski M., Yang M., Polejaeva I.A., Chen C. Efficient gene knockout in goats using CRISPR/Cas9 system. PLoS One., 2014.
- DOI: 10.1371/journal.pone.0106718
- Zhou W., Wan Y., Guo R., Deng M., Deng K., Wang Z., Zhang Y., Wang F. Generation of beta-lactoglobulin knock-out goats using CRISPR/Cas9. PLoS One., 2017, vol.12 (10): e0186056.
- DOI: 10.1371/journal.pone.0186056
- Wang X., Cai B., Zhou J., Zhu H., Niu Y., Ma B., Yu H., Lei An., Yan H., Shen Q., Shi L., Zhao X., Hua J., Huang X., Qu L., Chen Y. Disruption of FGF5 in Cashmere Goats Using CRISPR/Cas9 Results in More Secondary Hair Follicles and Longer Fibers. PLoS One., 2016. vol.11(10) e0164640.
- DOI: 10.1371/journal.pone.0164640
- Vilarino M., Rashid S.T., Suchy F.P., McNabb B.R., Meulen T., Fine E.J., Ahsan S., Mursaliyev N., Sebastiano V., Diab S.S., Huising M.O., Nakauchi H., Ross P.J. CRISPR/Cas9 microinjection in oocytes disables pancreas development in sheep. Sci Rep., 2017. no.7: 17472.
- DOI: 10.1038/s41598-017-17805-0
- Crispo M., Mulet A.P., Tesson L., Barrera N., Cuadro F., dos Santos-Neto P.C., Nguyen T.H., Crénéguy A., Brusselle L., Anegón I. Efficient Generation of Myostatin Knock-Out Sheep Using CRISPR/Cas9 Technology and Microinjection into Zygotes. PLoS One, 2015. no.10(8): e0136690.
- DOI: 10.1371/journal.pone.0136690
- Wang X., Niu Y., Zhou J., Yu H., Kou Q., Lei A., Zhao X., Yan H., Cai B., Shen Q., Zhou S., Zhu H., Zhou G., Niu W., Hua J., Jiang Y., Huang X., Ma B., Chenc Y. Multiplex gene editing via CRISPR/Cas9 exhibits desirable muscle hypertrophy without detectable off-target effects in sheep. Sci Rep., 2016, no.6: 32271.
- DOI: 10.1038/srep32271
- Muramatsu T., Mizutani Y., Ohmori Y., Okumura J.Comparison of three nonviral transfection methods for foreign gene expression in early chicken embryos in ovo. Biophys. Res. Commun., 1997. vol. 230. pp. 376-380.
- Oishi I., Yoshii K., Miyahara D., Kagami H., Tagami T. Targeted mutagenesis in chicken using CRISPR/Cas9 system. Sci Rep., 2016. no.6:23980.
- DOI: 10.1038/srep23980
- Schusser B., Collarini E.J., Yi H., Izquierdo S.M., Fesler J., Pedersen D., Klasing K.C., Kaspers B., Harriman W.D., van de Lavoir M.C., Etches R.J., Leighton P.A. Immunoglobulin knockout chickens via efficient homologous recombination in primordial germ cells. Proc Natl Acad Sci. U S A, 2013, vol.110, no. 50. pp. 20170-5.
- DOI: 10.1073/pnas.1317106110


