Ресвератрол: метаболизм, биологические механизмы и возможные побочные эффекты
Автор: Цейликман В.Э., Шатилов В.А., Жуков М.С., Патрикян Г.Н., Хайбулин Т.Л.
Рубрика: Медицина
Статья в выпуске: 3 (31), 2025 года.
Бесплатный доступ
Ресвератрол, природное соединение из класса стильбенов, содержащееся в винограде, ягодах и других растениях, привлекает значительный научный интерес благодаря широкому спектру заявленных полезных свойств, включая антиоксидантную, противовоспалительную, антивозрастную и кардиопротекторную активность. Данный обзор обобщает современные знания о ресвератроле, исследуя его сложную фармакокинетику — характеризующуюся высоким всасыванием, но низкой биодоступностью при пероральном приёме из-за интенсивного пресистемного метаболизма — и его многообразные механизмы действия. Подробно описана активация ключевых сигнальных путей, таких как SIRT1, AMPK, Nrf2 и PGC-1α, которые опосредуют его влияние на митохондриальный биогенез, антиоксидантную защиту и метаболический гомеостаз. Особое внимание уделено ключевой роли микробиоты кишечника в метаболизме ресвератрола до активных производных, таких как дигидроресвератрол и лунуларин, которые вносят существенный вклад в его биологические эффекты и модулируют состояние желудочно-кишечного тракта. Парадоксально, но в обзоре также рассматриваются потенциальные неблагоприятные эффекты соединения, изучается, как его окисление до реакционноспособной хинонной формы может приводить к про-оксидантным эффектам, генотоксичности, нарушению клеточной сигнализации и эндокринным нарушениям. Этот всесторонний анализ подчеркивает двойственную природу ресвератрола, выделяя как его терапевтический потенциал, так и зависящие от дозы риски, которые необходимо учитывать для его будущего применения в питании и медицине.
Ресвератрол, метаболиты, микробиота, метаболические пути, молекулярные механизмы действия, о-хинон
Короткий адрес: https://sciup.org/170211530
IDR: 170211530 | УДК: 616-092.9
Resveratrol: metabolism, biological mechanisms, and potential side effects
Resveratrol, a natural stilbenoid found in grapes, berries, and other plants, has attracted significant scientific interest due to its broad spectrum of reported health benefits, including antioxidant, anti-inflammatory, anti-aging, and cardioprotective properties. This review synthesizes current knowledge on resveratrol, exploring its complex pharmacokinetics — characterized by high absorption but low oral bioavailability resulting from extensive presystemic metabolism—and its multifaceted mechanisms of action. We detail the activation of key signaling pathways such as SIRT1, AMPK, Nrf2, and PGC-1α, which mediate its effects on mitochondrial biogenesis, antioxidant defense, and metabolic homeostasis. A special focus is placed on the crucial role of gut microbiota in metabolizing resveratrol into active derivatives like dihydroresveratrol and lunularin, which contribute significantly to its biological effects and modulate gut health. Paradoxically, the review also addresses the compound’s potential adverse effects, examining how its oxidation into a reactive quinone form can lead to pro-oxidant effects, genotoxicity, disruption of cellular signaling, and endocrine disruption. This comprehensive analysis underscores the dual nature of resveratrol, highlighting both its therapeutic potential and the dose-dependent risks that must be considered for its future application in nutrition and medicine.
Текст научной статьи Ресвератрол: метаболизм, биологические механизмы и возможные побочные эффекты
Введение. Ресвератрол, природный фитоалексин, впервые выделенный в 1940-х годах, представляет собой стильбеноид, синтезируемый растениями в ответ на стрессовые воздействия, такие как грибковая инфекция или ультрафиолетовое облучение. Польза ресвератрола для здоровья впервые была отмечена в начале 1990-х годов с тех пор ресвератролу были приписаны многочисленные фармакологические свойства, включая антиоксидантные, противовоспалительные, противоопухолевые, кардио- и нейропротекторные. Однако его применение затруднено из-за низкой биодоступности нативного соединения. Это связано с интенсивным пресистемным метаболизмом, в ходе которого в энтероцитах и печени образуются конъюгированные производные — глюкурониды и сульфаты. Эти метаболиты, а также новые биологически активные соединения, такие как дигидроресвератрол и лунуларин, образующиеся под действием микробиоты кишечника, во многом опосредуют конечные эффекты ресвератрола. Более того, микробиота не только метаболизирует ресвератрол, но и сама становится мишенью для его действия, что проявляется в улучшении состава микробного сообщества и укреплении кишечного барьера. Механизмы положительного воздействия ресвератрола сложны и включают активацию ключевых клеточных путей: SIRT1, AMPK, Nrf2 и PGC-1α, что ведет к усилению митохондриального биогенеза, антиоксидантной защиты и подавлению воспаления. В то же время, при высоких концентрациях ресвератрол демонстрирует способность окисляться до высокореактивного хинона. Эта форма инициирует каскад негативных эффектов, вклю- чая про-оксидантную активность, ковалентную модификацию белков, митохондриальную дисфункцию, генотоксичность и эндокринные нарушения. Таким образом, ресвератрол представляет собой соединение с выраженным дуализмом действия, где его конечный эффект зависит от множества факторов. Цель данного обзора — интегрировать разрозненные данные о фармакокинетике, механизмах действия, роли микробиоты и потенциальных рисках ресвератрола, чтобы предоставить целостное представление о его потенциале и ограничениях как объекта для нутрицевтического и терапевтического применения.
Адсорбция и метаболизм. Концентрации ресвератрола для обычных пищевых продуктов: арахис, оставшийся от оболочек семян содержит до 0,29 мг / л; в различных розовых винах 0,03-0,14 мг / г; так же он может быть извлечен из красного винограда приблизительно 92-1604 мг / кг; содержание в красных винах колеблется в пределах 0,361–1,972 мг / л; в кожице томатов 19 мг / г; концентрация в пиве колеблется в пределах 1,34–77,0 мг /л; в темный шоколаде 350 мг / кг; молочном шоколаде 100 мг / кг; чае Итадори 68 мг / 100 мл; в белых винах 0-1,089 мг / л; может быть выделен из белого винограда 59-1759 мг / кг и яблок 400 мг / кг свежего веса [1].
Исследование показало наличие ресвератрола в темпе, индонезийском блюде из ферментированных соевых бобов. В ходе исследования из темпе было извлечено 65,15 % ресвератрола, а из оболочки соевых бобов — 55,35 %. Кроме того, исследование показало, что ферментация соевых бобов при производстве темпе, вызванная присутствием типичных ферментирующих бактерий, приводит к повышению уровня транс-ресвератрола [2].
Значительное накопление транс-ресвератрола наблюдалось после обрезки побегов виноградной лозы, при этом максимальное увеличение составило 181 раз на 70-й день. Значительное увеличение содержания транс-ресвератрола в образцах побегов винограда можно объяснить действием структурных генов PAL, C4H, 4CL и STS , которые контролируют выработку транс-ресвератрола. Считается, что транс-форма накапливается до тех пор, пока ткани не высохнут, поскольку живые ткани растений могут воспринимать процесс высыхания во время хранения как сигнал о стрессе, что приводит к выработке ресвератрола [3].
Низкомолекулярные стильбены, такие как ресвератрол, преимущественно транспортируются в толстый кишечник, хотя небольшая часть полифенолов, содержащихся в пище, всасывается в тонком кишечнике. В процессе метаболизма сульфаты, глюкурониды и другие конъюгированные формы ресвератрола выводятся из кишечника с помощью белка-переносчика, устойчивого к раку молочной железы (BCRP). Сообщалось, что они могут попадать в просвет кишечника через белок множественной лекарственной устойчивости 2 (MRP2) на апикальной мембране и проникать в системный кровоток через MRP3 на базолатеральной мембране. Значительная часть принятого внутрь ресвератрола (примерно 70–75 %) подвергается метаболизму в кишечнике и микробиотой кишечника, при этом 25 % выводится без всасывания, и только 1–8 % попадает в кровоток. Неметабо-лизированный ресвератрол трудно обнаружить в плазме крови. По приблизительным оценкам, пиковые концентрации менее 10 нг/мл наблюдались в течение 0,5–2 часов после перорального приема.
Биодоступность ресвератрола значительно снижается при его приеме в пищу, особенно в контексте высокожировой диеты. Натуральные компоненты винограда, в составе которых присутствует ресвератрол, демонстрируют превосходство в усвоении над таблетированными формами, что свидетельствует о роли пищевой матрицы в оптимизации абсорбции [4].
Было обнаружено, что ресвератрол в таблетированной форме значительно дольше сохраняется в организме, что, в свою очередь, приводит к повышению уровня метаболитов [5]. Метаболиты ресвератрола имеют первостепенное значение ввиду того, что отдельные их представители, в частности дигидроресвератрол и лунуларин, проявляют высокую антиоксидантную активность. Важно подчеркнуть тот факт, что дигидроресвератрол, как было доказано, обладает более эффективными антиоксидантными свойствами, чем витамин Е [6].
В пищевых продуктах ресвератрол присутствует в основном в гликозилированной форме, известной как пицеид и полидатин [7]. После попадания в организм ресвератрол проходит через желудочно-кишечный тракт, при этом степень его усвоения составляет около 70 %. В кишечнике ресвератрол связывается с различными питательными веществами, что влияет на его способность к усвоению [8].
Однако свободная форма ресвератрола достигает низкой концентрации в крови, поскольку метаболизируется в основном в печени посредством процессов глюкуронизации и сульфатирования. Сульфат ресвератрола-3 и глюкуронид ресвератрола-3 были обнаружены в различных органах и тканях, таких как печень, жировая ткань и сердце. Кроме того, ресвератрол может метаболизироваться в другие производные, такие как пицеатаннол и дигидроресвератрол. Пицеатаннол образуется в результате гидроксилирования ресвератрола в печени, а дигидроресвератрол — в результате метаболизма кишечными бактериями [9].
Главным сайтом абсорбции ресвератрола при пероральном приеме является тонкий кишечник, в первую очередь, его верхние отделы (двенадцатиперстная и тонкая кишка). Энтероциты становятся главными клетками в этом процессе [10].
Проникновение ресвератрола в энтероциты осуществляется двумя основными путями. Главным образом ресвератрол попадает в энтероциты диффузией, будучи липофильным полифенолом, ресвератрол способен пассивно диффундировать через клеточные мембраны по градиенту концентрации. Этот процесс не требует затрат энергии и является основным путем его поступления в энте-роциты [10].
Существуют данные, указывающие на возможное участие мембранных транспортеров. Предполагается, что некоторые белки семейства ABC (ATP-binding cassette), такие как P-гликопротеин (P-gp/ABCB1), могут взаимодействовать с ресвератролом. Однако их роль двойственна, они могут как облегчать его поступление, так и выбросить его обратно в просвет кишки, что вносит вклад в сложную кинетику его абсорбции [10]. Попав в энтеро-циты, ресвератрол подвергается интенсивному ме- таболизму второй фазы, что ограничивает его биодоступность в организме. В цитозоле энтероцитов сосредоточены высокие концентрации ферментов конъюгации, например УДФ-глюкуронозилтранс-феразы (UGT), в частности UGT1A1 и UGT1A9, катализируют присоединение глюкуроновой кислоты с образованием ресвератрол-3-O-глюкурони-да (R3G) и других изомеров. Так же присутствуют Сульфотрансферазы (SULT), такие как SULT1A1 и SULT1A3, присоединяют сульфатную группу с образованием ресвератрол-сульфатов (например, ресвератрол-3-сульфата) [11].
Образованные в процессе полярные конъюгаты (глюкурониды и сульфаты) далее могут секретироваться обратно в просвет кишечника с помощью транспортеров, таких как MRP2 (ABCC2), расположенных на апикальной мембране. Или же могут транспортироваться через базолатеральную мембрану в портальный кровоток с помощью транспортеров типа MRP3 [10].
Только незначительная часть неизмененного (нативного) ресвератрола, и значительная доля его метаболитов, покидают энтероцит через базолатеральную мембрану и поступают в капилляры кишечника, а затем через воротную вену направляются в печень, где подвергаются дальнейшему метаболизму. Именно данный путь метаболизма является основной причиной чрезвычайно низкой биодоступности свободного ресвератрола (менее 1 %), в то время как в кровотоке преобладают его метаболиты, свободный ресвератрол составляет всего около 0.28 % от общего содержания ресвератрола и его метаболитов в крови [12].
Ресвератрол, обладая высокой степень абсорбции в ЖКТ (70-75%), характеризуется очень низкой биодоступностью в его свободной форме (<1%) из-за интенсивного пресистемного и печеночного метаболизма. Его фармакокинетический профиль отличается быстрой абсорбцией, сверхкоротким периодом полувыведения нативного соединения (8-14 мин) и значительно более длительной циркуляцией его основных метаболитов — глюкуронидов и сульфатов, от 30 минут и до 9 часов. Биотрансформация осуществляется преимущественно в энтероцитах и гепатоцитах с участием ферментов конъюгации UGT и SULT.
После перорального приема ресвератрол характеризуется относительно быстрой абсорбцией. Его пиковая концентрация (максимальная концентрация в системном кровотоке) достигается относительно быстро, в интервале от 0.8 до 1.5 часа после приема. Что указывает на очень эффективное всасывание в верхних отделах желудочно-кишечного тракта [12]. Так же стоить отметить относительно короткий период полувыведения. Фармакокинетика ресвератрола отличается очень быстрой элиминацией нативного вещества, но при этом его метаболиты ещё длительное время продолжают циркулировать в крови.
Свободный (нативный) ресвератрол обладает очень низким периодом полувыведения и составляет от 8 до 14 минут. Что свидетельствует о его интенсивном и быстром метаболизме [12]. Как уже упоминалось ранее метаболиты ресвератрола (сульфаты и глюкурониды) обладают значительно более длительным периодом полувыведения относительно ресвератрола, период полувыведения метаболитов может превышать 9 часов. Несмотря на быструю элиминацию исходного соединения, его производные остаются в системном кровотоке продолжительное время [12].
Исследования показывают, что в пищеварительной системе может усваиваться до 70–75% от принятой дозы ресвератрола. Такой высокий процент абсорбции, не приводит к высокой биодоступности ресвератрола т.к. большая часть всосавшегося ресвератрола незамедлительно подвергается пресистемному метаболизму в энтероцитах. При попадании в кровь, через воротную вену нативный ресвератрол попадает в печень, где подвергается дальнейшему метаболизму, вместе с метаболитами [12].
В результате биотрансформации в организме образуются в основном конъюгированные производные, в то время как концентрация свободного ресвератрола в плазме остаётся крайне мала.
Самими многочисленными производными ресвератрола являются:
Ресвератрол-3-O-глюкуронид (R3G): Основной метаболит, обнаруживается в плазме крови [11].
Ресвератрол-сульфаты (напр., ресвера-трол-3-сульфат): являются другим ключевым классом метаболитов, циркулирующих в системном кровотоке [12; 13].
Пицеатаннол: является продуктом окисления, катализируемого CYP450. Пицеатаннол сам по себе обладает биологической активностью и может вносить вклад в общие фармакологические эффекты.
Взаимодействие с микробиотой. Термин «микробиом человека» используется для обозначения триллионов микроорганизмов, которые обитают внутри нашего организма и на нашей коже. Со временем стало очевидно, что микробиота играет ключевую роль в формировании здоровья человека, влияет на течение болезней и регулирует физиологию хозяина [14].
В кишечнике человека преобладают бактерии двух основных групп: Firmicutes и Bacteroidetes. Также встречаются Proteobacteria и Actinobacteria. То, что мы едим, очень сильно влияет на то, какие бактерии живут в нашем кишечнике, потому что еда служит им пищей – одни бактерии от нее растут лучше, а другие – хуже. Поэтому, когда состав бактерий в кишечнике меняется, меняется и то, какие вещества они производят.
Многие исследования показали, что изменения в составе микробиоты кишечника и соотношении метаболитов связаны с различными заболеваниями, такими как нейродегенеративные заболевания [14], диабет [15], рак [16] и сердечно-сосудистые заболевания [17].
Исследования показали, что некоторые представители микробиоты кишечника, такие как Bac-teroidetes , Actinobacteria , Verrucomicrobia и Cyanobacteria , могут преобразовывать ресвератрол в 3,4′-дигидроксибибензил (лунуларин), в то время как Slackia equolifaciens и Adlercreutzia equolifa-ciens могут вырабатывать дигидроксиресвератрол и лунуларин [18].
Метаболизм ресвератрола в такие соединения как лунуларин и дигидроксиресвератрол имеет так же экспериментальное подтверждение. Группа американских исследователей, обнаружили ди-фицит данных соединений у мышей, получавших антибиотики широкого спектра действия. [19]
Так же, было обнаружено, что кишечные бактерии могут гидролизовать глюкозидную форму ресвератрола, пицеид, с образованием ресвератрола и наоборот [7]. Была открыта способность некоторых бактерий, в частности Bifidobacteria infanti и Lactobacillus acidophilus, синтезировать ресвератрол из пицеида [20; 21].
Ресвератрол и его предшественники могут метаболизироваться микробиотой кишечника с образованием метаболитов ресвератрола. Одним из первых идентифицированных метаболитов, производных ресвератрола, стал дигидроресвератрол, который вырабатывается, например такими микроорганизмами как Slackia equolifaciens и Adlercreutzia equolifaciens. [9] В последующем были выделены 3,4′-дигидрокси-транс-стильбен и 3,4′-дигидроксибибензил (лунуларин) [22]. Кроме того, дополнительные исследования показали, что за выработку пицеида отвечают другие бактерии, такие как Bacillus cereus, B. Infantis и L. Acidophilus [21]. Кишечные бактерии также могут метаболизировать пицеид с образованием дигидропицеида и дигидроресвератрола [23].
Влияние ресвератрола на кишечник и микробиоту. Дисбиоз кишечной микробиоты ассоциирован с этиопатогенезом широкого спектра хронических заболеваний. Исследования, посвященные изучению влияния изменений в составе и функциях микробиоты кишечника на здоровье человека, представляют собой активно развивающуюся область биомедицинских исследований. Экспериментальные модели, позволяющие изучать модуляцию микробиоты и ее влияние на течение заболеваний, являются важным инструментом для получения новых знаний.
Обширные исследования показали, что ресвератрол и его различные метаболиты способны положительно влиять на здоровье кишечника. Исследования на мышах показали, что добавление ресвератрола в рацион усиливает экспрессию белков zonula occludens 1 (ZO-1), zonula occludens 2 (ZO-2), окклюдина, молекулы адгезии плотных контактов A (JAM-A), муциновых белков (MUC 1 и MUC 2) и кателицидинов [24]. Это белки плотных контактов, повышенная экспрессия которых, как известно, благоприятно влияет на барьерную функцию слизистой оболочки.
Добавки с ресвератролом увеличивали высоту ворсинок тощей кишки, тем самым улучшая морфологию кишечника, что было продемонстриро-ванно в исследовании на примере поросят [25].
Экспериментальные данные, полученные в ходе изучения мышей с неалкогольным стеатозом печени, индуцированным рационом с высоким содержанием липидов, продемонстрировали, что ресвератрол вызывал статистически значимое удлинение ворсинчатого аппарата подвздошной кишки [24].
Представленные сведения способствуют оценке воздействия ресвератрола на кишечную морфологию, принимая во внимание фундаментальную роль кишечных ворсинок в процессах нутриент-ной абсорбции и транслокации.
Цю и др. продемонстрировали увеличение количества бактерий рода Roseburia в кишечнике поросят, получавших ресвератрол [25]. Значение данных микроорганизмов заключается в том, что эта бактерия играет ключевую роль в предотвращении патогенных инфекций и уменьшении воспаления в кишечнике.
Ресвератрол уменьшает фиброз печени, вызванный CCl4, подавляя рост Staphylococcus xylosus и Staphylococcus lentus. Staphylococcus был выявлен как преобладающий патоген у пациентов с хроническими заболеваниями печени и часто связан с возникновением муковисцидоза [27]. Способность ресвератрола взаимодействовать с микроорганизмами даёт положительные результаты, выходящие за рамки здоровья кишечника.
Биологическая активность ресвератрола и его метаболитов: механизмы действия и фармакологические свойства. Биологическая роль ресвератрола не ограничена воздействием его нативной формы. Как было приведено ранее, лишь мизерная доля поглощённого ресвератрола остаётся в кровотоке неизменной (не более 1%), в то время как его метаболиты продолжают циркулировать в организме. Из чего стоит сделать вывод, о том, что основную роль в оказании эффекта играет не сам ресвератрол, а его метаболиты.
Экспериментальные данные демонстрируют наличие самостоятельной биологической активности у метаболитов ресвератрола, в частности ресвера-трол-сульфатов. Было установлено, что они обладают антиоксидантной и противовоспалительной активностью, и способны модулировать клеточные сигналы [28].
Также было установлено, что сульфатированные формы метаболитов ресвератрола могут модулировать ферментативную активность, а конкретно обратимо связываться с цитохромом P450, снижая их активность, и потенциально усиливая эффект других лекарственных средств путём снижения их метаболизма, и увеличения времени полувыведения [28]. Так же Генри, К., и Витрак, Х. с коллегами установили, что ресвератрол-сульфаты влияют на активность транспортных белков таких как Р-гликопротеин, снижая их активность, что может приводить к увеличению не только эффекта используемых совместно препаратов, но и привести к повышению цитотоксичности лекарственных средств.
Ресвератрол, верее его метаболиты, оказывают поливалентное действие на ряд ферментов отвечающих за метаболизм экзогенных токсинов, например ингибирование цитохромов P450 (Фаза I метаболизма). Подробный обзорный анализ подтверждает, что нативный ресвератрол является ингибитором ряда изоформ CYP, в частности CY-P1A1, CYP1B1, CYP1A2 и других [11]. Что делает ресвератрол, и его метаболиты (в том числе пицеа-таннол), теоретически применимыми в модуляции фармакокинетики препаратов метаболизируемых цитохромами.
Так же было установлено, что ресвератрол и его метаболиты способны индуцировать ферменты второй фазы метаболизма. Параллельно с ингибированием ферментов первой фазы, ресвератрол способен индуцировать экспрессию и активность ферментов фазы II, таких как глутатион-S-транс-феразы (GST) и UGT. Это приводит к усилению конъюгации и ускоренному выведению потенциально токсичных соединений [11].
Обзор существующих данных позволяет утверждать, что основные метаболиты — ресвера-трол-сульфаты, ресвератрол-глюкурониды и продукт окисления пицеатаннол — не только являются субстратами для этих ферментных систем, но и могут самостоятельно регулировать их активность.
SIRT1. Одним из центральных механизмов действия ресвератрола является активация сиртуина 1 (SIRT1) — NAD ⁺-зависимой деацетилазы класса III. Молекулярный механизм активации SIRT1 ресвератролом был предметом интенсивных исследований и дискуссий. Современные данные показывают, что ресвератрол действует как стабилизатор белково субстратных взаимодействий, особенно для субстратов, содержащих объемные гидрофобные группы в положении 1 относительно ацетилированного лизина [29].
Кристаллографические исследования выявили, что три молекулы ресвератрола могут связываться с Nтерминальным доменом SIRT1, опосредуя взаимодействие между ферментом и субстратом. Ресвератрол не изменяет конформацию самого SIRT1, а создает дополнительные карманы связывания для объемных гидрофобных групп субстра- тов, восстанавливая прочное связывание между SIRT1 и определенными «слабосвязывающимися» субстратами [29].
Активация SIRT1 также возможна через ингибирование ресвератролом ферментов семейства фосфодиэстераз ( PDEs), Ресвератрол активирует сигнальный путь цАМФ/Epac1 за счет ингибирования PDE, что приводит к высвобождению Ca2+, в конечном итоге, к активации пути CamKKβ-AMPK, AMPK увеличивает биогенез и функцию митохондрий за счет увеличения уровня NAD+, что приводит к повышению активности SIRT1 [30; 31].
Ось PGC1α и митохондриальный биогенез. Ресвератрол индуцирует митохондриальный биогенез через активацию оси PGC1α (коактиватор1α рецептора, активируемого пролиферацией пероксисом). PGC1α является ключевым регулятором митохондриального биогенеза и функции, координирующим экспрессию ядерных и митохондриальных генов. SIRT1 деацетилирует PGC1α в ядре, предотвращая его убиквитинирование и деградацию, тем самым поддерживая высокие уровни экспрессии PGC1α в ядре и опосредуя митохондриальный биогенез [32].
Ресвератрол увеличивает экспрессию PGC1α и способствует его ядерной транслокации. Активированный PGC1α затем регулирует экспрессию NRF1 (ядерного респираторного фактора 1) и NRF2 (ядерного респираторного фактора 2), которые в свою очередь активируют TFAM (митохондриальный транскрипционный фактор A. TFAM необходим для репликации и транскрипции митохондриальной ДНК. Недавние исследования показали, что активация PGC1α ресвератролом происходит через PRKAA1 AMPK α1). При нокдауне PRKAA1 эффект ресвератрола на активацию PG-C1α значительно снижается, что указывает на то, что PRKAA1 является ключевым геном, опосредующим активацию PGC 1α ресвератролом [33].
Активация Nrf2 и антиоксидантная защита. Ресвератрол активирует транскрипционный фактор Nrf2 (ядерный фактор, связанный с эритроидным фактором 2) - ключевой регулятор внутриклеточного окислительно восстановительного баланса и антиоксидантной защиты. При окислительном стрессе Nrf2 транслоцируется в ядро и связывается с антиоксидант-респонсивными элементами (ARE) в генах, кодирующих антиоксидантные ферменты, такие как NADPH хинон оксидоредуктаза (NQO1), гемоксигеназа1 (HO1) и супероксиддисмутазы 1 и 2 (SOD1 и SOD2) [34].
Ресвератрол может потенцировать сигнализацию Nrf2 через блокаду Keap1 Kelch подобный ECHассоциированный белок 1), изменение медиаторов Nrf2, его экспрессии и ядерной транслокации. Исследования показали, что ресвератрол увеличивает экспрессию Nrf2 как в общем, так и в ядерном белке дозозависимым образом. Эффект ресвератрола на Nrf2 частично опосредован PI3K/ Akt и ERK1/2 сигнальными путями. Фармакологические ингибиторы PI3K LY294002 и MEK1/2 U0126 ослабляют индуцированную ресвератролом экспрессию HO1 [35; 36; 37].
NFκB сигнальный путь и противовоспалительное действие. Ингибирование NFκB пути ресвератролом тесно связано с активацией AMPK и SIRT1. Исследования показали, что ингибирование AMPKα или SIRT1 значительно снижает эффект ресвератрола на подавление NFκB пути, индуцированного высоким содержанием неэсте-рифицированных жирных кислот. Таким образом, ресвератрол снижает воспалительный ответ и улучшает патологические состояния через активацию пути AMPKα-SIRT1 с последующим ингибированием NFκB [38; 39].
Подавление NFκB приводит к снижению экспрессии множественных провоспалительных генов, включая COX2 (циклооксигеназу2), iNOS (индуцибельную NOсинтазу), TNFα (фактор некроза опухоли альфа), IL1β (интерлейкин1 бета), IL6 (интерлейкин6) и ICAM1 (молекула межклеточной адгезии1). Ресвератрол также уменьшает транслокацию HMGB1 (белка группы высокой подвижности 1) из ядра в цитоплазму, что важно для подавления воспалительного ответа [40; 41].
AMPK. Ресвератрол является мощным активатором AMPактивируемой протеинкиназы (AMPK) ключевого энергетического сенсора клетки. По мимо уже описного пути CamKKβ-AMPK, Активация AMPK происходит преимущественно через LKB1зависимый механизм [42; 43; 44].
Активированная AMPK фосфорилирует множественные нижестоящие мишени, включая аце-тил-КоА-карбоксилазу (ACC), что подтверждается увеличением фосфорилирования ACC после обработки ресвератролом. AMPK ингибирует АТФ-по-требляющие анаболические процессы и стимулирует АТФ-генерирующие катаболические пути для восстановления энергетического баланса клетки. [42,43]. Взаимная активация SIRT1 и AMPK вероятно связана с активацией SIRT1 пути LKB1/ AMPK, что приводит к повышению NAD+ и повы- шению активности SIRT1, образуя петлю обратной положительной связи между SIRT1-AMPK [42], представлен на рисунке 1.
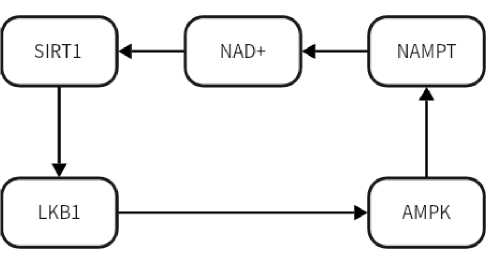
Рис. 1. Положительная обратная связь AMPK-LKB1
Fig. 1. Positive feedback AMPK-LKB1
Активация AMPK приводит к ингибированию mTOR (мишень рапамицина у млекопитающих) и ERK (внеклеточная сигнал-регулируемая киназа) сигнальных путей. Ресвератрол снижает фосфорилирование ERK и его нижестоящей мишени eIF4E (эукариотический фактор инициации трансляции 4E, а также подавляет активность mTOR пути, включая снижение фосфорилирования S6K (киназа рибосомального белка S6 и 4E BP1 (связывающий белок eIF4E 1). Эти изменения приводят к снижению кэп-зависимой трансляции белков и ингибированию клеточного роста [43].
Прямое ингибирование mTOR и индукция аутофагии. Недавние исследования выявили, что ресвератрол может напрямую ингибировать mTOR, связываясь с АТФ-связывающим карманом киназного домена mTOR, т.е. конкурируя с АТФ. In vitro киназные анализы показали, что ингибирование mTOR ресвератролом восстанавливается при добавлении АТФ, что подтверждает АТФ-кон-курентный механизм [45]. Помимо прямого ингибирования mTOR, ресвератрол через активацию AMPK также влияет на mTOR путь, поскольку AMPK прямо фосфорилирует ULK1 по серинам 555 и 317, что активирует аутофагию [45; 46; 47].
Регуляция PI3K/Akt сигнального пути. Ресвератрол оказывает двойственное действие на путь PI3K/Akt в зависимости от клеточного контекста и концентрации. В раковых клетках ресвератрол преимущественно ингибирует путь PI3K/Akt, что приводит к индукции апоптоза и остановке клеточного цикла. Ресвератрол подавляет PI3K/Akt сигнализацию главным образом путем ингибирования двух фосфорилированных субъединиц
PI3K — регуляторного домена p85 и каталитического домена p110, что приводит к каскаду событий, ингибирующих PIP2, PIP3 и PDK1 [48; 49; 50].
Ресвератрол также ингибирует комплекс MTA1/ HDAC1, что приводит к реактивации PTEN (фосфатаза и гомолог тензина) и последующему подавлению пути Akt. PTEN действует как негативный регулятор пути PI3K/Akt, дефосфорилируя PIP3 и превращая его в PIP2. Исследования показали, что обработка ресвератролом или ингибитором PI3K LY294002 очевидно снижала экспрессию p-AKT и AKT, что далее приводило к повышению регуляции p53 и снижению регуляции циклина B1, что приводило к остановке клеточного цикла на стадии G2/M [49].
В контексте защиты от ишемического повреждения ресвератрол может активировать путь PI3K/ Akt. Активация Akt ресвератролом приводит к фосфорилированию и инактивации GSK3β (гли-коген-синтаза-киназа3β), ключевой нижестоящей мишени пути PI3K/Akt. Фосфорилирование GSK3β по серину 9 инактивирует киназу и предотвращает её проапоптотическую активность. Ишемическое повреждение, вызванное окклюзией средней мозговой артерии (MCAO), снижает уровни фосфо-GSK3β, а ресвератрол ослабляет эти снижения. GSK3β индуцирует гибель клеток путем увеличения активности каспазы3 при ишемическом повреждении, поэтому фосфорилирование GSK3β киназой Akt является критическим процессом для ингибирования её проапоптотической активности [48; 50; 51].
Модуляция JAK/STAT сигнального пути. Ресвератрол ингибирует сигнальный путь JAK/STAT Janus киназа/преобразователь сигнала и активатор транскрипции) — важный механизм передачи сигнала в клетках, который тесно связан с клеточным окислительным стрессом, секрецией воспалительных цитокинов и регуляцией иммунного ответа. Связывание лиганда с рецептором индуцирует трансфосфорилирование JAK, активированная JAK вызывает фосфорилирование тирозина связанного рецептора, формируя сайт стыковки для STAT. На этом сайте стыковки JAK фосфорилирует STAT, а затем STAT диссоциирует от рецептора и формирует гомодимеры или гетеродимеры через взаимодействия SH2домен-фосфотирозин [52; 53; 54; 55].
Исследования на модели атеросклероза у крыс показали, что после введения ресвератрола JAK1 и STAT5позитивное окрашивание в артерии крысы было значительно меньше, и наблюдалось определенное снижение уровней мРНК (P 0,033, P 0,027) и белка генов JAK1 и STAT5 P 0,026, P 0,032. Это свидетельствует о том, что ресвератрол может улучшать липидный профиль крови у крыс с атеросклерозом, снижать воспалительный ответ in vivo и ингибировать белки, связанные с сигнальным путем JAK/STAT. In vitro исследования на клетках HT29 показали, что ресвератрол, используемый в концентрации в 20 раз ниже, чем 5аминосалициловая кислота, способен значительно снизить продукцию NO и PGE ₂. Ресвератрол снижает уровни активированного STAT1 в ядре цитокин-стимулированных клеток HT29 более эффективно, чем 5ASA. Клетки предварительно инкубировались с 25 мкМ ресвератрола или 500 мкМ 5ASA, а затем подвергались воздействию комбинации цитокинов в течение 30 минут. Уровни фос-фо-STAT1 по Tyr701 анализировались в ядерных экстрактах методом вестерн блоттинга, и результаты показали значительное снижение в группе ресвератрола по сравнению с группой, стимулированной только цитокинами [52; 53].
Потенциальный вред ресвератрола и его метаболитов. В живых системах окисление ресвератрола может осуществляться несколькими ферментативными путями. Цитохромы P450, особенно CYP1B1, способны метаболизировать ресвератрол в пицеатаннол (3,3’,4’,5-тетрагидрок-си-трансстильбен), который обладает собственным катехольным фрагментом. Этот метаболит может подвергаться дальнейшему окислению с образованием соответствующего о-хинона. Данный процесс может проходить под воздействием изоформ цитохромов P450 - CYP3A4, CYP1A1 и меньшей степени путем гидроксилирование ресвератрол до 3,5,3,4-тетраоксистильбена и его последующем окислении. Микросомальные ферменты печени, содержащие флавопротеины, включая NAD(P)H:хинон оксидоредуктазу NQO2, также могут участвовать в редокс-циклировании ресвератрола, генерируя активные кислородные радикалы в процессе восстановления хинонов до гидрохинонов [58; 59; 73].
Важным является тот факт, что RES-хинон оказался чрезвычайно нестабильным и быстро распадается в олигомерный продукт. Эти олигомеры, демонстрируют про-оксидантную активность, окисляя восстановленный глутатион (GSH) в окисленную форму (GSSG), таким образом «выключая» глутатион из антиоксидантной системы генерируя окислительный стресс [56].
Еще один механизм образования RES-хинона связан с тирозиназой. Образования RES-хинона представляет из себя циклический процесс в первом этапе которого тирозиназа окисляет ресвератрол (группа в положении 4’) в орто-дифенол через реакцию гидроксилирования. При этом к ароматическому ядру добавляется гидроксильная группа и образуется пицеатаннол — дифенольный промежуточный продукт. На втором этапе пицеатаннол подвергается окислению через дифенолазную активность тирозиназы в соответствующий о-хинон, обозначаемый как RES-хинон (4-(3’,5’-дигидрок-си-транс-стиренил)-1,2-бензохинон) [75].
S-глутатионилирование и образование дисульфидных связей с цистеином под действием RES-хинона. Помимо прямого присоединения цистеина, о-хинон ресвератрола может опосредованно модифицировать белки через S-глутатионилирование — процесс, при котором восстановленный глутатион (GSH) ковалентно присоединяется к цистеиновым остаткам белка в результате редокс-реакций. Исследования показали, что RES-хинон индуцирует дисульфидное образование между двумя молекулами цистеина, как это было демонстрировано на рекомбинантной проте-инкиназе G1α (PKG1α), а также, что RES-хинон реактивен по отношению к N-ацетилцистеину, формируя диадъюнкты и триадъюнкты. Образование триадъюнкта является редким явлением для о-хи-нонов и указывает на высокую реактивность RES-хинона [56; 57; 60; 63].
Мишени RES-хинона среди белковых регуляторов апоптоза и АФК. Критической особенностью механизма действия о-хинона ресвератрола является его способность модифицировать специфические регуляторные белки через образование дисульфидных мостиков и ковалентных аддуктов. Keap1 содержит два высокореактивных цистеиновых остатка в своём домене, богатым тиолом. RES-хинон может алкилировать эти остатки приводя к конформационным изменениям Keap1, предотвращающим убиквитирование и деградацию Nrf2. Это может активировать антиоксидантный ответ на низких дозах, но при высоких концентрациях о-хинона избыточное алкилирование Keap1 приводит к патологической активации или инактивации этого пути вызывая ингибирование синтеза и концентрации ферментов, например, NQO1, GPX, TXNRD1, SRXN1 и TXN1 играющих основную роль в снижении активных форм кислорода и их продуктов в щитовидной железе [61; 62; 72].
I-каппа-B-киназа (IKK) и компоненты NF-κB сигнального пути также являются потенциальными мишенями для о-хинона. S-нитрозилирование IKKβ и прямая модификация его цистеиновых остатков могут подавлять или усиливать активацию NF-κB в зависимости от локализации и типа модификации, что может нарушить эндогенное регулирование воспаления, приводя к патологической дерегуляции иммунитета [61].
Генерация АФК под действием RES –хино-на. RES-хинон является мощным генератором активных форм кислорода через ряд механизмов. Во-первых, редокс-циклирование семихинона приводит к прямому восстановлению молекулярного кислорода в суперокисид (- O₂⁻). Во-вторых, о-хинон может взаимодействовать с цитохромом P450, который в процессе детоксикации генерируют дополнительные АФК. В-третьих, взаимодействие о-хинона с NOX может усилить высвобождение суперокисида [61; 64; 65].
Также RES-хинон приводит к истощению митохондриального GSH и инактивации MnSOD, что вызывает образование пероксинитрита (ONOO⁻) [67; 68].
Влияние RES-хинона на митохондриальные структуры. О-хинон и ресвератрол могут прямым образом взаимодействовать с компонентами дыхательной цепи. Исследования показали, что при низких концентрациях ресвератрол активирует комплекс I, связываясь с NADH дегидрогеназным модулем, что приводит к повышению активности NADH окисления. Однако при высоких концентрациях ресвератрол ингибирует комплекс I, при этом запуская открытие пор перемен проницаемости (mPTP) [66].
Сам о-хинон может действовать как альтернативный акцептор электронов, обходя комплекс III и напрямую передавая электроны цитохрому c. Таким образом разрывая окислительное фосфорилирование, снижая синтеза ATP и повышая утечку электронов с образованием суперокисида. В клетках со сниженной антиоксидантной защитой данный эффект может привести к перекисному окислению липидов [66].
Генотоксичность и повреждение ДНК при действии RES-хинона и ресвератрола. При высоких концентрациях ресвератрол может действовать как про-оксидант, индуцируя массивное повреждение ДНК через прямое воздействие активных кислородных видов и косвенное воздействие через нарушение репарационных механизмов.
Наиболее опасным повреждением являются двухцепочечные разрывы. [61; 69].
Ресвератрол и его о-хинонный метаболит способны ингибировать рибонуклеотидредуктазу. Это приводит к глобальному снижению доступности дезоксирибонуклеотидов и торможению S-фазы клеточного цикла. Одновременно, про-оксидантная активность о-хинона нарушает несколько путей репарации ДНК, включая базовую эксцизионную репарацию (BER) и нуклеотидную эксцизионную репарацию (NER) [61].
Было продемонстрировано, что ресвератрол может действовать как яд для топоизомеразы II, что приводит к неконтролируемым разрывам ДНК. При лечении раковых клеток ресвератром наблюдается активация р53-зависимого апоптоза [61; 70].
В лейкемических клеточных линиях (MOLT-4) лечение ресвератролом в дозе 100 микромолярных приводит к ярко выраженной фрагментации хромосомной ДНК, по средствам активации апопто-тических каспаз, особенно каспазы-3 и каспазы-9, и деградации ДНК нуклеазами. При этом в клетках солидных опухолей (MCF-7, HepG2) ресвератрол индуцирует ранний апоптоз без фрагментации ДНК [70].
Негативные эффекты о-хинона на эндокринную систему. Ресвератрол и его метаболиты проявляют выраженное антитиреоидное действие. Так при низких концентрациях подавляется экспрессия генов, ответственных за синтез гормонов щитовидной железы. К ним относятся натриевый/йо-дидный симпортер, тиреопероксидаза, тиреоглобулин, а также ядерные транскрипционные факторы TTF-1, TTF-2 и Pax8 [71].
При микромолярных концентрациях ресвератрол подавляет биосинтез стероидных гормонов снижая приток холестерина в митохондрии. Более того, было продемонстрировано, что ресвератрол подавляет каталитическую активность CYP17A1, фермента, необходимого для синтеза андрогенов и кортизола, в клетках карциномы надпочечников человека [72].
Заключение. Проведенный анализ демонстрирует, что ресвератрол является соединением с выраженным дуализмом действия, где его конечный эффект критически зависит от дозы и метаболического контекста.
С одной стороны, ресвератрол проявляет многогранный благоприятный потенциал. Его способность активировать ключевые сигнальные пути SIRT1, AMPK, Nrf2 и PGC-1α лежит в ос- нове усиления митохондриального биогенеза, антиоксидантной защиты и подавления воспаления через ингибирование NF-κB. Важнейшую роль в реализации этих эффектов играет микробиота кишечника, которая трансформирует ресвератрол в биологически активные метаболиты, такие как дигидроресвератрол и лунуларин, одновременно улучшая состав микробного сообщества и укрепляя кишечный барьер.
С другой стороны, применение ресвератрола ограничивается его сложной фармакокинетикой: высокой абсорбцией, но крайне низкой биодоступностью нативной формы из-за интенсивного пресистемного метаболизма в глюкурониды и сульфаты. Более того, при высоких концентра- циях ресвератрол проявляет про-оксидантные свойства. Окисляясь до высокореактивного RES-хинона, он инициирует каскад токсических эффектов: генерацию АФК, истощение глутатиона, ковалентную модификацию белков (Keap1, IKK), митохондриальную дисфункцию, генотоксичность и эндокринные нарушения.
Таким образом, перспективы дальнейшего изучения и применения ресвератрола лежат в поиске путей преодоления его низкой биодоступности, углубленном исследовании роли микробиоты и ее метаболитов, а также в точном определении безопасных и эффективных дозировок, учитывающих его дозозависимый двуликий характер.


