Риск онкогематологической патологии у детей персонала радиационно опасного производства
Автор: Соснина С.Ф., Кабирова Н.Р., Сокольников М.Э., Окатенко П.В.
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Анализ риска здоровью в гигиене
Статья в выпуске: 1 (25), 2019 года.
Бесплатный доступ
Преконцептивное облучение считается одним из потенциальных факторов риска гемолимфобластозов у детей облученных лиц. Когорта работников ПО «Маяк», первого предприятия ядерного цикла России, уникальна для расчета канцерогенного риска у потомков. Был оценен риск гемолимфобластозов среди потомков персонала ПО «Маяк» с использованием индивидуальных преконцептивных суммарных поглощенных доз. Ретроспективное исследование по методу «случай - контроль» в когорте проведено среди всех резидентов г. Озерска, расположенного вблизи ПО «Маяк». «Случаи» определены как гемолимфобластозы, диагностированные у лиц до 25-летнего возраста в 1949-2009 гг. (81 человек), «Контроли» подобраны с учетом пола, года рождения, возраста родителей при рождении ребенка (324 человека). Произведен расчет отношения шансов и избыточного относительного риска на единицу дозы внешнего гамма-облучения с 95%-ным доверительным интервалом с использованием программного модуля PECAN пакета EPICURE. Острый лейкоз занимал ведущие позиции в структуре гемолимфобластозов с преобладанием острых лимфолейкозов...
Преконцептивное радиационное воздействие на работников, потомки, дозовая зависимость, оценка риска, злокачественные новообразования лимфоидной и кроветворной тканей
Короткий адрес: https://sciup.org/142220664
IDR: 142220664 | УДК: 613.95: | DOI: 10.21668/health.risk/2019.1.03
The risk of oncohematological pathology in children of workers employed at radiation hazardous production
Preconceptive irradiation is considered to be a potential risk factor that can cause hemolymphoblastosis in children conceived and borne by irradiated parents. A population cohort that comprises workers employed at "Mayak" Production Association (Mayak PA), the first nuclear cycle enterprise, is a unique sampling to calculate a carcinogenic risk in their children. Our research goal was to assess risk of hemolymphoblastosis among children conceived and borne by workers employed at Mayak PA with individual preconceptive accumulated absorbed dozes. Data and methods. We performed retrospective research as per "case-control" study among all the people living in the city of Ozersk located near Mayak PA. Hemolymphoblastosis diagnosed in people younger than 25 in 1949-2009 (81 people) were considered to be "cases"; "controls were chosen taking into account sex, birth date, and parents' age when a child was borne (324 people). We calculated odds ratio and excessive relative risk per external gamma-radiation dose unit (ERR/Gy) with 95 % confidence interval; to do that, we applied PEGAN program module of EPICURE software...
Текст научной статьи Риск онкогематологической патологии у детей персонала радиационно опасного производства
Многочисленные экспериментальные исследования рассматривают преконцептивное облучение как фактор риска генетической нестабильности, изменения уровня полиморфизма ДНК и восприимчивости потомства к неопластическим процессам [1–5]. Цитогенетические эффекты в качестве предикторов онкологических заболеваний и возможность их трансгенерационной передачи в поколениях облученных лиц описаны в ряде публикаций [6–9]. В то же время эпидемиологическая оценка последствий преконцептив-ного облучения неоднозначна. Единых выводов об особенностях и закономерностях бластомогенного процесса у потомков лиц, подвергшихся воздействию ионизирующей радиации, не получено [10, 11].
Злокачественные новообразования (ЗНО) лимфоидной и кроветворной тканей являются наиболее распространенной онкопатологией среди детского населения [12, 13]. Возможная причинно-следственная связь между преконцептивным облучением родителей и гемолимфобластозами у потомков интересовала многих исследователей. В 90-е гг. прошлого столетия был опубликован целый ряд работ, посвященных проверке так называемой «гипотезы Gardner»: о том, что отцовское облучение до зачатия может быть причиной лейкемии и неходжкинской лимфомы у их детей [14]. В большинстве этих публикаций связь преконцептивного облучения родителей с детскими лейкозами не подтвердилась [15, 16]
Окатенко Павел Викторович – руководитель группы компьютерного и программного обеспечения, лаборатория радиационной эпидемиологии (e-mail: ; тел.: 8 (351) 307-69-03; ORCID iD: .
или была недостаточно убедительной из-за малого числа онкогематологических случаев [17,18]. Противоречивые результаты оценки эффектов родительского облучения и связанного с ним риска неопластических процессов у потомков продолжают вызывать научные споры [11, 19–21].
Производственное объединение «Маяк» (ПО «Маяк») – первое в стране предприятие атомной промышленности, введенное в эксплуатацию в 1948 г. и включающее в себя радиохимическое, реакторное, плутониевое производства и ряд вспомогательных подразделений. В первые годы работы ПО «Маяк» персонал, четверть которого составляли женщины репродуктивного возраста, мог подвергаться пролонгированному воздействию внешнего гамма-облучения и внутреннего альфа-облучения инкорпорированным плутонием-239 в значительных дозах. В связи с этим когорта работников ПО «Маяк» является одной из самых показательных в мире для оценки эффектов родительского облучения, в том числе анализа онкогематологической патологии у потомков.
Цель работы – оценить риск ЗНО лимфоидной и кроветворной тканей среди потомков персонала ПО «Маяк» с использованием индивидуальных преконцептивных суммарных поглощенных доз.
Материалы и методы. Ретроспективное исследование проведено на основе регистров, созданных и поддерживаемых в лаборатории радиационной эпидемиологии ЮУрИБФ:
-
– регистр персонала ПО «Маяк», включающий 36 036 человек, нанятых в 1948–2015 гг. на основные и вспомогательные заводы предприятия, и послуживший источником данных о профессиональном маршруте родителей;
-
– канцер-регистр, содержащий сведения о более чем 15 000 случаях рака, диагностированных с 1948 г. среди населения г. Озерска, – закрытого административно-территориального образования (ЗАТО), близлежащего к ПО «Маяк»;
– детский регистр, объединяющий 90 835 человек 1934–2009 г.р., родившихся в г. Озерске или приехавших в город в детском возрасте и проживших в городе не менее года.
Использован статистический метод «случай – контроль» в когорте; «случай» определен как пациент до 25-летнего возраста с гемолимфобластозом, а «контроль» как лицо того же возраста без этого диагноза. Группа «Случай» включала всех зарегистрированных с 1949 по 2009 г. в г. Озерске больных гемо-лимфобластозом до 25 лет (81 ребенок: 49 мальчиков и 32 девочки). Группа «Контроль» формировалась методом сопоставимых пар путем подбора к каждому ребенку с гемолимфобластозом четырех «контролей» из детского регистра с матчированием по полу, году рождения ребенка и возрасту родителей при рождении ребенка. Формирование групп проведено среди всего детского населения г. Озерска, что нивелировало другие вероятные мешающие факторы, как, например, возможное техногенное воздействие на городское население за счет проживания вблизи ПО «Маяк». Для исследуемого периода также были характерны единое качество медицинского обслуживания и однотипный рацион питания для детей в организованных коллективах ЗАТО. В итоге группа «Контроль» состояла из 324 детей без онкозаболевания (мальчиков – 196, девочек – 128).
После формирования групп были установлены факт и доза преконцептивного облучения родителей с использованием сведений из регистра персонала ПО «Маяк», картотек ликвидаторов аварии 1957 г., участников ликвидации последствий аварии на ЧАЭС, переселенцев с Восточно-Уральского радиоактивного следа, сведения о строительных, воинских подразделениях, персонал которых мог получить радиационное воздействие до зачатия ребенка. Индивидуальные дозы внешнего гамма-облучения персонала ПО «Маяк» предоставлены службой радиационной безопасности ПО «Маяк» из «Дозиметрической системы работников “Маяк-2008”» [22, 23].
Структура ЗНО лимфоидной и кроветворной тканей представлена согласно действующим в исследуемый период международным статистическим классификациям болезней девятого и десятого пересмотров [24, 25].
В исследовании применены следующие методы статистического анализа:
-
– сравнение частот при помощи критерия χ² и точного критерия Фишера, различия считали достоверными при p < 0,05;
-
– расчет отношения шансов (ОШ) с 95%-ным доверительным интервалом (ДИ);
– расчет избыточного относительного риска (ИОР) на единицу дозы внешнего гамма-облучения с 95%-ным доверительным интервалом, проведенный с использованием программного модуля PECAN пакета EPICURE [26]. Данные в таблице человеко-лет распределялись по полу, дате рождения ребенка, нозологической форме ЗНО, дате диагноза ЗНО. Учитывались суммарные преконцептивные дозы внешнего гамма-облучения матерей и отцов на все тело и отдельно на гонады. Индивидуальные дозы были разбиты на интервалы по 250 мГр с расчетом средней дозы для каждого промежутка. За фоновый уровень принята детская заболеваемость гемолимфобластоза-ми при отсутствии радиационного воздействия на родителей с учетом различий по достигнутому возрасту, полу, году рождения. Значения р -тестов на статистическую значимость были рассчитаны с помощью методов максимального правдоподобия, различия считались статистически значимыми при p < 0,05.
Характеристика групп с учетом преконцептив-ного облучения родителей на производстве представлена в табл. 1.
Каждая группа была разделена на две подгруппы: дети, чьи родители имели накопленные дозы преконцептивного облучения, и дети, родители
Таблица 1
Характеристика групп
Персонал, контактировавший с источниками ионизирующих излучений на производстве до зачатия ребенка, мог подвергаться сочетанному облучению (внешнее гамма- и внутреннее альфа-излучение). Большинство родителей в сравниваемых группах являлись работниками радиохимического и реакторного производств ПО «Маяк». В данной работе анализ зависимости ЗНО лимфоидной и кроветворной тканей у детей от родительской дозы внутреннего облучения за счет инкорпорации плутония-239 не проведен из-за малого числа лиц, прошедших мониторинг внутреннего альфа-облучения.
Результаты и их обсуждение. В течение 60-летнего периода наблюдения (1949–2009 гг.) среди всех детей с ЗНО лимфоидной и кроветворной тканей (81 человек) мальчики заболевали чаще – 49 (60,5 %). Преобладание среди заболевших гемо-лимфобластозами лиц мужского пола (соотношение полов 1,53: 1,0) согласуется с региональной, национальной и мировой статистикой [13, 27, 28]. Временные периоды 1980–1989 гг. и 1990–1999 гг. характеризовались наибольшим числом случаев онкогематоло- гической патологии среди детей (по 18 и 19 случаев соответственно). Средний возраст возникновения гемобластозов среди мальчиков достигал 11,5 г., среди девочек – 9,5 г. Структура ЗНО лимфоидной и кроветворной тканей среди всего детского населения г. Озерска за 60 лет наблюдения представлена на рис. 1.
Острый лейкоз был ведущим в структуре всех ЗНО лимфоидной и кроветворной тканей – 45 случаев (55,6 %) с преобладанием острого лимфобластного лейкоза (23 случая (51,1 %) всех острых лейкозов), что соответствует литературным данным [13, 27, 28]. Миелолейкоз составил 26,7 % (12 случаев) среди всех острых лейкемий. Моноцитарный лейкоз зарегистрирован однократно у 5-летнего мальчика, чей отец на реакторном производстве подвергся суммарному преконцептивному внешнему гамма-облучению гонад в дозе 210 мГр.
Острый лейкоз неуточненного клеточного типа отмечен среди 9 детей, что составило пятую часть всех детских лейкемий. Большинство из неуточнен-ных лейкемий было диагностировано в 1960–1980 гг., в эти годы идентификация подтипа острого лейкоза была невозможна из-за отсутствия гистохимических, иммунологических и цитогенетических методов исследования.
В структуре всех гемолимфобластозов второе место занимал лимфогранулематоз (18,5 % – 15 случаев). Средний возраст манифестации лимфогранулематоза составил 16,2 г. без гендерных различий. Среди диффузных неходжкинских лимфом зарегистрированы две опухоли Беркитта: у 8-летней девочки и 21-летнего юноши, родившихся от необлу-ченных преконцептивно родителей. В подкласс «Другие злокачественные новообразования лимфоидной и гистиоцитарной тканей» вошли гистиоци-тарные лимфомы, злокачественные гистиоцитозы, занимая 11,1 % (9 случаев) всех гемолимфобласто-зов среди детей ЗАТО.
Структура гемолимфобластозов среди потомков лиц, подвергшихся преконцептивному облучению на производстве, подобна описанной выше. Отмечено преобладание острых лейкозов (62,1 % – 18 случаев); ведущая роль лимфобластного лейкоза
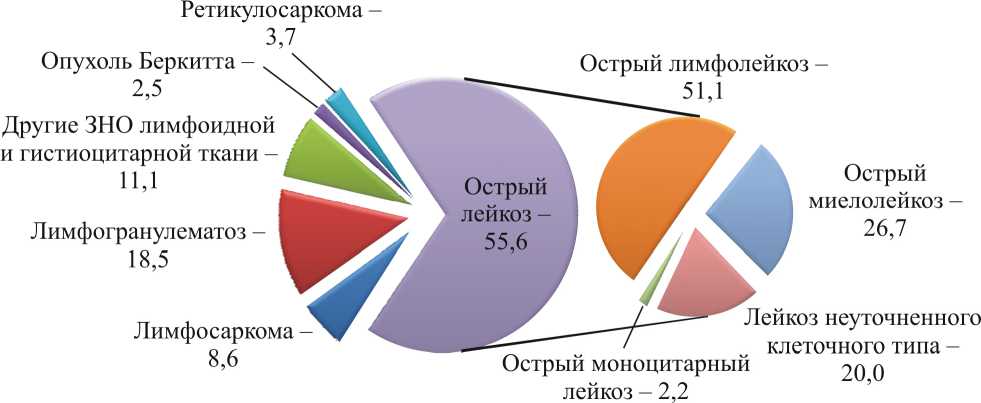
Рис. 1. Структура гемолимфобластозов (%) среди детей г. Озерска
Таблица 2
Характеристика преконцептивного внешнего гамма-облучения родителей
|
Доза внешнего |
Экспонированные родители в группе «Случай» |
Экспонированные родители в группе «Контроль» |
||
|
гамма-облучения, мГр |
отцы |
матери |
отцы |
матери |
|
Доза внешнего гамма-облучения на все тело |
||||
|
Средняя доза |
257,4 ± 122,9* |
244,3 ± 206,1 |
335,3 ± 52,4 |
458,1 ± 129,6 |
|
Медиана доз |
50,1 (19,5–177,6) ** |
42,1 (20,7–84,8) |
62,9 (25,0–325) |
125,5 (24,9–731,2) |
|
Диапазон доз |
2,7–3397,3 |
2,06–1272,9 |
0,3–3025,6 |
2,13–2797,8 |
|
Доза внешнего гамма-облучения на гонады |
||||
|
Средняя доза |
338,5 ± 188,3 |
275,2 ± 241,8 |
411,6 ± 70,4 |
452,9 ± 123,2 |
|
Медиана доз |
70,1 (37,9–210,2) |
49,5 (20,5–529,9) |
111,2 (31,2–337,7) |
127,7 (57,6–597,5) |
|
Диапазон доз |
4,33–3121,8 |
2,97–999,87 |
0,51–2899,3 |
2,83–2146,6 |
П р и м е ч а н и е : * – среднее квадратическое отклонение, ** – в скобках указан интерквартильный размах.
среди острых лейкемий (44,4 % – 8 случаев); мие-лобластный лейкоз занимал треть всех детских лейкемий (33,3 % – 6 случаев); диагностирован единичный случай моноцитарного лейкоза. Вклад лейкозов неуточненного клеточного типа несколько отличался – 16,7 % (3 случая) всех лейкемий. Доля лимфогранулематоза среди всех ЗНО лимфоидной и кроветворной тканей у потомков облученных была статистически незначимо выше, чем среди детей не облученных на производстве родителей (20,7 против 17,3 %, p > 0,05).
Следует отметить, что удельный вклад всех неоплазм лимфоидной ткани среди потомков облученных лиц не отличался от такового у детей интактных родителей (37,9 против 48,1 %, p > 0,05). Сравнение вклада лимфолейкоза и миелолейкоза в структуру онкогематологической патологии среди потомков экспонированных и неэкспонированных до зачатия родителей также показало отсутствие значимых статистических различий.
Существенной гендерной разницы в структуре ЗНО лимфоидной и кроветворной тканей среди потомков облученных родителей не найдено. Средний возраст возникновения ЗНО среди детей экспонированных лиц составил у мальчиков – 14,0 г., у девочек – 8,2 г.
В целом весомых отличий структуры детских гемолимфобластозов как среди потомков персонала атомного производства, так и среди всего детского населения ЗАТО от национальных и мировых статистических данных не найдено [13, 28].
Суммарные поглощенные дозы преконцептив-ного внешнего гамма-облучения родителей на производстве отличались широким диапазоном. Характеристика накопленных доз преконцептивного облучения представлена в табл. 2.
Средние суммарные поглощенные дозы пре-концептивного внешнего гамма-облучения родителей в группе детей без онкологической патологии превышали таковые у экспонированных родителей в группе «Случай». Однако максимальная прекон-цептивная доза внешнего гамма-облучения на все тело зафиксирована среди отцов в группе детей с онкогематологическим диагнозом и достигала 3397,3 мГр, в то время как максимальная доза среди матерей отмечена в группе «Контроль» и составила 2797,8 мГр.
Средние поглощенные дозы преконцептивно-го внешнего гамма-облучения на гонады у экспонированных родителей группы «Контроль» также преобладали над дозами облученных на производстве родителей группы «Случай». Лучевая нагрузка на гонады варьировалась в значительном диапазоне с наибольшей накопленной дозой около 3 Гр, зарегистрированной среди отцов в обеих группах: максимальная доза внешнего гамма-облучения на гонады в группе «Случай» достигала 3121,8 мГр, в группе «Контроль» – 2899,3 мГр.
Средние преконцептивные дозы внешнего гамма-облучения на гонады в некоторых случаях были более высокими, чем дозы на все тело, что объясняется, с одной стороны, неравномерным облучением персонала ПО «Маяк», с другой стороны, относительно малым числом индивидуальных доз на гонады среди персонала, и поэтому смещением средних оценок.
Распределение работников ПО «Маяк» по накопленной преконцептивной дозе внешнего гамма-облучения на все тело представлено на рис. 2.
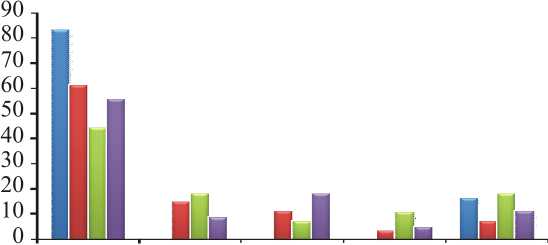
< 100 101-200 201-500 501-1000 >1000
Доза, мГр в Матери в основной группе н Матери в контрольной группе н Отцы в основной группе и Отцы в контрольной группе
Рис. 2. Распределение персонала ПО «Маяк» по суммарной преконцептивной дозе внешнего гамма-облучения на все тело (%)
Среди большинства облученных родителей накопленная доза не превышала 100 мГр. Преконцеп-тивное облучение матерей в группе «Случай» характеризовалось двумя крайними интервалами: от 2,06 до 100 мГр и свыше 1000 мГр. Матери в группе «Контроль» были представлены во всех дозовых категориях. Наименьшая доля отцов группы «Случай» подвергалась преконцептивному облучению в диапазоне доз 201–500 мГр, в то время как минимальное число отцов группы «Контроль» отмечалось в дозовой категории 501–1000 мГр. Распределение суммарных доз внешнего гамма-облучения до зачатия на гонады среди персонала ПО «Маяк» было аналогичным.
Большинство случаев ЗНО лимфоидной и кроветворной тканей у потомков облученных родителей отмечалось в диапазоне суммарных преконцеп-тивных доз внешнего гамма-облучения родителей на все тело до 500 мГр (79,3 % – 23 случая). Отмечено, что острый лейкоз диагностирован среди потомков при диапазоне доз родительского облучения 2,06–3397,3 мГр, со средней дозой на все тело 312,8 ± 170,8 мГр, на гонады – 391,5 ± 261,1 мГр. ЗНО лимфоидной ткани зарегистрированы в интервале родительских доз 2,7–1055,3 мГр, со средней дозой внешнего гамма-облучения на все тело 170,4 ± ± 78,4 мГр, на гонады – 233,7 ± 105,5 мГр.
С целью выявления статистической связи между фактором риска – преконцептивным облучением родителей на производстве – и исходом в виде ге-молимфобластозов у их детей проведен расчет показателя отношения шансов, представленный в табл. 3.
Результат ОШ в группах в целом – 0,76 (0,46–1,26) – показал отсутствие значимой статистической связи между родительским облучением и онкогематологической патологией у детей. Среди мальчиков показатель ОШ составил 0,81 (0,43–1,54), среди девочек – 0,69 (0,3–1,57), что также свидетельствует об отсутствии связи между фактором риска родительского облучения до зачатия и исходом у потомков в виде гемолимфобластозов.
Для выявления дозовой зависимости канцерогенного риска у потомков проведен анализ «доза – эффект» с расчетом величины избыточного относи- тельного риска гемолимфобластозов. В анализ были включены суммарные преконцептивные дозы родительского облучения на все тело и отдельно на гонады (табл. 4).
Оценка ИОР на основе линейной модели не показала статистически значимого увеличения заболеваемости гемобластозами в зависимости от дозы родительского облучения. Коэффициенты ИОР/Гр были незначимыми при анализе накопленной дозы внешнего гамма-облучения как на все тело, так и на гонады среди матерей и отцов-работников ПО «Маяк».
Продолжая дискуссию об индукции нестабильности генома при малых дозах радиации и учащения вследствие этого мутагенеза и канцерогенеза, А.Н. Котеров [29], рассматривая различные позиции авторов, отмечает результаты экспериментальных исследований, в которых не наблюдалось нестабильности генома при дозах менее 0,1–0,2 Гр, но вероятный порог для ее индукции составлял 0,5 Гр радиации с низким линейным переносом энергии.
Анализ наших данных с учетом дозовых категорий с интервалами преконцептивных доз по 250 мГр не показал какого-либо увеличения канцерогенного риска: в дозовых группах сохранялись статистически незначимые отрицательные оценки ИОР/Гр. В отдельных точках величина ИОР для гемолимфобла-стозов, соотнесенных с дозой внешнего гамма-облучения на гонады, имела неопределенность, связанную с небольшой статистикой.
Таким образом, предположение о повышенном риске ЗНО лимфоидной и кроветворной тканей, связанном с преконцептивным гамма-облучением родителей, в нашем анализе не подтвердилось.
В нашем исследовании было учтено влияние таких нерадиационных факторов, как пол, дата рождения ребенка, возраст родителей при рождении ребенка, возраст на момент диагноза ЗНО. Следует отметить, что к настоящему времени описаны многочисленные факторы, которые могут вызывать онкогенные процессы в кроветворной и лимфатической тканях. В качестве потенциальных причин детских гемолимфобластозов рассматривают
Таблица 3
Результаты вычисления отношения шансов
|
Группа |
Фактор риска есть |
Фактора риска нет |
ОШ (95%-ный ДИ) |
||||||
|
всего |
мальч. |
дев. |
всего |
мальч. |
дев. |
всего |
мальч. |
дев. |
|
|
Исход есть ( n =81) |
29 |
19 |
10 |
52 |
30 |
22 |
0,76 (0,46–1,26) |
0,81 (0,43–1,54) |
0,69 (0,3–1,57) |
|
Исхода нет ( n =324) |
137 |
86 |
51 |
187 |
110 |
77 |
|||
Таблица 4
Показатели ИОР гемолимфобластозов в зависимости от накопленных преконцептивных доз родителей
Полученные нами результаты согласуются с исследованиями [35, 36], не выявившими статистически значимого эффекта при анализе отдаленных последствий воздействия ионизирующей радиации.
Возможно также, что на оценку дозового эффекта в нашей работе повлияла изначально небольшая статистическая мощность исследования, учитывая относительно невысокую частоту злокачественных неоплазм в детском возрасте. Увеличение возраста наблюдения за когортой потомков облученных лиц до 25 лет, по сравнению с данными нашего предыдущего исследования [37], не изменило итоговые результаты.
Важно также подчеркнуть, что родители, подвергшиеся преконцептивному облучению, являлись работниками атомного производства, на которое проводился тщательный отбор персонала, в том числе по состоянию здоровья. В связи с этим группа облученных родителей могла иметь исходный уровень здоровья выше, чем у родителей группы сравнения. К тому же небольшое число экспонированных родителей в нашей выборке не позволяет с уверенностью утверждать отсутствие связи пролонгированного воздействия ионизирующего излучения до зачатия и развития злокачественных неоплазм у потомков.
Таким образом, зависимость оценки радиационно-индуцированного риска от статистической мощности исследуемой группы и многофакторность ЗНО дают основания для продолжения исследования последствий преконцептивного облучения на производстве для потомков.
Выводы. Анализ риска онкогематологической патологии у детей облученных лиц с использовани- ем метода «случай – контроль» в когорте и индивидуальных оценок доз внешнего гамма-облучения, накопленных до зачатия ребенка, был проведен в когорте потомков работников первого в стране предприятия ядерного цикла. Тестирование влияния преконцептивного облучения родителей на риск возникновения гемолимфобластозов у потомков осуществлено с помощью расчета отношения шансов и оценки зависимости «доза – эффект».
Несмотря на включение в анализ всех случаев ЗНО лимфоидной и кроветворной тканей до 25-летнего возраста среди детей работников ПО «Маяк», 60-летний период наблюдения когорты детского населения ЗАТО г. Озерска, насчитывающий более 90 тысяч человек, мы не нашли достоверного увеличения риска гемолимфобластозов среди потомков лиц, подвергшихся преконцептивному облучению на производстве.
Количественная оценка фактора преконцептив-ного облучения, выделенного среди многообразия потенциальных канцерогенных факторов, показала в нашей работе отсутствие связи между радиационным воздействием на родителей и повышением риска ЗНО у потомков. Величина ОШ составила в целом 0,76 (0,46–1,26). Коэффициент ИОР/Гр с учетом поглощенных доз на все тело среди отцов достигал –0,4 [–0,97; 0,14], среди матерей –0,0036 [–1,08; 0,93]. ИОР/Гр в зависимости от суммарной отцовской дозы на гонады составил –0,31 [–0,93; 0,26], от материнской – –0,22 [–1,57; 0,89]. Анализ ИОР, проведенный в дозовых категориях с интервалами по 250 мГр, не выявил значимых отклонений от предыдущих расчетов ИОР.
Однако относительно малое число случаев ЗНО лимфоидной и кроветворной тканей ограничивает силу выводов, поэтому мы не можем утверждать, что контакт с ионизирующим облучением на производстве до зачатия безопасен с позиции канцерогенного риска для потомков. Предрасположенность к неоплазмам у потомков и манифестация эффекта в виде солидного рака в старшем возрасте не исключаются, что требует продолжения наблюдения.
Финансирование. Работа выполнена в рамках Государственного контракта № 11.305.18.0 по теме НИР «Анализ последствий воздействия ионизирующих излучений на здоровье персонала ПО “Маяк” и их детей путем оценки радиогенных рисков».
Список литературы Риск онкогематологической патологии у детей персонала радиационно опасного производства
- Башлыкова Л.А. Наследование цитогенетических и молекулярно-клеточных эффектов в клетках костного мозга животных при хроническом воздействии ионизирующего излучения//Известия Самарского научного центра Российской академии наук. -2017. -Т. 19, № 2-3. -С. 420-425.
- Тканеспецифические изменения уровня полиморфизма простых повторов в ДНК потомков разного пола, рожденных от облученных самцов или самок мышей/М.Г. Ломаева, Л.А. Фоменко, Г.В. Васильева, В.Г. Безлепкин//Радиационная биология. Радиоэкология. -2016. -Т. 56, № 2. -С. 149.
- Increased Transgenerational Intestinal Tumorigenesis in Offspring of Ionizing Radiation Exposed Parent APC1638N/+ Mice/S. Suman, S. Kumar, B.H. Moon, A.J. Fornace, B. Kallakury, K. Datta//J. Cancer. -2017. -Vol. 8, № 10. -P. 1769-1773 DOI: 10.7150/jca.17803
- Transgenerational inheritance of enhanced susceptibility to radiation-induced medulloblastoma in newborn Ptch1+/-mice after paternal irradiation/L. Paris, P. Giardullo, S. Leonardi, B. Tanno, R. Meschini, E. Cordelli, B. Benassi, M.G. Longobardi, A. Izzotti, A. Pulliero, M. Mancuso, F. Pacchierotti//Oncotarget. -2015. -Vol. 6, № 34. -P. 36098-36112 DOI: 10.18632/oncotarget.5553
- Lord B.I., Hoyes K.P. Hemopoietic damage and induction of leukemia in offspring due to preconception paternal irradiation from incorporated plutonium-239//Radiat Res. -1999. -Vol. 152 (Suppl. 6). -S. 34-37.
- Индивидуальные особенности трансгенерационной геномной нестабильности у детей ликвидаторов последствий аварии на ЧАЭС (цитогенетические и иммуногенетические показатели)/И.И. Сусков, Н.С. Кузьмина, В.С. Сускова, А.В. Агаджанян, А.В. Рубанович//Радиационная биология. Радиоэкология. -2008. -Т. 48, № 3. -С. 278-286.
- Цитогенетические эффекты и возможности их трансгенерационной передачи в поколениях лиц, проживающих в регионах радионуклидного загрязнения после аварии на Чернобыльской АЭС/Л.С. Балева, T. Номура, А.Е. Сипягина, Н.М. Карахан, Е.Н. Якушева, Н.И Егорова//Российский вестник перинатологии и педиатрии. -2016. -№ 3. -С. 87-94.
- Изучение нестабильности генома потомков в семьях работников ПО «Маяк»: мини-сателлит СЕВ 1/Г.Г. Русинова, И.В. Глазкова, Т.В. Азизова, С.В. Осовец., Н.С. Вязовская//Генетика. -2014. -Т. 50, № 11. -С. 1354-1362.
- Анализ и ретроспективная оценка результатов цитогенетических обследований населения Казахстана, подвергашегося радиационному воздействию в результате испытаний ядерного оружия на Семипалатинском полигоне, и их потомков/К.Н. Апсаликов, Т.Ж. Мулдагалиев, Т.И. Белихина, З.А. Танатова, Л.Б. Кенжина//Медико-биологические проблемы жизнедеятельности. -2013. -Т. 9, № 1. -С. 42-49.
- Sources, effects and risks of ionizing radiation: UNSCEAR Report. Effects of radiation exposure of children//UNITED NATIONS. -New York, 2013. -Vol. II. -282 p.
- Evidence relevant to untargeted and transgenerational effects in the offspring of irradiated parents/M.P. Little, D.T. Goodhead, B.A. Bridges, S.D. Bouffler//Mutat Res. -2013. -Vol. 753, № 1. -P. 50-67
- DOI: 10.1016/j.mrrev.2013.04.001
- Epidemiology of childhood acute myeloid leukemia/S.E. Puumala, J.A. Ross, R. Aplenc, L.G. Spector//Pediatr. Blood Cancer. -2013. -Т. 60, № 5. -P. 728-733.
- The Childhood Leukemia International Consortium/C. Metayer, E. Milne, J. Clavel, C. Infante-Rivard, E. Petridou, M. Taylor, J. Schüz, L.G. Spector, J.D. Dockerty, C. Magnani, M.S. Pombo-de-Oliveira, D. Sinnett, M. Murphy, E. Roman, P. Monge, S. Ezzat, B.A. Mueller, M.E. Scheurer, B.K. Armstrong, J. Birch, P. Kaatsch, S. Koifman, T. Lightfoot, P. Bhatti, M.L. Bondy, J. Rudant, K. O'Neill, L. Miligi, N. Dessypris, A.Y. Kang, P.A. Buffler//Cancer Epidemiol. -2013. -Vol. 37, № 3. -P. 336-347.
- Results of case-control study of leukaemia and lymphoma among young people near Sellafield nuclear plant in West Cumbria/M.J. Gardner, M.P. Snee, A.J. Hall, Powell C.A., S. Downes, J.D. Terrell//Br. Med. J. -1990. -Vol. 300. -P. 423-429.
- Paternal radiation exposure and leukaemia in offspring: the Ontario case-control study/J.R. McLaughlin, W.D. King, T.W. Anderson, E.A. Clarke, J.P. Ashmore//BMJ. -1993. -Vol. 307, № 6910. -P. 959-966.
- Kinlen L.J, Clarke K., Balkwill A. Paternal preconceptional radiation exposure in the nuclear industry and leukaemia and non-Hodgkin's lymphoma in young people in Scotland//BMJ. -1993. -Vol. 306, № 6886. -P. 1153-1158.
- Cancer in the offspring of radiation workers: a record linkage study/G.J. Draper, M.P. Little, T. Sorahan, L.J. Kinlen, K.J. Bunch, A.J. Conquest, G.M. Kendall, G.W. Kneale, R.J. Lancashire, C.R. Muirhead, C.M. O'Connor, T.J. Vincent//BMJ. -1997. -Vol. 315, № 7117. -P. 1181-1188.
- Cancer in children of nuclear industry employees: report on children aged under 25 years from nuclear industry family study/E. Roman, P. Doyle, N. Maconochie, G. Davies, P.G Smith., V. Beral//BMJ. -1999. -Vol. 318, № 7196. -P. 1443-1450.
- Long-term effects of radiation exposure on health/K. Kamiya, K. Ozasa, S. Akiba, O. Niwa, K. Kodama, N. Takamura, E.K. Zaharieva, Y. Kimura, R. Wakeford//Lancet. -2015. -Vol. 386, № 9992. -P. 469-478. (15) 61167-9
- DOI: 10.1016/S0140-6736
- Risk of death among children of atomic bomb survivors after 62 years of follow-up: a cohort study/E.J. Grant, K. Furukawa, R. Sakata, H. Sugiyama, A. Sadakane, I. Takahashi, M. Utada, Y. Shimizu, K. Ozasa//Lancet Oncol. -2015. -Vol. 16, № 13. -P. 1316-1323. (15) 00209-0
- DOI: 10.1016/S1470-2045
- Wakeford R. Childhood leukaemia and radiation exposure of fathers -the end of the road, perhaps?//J. Radiol. Prot. -2003. -Vol. 23, № 4. -P. 359-362.
- Василенко Е.К. Дозиметрия внешнего облучения работников ПО «Маяк»: приборы, методы, результаты//Источники и эффекты облучения работников ПО «Маяк» и населения, проживающего в зоне влияния предприятия/под ред. М.Ф. Киселева и С.А. Романова. -Челябинск: Челябинский дом печати, 2009. -Ч. 1. -С. 51-100.
- Mayak Worker Dosimetry System 2008 (MWDS-2008): assessment of internal dose from measurement results of plutonium activity in urine/V.V. Khokhryakov, V.F. Khokhryakov, K.G. Suslova, V.V. Vostrotin, V.E. Vvedensky, A.B. Sokolova, M.P. Krahenbuhl, A. Birchall, S.C. Miller, A.E. Schadilov, A.V. Ephimov//Health Phys. -2013. -Vol. 4, № 104. -P. 366-378.
- Статистическая классификация болезней, травм и причин смерти (адаптированный вариант МКБ-9 для использования в СССР). -2-е изд. -М., 1986. -97 с.
- Международная статистическая классификация болезней и проблем, связанных со здоровьем. Десятый пересмотр. -М.: Медицина, 1995. -Т. 1, ч. 2. -633 с.
- Preston D.L., Lubin J.H., Pierce D.A. McConney M. EPICURE user’s Guide. -Seattle: Hirosoft International Corp., 1993. -330 p.
- Заболеваемость острыми лейкозами и их распространенность в детской популяции Челябинской области за период 1974-2003 гг./Е.В. Жуковская, И.И. Спичак, Е.В. Башарова, Д.К. Волосников, С.Г. Коваленко, И.А. Огошкова//Вопросы гематологии/онкологии и иммунопатологии в педиатрии. -2005. -Т. 4, № 1. -С. 20-24.
- Мень Т.Х., Рыков М.Ю., Поляков В.Г. Злокачественные новообразования у детей в России: основные показатели и тенденции//Российский онкологический журнал. -2015. -Т. 20, № 2. -С. 43-47.
- Котеров А.Н. Новые факты об отсутствии индукции нестабильности генома при малых дозах радиации с низкой ЛПЭ и соответствующие выводы о пороге эффекта в сообщении НКДАР-2012//Радиационная биология. Радиоэкология. -2014. -Т. 54, № 3. -С. 309-312.
- A systematic review and meta-analysis of the association between childhood infections and the risk of childhood acute lymphoblastic leukaemia/J. Hwee, C. Tait, L. Sung, J.C. Kwong, R. Sutradhar, J.D. Pole//Br. J. Cancer. -2018. -Vol. 118, № 1. -P. 127-137
- DOI: 10.1038/bjc.2017.360
- Risk of childhood leukaemia and non-Hodgkin's lymphoma after parental occupational exposure to solvents and other agents: the SETIL Study/L. Miligi, A. Benvenuti, S. Mattioli, A. Salvan, G.A. Tozzi, A. Ranucci, P. Legittimo, R. Rondelli, L. Bisanti, P. Zambon, S. Cannizzaro, U. Kirchmayer, P. Cocco, E. Celentano, G. Assennato, D.F. Merlo, P. Mosciatti, L. Minelli, M. Cuttini, V. Torregrossa, S. Lagorio, R. Haupt, S. Risica, A. Polichetti, C. Magnani//Occup. Environ. Med. -2013. -Vol. 70, № 9. -P. 648-655
- DOI: 10.1136/oemed-2012-100951
- Perinatal and familial risk factors for acute lymphoblastic leukemia in a Swedish national cohort/C. Crump, J. Sundquist, W. Sieh, M.A. Winkleby, K. Sundquist//Cancer. -2015. -Vol. 7, № 121. -P. 1040-1047.
- Tabrizi M.M., Hosseini S.A. Role of Electromagnetic Field Exposure in Childhood Acute LymphoblasticLeukemia and No Impact of Urinary Alpha-Amylase -a Case Control Study in Tehran, Iran//Asian Pac. J. Cancer Prev. -2015. -Vol. 17, № 16. -P. 7613-7618.
- SETIL: Italian multicentric epidemiological case-control study on risk factors for childhood leukaemia, non hodgkin lymphoma and neuroblastoma: study population and prevalence of risk factors in Italy / C. Magnani, S. Mattioli, L. Miligi, A. Ranucci, R. Rondelli, A. Salvan, L. Bisanti, G. Masera, C. Rizzari, P. Zambon, S. Cannizzaro, L. Gafà, L.L. Luzzatto, A. Benvenuti, P. Michelozzi, U. Kirchmayer, P. Cocco, P. Biddau, C. Galassi, E. Celentano, E. Guarino, G. Assennato, G. de Nichilo, D.F. Merlo, V. Bocchini, F. Pannelli, P. Mosciatti, L. Minelli, M. Chiavarini, M. Cuttini, V. Casotto, M.V. Torregrossa, R.M. Valenti, F. Forastiere, R. Haupt, S. Lagorio, S. Risica, A. Polichetti // Ital. J. Pediatr. - 2014. - Vol. 40. - Р. 103
- DOI: 10.1186/s13052-014-0103-5
- Draper G. Preconception exposures to potential germ-cell mutagens//Radiat. Prot. Dosimetry. -2008. -Vol. 132, № 2. -P. 241-245.
- Childhood cancer in the offspring born in 1921-1984 to US radiologic technologists/K.J. Johnson, B.H. Alexander, M.M. Doody, A.J. Sigurdson, M.S Linet., L.G. Spector, W. Hoffbeck, S.L Simon., R.M. Weinstock, J.A. Ross//Br. J. Cancer. -2008. -Vol. 99, № 3. -P. 545-550.
- Гемобластозы у потомков работников радиационно опасных производств/С.Ф. Соснина, Н.Р. Кабирова, М.Э. Сокольников, П.В. Окатенко//Анализ риска здоровью. -2016. -№ 4. -С. 23-30
- DOI: 10.21668/health.risk/2016.4.03


