Роль сероводорода и монооксида углерода в коллаген-индуцированной агрегации тромбоцитов пациентов с ишемической болезнью сердца
Автор: Беляева С.Н., Трубачева О.А.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 3 т.35, 2020 года.
Бесплатный доступ
Введение. На сегодняшний день имеются данные, что газотрансмиттеры сероводорода (H2S) и монооксида углерода (CO) принимают важное участие в регуляции функциональной активности различных органов и систем организма человека. Согласно ряду данных, СО и H2S рассматриваются как ингибиторы агрегации тромбоцитов. Цель исследования: изучить влияние доноров H2S и CO на коллаген-индуцированную агрегацию тромбоцитов здоровых доноров и пациентов с ишемической болезнью сердца (ИБС).Материал и методы. В ходе выполнения обследованы 37 человек. В контрольную группу вошли 13 здоровых доноров, группу пациентов с ИБС составили 24 человека. Все обследованные пациенты получали регулярную комбинированную базисную терапию в соответствии с современными рекомендациями для лечения ИБС. Агрегационную активность тромбоцитов исследовали турбидиметрическим методом на двухканальном лазерном анализаторе (220 LA «Биола», Россия). В качестве маркеров функциональной активности тромбоцитов определяли степень и скорость агрегации богатой тромбоцитами плазмы по кривым светопропускания и среднего размера агрегатов. Для индукции агрегации использовали коллаген в конечной концентрации 2 мг/мл. В качестве донора H2S применяли гидросульфид натрия (NaHS), в качестве донора CO CORM-II. Фактические данные представлены в виде Me (Q1 -Q3). Для проверки однородности парных или зависимых выборок использовали Т-критерий Вилкоксона. Различия считали статистически значимыми при уровне значимости р function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Агрегация, газотрансмиттеры, сероводород, монооксид
Короткий адрес: https://sciup.org/149125361
IDR: 149125361 | УДК: 616.12-005.4:616.155.2:616.151.4:546.221.1 | DOI: 10.29001/2073-8552-2020-35-3-86-92
The role of hydrogen sulfide and carbon monoxide in collagen-induced platelet aggregation in patients with coronary artery disease
Purpose of research. To study the effect of hydrogen sulfide and carbon monoxide donors on collagen-induced platelet aggregation in healthy donors and patients with coronary artery disease.Introduction. There is evidence that the hydrogen sulfide (H2S) and carbon monoxide (CO) gas transmitters play an essential role in regulating the functional activity of various organs and systems of the human body. According to previous reports, CO and H S are considered inhibitors of platelet aggregation.Material and Methods. A total of 37 participants were examined during the study. The control group included 13 healthy donors; group of patients with coronary artery disease comprised 24 people. All examined patients received regular combination baseline therapy in accordance with modern recommendations for the treatment of coronary artery disease. Platelet aggregation activity was studied by a turbidimetric method using a two-channel laser analyzer (220 LA Biola, Russia). The degree and rate of platelet aggregation were determined in platelet-rich plasma based on the curves of light transmission and the average size of aggregates as markers of the functional activity of platelets. Collagen at a final concentration of 2 mg/mL was used to induce platelet aggregation. Sodium hydrosulfide (NaHS) was used as a hydrogen sulfide donor. Carbon monoxide-releasing molecule-II (CORM-II) was used as a carbon monoxide donor. Experimental data are presented as Me (Q1 -Q3). Wilcoxon T-test was used to test the homogeneity of paired or dependent samples. Values were considered tatistically significant when p was function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Роль сероводорода и монооксида углерода в коллаген-индуцированной агрегации тромбоцитов пациентов с ишемической болезнью сердца
УДК 616.12-005.4:616.155.2:616.151.4:546.221.1
Беляева С.Н., Трубачева О.А. Роль сероводорода и монооксида углерода в коллаген-ин-дуцированной агрегации тромбоцитов пациентов с ишемической болезнью сердца. Сибирский журнал клинической и экспериментальной медицины. 2020;35(3):86–92.
Главными факторами, с которыми инициируется развитие атеросклероза и ишемической болезни сердца (ИБС), может быть дисфункция либо повреждение эндотелия, аккумуляция в сосудистой стенке холестерина [1]. Окисленные липопротеиды низкой плотности (ЛПНП) обладают высокой токсичностью, вызывая апоптоз сосудистых клеток. Гиперлипидемия имеет прямое отношение к образованию гиперактивных тромбоцитов [2]. Известно, что в патогенезе сердечно-сосудистых заболеваний, в частности ИБС, немаловажную роль играет нарушение структурно-функционального статуса тромбоцитов: активация кровяных пластинок способствует развитию внутрисосудистого тромбообразования. Показано, что при активации происходит увеличение среднего объема тромбоцитов [3], наблюдается повышенная чувствительность к агонистам, увеличение в цитозоле свободного кальция, повышение продукции эндогенных активных форм кислорода. Это приводит к усилению функциональной активности тромбоцитов и способности к агрегации. Применение ингибиторов агрегации тромбоцитов как основных средств выбора для профилактики тромбоза всегда сопряжено с повышенным риском кровотечений. Поэтому возникает необходимость не только выяснения фундаментальных основ их активации и вклада в прогрессирование сердечно-сосудистой патологии, но и разработки наиболее оптимальных подходов к коррекции возникших нарушений. Претендентами на эту роль в последнее время рассматриваются эндогенно синтезируемые газовые молекулы – сероводород (H2S) и монооксид углерода (CO). Известно, что главным источником СО служит эндотелий [4, 5], в то время как S продуцируется в основном гладкими мышцами, адипоцитами и эритроцитами [6]. Несмотря на хорошо известные токсические свойства СО и S, в отечественной и мировой литературе существует достаточно сведений о сигнальной функции этих молекул [7]. На сегодняшний день имеются данные, что H2S и СО принимают участие в регуляции функциональной активности различных органов и систем организма человека [8]. Согласно ряду данных, СО и H2S рассматриваются как ингибиторы агрегации тромбоцитов, но точно не установлено, через какие внутриклеточные сигнальные пути реализуется их действие.
Цель исследования: изучить влияние доноров H2S и СО на коллаген-индуцированную агрегацию тромбоцитов здоровых доноров и пациентов с ИБС.
Материал и методы
Проведено одномоментное исследование, в ходе выполнения которого обследованы 37 человек. В контрольную группу вошли 13 здоровых доноров в возрасте от 45 до 60 лет. Группу пациентов с ИБС составили 24 человека в возрасте от 41 до 75 лет. Все обследованные пациенты получали регулярную комбинированную базисную терапию в соответствии с современными рекомендациями для лечения ИБС. Критериями исключения из исследования являлись острые сосудистые осложнения давностью менее 6 мес., тяжелая сопутствующая патология, клинические и лабораторные признаки острого воспаления, отказ от участия в исследовании. Для получения тромбоцитов использовали периферическую венозную кровь, забираемую из локтевой вены утром, натощак в вакуумные пробирки, содержащие антикоагулянт (цитрат натрия 3,8%) в соотношении: одна часть антикоагулянта на девять частей крови. Кровь тщательно перемешивали с антикоагулянтом путем плавного покачивания, затем подвергали центрифугированию при 1500 об./мин в течение 7 мин. Отбирали надосадочный слой – богатую тромбоцитами плазму. Агрегационную активность изолированных тромбоцитов исследовали с помощью метода Г. Борна (1962) в модификации З.А. Габбасова (1989) на двухканальном лазерном анализаторе (220 LA «НПФ Биола», Россия). Метод основан на анализе флуктуаций светопропускания (ФСП-метод), вызванных случайным изменением числа частиц в оптическом канале. Относительная дисперсия таких флуктуаций пропорциональна среднему размеру агрегатов и используется для исследования кинетики агрегации. Метод отличается высокой чувствительностью, что делает его пригодным для исследования спонтанной агрегации, агрегации под действием низких концентраций индукторов, а также агрегации субклеточных частиц и макромолекул. В качестве маркеров функциональной активности тромбоцитов определяли степень и скорость агрегации богатой тромбоцитами плазмы по кривым светопропускания и среднего размера агрегатов. Наиболее информативным показателем кол-лаген-индуцированной агрегации тромбоцитов является степень агрегации по кривой светопропускания. Для индукции агрегации использовали коллаген в конечной концентрации 2 мг/мл.
В настоящем исследовании в качестве донора сероводорода использовали гидросульфид натрия (NaHS). В водном растворе NaHS диссоциирует до ионов Na+ и HS-. Последний в свою очередь взаимодействует с Н+ с формированием H2S. В качестве донора CO использовали CORM–2. Тромбоциты инкубировали с данными модификаторами в течение 30 мин при 37 °С. Анализ показателей проводили при помощи программы SPSS STATISTICS 17.0. Фактические данные представлены в виде Me ( Q 1– Q 3). При сравнении независимых выборок использовали U-критерий Манна – Уитни, а для зависимых выборок Т-критерий Вилкоксона с поправкой Бон-феррони. Различия считали статистически значимыми при уровне значимости р < 0,05.
Результаты и обсуждение
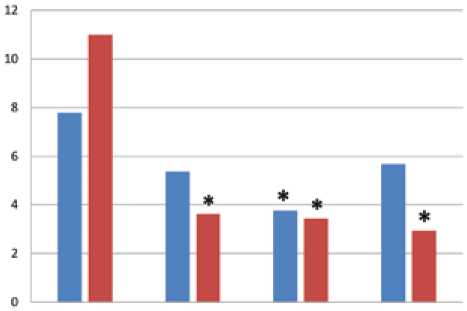
Установлено, что у пациентов с ИБС при использовании всех концентраций донора H2S статистически значимо снижалась коллаген-индуцированная агрегация тромбоцитов по кривой светопропускания при концентрации 10-5 М. По кривой среднего размера агрегатов происходило значимое снижение агрегации при добавлении донора H2S в концентрациях 10-5 M, 10-6 M. При значениях концентрации донора H2S 10-4, 10-5, 10-6 М скорость агрегации тромбоцитов статистически значимо снижалась по кривой среднего размера агрегатов у пациентов с ИБС (табл. 1, рис. 1).
У здоровых доноров происходило значимое снижение агрегационной активности по кривой светопропускания во всем диапазоне концентраций донора H2S (10–4–10–6 М). Скорость агрегации по кривой светопропускания статистически значимо уменьшалась при действии донора H2S в концентрации 10–6 М. При значении концентрации донора H2S 10–4 М статистически значимо снижалась агрегация по кривой среднего размера агрегатов.
Скорость агрегации по кривой среднего размера агрегатов статистически значимо уменьшалась при концентрациях 10–5 и 10–6 М (табл. 2, см. рис. 1).
в
з 1 s
Коллаген, 1 мг/мл
Collagen, 2 ng/ml
Коллаген + 10–4 M NaHS
Collagen + 10–4 M NaHS
Коллаген + 10–5 M NaHS
Collagen + 10–5 M NaHS
Коллаген + 10–6 M NaHS
Collagen + 10–6 M NaHS
-
■ пациенты с ИБС / patients with coronary heart disease
-
■ здоровые доноры / healthy donors
Рис. 1. Влияние донора сероводорода на агрегацию тромбоцитов здоровых доноров и пациентов с ишемической болезнью сердца по кривой светопропускания (%)
Fig 1. The effects of hydrogen sulfide donor on platelet aggregation based to the light transmission curve (%) in healthy donors and patients with coronary heart disease.
Примечание: * – р < 0,05 по сравнению со значениями коллаген-индуцированной агрегации без модификаторов.
Note: * – p < 0.05 compared to the values of collagen-induced aggregation without modifiers.
Таблица 1. Влияние донора сероводорода на коллаген-индуцированную агрегацию тромбоцитов пациентов с ишемической болезнью сердца Table 1. The effect of hydrogen sulfide donor on collagen-induced platelet aggregation in patients with coronary heart disease
|
Показатели Parameters |
Коллаген, 2 нг/мл Collagen, 2 ng/mL (n = 24) |
Коллаген +10-4 M NaHS Collagen + 10-4 M NaHS ( n = 24) |
Коллаген +10-5 M NaHS Collagen + 10-5M NaHS (n = 24) |
Коллаген +10-6 M NaHS Collagen +10-6M NaHS ( n = 24) |
|
I |
2,8 (2,34,2) |
2,6 (2,2–4,2) |
2,5* (2,1–3,3) |
2,5* (1,8–3,4) |
|
II |
7,8 (2,46,4) |
5,4 (2,9–6,9) |
3,8* (2,4–5,4) |
5,7 (3,6–7,0) |
|
III |
4,1 (3,28,2) |
3,33* (1,6–4,8) |
3,8* (1,1–5,3) |
3,0* (0,7–5,3) |
|
IV |
11,9 (8,816,3) |
12,7 (9,5–16,4) |
12,5 (9,7–16,5) |
15,4 (10,6–20,4) |
Примечание: * р < 0,05 по сравнению со значениями коллаген-индуцированной агрегации без модификаторов;
I – степень агрегации по кривой среднего размера агрегатов, отн. ед.;
II – степень агрегации по кривой светопропускания, %;
III – скорость агрегации по кривой среднего размера агрегатов, отн. ед./мин;
IV – скорость агрегации по кривой светопропускания, %/мин.
Note: * – p < 0.05 compared to the values of collagen-induced aggregation without modifiers;
I – degree of platelet aggregation based on the average aggregate size curve, relative units;
II – degree of platelet aggregation based on the light transmission curve, %;
III – speed of platelet aggregation based on the average aggregate size curve, relative units/min;
IV – speed of platelet aggregation based on the light transmission curve, %/min.
Таблица 2. Влияние донора сероводорода на коллаген-индуцированную агрегацию тромбоцитов здоровых доноров
Table 2. The effect of hydrogen sulfide donor on collagen-induced platelet aggregation in healthy donors
|
Показатели Parameters |
Коллаген,2 нг/мл Collagen, 2 ng/mL (n = 13) |
Коллаген +10-4 M NaHS Collagen + 10-4M NaHS ( n = 13) |
Коллаген + 10-5 M NaHS Collagen + 10-5M NaHS ( n = 13) |
Коллаген + 10-6 M NaHS Collagen + 10-6M NaHS ( n = 13) |
|
2,2 |
1,9* |
2,0 |
2,03 |
|
|
I |
(2,02,8) |
(1,52,0) |
(1,8–2,8) |
(1,72,4) |
|
II |
11,0 |
3,6* |
3,43* |
2,9* |
|
(5,950,2) |
(2,5–5,2) |
(2,8–6,1) |
(2,03,9) |
|
|
III |
3,7 |
1,9 |
2,6* |
2,4* |
|
(2,44,9) |
(0,8–3,1) |
(1,9–3,4) |
(1,02,7) |
|
|
IV |
18 |
12,2 |
13,3 |
9,8* |
|
(1437,1) |
(10,0–16,5) |
(11,1–19,2) |
(7,313,2) |
Примечание: * – р < 0,05 по сравнению со значениями коллаген-индуцированной агрегации без модификаторов;
I – степень агрегации по кривой среднего размера агрегатов, отн. ед.;
II – степень агрегации по кривой светопропускания, %;
III – скорость агрегации по кривой среднего размера агрегатов, отн. ед./мин;
IV – скорость агрегации по кривой светопропускания, %/мин.
Note: * – p < 0.05 compared to the values of collagen-induced aggregation without modifiers;
I – degree of platelet aggregation based on the average aggregate size curve, relative units;
II – degree of platelet aggregation based on the light transmission curve, %;
III – speed of platelet aggregation based on the average aggregate size curve, relative units/min;
IV – speed of platelet aggregation based on the light transmission curve, %/min.
У здоровых доноров антиагрегационный эффект донора H2S выражен сильнее по сравнению с группой пациентов с ИБС. Полученные результаты можно объяснить снижением концентрации эндогенного H2S в плазме у больных с сердечно-сосудистой патологией. Как правило, у пациентов с ИБС нарушен липидный обмен, в результате этого происходит дезорганизация фосфолипидного состава мембраны тромбоцитов с нарушением ее проницаемости. Другой причиной антиагрегационного эффекта H2S может быть снижение внутриклеточной концентрации ионов кальция при сердечно-сосудистой патологии. Для инициации агрегации тромбоцитов необходимо увеличение внутриклеточной концентрации ионов кальция, в некоторых исследованиях показано, что гидросульфид натрия снижает мобилизацию этих ионов, следовательно, тормозятся процессы агрегации [9].
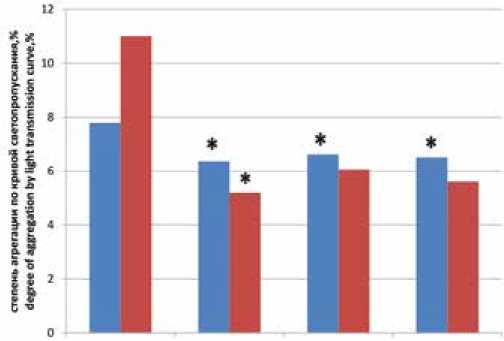
При использовании CORM-2 у пациентов с ИБС наблюдалось значимое снижение агрегационной активно- сти тромбоцитов по кривым среднего размера агрегатов и светопропускания при всех использованных концентрациях от 10-4 М до 10-6 М. Скорость агрегации по кривой среднего размера агрегатов значимо уменьшалась при концентрации CORM-2, равной 10-6 М. При концентрации донора CO 10-4 М скорость агрегации по кривой светопро-пускания статистически значимо снижалась у пациентов с ИБС (табл. 3, рис. 2).
Установлено, что у здоровых доноров происходило снижение степени коллаген-индуцированной агрегационной активности тромбоцитов по кривой среднего размера агрегатов под действием донора СО в концентрации 10-5 М. Снижение агрегационной активности по кривой светопропускания наблюдалось при значении концентрации донора CO 10-4 М. Скорость агрегации по кривой среднего размера агрегатов значимо снижалась при концентрации СО 10-5 М у здоровых доноров (табл. 4, см. рис. 2).
Таблица 3. Влияние СОRM-2 на коллаген-индуцированную агрегацию тромбоцитов пациентов с ишемической болезнью сердца
Table 3. The effect of CORM-2 on collagen-induced platelet aggregation in patients with coronary heart disease
|
Показатели Parameters |
Коллаген, 2 нг/мл Collagen, 2 ng/mL ( n = 24) |
Коллаген + 10-4 M СОRM-2 Collagen + 10-4M СОRM-2 ( n = 24) |
Коллаген + 10-5 M СОRM-2 Collagen + 10-5M СОRM-2 ( n = 24) |
Коллаген + 10-6 M СОRM-2 Collagen + 10-6M СОRM-2 ( n = 24) |
|
I |
2,8 (2,3–4,2) |
2,8* (1,7–4,2) |
2,9* (2,3–4,2) |
2,6* (1,84–4,14) |
|
II |
7,8 (2,4–6,4) |
6,4* (4,3–15,9) |
6,6* (3,64–20,2) |
6,6* (4,3–16,0) |
|
III |
4,1 (3,2–8,2) |
3,8 (1,5–8,2) |
4,4 (2,4–6,9) |
3,6* (1,9–5,4) |
|
IV |
11,9 (8,8–16,3) |
15,0* (11,2–23,4) |
14,9 (10,3–39,5) |
15,4 (10,9–38,5) |
Примечание: * р < 0,05 по сравнению со значениями коллаген-индуцированной агрегации без модификаторов;
I степень агрегации по кривой среднего размера агрегатов, отн. ед.;
II степень агрегации по кривой светопропускания, %;
-
III скорость агрегации по кривой среднего размера агрегатов, отн. ед./мин;
-
IV скорость агрегации по кривой светопропускания, %/мин.
Note: * – p < 0.05 compared to the values of collagen-induced aggregation without modifiers;
-
I – degree of platelet aggregation based on the average aggregate size curve, relative units;
-
II – degree of platelet aggregation based on the light transmission curve, %;
-
III – speed of platelet aggregation based on the average aggregate size curve, relative units/min;
-
IV – speed of platelet aggregation based on the light transmission curve, %/min.
Таблица 4. Влияние СОRM–2 на коллаген-индуцированную агрегацию тромбоцитов здоровых добровольцев Table 4. The effect of CORM-2 on collagen-induced platelet aggregation in healthy volunteers
|
Показатели Parameters |
Коллаген, 2 нг/мл Collagen, 2 ng/mL (n = 13) |
Коллаген + 10-4M СОRM-2 Collagen + 10-4M СОRM-2 ( n = 13) |
Коллаген + 10-5M СОRM-2 Collagen + 10-5M СОRM-2 ( n = 13) |
Коллаген + 10-6 M СОRM-2 Collagen + 10-6M СОRM-2 ( n = 13) |
|
I |
2,1 (1,9–2,8) |
2,5 (1,9–2,7) |
1,6* (1,4–1,9) |
2,4 (1,3–2,4) |
|
II |
11,0 (5,9–50,2) |
5,19* (4,0–6,4) |
6,07 (5,1–9,2) |
5,6 (4,0–8,3) |
|
III |
3,71 (2,4–4,9) |
3,30 (1,2–4,9) |
1,52* (0,6–2,8) |
2,6 (1,2–3,8) |
|
IV |
18 (14,0–37,1) |
10,9 (9,4–16,5) |
11,7 (10,1–21,5) |
10,3 (8,1–15,5) |
Примечание: * – р < 0,05 по сравнению со значениями коллаген-индуцированной агрегации без модификаторов;
-
I – степень агрегации по кривой среднего размера агрегатов, отн. ед.;
-
II – степень агрегации по кривой светопропускания, %;
-
III – скорость агрегации по кривой среднего размера агрегатов, отн. ед./мин;
-
IV – скорость агрегации по кривой светопропускания, %/мин.
Note: * – p < 0.05 compared to the values of collagen-induced aggregation without modifiers;
-
I – degree of platelet aggregation based on the average aggregate size curve, relative units;
-
II – degree of platelet aggregation based on the light transmission curve, %;
-
III – speed of platelet aggregation based on the average aggregate size curve, relative units/min;
-
IV –speed of platelet aggregation based on the light transmission curve, %/min.
Коллаген, 1 мг/мл
Collagen, 2 ng/ml
Коллаген + 10–4 M CO
Collagen + 10–4 M NaHS
Коллаген + 10–5 M CO
Collagen + 10–5 M CO
Коллаген + 10–6 M CO
Collagen + 10–6 M CO
■ пациенты с ИБС / patients with coronary heart disease ■ здоровые доноры / healthy donors
Рис. 2. Влияние донора монооксида углерода на агрегацию тромбоцитов здоровых доноров и пациентов с ишемической болезнью сердца по кривой светопропускания (%)
Fig 2. The effects of carbon monoxide donor on platelet aggregation based on the light transmission curve (%) in healthy donors and patients with coronary heart disease
Примечание: * – р < 0,05 по сравнению со значениями коллаген-индуцированной агрегации без модификаторов.
Note: * – p < 0.05 compared to the values of collagen-induced aggregation without modifiers.
При сравнении параметров агрегации между исследуемыми группами статистически значимые различия отмечались при концентрации донора CO 10-5 М. Агрегация уменьшалась у здоровых доноров по кривой среднего размера агрегатов, а также скорость агрегации снижалась по кривой среднего размера агрегатов по сравнению с пациентами с ИБС. Из литературных данных известно, что донор CO блокирует коллаген-индуцированную агрегацию тромбоцитов благодаря воздействию на фазу активации фибриногена, как следствие, не образуются фибриновые мостики, и механизм агрегации нарушается [10]. Отсутствие статистически значимых различий в эффектах газотрансмиттеров в исследуемой группе и в группе здоровых доноров может объясняться тем, что пациенты с ИБС находились на антиагрегационной терапии, поэтому подобранные концентрации газотрансмит-теров H2S и CO оказались недостаточно информативными в данных условиях.
Заключение
Донор H2S вызывает снижение коллаген-индуциро-ванной агрегации тромбоцитов по кривой светопропуска-ния как у здоровых доноров, так у и пациентов с ИБС. Коллаген-индуцированная агрегация тромбоцитов по кривой светопропускания снижается под действием донора CO, у здоровых доноров эффект более выражен, чем у пациентов с ИБС. В настоящем исследовании показано, что эффекты газовых трансмиттеров донора H2S и донора CO на коллаген-зависимую агрегацию тромбоцитов однонаправленные у здоровых доноров и пациентов с ИБС.
Список литературы Роль сероводорода и монооксида углерода в коллаген-индуцированной агрегации тромбоцитов пациентов с ишемической болезнью сердца
- Горбачев В.В. Ишемическая болезнь сердца. М.: Вэшайшая школа; 2008:480.
- Медицина неотложных состояний. Избранные клинические лекции. Т. 2; под ред. В.В. Никонова, А.Э. Феськова, Б.С. Федака. Донецк: ИД Заславский; 2007:408.
- Барсуков А.В., Шустов С.Б. Артериальная гипертензия. Клиническое профилирование и выбор терапии. М.: ЭЛБИ-СПб; 2014:249.
- Hartsfield C.L. Cross talk between carbon monoxide and nitric oxide. Antioxid. Redox. Signal. 2002;4(2):301-307. DOI: 10.1089/152308602753666352
- Li L., Hsu А., Moore P.K. Actions and interactions of nitric oxide, carbon monoxide and hydrogen sulphide in the cardiovascular system and in inflammation - a tale of three gases! Pharmacol. Ther. 2009;123(3):386- 400. DOI: 10.1016/j.pharmthera.2009.05.005
- Wang R. Two's company, three's a crowd: can H S be the third endogenous gaseous transmitter? FASEB J. 2002;16(3):1792-1798. DOI: 10.1096/fj.02-0211hyp
- Чирков Ю.Ю., Белушкина Н.Н., Тыщук И.А., Северина И.С. Изменения в активности гуанилатциклазы тромбоцитов человека при АДФ-индуцируемой агрегации. Бюллетень экспериментальной биологии и медицины. 1991;52(2):152-154.
- Truss N.J., Warner T.D. Gasotransmitters and platelets. Pharmacol. Ther. 2011;132(2):196-203. DOI: 10.1016/j.pharmthera.2011.07.001
- Петрова И.В., Трубачева О.А., Мангатаева О.С., Суслова Т.Е., Ковалев И.В., Гусакова С.В. Влияние сероводорода на коллаген-индуцированную агрегацию тромбоцитов человека. Российский физиологический журнал им. И.М. Сеченова. 2015; 101(10):1191-1201.
- Kramkowski K., Leszczynska A., Mogielnicki A., Chlopicki S., Fedorowicz A., Grochal E. et al. Antithrombotic рroperties of water-soluble carbon monoxide-releasing molecules. Arterioscler. Thromb. Vasc. Biol. 2012;32(9):2149-2156. DOI: 10.1161/ATVBAHA.112.253989


