Роль визуализационных методов исследования в диагностике первичных мышечных дистоний (обзор)
Автор: Бушуева О.О., Антипенко Е.А.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Нервные болезни
Статья в выпуске: 3 т.18, 2022 года.
Бесплатный доступ
Цель: анализ данных литературы о возможностях методов нейровизуализации в диагностике мышечных дистоний. В статье рассматриваются результаты исследований диффузионно-тензорной магнитно-резонансной томографии (МРТ) с трактографией, воксельной МР-морфометрии, функциональной МРТ (фМРТ), МР-спектроскопии, позитронно-эмиссионной томографии (ПЭТ) и однофотонной эмиссионной компьютерной томографии (КТ) головного мозга при первичных мышечных дистониях. Материалом исследования послужили публикации из баз данных PubMed и eLibrary. Период электронного поиска составил 1976-2021 гг., использовались комбинации ключевых слов «dystonia» и «neuroimaging». Для написания обзора использованы 34 источника. Несмотря на то, что постановка диагноза мышечной дистоний основывается на клинической картине, достижения современных методов нейровизуализации могут помочь в дифференциальной диагностике ее первичных и вторичных форм, а также определения тактики хирургического лечения. Для установления функциональных нейроанатомических субстратов наиболее предпочтительным методом нейровизуализации является фМРТ с измерением функциональной активности коры головного мозга, что особенно важно при действие-специфических формах дистоний и выборе тактики лечения в функциональной нейрохирургии.
Двигательные расстройства, дистония, магнитно-резонансная томография, нейровизуализация
Короткий адрес: https://sciup.org/149141767
IDR: 149141767 | УДК: 616.74-009.51
The role of visualization research methods in the diagnosis of primary muscle dystonia (review)
Objective: to analyze the literature data on the possibilities of neuro-imaging methods in the diagnosis of muscular dystonia. This article discusses the results of studies of diffusion tensor magnetic resonance imaging (MRI) with tractography (DT-MRI), voxel MR morphometry (VOM), functional MRI (fMRI), MR spectroscopy, positron emission tomography (PET) and single-photon emission computed tomography (SPECT) of the brain in primary muscular dystonia. The research material was the analysis of literary data published in the PubMed and eLibrary databases. The period of electronic search was 1976-2021, combinations of the keywords "dystonia" and "neuro-imaging" were used. 34 sources were used to write the review. Despite the fact that the diagnosis of muscular dystonia is based on the clinical picture, the achievements of modern neuro-imaging methods can help in the differential diagnosis of primary and secondary forms of muscular dystonia, as well as determining the tactics of surgical treatment. To determine functional neuroanatomic substrates, the most preferred method of neuro-imaging is fMRI with measurement of the functional activity of the cerebral cortex, which is especially important for action-specific forms of dystonia and the choice of treatment tactics in functional neurosurgery.
Текст научной статьи Роль визуализационных методов исследования в диагностике первичных мышечных дистоний (обзор)
1 Введение. Мышечная дистония — это синдром, характеризующийся устойчивыми или прерывистыми мышечными сокращениями, вызывающими ненормальные, часто повторяющиеся движения, позы или и то и другое. Дистонические движения обычно однотипны и имеют вращательный характер, а также могут сопровождаться дрожанием. Дистония часто инициируется или усугубляется произвольными движениями и связана с избыточной активацией мышц [1]. В последние годы, благодаря развитию нейрови-зуализационных инструментов, значительно расширены знания об этиологии и патогенезе мышечных дистоний, раскрыты новые пути патогенеза.
В классическом понимании в основе патогенеза дистонии лежит дисфункция базальных ганглиев.
Фундаментальная схема функционирования базальных ганглиев включает два основных пути: активирующий прямой путь (кора — полосатое тело — внутренний сегмент бледного шара — таламус — кора) и непрямой путь, оказывающий тормозящее действие (кора — полосатое тело — наружный сегмент бледного шара — субталамическое ядро — внутренний сегмент бледного шара — таламус — кора).
В настоящее время данная концепция претерпевает изменения и взамен предлагается патогенетическая модель обширной подкорковой сети (рис. 1). В этой модели базальные ганглии рассматриваются как «круги», организованные для выбора желаемых действий и подавления потенциально конкурирующих нежелательных действий, имеющие многочисленные афферентные и эфферентные связи с разными отделами головного мозга, в результате чего формируются сложные кольцевые пути, которые
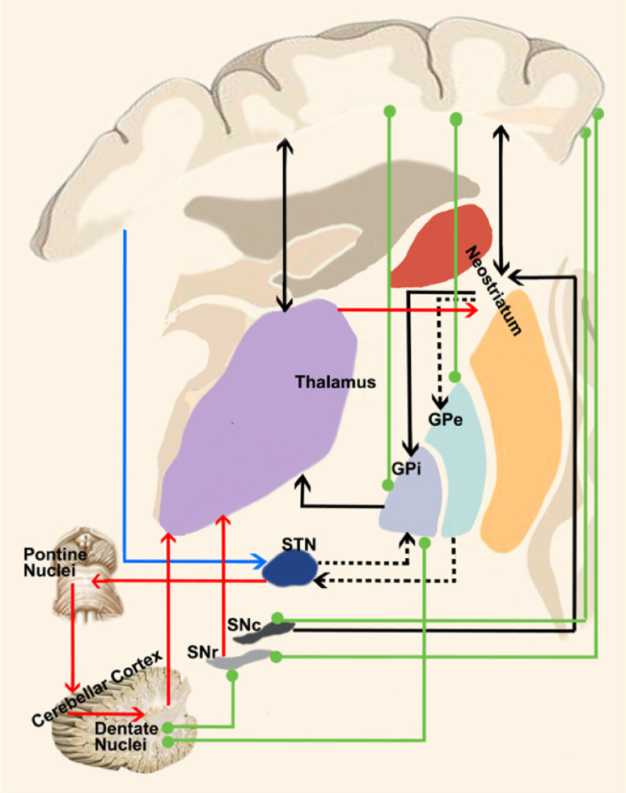
Рис. 1. Модель патогенеза дистонии по A. Quartarone и соавт. [2].
Предлагаемая модель объединяет «классические» и «новые» кортикобазально-мозжечковые пути. Сплошные черные линии демонстрируют «прямой» путь. Пунктирные черные линии изображают «непрямой» путь. Синие линии — «гиперпрямой» путь. Красные линии указывают на связи мозжечка с базальными ганглиями. Зеленые линии демонстрируют недавно выявленные связи между корой головного мозга, внутренним сегментом бледного шара (GPi), наружным сегментом бледного шара (GPe) и черной субстанцией (STN), а также дополнительные цепи между зубчатым ядром. SNr — ретикулярная часть черной субстанции. SNc — компактная часть черной субстанции способны как возбуждать, так и тормозить корковые отделы [2].
Новый взгляд на патофизиологию дистоний стал активно развиваться после внедрения новых инструментальных методов диагностики, в первую очередь методов нейровизуализации, таких как диффузионно-тензорная МРТ (ДТ-МРТ) с трактографией, вок-сельная МР-морфометрия, фМРТ, МР-спектроскопия, ПЭТ и однофотонная эмиссионная КТ.
Цель — анализ данных литературы о возможностях методов нейровизуализации в диагностике мышечных дистоний.
В данной статье проанализированы основные исследования в области нейровизуализации и объяснены новые идеи в патофизиологии дистоний, а также отражено участие разных структур головного мозга в патогенезе заболевания. Благодаря внедрению современных методов нейровизуализации облегчится дифференциальная диагностика первичных и вторичных форм мышечной дистонии, а также расширятся возможности ее хирургического лечения.
Материалом исследования послужили публикации из баз данных PubMed и eLibrary. Период электронного поиска составил с 1976 по 2021 г., использовались комбинации ключевых слов «dystonia» и «neuroimaging». Для написания обзора использованы 34 источника.
Диффузионно-тензорная магнитно-резонансная томография с трактографией. ДТ-МРТ способна оценивать региональную организацию белого вещества путем измерения диффузии воды, а также in vivo реконструировать тракты белого вещества с использованием детерминированной и вероятностной трактографии. В патофизиологии дистоний доминирующей концепцией является формирование функционального коннектома, при котором происходит дезорганизация путей, связывающих базальные ганглии, таламус, мозжечок и корковое представительство. В дополнение к глубоко измененной функциональной сети структурный коннектом характеризуется реорганизацией нормальной структуры белого вещества. Так, при действие-специфичных дистониях выявлена реорганизация островка и верхней лобной извилины [3].
Благодаря трактографии в 2002 г. описан гиперпрямой путь, связывающий кору конечного мозга с наружным и внутренним сегментами бледного шара через субталамическое ядро (кортикопаллидный путь) [4]. Продемонстрировано также взаимодействие между мозжечком и базальными ганглиями. In vivo описан афферентный путь, идущий от субталамического ядра к коре мозжечка с переключением в ядрах моста [5, 6], у приматов описаны пути, соединяющие зубчатое ядро со скорлупой и наружным сегментом бледного шара, проходящий через таламус [7], также приведены доказательства вероятного существования прямых связей зубчатого ядра мозжечка с внутренним сегментом бледного шара и черной субстанцией [8].
При цервикальной дистонии в нескольких исследованиях продемонстрированы высокие показатели фракционной анизотропии в скорлупе с двух сторон и снижение данного показателя в мозолистом теле и префронтальной коре [9, 10], что объясняется возможной повышенной клеточностью базальных ганглиев и, наоборот, потерей нейронов в областях с пониженной фракционной анизотропией [11].
Таким образом, на основании данных, полученных с помощью нейровизуализационных методов, в частности ДТ-МРТ с трактографией, предлагается пересмотреть патофизиологическую модель фокальной дистонии как расстройства не только функциональных, но и структурных коннектомов [12].
Воксельная МР-морфометрия и измерение толщины коры. Метод МР-морфометрии заключается в повоксельном сравнении серого и белого веществ между пациентами и группой контроля, сопоставимых по полу и возрасту [13]. С помощью воксельной МР-морфометрии можно обнаружить и количественно оценить различия в объеме серого и белого веществ головного мозга. Этот метод дополняет возможность измерения толщины коры на основании определения внутренних и внешних границ.
Согласно данным многочисленных исследований у пациентов с первичными фокальными формами дистоний обычно наблюдается двустороннее увеличение объема базальных ганглиев, преимущественно скорлупы, а также области сенсомоторной коры [14–16].
Однако опубликованы работы с противоположными результатами. Так, в исследовании M. Obermann с соавт. обнаружено значительное двустороннее уменьшение серого вещества в скорлупе вместе с двусторонним увеличением серого вещества в хвостатом ядре у пациентов с цервикальной дистонией и блефароспазмом в сравнении с контролем [17]. В исследовании D. Martino с соавт. 2011 г., посвящен- ном анализу объема серого вещества у пациентов с блефароспазмом, выявлено различие в объеме серого вещества исключительно в областях коры головного мозга (в левой постцентральной извилине и левой верхней височной извилине), что объясняет наличие сенсомоторной дезинтеграции как важнейшего звена патогенеза в модуляции моторных феноменов дистонии [18].
Для действие-специфичных дистоний продемонстрировано увеличение объема серого вещества в области первичной моторной коры на контрлатеральной стороне по отношению к пораженной руке, двустороннее увеличение объемов серого вещества сенсомоторной коры [19, 20]. Это связано с тем, что выполнение сложных двигательных актов требует значительного участия корковых отделов, в первую очередь таких, как лобные и теменные доли. Эти находки подтверждают, что аномальная функциональная организация корковых отделов — один из основных компонентов патофизиологии мышечных дистоний [21].
Не обнаружено корреляции между выявленными структурными аномалиями и продолжительностью и тяжестью цервикальной дистонии, за исключением миоклонической дистонии, для которой продемонстрирована положительная корреляция между тяжестью дистонии и двусторонним увеличением скорлупы [22, 23].
В клинической картине дистонии в настоящее время большое внимание уделяется немоторным симптомам, таким как тревога и депрессия. Интересные результаты опубликованы в 2020 г., где вок-сельная МР-морфометрия проводилась пациентам с синдромом Мейжа с сопутствующей депрессией и без таковой. Участие базальных ганглиев как обязательной анатомической основы развития дистонии также не было подтверждено, но продемонстрировано четкое вовлечение гиппокампа и клина затылочной доли у пациентов с сопутствующими психоэмоциональными нарушениями [24].
Функциональная магнитно-резонансная томография. фМРТ — методика, измеряющая гемодинамический ответ, вызванный нейронной активацией на основании соотношения оксигемоглобина и дезоксигемоглобина. Существует два основных способа проведения функциональной МРТ с измерением функциональной активности коры головного мозга: при выполнении определенного задания в сравнении с его активностью в покое/с контрольным заданием (task fMRI); в покое (resting state fMRI (RS-fMRI) [13].
Сегодня фМРТ является наиболее часто используемым методом визуализации в исследованиях у пациентов с фокальной дистонией. Это связано с тем, что данная методика позволяет изучать дистонию как динамический кинезиогенный феномен, так как во время проведения фМРТ-сканирования можно выполнять различные действия, например письмо, рисование или любые другие движения руками, моргание, тесты на визуальную и тактильную стимуляцию.
Большое количество исследований фМРТ подтвердило участие базальных ганглиев, таламуса, мозжечка, сенсомоторной коры в патофизиологии дистоний. При выполнении движений, вызывающих дистонический феномен, характерно увеличение активности данных областей. Так, при писчем спазме после письма отмечается повышенная активность контралатерального таламуса, базальных ганглиев, первичной сенсомоторной коры и мозжечка с ипси- латеральной стороны, одно- или двусторонняя активация скорлупы при зажмуривании и активация зрительной коры при спонтанном моргании у пациентов с блефароспазмом. И наоборот, задачи, которые не вызывают дистонию, приводят к снижению активации вышеперечисленных областей.
Благодаря фМРТ во время сенсорной стимуляции обнаружено уменьшение расстояния между корковым представительством 2–5-го пальцев в первичной сенсорной коре при писчем спазме [12]. В исследовании K. Uehara и соавт. продемонстрирована аномальная соматотопия при амбушюрных дистониях и аномальная мозговая активность в первичных моторных и сенсорных областях справа, левой скорлупе и мозжечке при сохраненной соматотопии при действие-специфичных дистониях. Вероятно, аномальная мозговая активность и измененная со-матотопическая проекция связаны с различными аспектами дистонических симптомов [25].
Продемонстрированы эффекты ботулинического токсина на центральную нервную систему. При цервикальной форме дистонии увеличение активации сенсомоторной коры по данным фМРТ выявлено даже после первой инъекции ботулинического токсина [26].
Магнитно-резонансная спектроскопия. МР-спектроскопия — активно развивающийся метод диагностики, позволяющий неинвазивно оценить концентрацию различных метаболитов в заданных областях головного мозга. Данный метод применен в исследовании количественной оценки уровня гамма-аминомасляной кислоты (ГАМК) в структурах головного мозга у пациентов с дистониями.
Первые исследования продемонстрировали сниженный уровень ГАМК в сенсомоторной коре и чечевицеобразном ядре, противоположных пораженной руке, у пациентов с фокальной дистонией кисти по сравнению со здоровыми испытуемыми [27]. Согласно исследованию K. Simonyan, ГАМК-ергический дефицит может быть результатом потери или снижения плотности ГАМК-рецепторов, аномальных связывающих свойств этих рецепторов или снижения синтеза ГАМК из-за потери ингибирующих интернейронов при дистонии [28]. Снижение доступности ГАМК-рецепторов в нижней теменной коре связано с увеличением объема серого вещества и повышенной активностью мозга [29]. По всей вероятности, дисфункция в работе ГАМК-ергической системы может играть определенную роль в патофизиологии дистонии.
В качестве иллюстрации приводим собственное наблюдение пациента.
Пациентка Б., 57 лет, обратилась с жалобами на насильственное зажмуривание глаз, непроизвольные движения в области нижней трети лица, поворот и подергивания головы влево, подъем левого плеча.
Считает себя больной с 20-летнего возраста, когда впервые появились частые моргания, зажмуривания глаз, затем постепенно в течение нескольких лет присоединились дистонические симптомы в нижней трети лица в виде оромандибулярной дистонии, в области шеи в виде тортилатероколлиса влево с дистоническим тремором и подъемом левого плеча. В неврологическом статусе: черепно-мозговые нервы — зрачки d=s, движения глазных яблок в полном объеме, двусторонний блефароспазм, лицо симметрично, бульбарных нарушений нет, насильственные движения в нижней трети лица в виде оромандибу-лярной дистонии. Сухожильные рефлексы d=s. Мышечная сила 5 баллов, чувствительность сохранена.
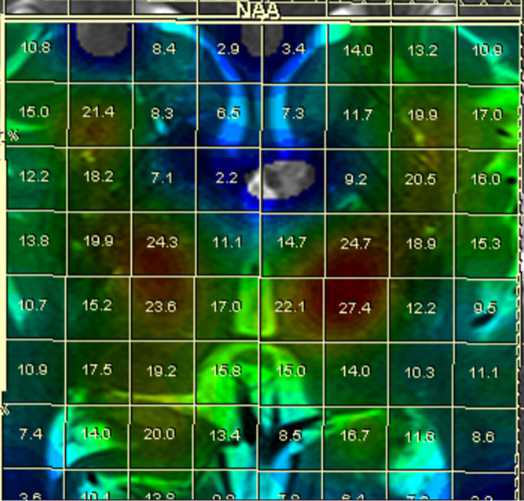
Рис. 2. Результат спектроскопии.
На цветной карте отражается повышение NAA в области базальных ганглиев (красный цвет)
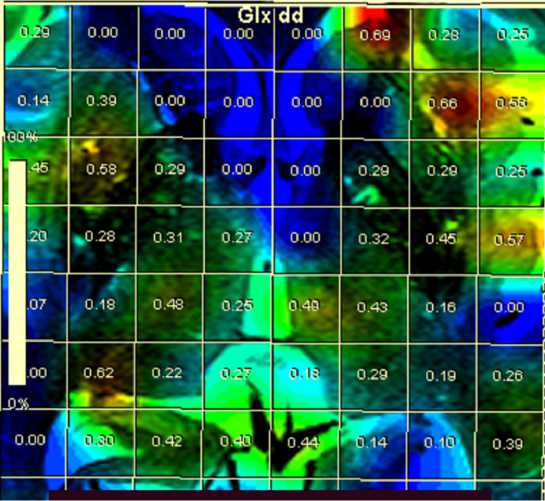
Рис. 3. Результат спектроскопии.
На цветной карте отражено распределение Glx, являющегося предшественником ГАМК. Отмечено снижение индекса Glx/NAA в области базальных ганглиев
Дистоническая установка головы и шеи в виде торти-латероколлиса влево, а также дистонический тремор головы по типу «нет — нет» и подъем левого плеча. В позе Ромберга устойчива, координаторные пробы выполняет удовлетворительно. Патологических знаков не определяется. Пациентке установлен диагноз сегментарной формы мышечной дистонии и рекомендованы регулярные инъекции ботулинического токсина типа А с кратностью 1 раз в 4 мес. С учетом постепенной генерализации процесса было проведено МРТ головного мозга с режимом спектроскопии.
По данным исследования (рис. 2) обнаружены пики NAA (N-ацетиласпартата) в области базальных ганглиев, что характерно для неповрежденных нейронов и, вероятно, связано с их высокой функциональной активностью, а также снижение индекса Glx (глутамата и глутамина)/NAA (рис. 3), что косвенно указывает на низкий уровень ГАМК в базальных ганглиях, тем самым подтверждает значимость нейромедиаторных нарушений в патогенезе дистоний на примере конкретного клинического случая.
Позитронно-эмиссионная томография. ПЭТ — это сцинтиграфический метод, основанный на регистрации гамма-квантов после аннигиляции позитронов с электронами. Двумя радиофармпрепаратами, обычно используемыми в исследованиях ПЭТ при фокальной дистонии, являются [18F]-фтордезоксиглюкоза и [15О]-Н 2 О. Поглощение [18F]-фтордезоксиглюкозы отражает региональный метаболизм глюкозы, а [15O]-H2O количественно определяет региональный мозговой кровоток (rCBF). Кроме того, существуют радиофармпрепараты для ПЭТ которые связываются с рецепторами дофамина D2/3 — [11C]-N-метил-спиперон ([11C]-NmSp) и [18F]-спиперон ([18F]-SP). Метаболизм глюкозы чаще был повышен в базальных ганглиях, таламусе, мозжечке и варолиевом мосту. В большинстве исследований было обнаружено снижение регионального мозгового кровотокав первичной сенсомоторной коре и увеличение регионального мозгового кровотока в лобных и теменных ассоциативных областях [11].
В работе V. Belenky с соавт. сравнивалась ПЭТ с [18F]-фтордезоксиглюкозой у пациентов с эссенциальным тремором и дистонией. Исследование де- монстрирует сниженный метаболизм глюкозы в области таламуса и лентикулярного ядра у пациентов с дистонией и сниженный метаболизм глюкозы в области моста и поясной извилины в группе эссенциального тремора [30]. При цервикальной дистонии при проведении ПЭТ описана двусторонняя активация зрительной коры у пациентов, которые использовали сенсорный трюк. Зрительная кора участвует в тактильной ориентации, что, по-видимому, помогает определить положение головы относительно туловища и, соответственно, скорректировать это положение [31].
Однофотонная эмиссионная компьютерная томография. Однофотонная эмиссионная КТ также является сцинтиграфическим методом, при котором радиофармпрепараты метятся изотопами, способными связываться со специфическими рецепторами или транспортерами в головном мозге.
По данным J. Hierholzer и соавт., у пациентов с цервикальной дистонией наблюдалось более высокое связывание рецепторов D2/3R в полосатом теле, с противоположной стороны по отношению к вращению головы, что может указывать на снижение плотности постсинаптических рецепторов D2/3 в чечевицеобразном ядре [32]. При фокальной дистонии кисти результаты также указывают на дисфункцию дофаминергической системы [33].
Компьютерная томография и магнитно-резонансная томография шейного отдела и мягких тканей шеи. Для более точного выбора мышц-мишеней для ботулинотерапии при цервикальной дистонии было проведено исследование, где пациентам выполнялись послойные КТ-снимки мягких тканей шеи и МРТ шейного отдела позвоночника и мягких тканей. В подавляющем большинстве наблюдалось вовлечение мышц, осуществляющих движения в области соединения черепа и шейного отдела позвоночника и мышц, которые приводят в движение только шейный отдел позвоночника. КТ-снимки на уровнях С1, С2 и С7 наиболее полезны для дифференцирования тор-тикапута и тортиколлиса. Для остальных форм цервикальной дистонии может быть полезна МРТ мягких тканей шеи, где возможно увидеть асимметрию мышц, а для дифференциальной диагностики латерокапута и латероколлиса достаточно простого рентгеновского снимка в переднезадней проекции [34].
Заключение. Развитие методов и инструментов нейровизуализации привело к расширению знаний о нейронных изменениях при дистониях. Мышечные дистонии — это синдром, патогенез которого не ограничивается дисфункцией базальных ганглиев, в его основе лежит нарушение функционирования целой нейрональной сети, включающей подкорковые и корковые области. С помощью ДТ-МРТ описаны новые пути взаимодействия базальных ганглиев с мозжечком и корковыми отделами, что позволяет рассматривать патофизиологию мышечных дистонией как кор-тикобазально-мозжечковый коннектом, с наличием не только функциональных, но и структурных изменений. Продемонстрировано активное участие коры головного мозга, базальных ганглиев в патогенезе заболевания с помощью воксельной МР-морфометрии, изменение содержания нейрометаболитов в базальных ганглиях по данным МР-спектроскопии. Результаты сцинтиграфических методов исследования головного мозга (ПЭТ, однофотонная эмиссионная КТ) подтверждают вовлечение разных областей мозга, а также дисфункцию дофаминергической системы при мышечных дистониях.
Безусловно, современные методы нейровизуализации будут активно внедряться в клиническую практику, в первую очередь для дифференциальной диагностики первичных и вторичных форм мышечных дистоний.
Для определения функциональных нейроанато-мических субстратов наиболее предпочтительным методом нейровизуализации является фМРТ с измерением функциональной активности коры головного мозга, что особенно важно при действие-специфи-ческих формах дистоний и выборе тактики лечения в функциональной нейрохирургии.
Список литературы Роль визуализационных методов исследования в диагностике первичных мышечных дистоний (обзор)
- Albanese A, Bhatia K, Bressman SB, et al. Phenomenology and classification of dystonia: a consensus update. Mov Disord 2013; 28 (7): 863–73. DOI: 10.1002 / mds.25475.
- Quartarone A, Cacciola A, Milardi D, et al. New insights into cortico-basal-cerebellar connectome: clinical and physiological considerations. Brain 2020; 143 (2): 396–406. DOI: 10.1093 / brain / awz310.
- Bianchi S, Fuertinger S, Huddleston H, et al. Functional and structural neural bases of task specificity in isolated focal dystonia. Mov Disord 2019; 34 (4): 555–63. DOI: 10.1002 / mds.27649.
- Nambu A, Tokuno H, Takada M. Functional significance of the cortico-subthalamo-pallidal ‘hyperdirect’ pathway. Neurosci Res 2002; 43 (2): 111–7. DOI: 10.1016 / s0168-0102(02)00027–5.
- Bostan AC, Dum RP, Strick PL. The basal ganglia communicate with the cerebellum. Proc Natl Acad Sci USA. 2010; 107 (18): 8452–6. DOI: 10.1073 / pnas.1000496107.
- Milardi D, Arrigo A, Anastasi G, et al. Extensive direct subcortical cerebellum-basal ganglia connections in human brain as revealed by constrained spherical deconvolution tractography. Front Neuroanat 2016; 10: 29. DOI: 10.3389 / fnana.2016.00029.
- Hoshi E, Tremblay L, Féger J, et al. The cerebellum communicates with the basal ganglia. Nat Neurosci 2005; 8 (11): 1491–3. DOI: 10.1038 / nn1544.
- Snider RS, Maiti A, Snider SR. Cerebellar pathways to ventral midbrain and nigra. Exp Neurol 1976; 53 (3): 714–28. DOI: 10.1016 / 0014-4886(76)90150-3.
- Fabbrini G, Pantano P, Totaro P, et al. Diffusion tensor imaging in patients with primary cervical dystonia and in patients with blepharospasm. Eur J Neurol. 2008; 15 (2): 185–9. DOI: 10.1111 / j.1468–1331.2007.02034.x.
- Zoons E, Booij J, Nederveen AJ, et al. Structural, functional and molecular imaging of the brain in primary focal dystonia — a review. Neuroimage 2011; 56 (3): 1011–20. DOI: 10.1016 / j.neuroimage.2011.02.045.
- Hanekamp S, Simonyan K. The large-scale structural connectome of task-specific focal dystonia. Hum Brain Mapp 2020; 41 (12): 3253–65. DOI: 10.1002 / hbm.25012.
- Colosimo C, Pantano P, Calistri V, et al. Diffusion tensor imaging in primary cervical dystonia. J Neurol Neurosurg Psychiatry 2005; 76 (11): 1591–3. DOI: 10.1136 / jnnp. 2004.056614.
- Krotenkova MV, Brjuhov VV, Morozova SN et al. Modern neuroimaging technologies. Radiology — Practice 2017; 2 (62): 47–63. Russian (Кротенкова М. В., Брюхов В. В., Морозова С. Н. и др. Современные технологии нейровизуализации (лекция). Радиология — практика. 2017; 2 (62): 47–63).
- Etgen T, Mühlau M, Gaser C, et al. Bilateral grey-matter increase in the putamen in primary blepharospasm. J Neurol Neurosurg Psychiatry 2006; 77 (9): 1017–20. DOI: 10.1136 / jnnp.2005.087148.
- Bradley D, Whelan R, Walsh R, et al. Temporal discrimination threshold: VBM evidence for an endophenotype in adult onset primary torsion dystonia. Brain 2009; 132 (Pt 9): 2327–35. DOI: 10.1093 / brain / awp156.
- Black KJ, Ongür D, Perlmutter JS. Putamen volume in idiopathic focal dystonia. Neurology 1998; 51 (3): 819–24. DOI: 10.1212 / wnl.51.3.819.
- Obermann M, Yaldizli O, De Greiff A, et al. Morphometric changes of sensorimotor structures in focal dystonia. Mov Disord 2007; 22 (8): 1117–23. DOI: 10.1002 / mds.21495.
- Martino D, Di Giorgio A, D’Ambrosio E, et al. Cortical gray matter changes in primary blepharospasm: a voxel-based morphometry study. Mov Disord 2011; 26 (10): 1907–12. DOI: 10.1002 / mds.23724.
- Delmaire C, Vidailhet M, Elbaz A, et al. Structural abnormalities in the cerebellum and sensorimotor circuit in writer’s cramp. Neurology 2007; 69 (4): 376–80. DOI: 10.1212 / 01.wnl.0000266591.49624.1a.
- Garraux G, Bauer A, Hanakawa T, et al. Changes in brain anatomy in focal hand dystonia. Ann Neurol 2004; 55 (5): 736–9. DOI: 10.1002 / ana.20113.
- Tomić A, Agosta F, Sarasso E, et al. Brain structural changes in focal dystonia-what about task specificity? A multimodal MRI study. Mov Disord 2021; 36 (1): 196–205. DOI: 10.1002 / mds.28304.
- Nevrlý M, Hluštík P, Hok P, et al. Changes in sensorimotor network activation after botulinum toxin type A injections in patients with cervical dystonia: a functional MRI study. Exp Brain Res 2018; 236 (10): 2627–37. DOI: 10.1007 / s00221‑018‑5322‑3.
- Beukers RJ, van der Meer JN, van der Salm SM, et al. Severity of dystonia is correlated with putaminal gray matter changes in myoclonus-dystonia. Eur J Neurol 2011; 18 (6): 906–12. DOI: 10.1111 / j. 1468-1331.2010.03321.x.
- Liu J, Li L, Chen L, et al. Grey matter changes in Meige syndrome: A voxel-based morphology analysis. Sci Rep 2020; 10 (1): 14533. Published 2020 Sep 3. DOI:10.1038 / s41598‑020‑71479‑9.
- Uehara K, Furuya S, Numazawa H, et al. Distinct roles of brain activity and somatotopic representation in pathophysiology of focal dystonia. Hum Brain Mapp 2019; 40 (6): 1738–49. DOI: 10.1002 / hbm.24486.
- Opavský R, Hluštík P, Otruba P, Kaňovský P. Somatosensory cortical activation in cervical dystonia and its modulation with botulinum toxin: an fMRI study. Int J Neurosci 2012; 122 (1): 45–52. DOI: 10.3109 / 00207454.2011.623807.
- Levy LM, Hallett M. Impaired brain GABA in focal dystonia. Ann Neurol 2002; 51 (1): 93–101.
- Simonyan K. Neuroimaging applications in dystonia. Int Rev Neurobiol 2018; (143): 1–30. DOI: 10.1016 / bs.irn.2018.09.007.
- Gallea C, Herath P, Voon V, et al. Loss of inhibition in sensorimotor networks in focal hand dystonia. Neuroimage Clin 2017; (17): 90–7. Published 2017 Oct 13. DOI: 10.1016 / j.nicl.2017.10.011.
- Belenky V, Stanzhevsky A, Klicenko O, et al. Brain positron emission tomography with 2-18F-2‑deoxi-D-glucose of patients with dystonia and essential tremor detects differences between these disorders. Neuroradiol J 2018; 31 (1): 60–8. DOI: 10.1177 / 1971400917719912.
- Naumann M, Magyar-Lehmann S, Reiners K, et al. Sensory tricks in cervical dystonia: perceptual dysbalance of parietal cortex modulates frontal motor programming. Ann Neurol 2000; 47 (3): 322–8.
- Hierholzer J, Cordes M, Schelosky L, et al. Dopamine D2 receptor imaging with iodine-123‑iodobenzamide SPECT in idiopathic rotational torticollis [published correction appears in J Nucl Med 1995; 36 (4): 568]. J Nucl Med 1994; 35 (12): 1921–7.
- Horstink CA, Praamstra P, Horstink MW, et al. Low striatal D2 receptor binding as assessed by [123I] IBZM SPECT in patients with writer’s cramp. J Neurol Neurosurg Psychiatry 1997; 62 (6): 672–3.
- Reichel G, Stenner A, Jahn A. Cervical dystonia: clinical-radiological correlations and recommendations for the correction of botulinum therapy. S. S. Korsakov Journal of Neurology and Psychiatry 2012; 112 (1): 73–9. Russian (Reichel G, Stenner A, Jahn A. Цервикальные дистонии: клинико-радиологические корреляции рекомендации по коррекции ботулинотерапии. Журнал неврологии и психиатрии им. С. С. Корсакова 2012; 112 (1): 73–9).


