Схема кроветворения (лекция, часть 1)
Автор: Зенина М.Н., Бессмельцев С.С.
Журнал: Вестник гематологии @bulletin-of-hematology
Рубрика: Гематология: вчера, сегодня, завтра
Статья в выпуске: 2 т.20, 2024 года.
Бесплатный доступ
Схема кроветворения, изучение гемопоэза – это динамический процесс, вносящий коррективы по мере внедрения новых методов и накопления данных множественных экспериментов. В лекции представлен современный взгляд на кроветворение и его регуляцию, строение и функции клеток крови у человек. Совокупность полученных данных меняет устоявшиеся взгляды на гемопоэз и позволяет рассматривать его как процесс, происходящий в условиях динамического равновесия.
Кроветворение, созревания клеток крови, эритроциты, лейкоциты, тромбоциты
Короткий адрес: https://sciup.org/170204384
IDR: 170204384
Scheme of hematopoiesis
The scheme of hematopoiesis, the study of hematopoiesis is a dynamic process that makes adjustments as new methods are introduced and data from multiple experiments are accumulated. The lecture presents a modern view of hematopoiesis and its regulation, the structure and functions of blood cells in humans. The totality of the data obtained changes the established views on hematopoiesis and allows us to consider it as a process taking place in conditions of dynamic equilibrium.
Текст научной статьи Схема кроветворения (лекция, часть 1)
«Душа тела в крови» — так звучат слова Ветхого Завета. Во все времена люди понимали, какое большое значение для организма имеет кровь. Множество легенд, суеверий, надежд на здоровье и долголетие связывали с ней. Постепенно, с развитием науки, наши знания о функциях кровеносной системы в обеспечении жизнедеятельность всего человеческого организма пополнялись и стали основой современного понимания физиологии крови.
Представление о крови, как системе, объединяющей непосредственно кровь, органы кроветворения, разрушения и аппарат регуляции органы кроветворения (костный мозг, селезенка, лимфоузлы, тимус), предложил в 1939 году наш соотечественник, Георгий Фёдорович Ланг — выдающийся терапевт прошлого века (рис. 1).

Рисунок 1. Ланг Г.Ф.

Рисунок 2. Профессор Максимов А.А.

Рисунок 3. Публикация статьи.
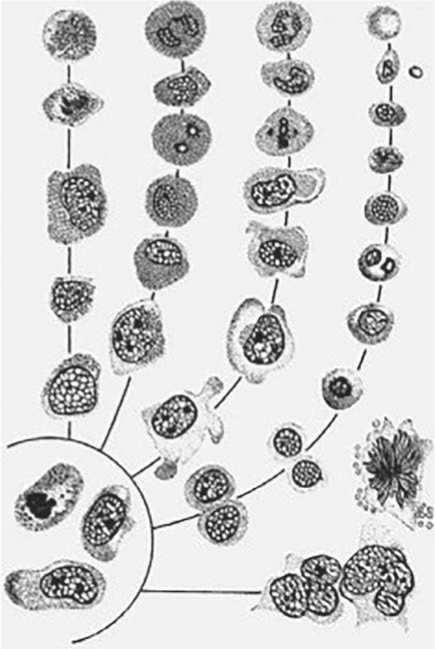
Рисунок 4. Схема кроветворения по Максимову А.А.
Задолго до этого, в 1906–1910 годах профессор А.А. Максимов (Рисунок 2) провел цикл исследований и завершил их работой «Der Lymphozyt als gemeinsame Stammzelle der verhidenen Blutelemente in der embryonalen Entwiclung und im postfetalen Leben den Sugetiere» (Рисунок 3) – «Лимфоцит, как общая стволовая клетка разнообразных элементов крови в эмбриональном развитии и постфетальной жизни млекопитающих». Впервые в отечественной и мировой медицинской литературе был применен термин «стволовая клетка», предложенный Х. Шри-де в 1907 году, и что самое главное – обосновано существование как в эмбриогенезе, так и во взрослом состоянии родоначальной (стволовой) клетки всех форменных элементов крови. По сути, была сформулирована концепция унитарной теории кроветворения, согласно которой все клетки крови развиваются из одной родоначальной стволовой кроветворной клетки (ГСК).
До Максимова существовало несколько теорий о гистогенезе крови как ткани. Так, дуалистическая теория, основателями которой являлись М. Нагели, Д. Тюрк, Т. Шридд и К. Паней (1900-1923), гласила, что существует две стволовые клетки крови: для миелопоэза и лимфопоэза. Для миелопоэза материнской (т.е. стволовой) клеткой считался эндоте-лиоцит кровеносных сосудов, дающий миелобла-сты, тогда как лимфобласты лимфатических узлов развивались из эндотелия лимфатических сосудов и обеспечивали лимфоидное кроветворение. Соглас- но полифилетической теории (основоположники П. Эрлих, Э. Розенталь и соавт., 1891-1920), каждая разновидность форменных элементов крови имеет свою стволовую клетку-предшественницу, но все они развиваются из единой мезенхимной клетки. И, наконец, триалистическая теория (сформулирована Л. Ашоффом, К. Шиллингом, Д. Волленбергом и др., 1914-1926) помимо стволовых клеток для миелопо-эза и лимфопоэза предполагала наличие стволовой клетки для моноцитов-макрофагов. Они, по представлениям авторов теории, развивались из клеток ретикуло-эндотелиальной системы (РЭС).
Унитарная (монистическая) теория кроветворения, предложенная А.А. Максимовым, до сих пор является ведущей теорией и говорит о том, что в основе гемопоэза лежит одна- единственная клетка, дающая начало всем росткам кроветворной ткани (свойство полипотентности). Максимов был гистологом и пытался найти морфологические признаки ГСК. Он считал, что это лимфоцитоподобная, мезенхимная по своему происхождению клетка (рис. 4).
Экспериментальное же подтверждение существования ГСК было получено только в 1961 г. в опытах известных канадских исследователей J. Till и E. McCulloch. Исследователи вводили взвесь костного мозга внутривенно смертельно облученным мышам, у которых в селезенке на 7-14 сутки формировались макроколонии, состоящие из разного типа миелоидных элементов (гранулоциты, эритроциты, мегакариоциты, смешанные колонии), впослед- ствии обнаружены были и лимфоидные клетки.
Разделение клеток-предшественников лимфо- и миелопоэза обнаружили в 1960-61 гг. исследователи Ноуэл и Хунгерфорд (G.Nowell, D.Hungerford, США), когда в клетках костного мозга у 90-95 % обследованных больных ХМЛ обнаружили Ph-хромосому только в миелоидных клетках и выдвинули гипотезу, что есть отдельные клетки-предшественники миелопоэза и лимфопоэза. В дальнейшем культуральные работы подтвердили это утверждение и доказали наличие общего прекурсора миелопоэза. Последующее развитие культуральной техники этого направления исследований позволило уточнить схему кроветворения у ранних предшественников гемопоэза.
После многих лет исследований стало понятно, что клетки крови представляют собой сложную систему, жизнедеятельность которой состоит из нескольких этапов: рождение и созревание клеток крови в костном мозге; пребывание и функционирование в кровеносном русле; пребывание и функционирование в тканях.
Основной задачей кроветворения является поддержание постоянства количественного и качественного состава отдельных звеньев системы крови. В основе этого процесса, в условиях постоянно меняющихся потребностей организма в клетках крови, лежит соблюдение основного закона кинетики кроветворения: «В единицу времени рождается и умирает одно и то же количество клеток». Соблюдение этого закона обеспечивается сложными механизмами регуляции кроветворения. Учитывая, что большинство форменных элементов крови имеет короткий жизненный цикл (скорость распада эритроцитов, например, составляет 10 млн в секунду), необходимо постоянное обновление различных клеточных популяций крови.
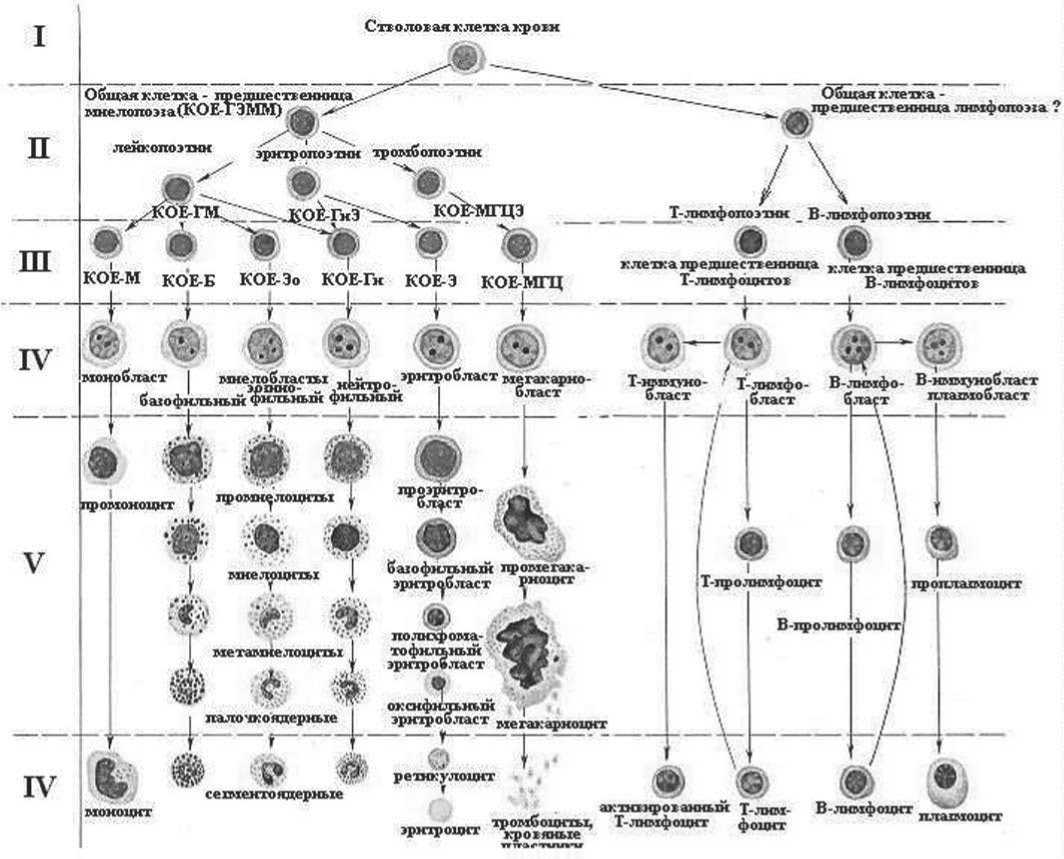
Рисунок 5. Схема кроветворения. Схема кроветворения и основные факторы транскрипции (Руководство по гематологии: в 3 т. Т. 1. Под ред. А.И. Воробьева. 2002)
Таким образом, мы подошли к формулировке понятия кроветворения. Кроветворение (гемопоэз) — это процесс образования, развития и созревания клеток крови (эритроцитов, лейкоцитов, тромбоцитов).
Выделяют эмбриональный и постэмбриональный гемопоэз. Эмбриональный гемопоэз – это процесс образования крови как ткани. Постэмбриональный гемопоэз – процесс образования форменных элементов крови в ходе физиологической и репаративной регенерации.
Признание существования единой полипотент-ной гемопоэтической стволовой клетки (ПГСК) послужило основой для создания современной схемы кроветворения (Рисунок 5), представленной практически одновременно, в 1971-1973 гг., Mathe с со-авт., И.Л. Чертковым и А.И. Воробьевым, Metcalf и Moore.
Принцип построения ее следующий:
– в каждом вертикальном ряду находятся клетки одного вида, последовательных стадий созревания
-
– в каждом горизонтальном ряду – клетки разных видов, одной стадии зрелости
-
– в верхних отделах – молодые клетки
-
– в нижних – зрелые
-
– в двух нижних горизонтальных рядах представлены зрелые клетки, совместно пребывающие в циркуляции.
Гемопоэтические стволовые клетки (ГСК) дают начало прогениторным клеткам и клеткам предшественникам, которые делятся и дифференцируются в зрелые клетки определенного типа ткани. Такие клетки называют еще коммитированными.
Клетки предшественники образуют дифференцированные клетки через ряд поколений промежуточных клеток, становящихся все более зрелыми. Таким образом, гемопоэтические клетки подразделяются на 5 классов, в зависимости от уровня дифференцировки.
Разберем подробнее классы гемопоэтических клеток.
Класс I. Стволовая гемопоэтическая клетка (ГСК)
Особенность клеточного пула стволовых клеток заключается в том, что постоянство его количественного состава (у человека около 0,01 % ядросодержащих клеток костного мозга) обеспечивается функцией самих стволовых клеток — одновременной способностью как к самообновлению, так и к дифференцировке. Считалось, что более 90 % стволовых клеток находятся в покоящемся состоянии (G0-фазе). Во взрослом организме человека ГСК в норме локализованы в костном мозге (0,05% от всех клеток костного мозга), однако в низких концентрациях они присутствуют также в периферической крови (0,0001% от всех лимфоцитов). Богатым источником ГСК является пуповинная кровь и плацента.
Свойства ГСК:
Плюрипотентность . ГСК способна к дифференцировке в различных направлениях и даёт начало любому виду форменных элементов крови (эритроцитам, лейкоцитам, кровяным пластинкам), поэтому ГСК называют родоначальными клетками.
Способность к самоподдержанию. ГСК способны поддерживать постоянство численности своей популяции за счёт того, что после деления стволовой клетки одна из дочерних клеток остается стволовой, сохраняя все свойства родительской клетки; вторая дочерняя клетка дифференцируется в полу-стволовую (коммитированную) стволовую клетку. Такой митоз называется асимметричным
Способность к делению (пролиферации). ГСК -долгоживущая клетка; срок её жизни - жизнь индивидуального организма.
Устойчивость к действию повреждающих факторов. Вероятно вследствие того, что ГСК делятся редко, большую часть своей жизни они пребывают в состоянии покоя; при необходимости могут вновь вступать в клеточный цикл (например, при значительных кровопотерях и при воздействии факторов роста), кроме того, ГСК защищены своим местоположением.
Морфологически ГСК не идентифицируются . ГСК выглядит как любой малый лимфоцит, их нельзя различить обычными методами под световым, или электронным микроскопом, но они имеют свой фенотип (антигенный профиль) и отсутствие ряда маркеров, свойственных зрелым клеткам крови (Lin-негативность). Благодаря определенному фенотипу ГСК можно выявить методами иммуноцитохимии (с помощью меченых моноклональных антител). Основное место локализации ГСК – красный костный мозг.
Численность ГСК составляет 1 на 2000 клеток красного костного мозга, или 1 ГСК на 1 000 000 лейкоцитов периферической крови).
Класс II. Мультипотентные коммитированные, частично детерминированные (полустволовые) клетки
Мультипотентные коммитированные клетки дают начало форменным элементам крови нескольких, но не всех, видов.
Этот класс представлен 2 типами клеток:
–родоначальной клеткой миелопоза – КОЕ-ГЭММ: эта клетка даёт начало гранулоцитам, эритроцитам, моноцитам и мегакариоцитам,
– родоначальной клеткой лимфопоэза: эта клетка даёт начало В- и Т-лимфоцитам, натуральным киллерам и некоторым дендритным клеткам. Клетки этого класса способны к ограниченному самопод-держанию. Митотическая активность клеток этого класса по-прежнему низкая. Морфологически не идентифицируются (на вид малые лимфоциты).
Мультипотентные коммитированные клетки, как и клетки следующего класса, также называют колониеобразующими единицами (КОЕ), поскольку в экспериментах на летально облученных мышах они способны образовывать колонии кроветворных клеток в их органах (селезенке). Каждая колония возникает как результат деления одной клетки, поэтому анализируя клеточный состав колонии, можно сделать вывод о потентности клетки, давшей начало этой колонии. КОЕ-ГЭММ – означает, что эта клетка даёт селезеночную колонию, состоящую из гранулоцитов (Г), эритроцитов (Э), моноцитов (М) и мегакариоцитов (М).
Класс III. Унипотентные (коммитированные) родоначальные клетки (прогениторные)
Клетки этого класса унипотентны, т.е. детерминированы в направлении развития только одного вида форменных элементов (за исключением бипо-тентной КОЕ-ГМ) [детерминация – выбор направления развития]. У них низкий потенциал самопод-держания, митотическая активность выше, чем у клеток 2-го класса, морфологически не идентифицируются (малый лимфоцит) и образуют «чистые» колонии (из одного вида форменных элементов).
Класс IV. Клетки-предшественники (бласты)
Представляют отдельные линии развития форменных элементов, их пролиферативная активность ограничена, но выше, чем у 3-го класса. Бласты обладают способностью к самоподдержанию и, что особо ценно для морфологического анализа, распознаваемы. Несмотря на то, что клетки этого класса сходны друг с другом, их можно идентифицировать при использовании стандартных методов окраски, они имеют вид крупных клеток с крупным светлым овальным ядром, в котором хорошо определяются ядрышки, и базофильной цитоплазмой.
Класс V. Созревающие клетки
Клетки этого класса подвергаются структурной и функциональной дифференцировке, в ходе которой утрачивают способность к делению (за исключением лимфоцитов и моноцитов). Идентифицируются морфологически.
Мы разобрали «горизонтальные» линии схемы кроветворения. Если рассмотреть «вертикальные» линии созревания клеток, получим совокупность составляющих ту или иную линию дифференцировки от стволовых (наименее дифференцированных) клеток до терминально (наиболее зрелых) дифференцированных. И называются такие группы дифферонами. Многие ткани содержат несколько различных дифферонов, которые взаимодействуют друг с другом.
Эритропоэз
Дифферон эритроцитарного ряда:
ГСК → КОЕ-ГЭММ → БОЕ-Э → КОЕ-Э → ПРОЭРИТРОБЛАСТ → БАЗОФИЛЬНЫЙ ЭРИТРОБЛАСТ → ПОЛИХРОМАТОФИЛЬНЫЙ ЭРИТРОБЛАСТ → ОКСИФИЛЬНЫЙ ЭРИТРОБЛАСТ → РЕТИКУЛОЦИТ → ЭРИТРОЦИТ
Начало эритроидного ряда – взрывообразующая единица эритропоэза – БОЕ-Э (BFU-E). При активации и делении БОЕ-Э образуется множество унипотентных КОЕ-Э, реагирует на интерлейкин 3, но в отличие от КОЕ-Э не чувствительна к эритропоэтину, образующемуся в почке. Из проэритробласта последовательно образуются: базофильный эритробласт (накопление рибосом и начало синтеза Hb); полихроматофильный эритробласт (накопление Hb); оксифильный эритробласт (высокое содержание Hb и остатки белоксинтезирущего аппарата, потеря способности к делению (Рисунок 6).
При дифференцировке предшественников эритроцитов в зрелые эритроциты происходят следующие процессы: уменьшение размеров клетки, выработка и накопление гемоглобина в цитоплазме, постепенное снижение числа органелл, изменение окраски цитоплазмы от базофильной (в связи с большим числом полирибосом) до оксифильной (обусловленной накоплением гемоглобина); снижение, а в дальнейшем утрата способности к делению, уменьшение размера, конденсация хроматина и выталкивание ядра из клетки.
Гранулоцитопоэз
Дифферон гранулоцитопоза:
ГСК → КОЕ-ГЭММ → КОЕ-ГнМ → КОЕ-Гн → МИЕ-ЛОБЛАСТ → ПРОМИЕЛОЦИТ → МИЕЛОЦИТ → МЕТА-МИЕЛОЦИТ→ ПАЛОЧКОЯДЕРНЫЙ НЕЙТРОФИЛ → СЕГМЕНТОЯДЕРНЫЙ НЕЙТРОФИЛ
Гранулоциты при развитии проходят следующие стадии: миелобласт (не имеет гранул), промиелоцит (первичные, азурофильные гранулы), миелоцит (появление специфических гранул, округлое ядро), метамиелоцит (бобовидное ядро), палочкоядерный и сегментоядерный нейтрофил (Рисунок 7).
По мере созревания гранулоцитов в зрелые клетки происходит уменьшение размеров клетки, изменение формы их ядер от округлой до сегментированной, накопление и изменение состава гранул
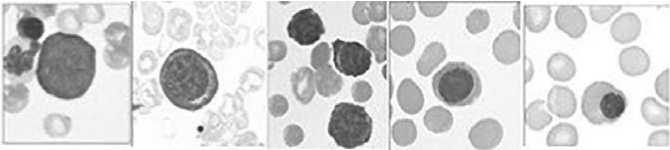
Рисунок 6. Эритробласт, проэритробласт, базофильный эритробласт, полихроматофильный эритробласт, оксифильный эритробласт.
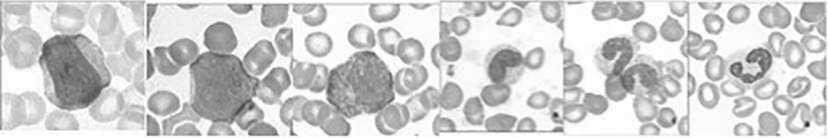
Рисунок 7. Развитие клеток нейтрофильного ряда: миелобласт, промиелоцит, миелоцит, метамиелоцит, палочкоядерный нейтрофил, сегментоядерный нейтрофил.
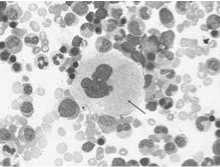
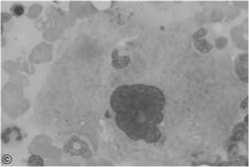
Рисунок 8. Мегакариоцит – очень крупная клетка (до 150 мкм в диаметре) имеет крупное, дольчатое полиплоидное ядро (до 64n), цитоплазму разной степени базофилии.
в цитоплазме (постепенное увеличение доли специфических гранул), утрата способности к делению, нарастание подвижности клеток и приобретение разнообразных рецепторов плазмолеммы, обеспечивающих выполнение главных функций клеток (фагоцитоз, хемотаксис и др.).
Тромбоцитопоэз
Последовательность дифференцировки можно представить следующим рядом клеток:
ГСК → КОЕ-ГЭММ → КОЕ-МГЦ →МЕГАКАРИО-БЛАСТ → ПРОМЕГАКАРИОЦИТ →МЕГАКАРИОЦИТ → ТРОМБОЦИТЫ (кровяные пластинки) (Рисунок 8).
Процесс образования и созревания тромбоцитов происходит в миелоидной ткани. Тромбоциты (кровяные пластинки) образуются в результате частичной фрагментации цитоплазмы мегакариоцитов.
Мегакариоцит – очень крупная клетка (до 150 мкм в диаметре); имеет крупное, дольчатое полиплоидное ядро (до 64n), базофильную цитоплазму. В ходе дифференцировки происходит образование и накопление гранул, характерных для тромбоцитов и содержащих специфические для них белки; формирование системы мембран (демаркационных каналов), разрезающих цитоплазму мегакариоцита на участки размером 2-4 мкм, соответствующие размерам будущих тромбоцитов; образование филоподий (протромбоцитов) – узких длинных отростков мегакариоцитов, которые через поры эндотелия синусов красного костного мозга проникают в их просвет и распадаются на отдельные кровяные пластинки (Рисунок 9).
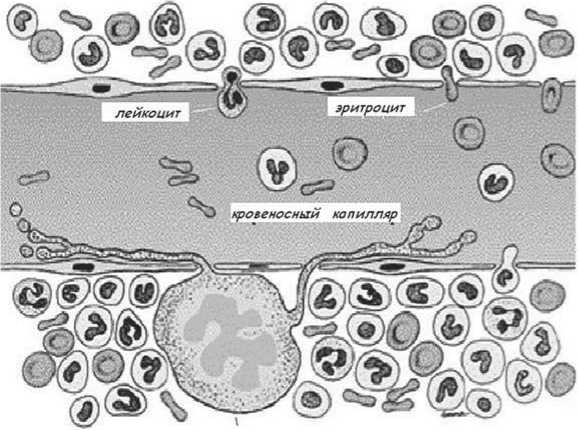
мегакариоцит
Рисунок 9. Образование тромбоцитов.
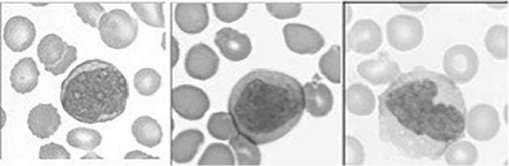
Рисунок 10. Монобласт, промоноцит, моноцит (слева направо).
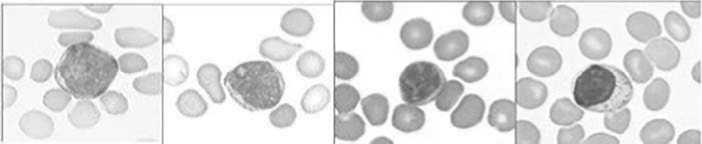
Рисунок 11. Лимфобласт, пролимфоцит, лимфоцит, широкоплазменный лимфоцит.
Моноцитопоэз
Образование моноцитов происходит из стволовых клеток костного мозга по схеме: ГСК → КОЕ-ГЭММ → КОЕ-М → монобласт → промоноцит → моноцит (Рисунок 10).
Моноциты из крови поступают в ткани, где являются источником развития различных видов макрофагов.
Иммуноцитопоэз
Лимфоидная ткань у человека имеется в составе лимфатических узлов, селезенки, миндалин, аппендикса и в других лимфоидных образованиях по ходу пищеварительного тракта. В лимфоидной ткани происходит лимфопоэз (Рисунок 11).
Исходными клетками лимфопоэза являются стволовые клетки красного костного мозга. Через стадию мультипотентных клеток (КОЕ-Л) они дифференцируются в родоначальные про-Т- и про-Влимфобласты и далее в Т- и В-лимфобласты, Т- и Впролимфоциты и Т- и В-лимфоциты. Процесс дифференцировки Т-лимфоцитов в тимусе приводит к образованию из унипотентных предшественников Т-бластов, из которых формируется эффекторные лимфоциты- киллеры, хелперы, супрессоры. В лим-фоцитопоэзе в тимусе возникают субпопуляции Т клеток с различными рецепторами (так называемая антигеннезависимая пролиферация и дифференци- ровка). Т-лимфоциты участвуют в формировании клеточного иммунитета.
Другой ряд дифференцировки в лимфопоэзе приводит к образованию из В-лимфоцитов через стадии плазмобласта и проплазмоцита — плазматических клеток (плазмоцитов) (Рисунок 12). Эти клетки вырабатывают антитела, обеспечивая гуморальный иммунитет.
В 2005 году схема кроветворения была дополнена и в нижних этажах кроветворного дерева появились еще три линии дифференцировки:
-
1) натуральные киллеры – с морфологией больших гранулярных лимфоцитов (обеспечивают естественный и противоопухолевый иммунитет);
-
2) дендритные клетки (профессиональные АПК) – имеют миелоидное (из моноцитов) и напрямую из ГСК происхождение (Рисунок 13);
-
3) тучные клетки (отдельно от базофилов).
Таким образом, мы разобрали классы гемопоэтических стволовых клеток, то есть «горизонтальные» линии схемы кроветворения. Кроме того, подробно рассмотрели «вертикальные» линии созревания клеток, получив, таким образом, совокупность составляющих ту или иную линии дифференцировки от стволовых клеток до терминально дифференцированных (продолжение лекции в следующем номере журнала).
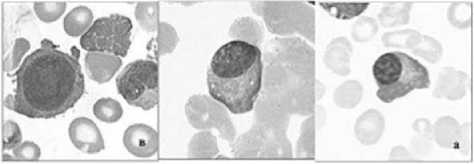
Рисунок 12. Плазмобласт, проплазмоцит, плазмоцит
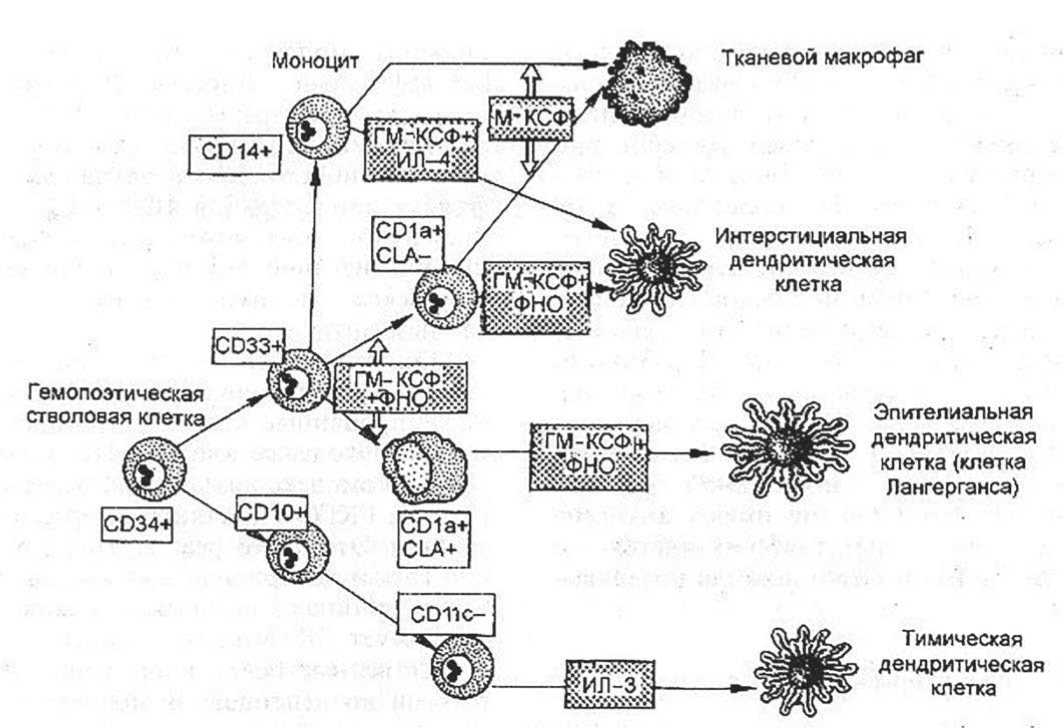
Рисунок 13. Происхождение дендритных клеток.
Список литературы Схема кроветворения (лекция, часть 1)
- Bryder D., Rossi D.J., Weissman I.L. Hematopoietic stem cells: the paradigmatic tissue-specific stem cell // Am. J. Pathol. - 2006. - Vol. 169, N 2. - P. 338–346.
- Carreras P., González I., Gallardo M. et al. Long-term hu- man hematopoietic stem cell culture in microdroplets // Micromachines (Basel). - 2021. - Vol. 12, N 1. - P. 90.
- Шевелева О. Н., Лядоваa И. В. Гемопоэтическая стволовая клетка и начальные стадии гемопоэза: методы исследований и современные представления// Онтогенез. – 2022. – Т. 53, № 6. – С. 419–436.
- Владимирская Е.Б. Нормальное кроветворение и его регуляция// Клин. Онкогематол. – 2015. – Т. 8, № 2. – С. 109–119.
- Дризе Н.И., Чертков И.Л. Стволовая кроветворная клетка. В кн.: Гериатрическая гематология. Заболевания системы крови в старших возрастных группах. / Под ред. Л.Д. Гриншпун, А.В. Пивника. - Т. 1. М.: Медиум, 2011. – С. 11–20.
- Orkin S.H., Zon L.I. Hematopoiesis: an evolving paradigm for stem cell biology. // Cell. – 2008. – Vol. 132. – P. 631–644.
- Чертков И.Л., Воробьев А.И. Современная схема кроветворения. // Проблемы гематологии и переливания крови. – 1973. – Т. 18, № 10. – С. 3–13.
- Чертков И.Л., Дризе Н.И., Воробьев А.И. Схема кроветворения: 2005. // Терапевтический архив. – 2006. – Т. 78, № 7. – С. 5–12.


