Синдром дисплазии соединительной ткани сердца у больных глаукомой
Автор: Кулешова О.Н., Лукша Е.Б., Волкова И.И.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Опыт регионов
Статья в выпуске: 3 т.22, 2007 года.
Бесплатный доступ
Цель исследования - комплексная клинико-ультразвуковая оценка и сравнительный анализ дисплазии соединительной ткани сердца (ДСТС) у больных первичной ювенильной глаукомой (ПЮГ) Обследовано 22 больных ПЮГ II, III стадий (средний возраст - 26,4±8,6 года). Выделено две группы: I группа - 14 больных, у которых при генеалогическом анализе определялся полигенный тип наследования и спорадические случаи; II группа - 8 больных с аутосомно-доминантным типом наследования. У больных ПЮГ в 72,7% встречается синдром ДСТС, наиболее часто проявляющийся пролапсом митрального клапана (54,5%), аномально расположенными хордами и трабекулами левого желудочка (63,6%) и их сочетаниями. Пролапс митрального клапана у больных ПЮГ встречается статистически значимо чаще в сравнении с популяцией (р = 0,023). При полигенном типе наследования и в спорадических случаях проявления ДСТС различной степени выраженности встречаются у 100% больных, у пациентов с аутосомно-доминантным типом наследования в 25% случаев. Наличие различных проявлений ДСТС у больных ПЮГ является основанием для проведения ультразвукового исследования сердца. При диагностике клинически значимых признаков ДСТС показано диспансерное наблюдение кардиолога, динамическое ультразвуковое исследование.
Ювенильная глаукома, дисплазия соединительной ткани сердца
Короткий адрес: https://sciup.org/14918762
IDR: 14918762 | УДК: 616.12-007:617.7-007.681-053.2
Heart connective tissue dysplasia at primary juvenile glaucoma patients
The ultrasonic research of heart was carried out on 22 patients with primary juvenile glaucoma. It is revealed, that heart connective tissue dysplasia meets in 72.7% of cases. Mitral valve prolapse was revealed in 54,5% of cases, abnormal located chords and trabecules of left ventricle of heart and their combinations were found in 63,6%. The manifestations of heart connective tissue dysplasia were in 100% of the patients at polygenic type of inheritance juvenile glaucoma and in 25% at autosomal dominant juvenile glaucoma. The realization of heart ultrasonic research and supervision are necessary for the primary juvenile glaucoma patients.
Текст научной статьи Синдром дисплазии соединительной ткани сердца у больных глаукомой
Дисплазия соединительной ткани (ДСТ) – одно из часто встречающихся наследственных аутосомно-доминантных полиорганных заболеваний людей молодого и среднего возраста, которое определяют как нарушение развития соединительной ткани в эмбриональном и постнатальном периодах вследствие генетически измененного фибриллогенеза внеклеточного матрикса, приводящее к расстройству гомеостаза на тканевом, органном и организменном уровнях в виде различных морфофункциональных нарушений висцеральных и локомоторных органов с проградиентным течением [1].
Выделяют две группы ДСТ. К первой относят дифференцированные соединительнотканные дисплазии, которые имеют определенный тип наследования и четко выраженную симптоматику (синдромы Марфана, Элер-са–Данлоса, Холта–Омара, несовершенный остеогенез и эластическая псевдоксантома). Во вторую группу включены недифференцированные дисплазии соединительной ткани с локомоторными и висцеральными проявлениями без четко выраженной симптоматики. Среди недифференцированных дисплазий различают сочетание внешних фенотипических признаков дисплазии и дисфункции вегетативной нервной системы с признаками дисплазии одного или нескольких внутренних органов, а также изолированную соединительнотканную дисплазию, при которой поражается лишь один орган, и внешние фенотипические признаки отсутствуют [2].
Синдром дисплазии соединительной ткани сердца (ДСТС) был выделен в самостоятельную нозологическую форму на симпозиуме в г. Омске (1990), посвященном проблеме врожденной дисплазии соединительной ткани и в классификации заболеваний сердечно-сосудистой системы Нью-Йоркской Ассоциации Кардиологов. К ДСТС в настоящее время относят пролапс митрального клапана (ПМК) и других клапанов, изолированную аортальную регургитацию, выбухание аортального кольца, аномалии магистральных артерий, аневризмы перегородок сердца, открытое овальное окно, аномалии правого предсердия (удлиненный и пролабирующий евстахиев клапан, пролабирующие гребенчатые мышцы). К ним также относят аномально расположенные трабекулы (АРТ) и хорды желудочков (АРХ). Эти аномалии также часто обозначают термином “малые аномалии развития сердца”, под которыми понимают анатомические изменения архитектоники сердца и магистральных сосудов, не приводящие к грубым нарушениям функции сердечнососудистой системы [3-7]. Неоднозначная клиническая симптоматика малых аномалий сердца, отсутствие четких диагностических критериев, противоречивые представления о механизмах формирования выявляемых синдромов свидетельствуют о необходимости изучения таких наиболее частых проявлений дисплазии соединительной ткани, как ПМК и АРХ, оценки их клинической значимости у различных категорий больных.
Частые сочетания ДСТС с различными внешними и внутренними признаками соединительнотканной дисплазии привлекают к себе внимание врачей различных специальностей. Многие авторы отмечают связь ДСТС с заболеваниями костно-мышечной, мочевыделительной, эндокринной, репродуктивной систем, желудочнокишечного тракта, бронхиальной астмой, трахеобронхиальной дискинезией [3,4,6,7,9-12]. Менее изучены и детализированы ассоциации ДСТС с заболеваниями глаза, в частности глаукомой и миопией.
Первичная ювенильная глаукома (ПЮГ) возникает в возрасте от 11 до 35 лет, в 86% случаев сочетается с миопией. Ранее эту группу пациентов определяли как смешанную, относя к ней случаи врожденных изменений и раннюю первичную открытоугольную глаукому. Однако в последние годы эту нозологию относят к группе врожденных заболеваний [13,14]. Особенностями ювенильной глаукомы являются длительный латентный период, так как некоторое время компенсаторное растяжение фиброзной капсулы глаза предохраняет повреждение головки зрительного нерва повышенным внутриглазным давлением, при этом имеет место появление близорукости и долгое отсутствие кардинальных признаков глаукомы. Манифестация наступает при необратимой потере зрительных функций. В некоторых случаях к моменту постановки диагноза один глаз оказывается уже слепым, или на обоих глазах имеется процесс в развитой и далеко зашедшей стадиях. Результатом этого является инвалидизация людей молодого возраста [15-17].
В связи с этим целью исследования являлась комплексная клинико-ультразвуковая оценка и сравнительный анализ ДСТС у больных первичной ювенильной глаукомой.
МАТЕРИАЛ И МЕТОДЫ
Комплексное клинико-ультразвуковое исследование сердца было проведено 22 больным первичной ювенильной глаукомой II, III стадий в возрасте от 17 до 35 лет (средний возраст – 26,4±8,6 года). Отмечалось преобладание лиц женского пола: 19 женщин (86,4%), 3 мужчины (13,6%). Обследованные больные были разделены на две группы в зависимости от типа наследования. Первую группу (I группа) составили 14 больных (средний возраст – 20,33±7,33 лет), у которых при генеалогическом анализе определялся полигенный тип наследования и спорадические случаи. Вторую группу (II группа) составили 8 больных (средний возраст – 34,51±2,36 лет), у которых прослеживался аутосомно-доминантный тип наследования.
Эхокардиографию (ЭхоКГ) с допплерографией выполняли на аппарате “SonoAse 8000 EX” (“Medi-son”) с помощью секторального датчика 2 – 5 МГц с использованием ультразвукового секторального сканирования (В-режим), одномерной эхокардиографии (М-режим), допплерографии в импульсно-вол- непрерывно-волнового режимов и цветного картирования допплеровских данных с оценкой кровотока на всех клапанах по стандартным методикам [18].
Статистический анализ полученных данных осуществлялся при помощи компьютерной программы “Биостатистика” (“Primer of Biostatistics Version 4.03 by Stanton A. Glantz”) и в созданной на основе «Microsoft Excel 2003» базе данных результатов исследования. Для выявления различий между сравниваемыми группами использовали сопоставление средних величин и стандартного отклонения с применением t-критерия Стьюдента для количественных показателей, критерия χ 2 для качественных показателей. Результаты считались статистически значимыми при р<0,05 [19].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При клинико-ультразвуковом исследовании из 22 больных ПЮГ у 16 (72,7%) были выявлены признаки дисплазии соединительной ткани сердца. Один признак выявлен в 5 случаях (31,25% от всех выявленных), два признака – в 9 случаях (56,25%), в 2 случаях новом, постоянно-волновом режимах и в режиме цветного допплеровского картирования. ЭхоКГ проводили в соответствии с рекомендациями Комитета по номенклатуре и стандартизации эхокардиографии Американского общества по эхокардиографии [18]. В В-режиме оценивали основные структуры сердца: полости сердца, клапанный аппарат, состояние локальной и глобальной сократимости миокарда. В В-режиме проводилось измерение конечного диастолического объема ЛЖ (КДО), конечного систолического объема ЛЖ (КСО), ударного объема ЛЖ (УО), фракции выброса ЛЖ (ФВ) из четырехкамерной апикальной позиции по методу Симпсона. В М-режиме измерялись диаметр аорты (АО), левое предсердие (ЛП), правый желудочек (ПЖ), конечный диастолический размер ЛЖ (КДР), конечный систолический размер ЛЖ (КСР), межжелудочковая перегородка в диастолу (МЖПд), задняя стенка ЛЖ в диастолу (ЗСЛЖд). Допплерографическое исследование осуществляли с использованием импульсного,
Таблица 1
Признаки дисплазии соединительной ткани сердца у больных первичной ювенильной глаукомой
|
Признаки ДСТС |
Количество пациентов, n=22, n (%) |
Популяционные данные, n=1061, % |
Р |
|
Пролапс митрального клапана (ПМК) |
12 (54,5%) |
22,5 % |
0,023* |
|
Пролапс трикуспидального клапана (ПТК) |
2 (9,09%) |
7,7 % |
0,856 |
|
Аномально расположенные хорды (АРХ) и трабекулы (АРТ): всего - из них - единичные - множественные |
14 (63,6%) 12 (54,54%) 2 (9,09%) |
44,0 % |
0,375 |
|
Аневризма межпредсердной перегородки |
1 (4,54%)) |
0,9% |
0,570 |
|
* р < 0,05 |
|||
70,00%
60,00%
50,00%
40,00%
30,00%
20,00%
10,00%
0,00%
Наше исследование
Популяционные данные
12 2
Пролапс трикуспидального клапана (ПТК)
Пролапс митрального клапана (ПМК)

Аномально расположенные хорды и трабекулы
Аневризма межпредсердной перегородки
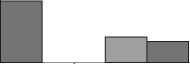
Рис. 1. Признаки дисплазии соединительной ткани сердца у больных первичной ювенильной глаукомой
(12,5%) выявлено три признака ДСТС. В структуре ДСТС у больных ювенильной глаукомой ведущее место принадлежало ПМК (54,5%) а также АРТ и АРХ (63,6%) в левом желудочке (табл. 1, рис. 1).
В нашем исследовании частота ПМК у больных ПЮГ статистически значимо превышала данные популяции (55,4% и 22,5% соответственно, р = 0,023). Во всех случаях ПМК соответствовал I степени, в 4 случаях (44,5%) имелась митральная регургитация, не превышающая уровня I степени, в остальных 5 случаях (55,5%) регургитации зарегистрировано не было.
Пролапс трикуспидального клапана (ПТК) в нашем исследовании наблюдался реже, чем ПМК, выявлен ПТК в 2 случаях (9,09%) и по частоте статистически значимо не превышал данные популяции (9,09% и 7,7% соответственно, р = 0,856). В обоих случаях степень ПТК была незначительной, не превышала I степени, и ПТК сочетался с трикуспидальной регургитацией, не превышающей уровня I степени.
В одном случае (4,54%) выявлена аневризма межпредсердной перегородки (МПП) небольших размеров (7 мм). Аневризма МПП сочеталась с ПМК I степени без регургитации и АРХ. Данные признаки ДСТС у больной 23 лет были случайной находкой при исследовании, пациентка жалоб не предъявляла (рис. 2).
Пациенты с пролапсом митрального клапана и аневризмой межпредсердной перегородки нуждаются в наблюдении кардиолога. Необходима диспансеризация этих больных, включая мероприятия по профилактике инфекционного эндокардита и динамическое эхокардиографическое наблюдение в зависимости от группы риска через 2-3 года у пациентов со средним риском, через 5 лет у больных с низким риском [20].
Аномально расположенные трабекулы и хорды представляют собой дериваты внутреннего мышечного слоя примитивного сердца, возникающие в эмбриональном
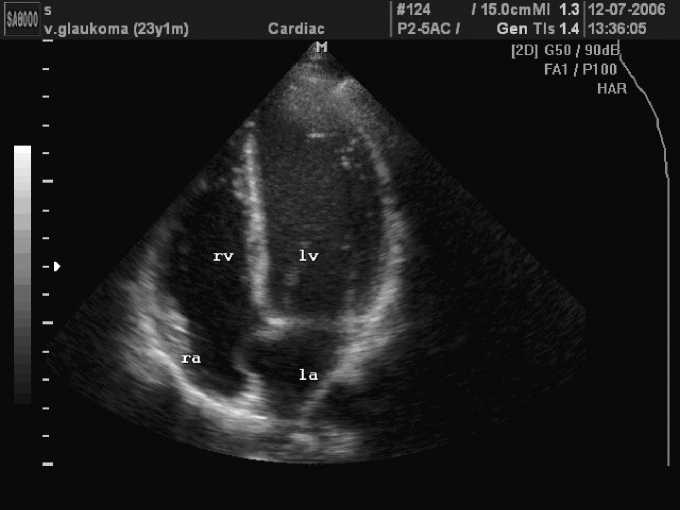
Рис. 2. Больная С., 23 г. Аневризма межпредсердной перегородки
периоде при отшнуровке папиллярных мышц. Отличие данных внутрисердечных образований заключается в том, что АРТ прикрепляются к стенкам желудочка, а АРХ соединяют папиллярные мышцы митрального клапана между собой, со стенкой желудочка или с межжелудочковой перегородкой. Частота данных структур значительно возросла с момента их описания при ультразвуковом исследовании Nishimura T. и соавторами в 1981 г. [21], особенно при различных заболеваниях связанных с ДСТ. Увеличение частоты выявляемости АРХ и АРТ возможно и с улучшением качества и повышением разрешающей способности ультразвукового оборудования. В нашем исследовании частота встречаемости АРТ и АРХ была выше в сравнении с популяционными данными (63,6 и 44,0% соответственно), однако статистически значимо не различалась (р = 0,375). АРТ и АРХ в левом желудочке являются одной из причин неорганических (функциональных) шумов. В нашем исследовании у 9 больных с АРХ и АРТ имелся функциональный шум различной степени интенсивности (64,3% от всех больных с АРХ и АРТ). АРХ и АРТ не являются патологическими образованиями, и такие пациенты не нуждаются в наблюдении кардиолога при отсутствии других патологических изменений в сердце, отсутствии жалоб и клинических признаков сердечно-сосудистых заболеваний [18, 22].
У обследованных больных отмечалось частое сочетание АРТ и АРХ с ПМК и ПТК, что в литературе объясняется как общим проявлением аномалии развития в различных структурах сердца в период эмбриогенеза [23], так и влиянием АРТ и АРХ на относительную деформацию полости левого желудочка, что приводит к относительному преобладанию хордально-створоч-ного аппарата и возникновению ПМК [24].
Различные сочетания синдрома дисплазии соединительной ткани сердца, превышающие пороговые значения (более 3), являются своеобразным индикатором возможного неблагополучия как в отношении факторов, влияющих на формирование здоровья, так и факторов, характеризующих его [4]. В нашем исследовании различные сочетания малых аномалий развития сердца выше порогового уровня (т.е. более трех) были выявлены в 9,1% случаях, что ниже популяционных данных (31,8%). Однако необходимо отметить, что популяционные данные представлены детской популяцией. В нашем же исследовании средний возраст больных ювенильной глаукомой на момент выполнения ЭхоКГ составил 26,4±8,6 года.
Полученные данные свидетельствуют о том, что у 72,7% обследуемых больных имели место малые признаки дисплазии соединитель- ной ткани. Выявленные изменения не вызывали жалоб со стороны больных и явились случайными находками при проведении целенаправленного исследования.
У больных I группы (n = 14), у которых при генеалогическом анализе определялся полигенный тип наследования и спорадические случаи глаукомы, на фоне дисплазии соединительной ткани, подтвержденной данными обследования опорно-двигательного аппарата (сколиоз различной степени, нестабильность шейного отдела, плоскостопие), имело место начало ПЮГ в молодом возрасте. Ультразвуковое исследование выявило у всех 14 больных этой группы признаки ДСТС (100%): ПМК, ПТК, одиночные и множественные АРХ и АРТ, аневризму межпредсердной перегородки.
При анализе индивидуальных офтальмологических и эхокардиологических данных обнаружено, что в случаях с генетической предрасположенностью к глаукоме (полигенный тип наследования) и аутосомно-доминантным типом наследования миопии имеют место болеe выраженные проявления внешней и внутренней ДСТ. Таким образом, можно предположить, что возникновение глаукомы у этих больных связано со структурно-функциональными нарушениями соединительной ткани, приводящими к изменениям в трабекулярном аппарате и склеральной оболочке глаза, следствием чего является ухудшение оттока внутриглазной жидкости и развитие симптомокомплекса глаукомы.
У больных II группы (n=8) прослеживался аутосомно-доминантный тип наследования, имело место наличие больных глаукомой в двух и более поколениях и отмечались минимальные изменения со стороны опорно-двигательного аппарата (нестабильность шейного отдела, плоскостопие). При эхокардиографии обнаружены множественные и единичные хорды у 2 больных (25%), и не было выявлено существенных
Эхокардиографические показатели у больных первичной ювенильной глаукомой
|
Все (n = 22) |
I группа (n = 14) |
II группа (n = 8) |
P |
|
|
Возраст, лет |
26,4±12,2 |
20,33±7,33 |
34,51±2,36 |
0,006* |
|
АО, см |
2,89±0,26 |
2,79±0,25 |
2,99±0,17 |
0,059 |
|
ЛП, см |
3,10±0,29 |
3,12±0,23 |
3,08±0,62 |
0,828 |
|
КДР ЛЖ, см |
4,49±0,42 |
4,62±0,4 |
4,34±0,58 |
0,195 |
|
КСР ЛЖ, см |
2,82±0,37 |
2,89±0,33 |
2,64±0,33 |
0,051 |
|
КДО, мл |
91,96±6,28 |
98,33±10,14 |
87,90±9,61 |
0,071 |
|
КСО, мл |
30,08±10,04 |
31,94±8,28 |
28,89±10,04 |
0,450 |
|
ФУ, % |
37,41±5,06 |
35,4±5,29 |
39,26±0,46 |
0,055 |
|
ФВ, % |
67,21±6,96 |
64,45±7,39 |
70,02±6,07 |
0,086 |
|
УО, мл |
50,1±21,84 |
55,42±16,83 |
49,73±13,15 |
0,280 |
|
МЖМд |
0,83±0,14 |
0,79±0,14 |
0,97±0,04 |
0,002* |
|
ЗСЛЖд |
0,90±0,12 |
0,89±0,14 |
0,97±0,12 |
0,191 |
|
ИММЛЖ |
74,98±12,41 |
75,32±12,85 |
82,6±3,66 |
0,136 |
|
*р < 0,05 |
||||
изменений у 6 пациентов. Следовательно, у больных II группы развитие глаукомы может объясняться врожденными, генетическими обусловленными изменениями трабекулярной сети угла передней камеры глаза.
Все измеряемые количественные показатели сердца у обследуемых больных были не изменены (табл. 2). Статистически значимых различий количественных показателей сердца между подгруппам не было, за исключением МЖПд, что объясняется возрастными различиями в подгруппах. Статистически значимые возрастные различия в подгруппах имели место на момент выполнения ультразвукового исследования сердца. При сравнении же возраста больных в подгруппах на момент выявления ПЮГ статистически значимых различий между подгруппами выявлено не было.
Зависимости стадии глаукомы от кардиологических изменений не отмечено. Этот факт можно объяснить тем, что клиническая стадия глаукомы зависит только от продолжительности заболевания. Прогрессирование атрофии зрительного нерва происходит по общим для глаукомы закономерностям и клинических особенностей не имеет.
Наши исследования показали, что высокая частота синдрома ДСТС у больных первичной ювенильной глаукомой связана с едиными патофизиологическими процессами, протекающими в соединительной ткани, с ее всеобъемлющей распространенностью в организме человека, составляющей строму всех органов и тканей. Генетически предопределенные дефекты компонентов соединительной ткани обуславливают снижение ее стабильности и ведут к возникновению клиникофункциональных нарушений многих органов и тканей, в которых нормальное развитие соединительной ткани имеет особое значение.
Таким образом, полученные данные свидетельствуют о том, что в патогенезе первичной ювенильной глаукомы одна из ведущих ролей принадлежит дисплазии соединительной ткани. Изменение структуры соединительной ткани является причиной слабости склеральной оболочки глаза и появления миопии. Сочетание ригидности цилиарной мышцы и функциональной неполноценности трабекулярной сети создает условия в дренажной зоне угла передней камеры для снижения оттока внутриглазной жидкости. Результатом этого является повышение внутриглазного давления и развитие атрофии зрительного нерва с необратимым снижением зрительных функций, приводящие к слепоте.
Таблица 2
ВЫВОДЫ
-
1. У больных первичной ювенильной глаукомой в 72,7% встречается синдром дисплазии соединительной ткани сердца. При полигенном типе наследования и в спорадических случаях проявления дисплазии соединительной ткани сердца различной степени выраженности встречаются у всех больных, при аутосомно-доминантном типе наследования – в 25% случаев.
-
2. Синдром дисплазии соединительной ткани сердца у больных глаукомой наиболее часто проявляется пролапсом митрального клапана (54,5%), аномально расположенными хордами и трабекулами левого желудочка (63,6%) и их сочетаниями. Пролапс митрального клапана у больных ювенильной глаукомой встречается статистически значимо чаще в сравнении с популяцией (р = 0,023).
-
3. Наличие различных проявлений дисплазии соединительной ткани сердца у больных первичной ювенильной глаукомой является показанием для проведения ультразвукового исследования сердца. В случаях выявления клинически значимых признаков дисплазии соединительной ткани сердца показано диспансерное наблюдение кардиолога, динамическое ультразвуковое исследование.
Список литературы Синдром дисплазии соединительной ткани сердца у больных глаукомой
- Яковлев В.М // Яковлев В.М., Нечаева Г.И., Викторова И.А. и др. Терминология, определенная с позиций клиники, классификация врожденной дисплазии соединительной ткани // Тезисы симпозиума: Врожденные дисплазии соединительной ткани. Омск, 1990. - С. 3-5
- Земцовский Э.В.//Земцовский Э.В. Соединительнотканные дисплазии сердца. СПб.: Политекс-Норд-Вест, 2000. -115 с.
- Клеменов А.В.//Клеменов А.В. Недифференцированная дисплазия соединительной ткани: клинические проявления, возможности диагностики и патогенетического лечения. М.: Информтех, 2005. -136 с.
- Гнусаев С.Ф.//Гнусаев С.Ф. Значение малых аномалий сердца у здоровых детей и при сердечно-сосудистой патологии по данным клинико-эхокардиографических исследований: Автореф.дис. докт.мед.наук. М., 1996. -48 с.
- Мутафьян О.А.//Мутафьян О.А. Пороки и малые ано-малии сердца у детей и подростков. СПб.: Издательский дом СПбМАПО, 2005. -480 с.
- Ягода А.В.//Ягода А.В., Гладких Н.Н. Малые аномалии сердца. Ставрополь: СтГМА, 2005. -248 с.
- Тарасова А.А. // Тарасова А.А., Дзис М.С., Гаврюшова Л.П. и др. Малые аномалии развития сердца у детей в возрастном аспекте // Ультразвуковая и функциональная диагностика. 2005. - №2. - С. 171-172.
- Домницкая Т.М.//Домницкая Т.М. Аномально расположенные хорды сердца. М., 2000. -98 с.
- Гаврилова В.А.//Гаврилова В.А. Синдром дисплазии соединительной ткани сердца у детей с заболеваниями мочевой системы: Автореф.дис. докт.мед.наук. М., 2002. -55 с.
- Науменко Е.И. // Науменко Е.И. Дисплазия соединительной ткани и бронхиальная астма // Тезисы Всероссийского конгресса "Детская кардиология 2002". М., 2002. - С. 120-121.
- Корнопелева Л.С.//Корнопелева Л.С. Синдром дисплазии соединительной ткани сердца при воспалительных заболеваниях желудочно-кишечного тракта у детей: Автореф.дис. канд.мед.наук. М., 2003. -22 с.
- Тарасова А.А. // Тарасова А.А. Дисплазия соединительной ткани сердца и заболевания щитовидной железы у детей // Ультразвуковая и функциональная диагностика. 2006. - №4. - С. 42-54.
- Егоров Е.А. // Егоров Е.А., Алексеев В.Н., Мартынова Е.Б. и др. // Патогенетические аспекты лечения первичной ювенильной глаукомы. - М., 2001. - 118 с.
- Тимошкина Н.Т. // Тимошкина Н.Т., Анисимова С.Ю.,Анисимов С.И. Открытоугольная глаукома у лиц молодого возраста. // Офтальмохирургия. 1995. - №1. - С.16-21.
- Кондратенко Ю.Н. // Кондратенко Ю.Н., Сергиенко Н.М. Гипотеза патогенеза близорукости // Офтальмол. журнал. 1988. - №3. - С.138-143.
- Сидоров Э.Г.//Сидоров Э.Г., Мирзаянц М.Г. Врожденная глаукома и ее лечение. М., Мед., 1991. -208 с.
- Либман Е.С. // Либман Е.С., Шахова Е.В. Слепота и инвалидность по зрению в населении России. // Съезд офтальмологов России, 8-й (1-4 июня 2005г.): Тез.докл. - М., 2005. - С.78-79.
- Feigenbaum H. // Feigenbaum H. Echocardiography 4th // Philadelphia: Lea Feibiger.- 1986.
- Гланц С.//Гланц С. Медико-биологическая статистика. М: Практика. -1999. -459 с.
- Шиллер Н.//Шиллер Н., Осипов М.А. "Клиническая эхокардиография", второе издание, "Практика", Москва, 2005. -С. 140.
- Nishimura T. // Nishimura T., Kondo M., Umadome H.et al. Echocardiographic features of the false tendons in the left ventricle // Am.J.Cardiol. 1981.V.48. №1. P.177-183.
- Клиническое руководство по ультразвуковой диагностике под редакцией В.В. Митькова, В.А. Сандрикова//М.-ВИДАР. 1998. -Т.5.
- Celano V. // Celano V., Pieroni D.R., Morera J.A. et al. Twodimensional echocardiographic examination of mitral valve abnormalities associated with coarctation of the aorta // Circulation. 1984. V.69. №5. P.924-932.
- Сторожаков Г.И. // Сторожаков Г.И., Блохина И.Г.,Гендлин Г.Е. Ложные хорды левого желудочка сердца // Кардиология. 1994. - №8. - С.75-79.


