Синтез индол 3 уксусной кислоты при совместном культивировании дрожжей и бактерий
Автор: Пронин А.С., Колмыкова Т.С., Лукаткин А.С.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Пищевая биотехнология
Статья в выпуске: 4 (98) т.85, 2023 года.
Бесплатный доступ
Работа посвящена исследованию штаммов дрожжей и бактерии, которые являются потенциальными компонентами для состава при разработке биопрепаратов для растений. Эксперименты с совместным культивированием бактерий и дрожжей способные к стимуляции роста растений предоставляют основу для разработки комплексных биопрепаратов, которые могут воздействовать на сельскохозяйственные культуры и оцениваться по их фитогормональной активности .В работе дана оценка возможности синтеза индо-3 уксусной кислоты при совместном культивировании бактерии Pseudomonas chlororaphis subsp. auerofaciens B5326 и дрожжей Saccharomyces cerevisiae Y4317. Мы использовали современные методы для оценки метаболитов микроорганизмов такие как, тонкослойная хроматография для оценки аминокислотного состава, и реакцию сальковского для обнаружения индол-3 уксусной кислоты в культуральной жидкости. На первом этапе работы мы показали, что конкурентного взаимодействия между бактериями и грибами не было. Максимальная концентрация колония образующих единиц при совместном культивирование P. chlororaphis и S. Сerevisiae. составила (3 ± 0,2)×108 и (8 ± 0,2)×106 КОЕ/мл. В ходе исследования обнаружили, что микроорганизмы P.chlororaphis и S.cerevisiae при совместном культивировании способны синтезировать индол-3 уксусную кислоту.. В исследованиях с добавлением триптофана обнаружили, что экзогенное введение аминокислоты стимулирует накопление фитогормонов в КЖ только у P.chlororaphis. Таким образом, мы предполагаем, что основным источником триптофана при совместном культивировании микроорганизмов является S. cerevisiae. Полученные данные являются предпосылкой к созданию комплексного биологического препарата для обработки растений и подтверждает нашу гипотезу о возможности совместного культивирвоания микроорганизмов относящихся к различной таксономическим категориям.
Pseudomonas chlororaphis, Saccharomyces cerevisiae, индол 3 уксусная кислота, триптофан, PGBPB, PGPF
Короткий адрес: https://sciup.org/140304454
IDR: 140304454 | УДК: 640 | DOI: 10.20914/2310-1202-2023-4-91-95
Synthesis of indole 3 acetic acid during co-cultivation of yeast and bacteria
The work is dedicated to the study of yeast and bacterial strains that are potential components for developing bio-preparations for plants. Experiments involving the co-cultivation of bacteria and yeast capable of stimulating plant growth provide a basis for the development of complex bio-preparations that can impact agricultural crops and be evaluated based on their phytohormonal activity. The study evaluates the possibility of synthesizing indole-3-acetic acid during the co-cultivation of Pseudomonas chlororaphis subsp. auerofaciens B 5326 bacteria and Saccharomyces cerevisiae Y 4317 yeast. Modern methods were employed to assess the microorganisms' metabolites, such as thin-layer chromatography for amino acid composition evaluation and the Salkowski reaction for detecting indole-3-acetic acid in the culture fluid. In the initial stages of the work, it was demonstrated that there was no competitive interaction between bacteria and fungi. The maximum concentration of colony-forming units during the co-cultivation of P. chlororaphis and S. cerevisiae was (3 ± 0.2) × 10^8 and (8 ± 0.2) × 10^6 CFU/ml, respectively. The study revealed that P. chlororaphis and S. cerevisiae could synthesize indole-3-acetic acid during co-cultivation. Experiments with the addition of tryptophan showed that the exogenous introduction of the amino acid stimulates the accumulation of phytohormones in the culture fluid only for P. chlororaphis. Therefore, we hypothesize that S. cerevisiae is the main source of tryptophan during the co-cultivation of microorganisms. The obtained data serve as a basis for creating a complex biological preparation for plant treatment and confirm our hypothesis regarding the possibility of co-cultivating microorganisms belonging to different taxonomic categories.
Текст научной статьи Синтез индол 3 уксусной кислоты при совместном культивировании дрожжей и бактерий
На сельскохозяйственном мировом рынке наблюдается растущий интерес к использованию биологических средств защиты растений и ростовых стимуляторов. Эта тенденция подчеркнута исследованиями [3]. Производство таких препаратов включает использование различных культур микроорганизмов, таких как ростопромо-тирующие бактерии (PGPB) и грибы (PGPF) [4, 5]. Современные исследования акцентируют внимание на способности PGPB и PGPF к синтезу природных гормонов роста, таких как ауксины, цитокинины и гиберилины [1, 7, 8]. Производство этих веществ микробиологическим путем может привести к экономическому эффекту в сельском хозяйстве. Некоторые исследования демонстрируют, что определенные штаммы Pseudomonas не только обладают фунгицидными свойствами, но и способны синтезировать ауксины [6]. Наши исследования фокусировались на совместном культивировании бактерии Pseudomonas chlororaphis subsp. auerofaciens B 5326 и дрожжей Saccharomyces cerevisiae Y 4317, где мы выявили их способность синтезировать фитогормоны и накапливать их в культуральной жидкости. Эксперименты с совместным культивированием PGPB [13] и PGPF [14, 15] предоставляют основу для разработки комплексных биопрепаратов, которые могут воздействовать на сельскохозяйственные культуры и оцениваться по их фитогормональ-ной активности.
Материалы и методы
Цель исследования: оценка возможности синтеза IAA при совместном культивировании бактерии Pseudomonas chlororaphis subsp . auerofaciens B-5326 и дрожжей Saccharomyces cerevisiae Y-4317.
Задачи: 1) исследование возможности совместного культивирования PGPB и PGPF 2) исследование способности синтезировать IAA P. chlororaphis и S. Сerevisiae в присутствии/ отсутствии L-триптофана 3) Оценка способности S. Сerevisiae синтезировать триптофан.
В качестве посадочного материала использовали штаммы бактерии Pseudomonas chlororaphis subsp. aureofaciens B-5326 и дрожжей Saccharo-myces cerevisiae Y-4317 (Всероссийской коллекции промышленных микроорганизмов НИЦ «Курчатовский институт» – ГосНИИгенетика).
Режимы культивирования микроорганизмов и состав питательной среды. На первом этапе культивирование исследуемых микроорганизмов осуществляли раздельно в колбах объемом 250 мл на шейкере-инкубаторе SPH-2102 (BIORUS, Минск, Беларусь) при температуре 28 °С и частоте перемешивания 130 RPM. Среда для выращивания микроорганизмов содержала глюкозу 10 г/л, NaNO3, (NН4)2SO4, NH4NO3, КН2РО4 – по 0,5 г/л.
дрожжевой экстракт 1 г/л. Спустя 48 ч титр посадочного материала составил 107 и 105 КОЕ/мл для P. chlororaphis и S .сerevisiae , соответственно. На втором этапе из двух колб отбирали по 15 мл культуральной жидкости и переносили в колбу объёмом 500 мл. Состав питательной среды для совместного роста микроорганизмов: свекловичная меласса 25 г/л пептон 0,5 г/л, дрожжевой экстракт 1 г/л, NaNO 3 , (NН 4 ) 2 SO 4 , NH 4 NO 3 , КН 2 РО 4 – по 0,5 г/л.
Определение содержания аминокислот: определяли методом ТСХ. Использовали стандарты 20 аминокислот фирмы Sigma (США). Пробы культуральной жидкости, отбирали по 1,5 мл, центрифугировали на центрифуге MiniSpin® (Eppendorf, Гамбург, Германия) при 6000 об/мин в течение 20 мин. ТСХ-пластинки промывали смесью хлороформ-метанол (1:1 по объему) и активировали в течение 15 мин при 120 °С. Объем наносимых проб – 0,5 мкл. Подвижная фаза состояла из изобутанола, изопропанола, воды и ледяной уксусной кислоты (5:4:3:0.2 по объему), Насыщение камеры – 1,0–1,5 ч. Время разделения 1,5–2 ч.
Количественно аминокислоты определяли на денситометре CS-920 фирмы Shimadzu (Киото, Япония) и TLC Scanner 3 (Camag, Муттенц, Швейцария) при длине волны 500 нм.
Подсчёт клеток микроорганизмов осуществляли на фиксированных окрашенных мазках метод Виноградского-Брида (Теппер, 2004).
Для обнаружения в культуральной жидкости ауксина и определения его концентрации проводили реакцию Сальковского [9]. После прохождения цветной реакции концентрацию IAA определяли фотометрически на спектрофотометре UV-1900 ( Shimadzu, Киото, Япония ) при длине волны 546 нм.
Результаты
На первом этапе работы проводили совместное культивирование P. chlororaphis и S. Сerevisiae . В ходе исследования мы обнаружили активный рост колоний бактерий и дрожжей при совместном культивировании на мелассной среде. Анализируя полученную картину исследования, мы не обнаружили конкурентного взаимодействия между микроорганизмами двух таксономических групп. Это позволило нам предположить, что в КЖ отсутствуют ростингибирующие для данных организмов метаболиты.
Максимальная концентрация при совместном культивирование P. chlororaphis и S. Сerevisiae . составила (3 ± 0,2)×108 и (8 ± 0,2)×106 КОЕ/мл (рисунок 1).
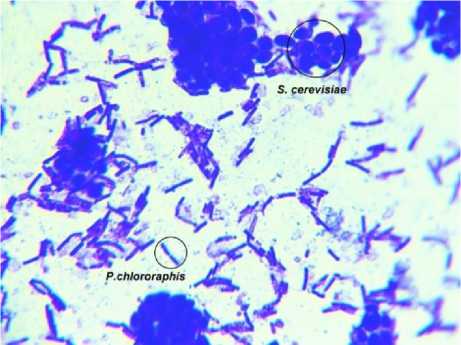
Рисунок 1. Микроскопия P. chlororaphis и S. Сerevisiae при совместном культивирование
Figure 1. Microscopy of P. chlororaphis and S. Cerevisiae during co-cultivation
культивировании P. chlororaphis и S. cerevisiae мы зафиксировали увеличение содержания IAA в культуральной жидкости более чем в два раза, по сравнению с раздельным способом культивирования. Без добавления L-триптофана содержания IAA составило 102 ±5, при добавлении аминокислоты содержание IAA увеличилось незначительно в пределах ошибки (111±7 мкг/мл).
Поэтому на следующем этапе мы экспериментальным методом изучили способность данного штамма дрожжей продуцировать L-триптофан. Методом ТСХА обнаружили, что в ходе роста исследуемого штамма дрожжей в КЖ накапливается аминокислота триптофан в концентрации 44 мкг/мл (рисунок 3).
Основным показателем эффективности биопрератов является жизнеспособность клеток микроорганизмов и их способность синтезировать в среду биологически активные вещества, в нашем случае – фитогормоны [17–18]. В нашем исследовании в качестве фитогормонального-маркера в КЖ служила индол 3-уксусная кислота. Мы сравнили способность синтезировать IAA микроорганизмами при раздельном культивировании при добавлении аминокислоты триптофана (100 мкг/мл) и в её отсутствии (контроль) [19–20]
IAA, «J
Hg/ml «
P.chlororaphis P.chlororaphis
Ury
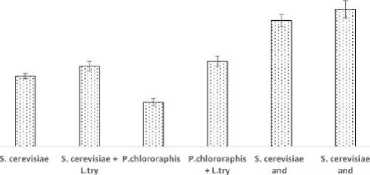
Рисунок 2. Содержание IAA в культуральной жидкости исследуемых микроорганизмов
Figure 2. IAA content in the culture liquid of the studied microorganisms
При раздельном культивировании микроорганизмов содержание IAA в культуральной жидкости S. cerevisiae составило 57±3 мкг/мл и 36±2 мкг/мл в КЖ P. chlororaphis (рисунок 2). Очевидно, что дрожжи являются основным продуцентом IAA. При добавлении в среду для роста клеток аминокислоты L-триптофан, содержание IAA достоверно увеличилось по сравнению со средой без добавления аминокислоты только в вариантах с бактериями P. chlororaphis B-5326. Содержание IAA увеличилось по сравнению с контролем на 78%. В вариантах с дрожжами S. cerevisiae содержание IAA увеличивалось пор сравнению с контролем только на 14%. Мы предположили, что дрожжи способны самостоятельно синтезировать L-триптофан. При совместном val try tyr
Рисунок 3. Хроматограмма аминокислотного состава Saccharomyces cerevisiae Y-4317
Figure 3. Chromatogram of the amino acid composition of Saccharomyces cerevisiae Y 4317
Полученные данные подтверждают, что при совместном росте P. chlororaphis B-5326 и Saccharomyces cerevisiae Y-4317 , последние выделяют в среду достаточно аминокислоты для биосинтеза IAA микроорганизмами. Следовательно, совместное культивирование дрожжей и бактерий позволяет не только повысить жизнеспособность бактерий в логарифмическаю фазу роста, но и накапливать в среде больше IAA за счёт синтеза дрожжами триптофана.
Обсуждение
Известно, что L-триптофан является предшественников индол-3 – уксусной кислоты в метаболизме растений, некоторых бактерий и грибов. Бактерии рода Pseudomonas способны синтезировать IAA по индол-3-ацетамидному пути, где основным компонентом является L-триптофан. Ключевым ферментом при синтезе является индолацетамид гидролаза [2] основным предшественником – L-триптофан. В ранее проведенных исследованиях [3] показано, что бактерии Pseudomonas putida, Pseudomonas sp способны синтезировать IAA в концентрации 16 μg/mL без присутствия экзогенного L-триптофана и 108 μg/mL при его добавлении в среду в концентрации 0,2 g/L [16] Результаты нашего эксперимента согласуются с вышеописанными.
Pronin A.S. et al. Proceedings of VSUET, 2023, vol. 85, no. 4, pp. 91-95
Но в своей работе мы использовали более низкую концентрацию триптофана.
Другие авторы так же отмечают способность некоторых дрожжей таких как Sporobolomyces, Taphrina, Metschnikowia, Aureobasidium синтезировать ауксины [11]. В исследованиях [10], показано, что S. cerevisiae с делециями в двух генах (Ald) не способен конвертировать радиоактивно меченый Trp в IAA, но продуцирует IAA в отсутствие L-Trp и на уровнях выше, чем у дикого типа штамма дрожжей. Эти данные предполагают, что дрожжи могут иметь несколько путей синтеза IAA. Таким образом, при совместном росте с S. cerevisiae и P. chlororaphis увеличение синтеза IAA у последних, можно объяснить способностью накапливать триптофан в культуральной жидкости S. cerevisiae .
Заключение
Настоящая работа посвящена изучению возможности совместного культивирования PGPB и PGPF микроорганизмов. Мы показали,
(8 ± 0,2)×106 КОЕ/мл.
В ходе исследования обнаружили, что микроорганизмы P. chlororaphis и S. cerevisiae при совместном культивировании способны синтезировать IAA в максимальной концентрации 111±7 мкг/мл. В исследованиях с добавлением триптофана обнаружили, что экзогенное введение аминокислоты стимулирует накопление IAA в КЖ только у P. chlororaphis . Таким образом, мы предполагаем, что основным источником триптофана при совместном культивировании микроорганизмов является S. cerevisiae . Полученные данные являются предпосылкой к созданию комплексного биологического препарата для обработки растений и подтверждает нашу гипотезу о возможности совместного культи-вирвоания PGPB и PGPF.
Список литературы Синтез индол 3 уксусной кислоты при совместном культивировании дрожжей и бактерий
- Batabyal B. Plant Growth Promoting Fungi: Mechanisms and Applications for Crop Productivity // International Journal of Pharmacy & Life Sciences. 2021. V. 12. №. 1.
- Duca D.R., Glick B.R. Indole-3-acetic acid biosynthesis and its regulation in plant-associated bacteria // Applied microbiology and biotechnology. 2020. V. 104. P. 8607-8619.
- Kocira S., Hara P., Szparaga A., Czerwińska E. et al. Evaluation of the Effectiveness of the Use of Biopreparations as Seed Dressings // Agriculture. 2020. V. 10. №. 4. P. 90.
- Kumar A., Singh S., Gaurav A.K., Srivastava S. et al. Plant growth-promoting bacteria: biological tools for the mitigation of salinity stress in plants // Frontiers in Microbiology. 2020. V. 11. P. 1216. doi: 10.3389/fmicb.2020.01216
- Li M., Wang J., Yao T., Wang Z. et al. Isolation and characterization of cold-adapted PGPB and their effect on plant growth promotion // Journal of Microbiology and Biotechnology. 2021. V. 31. №. 9. P. 1218. doi: 10.4014/jmb.2105.05012
- McClerklin S.A., Lee S.G., Harper C.P., Nwumeh R. et al. Indole-3-acetaldehyde dehydrogenase-dependent auxin synthesis contributes to virulence of Pseudomonas syringae strain DC3000 // PLoS pathogens. 2018. V. 14. №. 1. P. e1006811.
- Olanrewaju O.S., Glick B.R., Babalola O.O. Mechanisms of action of plant growth promoting bacteria //World Journal of Microbiology and Biotechnology. 2017. V. 33. P. 1-16.
- Oliveira J.T.C., Pereira A., Souza A.J., Silva G.T. et al. Plant growth-promoting mechanisms and genetic diversity of bacteria strains isolated from Brachiaria humidicola and Brachiaria decumbens // Anais da Academia Brasileira de Ciências. 2021. V. 93.
- Patten C.L., Glick B.R. Role of Pseudomonas putida indoleacetic acid in development of the host plant root system // Applied and environmental microbiology. 2002. V. 68. №. 8. P. 3795-3801. doi: 10.1128/AEM.68.8.3795-3801.2002
- Rao R.P., Hunter A., Kashpur O., Normanly J. Aberrant synthesis of indole-3-acetic acid in Saccharomyces cerevisiae triggers morphogenic transition, a virulence trait of pathogenic fungi // Genetics. 2010. V. 185. №. 1. P. 211-220. doi: 10.1534/genetics.109.112854
- Streletskii R.A., Kachalkin A.V., Glushakova A.M., Demin V.V. et al. Quantitative determination of indole-3-acetic acid in yeasts using high performance liquid chromatography—tandem mass spectrometry // Microbiology. 2016. V. 85. P. 727-736.
- Теппер Е.3., Шильникова В.К., Переверзева Г.И. Практикум по микробиологии: учебное пособие для вузов; 5-е изд., перераб. и доп. М.: Дрофа, 2004. Ajijah N., Fiodor A., Pandey A.K., Rana A. et al. Plant Growth-Promoting Bacteria (PGPB) with biofilm-forming ability: A multifaceted agent for sustainable agriculture // Diversity. 2023. V. 15. №. 1. P. 112.
- Wang C., Lin Y., Huang J., Song H. et al. Pseudomonas aeruginosa targeting cascade photodynamic nanoassemblies for efficient antibacterial and anti-inflammatory therapy // Nano Today. 2023. V. 51. P. 101892. doi: 10.1016/j.nantod.2023.101892
- Rabert G.A., Dhivya A., Navaneetha P., Mathivanan S. et al. A study on the impact of Plant Growth Promoting Fungus (PGPF) and Plant Growth Promoting Rhizobacteria (PGPR) as biofertilizers for Abelmoschus esculentus (L.) Moench // Innovations in Agriculture. 2023. V. 4. P. 1-1.
- Onrit N., Boonlue S., Mongkolthanaruk W., Jogloy S. et al. Alternative Nitrogen Source for Producing Crude Extracted IAA and Suitable Method for Enhancing the Germination of Jerusalem Artichoke // Waste and Biomass Valorization. 2023. V. 14. №. 5. P. 1497-1508.
- Завалин А.А., Накаряков А.М. Эффективность применения биопрепаратов в посеве озимой пшеницы на светло-серой лесной почве // Земледелие. 2021. №. 1. С. 27-30.
- Djami-Tchatchou A.T., Harrison G.A., Harper C.P., Wang R. et al. Dual role of auxin in regulating plant defense and bacterial virulence gene expression during Pseudomonas syringae PtoDC3000 pathogenesis // Molecular Plant-Microbe Interactions. 2020. V. 33. №. 8. P. 1059-1071.
- Uzma M., Iqbal A., Hasnain S. Drought tolerance induction and growth promotion by indole acetic acid producing Pseudomonas aeruginosa in Vigna radiata // PloS one. 2022. V. 17. №. 2. P. e0262932. doi: 10.1371/journal.pone.0262932
- Zhang B.X., Li P.S., Wang Y.Y., Wang J.J. et al. Characterization and synthesis of indole-3-acetic acid in plant growth promoting Enterobacter sp // RSC advances. 2021. V. 11. №. 50. P. 31601-31607. doi: 10.1039/D1RA05659J


