Синтез инсулина путем генной инженерии и применение его в медицине
Автор: Балохин С. Д., Гнездилова О. А., Мазовка Д. А., Осинина А. Т.
Рубрика: Сообщения молодых ученых
Статья в выпуске: 4 (16), 2021 года.
Бесплатный доступ
Быстрое увеличение числа больных сахарным диабетом во всем мире и изучение альтернативных методов доставки инсулина, таких как ингаляционный или пероральный путь, которые основаны на более высоких дозах, неизбежно увеличат спрос на рекомбинантный инсулин в ближайшем будущем. Современные технологии производства не смогут удовлетворить растущий спрос на доступный инсулин из-за ограниченности производственных мощностей и высокой себестоимости. Производство терапевтических рекомбинантных белков требует соответствующего организма-хозяина с эффективным оборудованием для посттрансляционных модификаций и рефолдинга белка. Рекомбинантный человеческий инсулин был получен преимущественно с использованием E.coli и Saccharomyces cerevisiae для терапевтического применения у человека. В этом обзоре мы сосредоточимся на различных подходах, которые могут быть использованы для увеличения выработки биологически активного инсулина и его аналогов в кишечной палочке и дрожжах.
Инсулин, диабет, синтез, дрожжи, кишечная палочка, микроорганизмы, гормоны, ген, препараты, глюкоза
Короткий адрес: https://sciup.org/170191362
IDR: 170191362 | УДК: 577.175.722 | DOI: 10.24411/2409-4102-2021-10406
Insulin synthesis by genetic engineering and its application in medicine
The rapid increase in the number of patients with diabetes mellitus worldwide and the study of alternative methods of delivery of insulin, such as inhalation or oral route, which are based on higher doses, will inevitably increase the demand for recombinant insulin in the near future. Modern production technologies will not be able to meet the growing demand for affordable insulin due to limited production capacity and high production costs. The production of therapeutic recombinant proteins requires an appropriate host organism with efficient equipment for post-translational modifications and protein refolding. Recombinant human insulin has been obtained predominantly using E. coli and Saccharomyces cerevisiae for therapeutic use in humans. In this review, we will focus on various approaches that can be used to increase the production of biologically active insulin and its analogs in E. coli and yeast.
Текст научной статьи Синтез инсулина путем генной инженерии и применение его в медицине
белков, особенно инсулина. В 1963 г. был синтезирован искусственный инсулин [1].
Рекомбинантный человеческий инсулин был впервые произведен в E. coli компанией Genentech в 1978 г. с использованием подхода, который требовал экспрессии химически синтезированной кДНК, кодирующей цепи α и β инсулина отдельно в E. coli. После независимой экспрессии две цепи очищают и совместно инкубируют в оптимальных условиях реакции, которые способствовали образованию интактного и биоактивного инсулина за счет образования дисульфидной связи.
Первый коммерческий рекомбинантный инсулин был разработан для терапевтического применения у человека с помощью этой двухцепочечной комбинированной процедуры. Другой подход включает экспрессию единственной химически синтезированной кДНК, кодирующей проинсулин человека, в E. coli, с последующей очисткой и последующим удалением С-пептида протеолитическим расщеплением. Этот подход был более эффективным и удобным для крупномасштабного производства терапевтического инсулина по сравнению с подходом с двухцепочечной комбинацией и коммерчески использовался с 1986 г. Eli Lilly использовала эту технологию для производства хумулина, первого рекомбинантного инсулина, одобренного в 1982 г. для лечения пациентов с диабетом. Эти рекомбинантные инсулины первого поколения имеют аминокислотную последовательность, идентичную нативному человеческому инсулину, и предпочтительнее, чем продукты инсулина животного происхождения. Однако прогресс в области генной инженерии и разработка технологий химического синтеза генов с измененной нуклеотидной последовательностью облегчили разработку аналогов инсулина с измененной аминокислотной последовательностью [3].
Было замечено, что нативный инсулин в коммерческих препаратах обычно существует в олигомерной форме, как цинксодержащий гексамер из-за очень высокой концентрации, но в крови биологически активный инсулин находится в мономерной форме. Следовательно, этот олигомерный комплекс должен диссоциировать, чтобы инсулин мог абсорбироваться из места инъекции в кровь. Из-за этого рекомбинантный инсулин, вводимый подкожно, обычно имеет медленное начало с максимальной концентрацией в плазме после 2 часов с момента инъекции и большей продолжительностью действия, которая длится 6—8 часов.
Следовательно, для разработки быстродействующего аналога инсулина потребовалось модифицировать аминокислотные остатки, боковые цепи которых участвуют в образовании димера или олигомера [1].
Lispro, разработанный Eli Lilly, был первым аналогом инсулина быстрого действия, получившим разрешение регулирующих органов в 1996 г. для терапевтического использования. Инсулин Lispro разработан таким образом, что он имеет аминокислотную последовательность, аналогичную природному инсулину, но имеет инверсию пролин-лизиновой последовательности в положениях 28 и 29 B-цепи, что приводит к снижению гидрофобных взаимодействий и, таким образом, предотвращает образование димеров.
Для коммерческого производства инсулина Lispro синтетическая кДНК, кодирующая про-инсулин Lys B28 — Pro B29 человека, была экспрессирована в E. coli, и инсулин Lispro был протеолитически вырезан из проинсулина обработкой трипсином и карбоксипептидазой. Другой аналог инсулина быстрого действия, продуцируемый E. coli. представляет собой глу-лизин (Apidra), который был разработан Aventis Pharmaceuticals и одобрен регулирующими органами США в 2004 г. Инсулин Глулизин был получен путем замены аспарагина B3 на лизин и лизина B29 на глутаминовую кислоту [3].
Чтобы избежать многократных инъекций, также были созданы аналоги инсулина пролонгированного действия с увеличенной продолжительностью действия. Инсулин Гларгин — один из таких аналогов инсулина длительного действия, который был разработан Aventis Pharmaceuticals и одобрен регулирующими органами США и ЕС в 2000 г. Инсулин Гларгин был получен путем замены С-концевого аспарагина А-цепи остатком глицина и C-конец B-цепи был модифицирован путем добавления двух остатков аргинина. Эти модификации привели к увеличению изоэлектрической точки (pI) с 5,4 до нейтральных значений. Гларгин продуцируется в виде проинсулина и экспрессируется в E. coli, и, наконец, был составлен при pH 4 в растворимой форме. Однако после подкожного введения он выпадал в осадок из-за нейтрального pH в подкожной клетчатке. Ресолюбилизация инсулина происходит медленно, что увеличивает продолжительность его высвобождения в кровь [5].
Система экспрессии дрожжей для производства инсулина
Дрожжи являются очень привлекательный системой экспрессии, позволяющей сочетать дешевизну прокариотического культивирования с эукариотическим процессингом белков. Дрожжи являются одноклеточным организмом, генетика и физиология которого детально изучены и который можно выращивать как в небольших лабораторных колбах, так и в промышленных культиваторах [7].
Для эффективной экспрессии и секреции рекомбинантного проинсулина в дрожжах была сконструирована конструкция инсулина, содержащая нативную α-цепь и β-цепь, лишенную C-концевого треонина B30, либо непосредственно слитого, либо связанного через короткий синтетический C-пептид (например, AAK). Последовательность кДНК, кодирующая эту конструкцию, была слита с сигнальной последовательностью α-фактора Saccharomyces cerevisiae для секретируемой экспрессии проинсулина, которая дала выход до 80 мг/мл инсулина. Одноцепочечный проинсулин очищали и превращали в активный инсулин с помощью реакции транс-пептидации, опосредованной трипсином, в присутствии эфира треонина.
Помимо природного рекомбинантного инсулина, в S. cerevisiae также производятся различные аналоги инсулина [2].
Инсулин Аспарт — аналог инсулина быстрого действия, который был произведен в S. cerevisiae, разработанный Novo Nordisk и одобренный FDA США в 2001 г. для терапевтического использования у человека. Инсулин Аспарт получали заменой остатка пролина в положении 28 на аспарагиновую кислоту в β-цепи. Эта генетическая модификация привела к увеличению отталкивания межцепочечных зарядов, снижению самоассоциации и, таким образом, к быстрому проникновению в кровь из места подкожной инъекции [4].
Инсулин Детемир — рекомбинантный аналог инсулина длительного действия, коммерчески производимый в S. cerevisiae, разработанный Novo Nordisk и одобренный для терапевтического использования у человека в 2004 г. европейскими регулирующими органами.
Рекомбинантный Детемир был получен путем удаления остатка треонина в положении 30 β-цепи и цепи жирной кислоты C14, ковалентно присоединенной к остатку лизина в положении 29 β-цепи. Эти генетические изменения привели к связыванию инсулина с альбумином в плазме, что обеспечивало медленное и постоянное высвобождение инсулина и, таким образом, увеличивало продолжительность его действия до 24 часов [4].
Одна из основных проблем, связанных с получением терапевтического гликопротеина для применения человеком, заключается в том, что дрожжевое N-гликозилирование относится к типу высокоманнозного, что обеспечивает короткий период полужизни в пробирке и гипериммуногенность и, таким образом, снижает эффективность терапевтического гликопротеина.
Система экспрессии кишечной палочки для производства инсулина
E. coli является предпочтительным микроорганизмом для крупномасштабного производства инсулина [9].
Инсулин — это пептидный гормон поджелудочной железы, который состоит из 51 аминокислотного остатка и двух полипептидных цепей, связанных между собой двумя дисульфидными мостиками. Синтезируется он в виде одноцепочечного предшественника — препроинсулина, содержащего концевой сигнальный пептид (23 аминокислотных остатка) и 35-звенный соединительный пептид (С-пептид). При удалении сигнального пептида в клетке образуется проинсу-лин из 86 аминокислотных остатков, в котором А- и В-цепи инсулина соединены С-пептидом, обеспечивающим им необходимую ориентацию при замыкании дисульфидных связей. После протеолитического отщепления С-пептида образуется инсулин [2].
Ген, синтезирующий человеческий проинсулин (INS), находится в 11 хромосоме.
Путем комплементарной ДНК получили копию INS-гена. Он состоит из комплементарных цепей и «липких концов» (комплементарная последовательность оснований). Полученный ген подстраивается к 3’-концу β-галактозидазы и вводится в раскрытую (разрезанную) ферментом (эндонуклеаза рестрикции), оставляющим «липкие концы», плазмиду PBR322 (рис. 1) [11].
«Липкие концы» чужеродной ДНК и плазмиды PBR322 взаимодействуют друг с другом, образуя комплементарные пары оснований. Затем плазмида замыкается, встраивая в себя новый ген. Фермент ДНК-лигаза окончательно запечатывает плазмиду [6].
Такая рекомбинантная ДНК встраивается в тело E. Coli, в которой плазмида ведет себя как вектор (переносчик) нового гена. В результате, такой вид гена будет реплицироваться в новом поколении E. Coli [8].
В результате жизнедеятельности, такие генно-модифицированные бактерии, осуществляют синтез проинсулина человека, от которого после частичного протеолиза отщепляется С-пептид, превращая его в инсулин.
Полученный инсулин очищают.
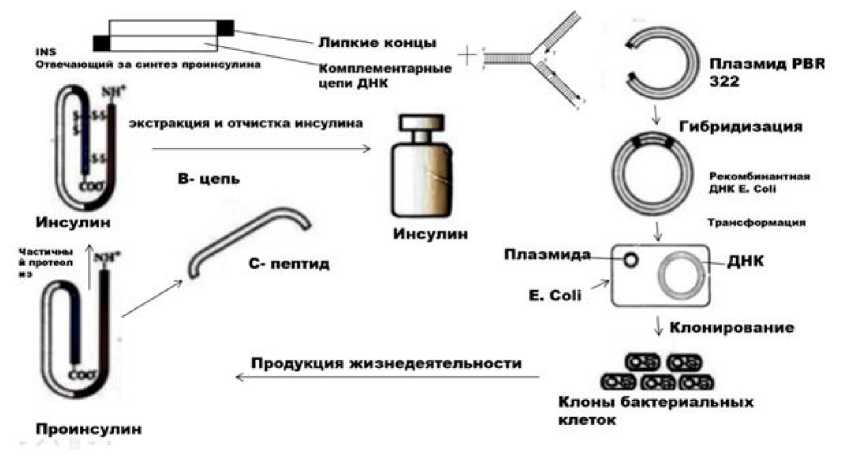
Рис 1. Схема искусственного получения инсулина
Инсулинотерапия при сахарном диабете 1 типа
Интенсивная инсулинотерапия (ИКТ) и инсулиновая помповая терапия (непрерывная подкожная инфузия инсулина; ППИ) являются наиболее распространенными методами инсулиновой терапии для людей с диабетом 1 типа. Обычная инсулино-терапия (КТ) с двумя ежедневными инъекциями предварительно смешанного инсулина используется у людей с диабетом 1 типа только в исключительных случаях [5].
Инсулиновая помпа — это небольшое компьютеризированное устройство, которое непрерывно подает небольшие дозы инсулина для удовлетворения базовых потребностей (почасовая базальная скорость) [10]. Согласно действующим руководствам, интенсивная инсулинотерапия считается золотым стандартом лечения людей с диабетом 1 типа. Помповую инсулинотерапию (ППИИ) назначают только для определенных условий, таких как очень низкая потребность в инсулине. Нет явных преимуществ в пользу того или иного способа применения инсулина при диабете 1 типа. Тем не менее есть некоторые очевидные медицинские причины для использования непрерывной подкожной инфузии инсулина, такие как очень низкая потребность в инсулине или ярко выраженный феномен рассвета. В большинстве случаев столь однозначных причин в пользу непрерывной подкожной инфузии инсулина не существует. Помповая инсулиновая терапия сложна и подходит не всем [5].
Вывод
Проанализировав научные работы, можно сделать вывод, что последние разработки были сосредоточены на сочетании генетической и химической инженерии с фармацевтической оптимизацией для создания аналогов инсулина сверхбыстрого и сверхдлительного действия, научные усилия в области молекулярной инженерии включали реализацию мечты о доставке инсулина, реагирующего на глюкозу. Рекомбинантный человеческий инсулин производится преимущественно с использованием E. coli и Saccharomyces cerevisiae для терапевтического применения у человека. Тем не менее существует острая необходимость в увеличении в несколько раз производства биологически активного инсулина и его аналогов из кишечной палочки и дрожжей с использованием новейших эффективных технологий. Еще одна стратегия с использованием другого экспрессирующего хозяина, отличного от E. coli и Saccharomyces cerevisiae. Системы экспрессии на основе растений обладают огромным потенциалом для высокопроизводительного производства инсулина очень рентабельным способом. Разработанные методики синтеза инсулина предоставили возможность стабилизировать состояние пациентов с сахарным диабетом. Текущие производственные технологии не смогут удовлетворить растущий спрос на инсулин из-за ограниченных производственных мощностей и высокой стоимости производства.
Список литературы Синтез инсулина путем генной инженерии и применение его в медицине
- Практическая эндокринология / под ред. Г. А. Мельниченко. — Москва : Практическая медицина, 2009. — 351 с.
- Baeshen, N. A. Cell factories for insulin production / N. A. Baeshen, M. N. Baeshen, A. Sheikh [et al.] // Microb Cell Fact. — 2014. — Vol. 13. — № 141. — https://doi.org/10.1186/s12934-014-0141-0.
- Актуальные вопросы эндокринологии в терапевтической практике : рук.для врачей / М. Н. Ка-линкин, Л. В. Шпак, Ю. А. Волкова, Е. И. Березина [и др.] ; под ред. М. Н. Калинкин, Л. В. Шпак. — Тверь : Фактор и К, 2014 . — 698 с.
- Ajlouni K. Metabolic syndrome amongst adults in Jordan: prevalence, trend, and its association with socio-demographic characteristics / K. Ajlouni, Y. Khader, M. Alyousfi [et al.] // Diabetol Metab Syndr. — 2020. — Vol. 12. — № 100. — https://doi.org/10.1186/s13098-020-00610-7
- Сахарный диабет и нарушения углеводного обмена / Г. М. Кроненберг, Ш. Мелмед, К. С. Полон-ски : пер. с англ. ; под ред. И. И. Дедова, Г. А. Мельниченко. — Москва : Рид Элсивер, 2010. — 437 с.
- Balbas, P. Back to basics: pBR322 and protein expression systems in E. coli / P. Balbas, F. Bolivar // Methods Mol Biol. — 2004. — Vol. 267. — P. 77-90. doi: 10.1385/1-59259-774-2:077.
- Baeshen, M. N. Production of Biopharmaceuticals in E. coli: Current Scenario and Future Perspectives / A. M. Al-Hejin, R. S. Bora, M. M. Ahmed [et al.] // J Microbiol Biotechnol. — 2015. — Vol. 25. — № 7. — P. 953—962. DOI: 10.4014/jmb.1412.12079.
- Thomason LC, Recombineering: genetic engineering in bacteria using homologous recombination / L. C. Thomason, J. A. Sawitzke, X. Li [et al.] // Curr Protoc Mol Biol. — 2014. — Vol. 106. — P. 1.16.1— 1.16.39. DOI: 10.1002/0471142727.mb0116s106.
- Sawitzke, J. A. Recombineering: in vivo genetic engineering in E. coli, S. enterica, and beyond / J. A. Sawitzke, L. C. Thomason, N. Costantino, M. Bubunenko [et al.] // Methods Enzymol. — 2007. — Vol. 421. — P. 171—199. DOI: 10.1016/S0076-6879(06)21015-2.
- Nimri, R. Insulin Pump Therapy / R. Nimri, J. Nir, M. Phillip // Am J Ther. — 2020. — Vol. 27. — № 1. — P. e30—e41. DOI: 10.1097/MJT.0000000000001097.
- Balbas, P. The plasmid, pBR322 / P. Balbas, X. Soberon, F. Bolivar, R. L. Rodriguez // Biotechnology. — 1988. — Vol. 10. — P. 5—41. DOI: 10.1016/b978-0-409-90042-2.50007-6.


