Случай рН-положительного хронического миелоидного лейкоза с вариантной транслокацией Т(7;9;22)
Автор: Каримов Х.Я., Бобоев К.Т., Ассесорова Ю.Ю., Алланазарова Б.Р., Мустафина Л.К.
Журнал: Вестник гематологии @bulletin-of-hematology
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.13, 2017 года.
Бесплатный доступ
Хромосомные перестройки, приводящие к появлению атипичной Ph-хромосомы, выявляются у 5-10 % пациентов с ХМЛ. Вариантные транслокации возникают в результате вовлеченияв перестройку не только хромосом 9 и 22,но и других хромосом. Проведение стандартного цитогенетического исследования у больных ХМЛ дает возможность выявлять атипичные реаранжирокви, которые могут являться не только диагностическими маркерами, но и обуславливать вариант течения заболевания. Представленный случай наблюдения описывает новую вариантную транслокацию t(7,9,22)(q22; q34; qll)у больного ХМЛ в хронической стадии. Кроме того, показана значимость метода стандартного цитогенетического исследования для выявления атипичных реаранжировок и определения цитогенетических регионов разрывов.
Хронический миелолейкоз, ph-хромосома, вариантная транслокация
Короткий адрес: https://sciup.org/170171601
IDR: 170171601
The case of pH-positive chronic myeloid leukemia with variant translocation T(7;9;22)
Chromosomal rearrangements leading to the emergence of an atypical Ph-chromosomeare detected in 5-10% of patients with CML. Variant translocations arise as a result of the involvement in the rearrangement of not only chromosomes9 and 22, but also other chromosomes. The standardcytogenetic studies in patients with CML gives theopportunity to identify atypical rearrangements,which may not only be diagnostic markers, but alsodetermine the course of the disease. The presentedcase observation describes a new variant translocation t(7,9,22)(q22; q34; ql 1) in patient with CML inthe chronic stage. In addition, it shows the importance of the standard cytogenetic studies to detectatypical rearrangements and determination of thecytogenetic regions of gap.
Текст научной статьи Случай рН-положительного хронического миелоидного лейкоза с вариантной транслокацией Т(7;9;22)
Введение. Развитие хронического миелоидного лейкоза (ХМЛ) обусловлено реципрокной транслокацией t(9;22)(q34; qll.2), приводящей к образованию химерного гена BCR-ABL. Цитогенетическим проявлением данной транслокации является дериватная хромосома 22, называемая филадельфийской (Ph) хромосомой. Стандартным цитогенетическим исследованием (СЦИ) Ph-хромосому находят примерно у 90% больных ХМЛ. Однако у 5-10% пациентов дериват хромосомы 22 отличается от классической Ph-хромосомы и часто не обнаруживается методом СЦИ [1]. При этом молекулярно-генетические исследования, как правило, подтверждают наличие BCR-ABL [2,3]. Атипичность Ph-хромосомы обусловлена вовлечением в транслокацию не только хромосом 9и22,ноидругиххромосом. В литературе описано множество случаев дополнительного участия в патогенетической мутации ХМЛ от одной до трех дополнительных хромосом [4,5,6,1]. Каждый описанный случай является уникальным генетическим событием, приводящим к структурно-функциональным изменениям ряда генов. В зависимости от функции вовлеченных генов и молекулярных точек разрывов, такие мутации могут не иметь последствий, но также могут стать причиной изменения течения заболевания и ухудшения прогноза. В настоящее время среди исследователей нет единого мнения о прогностической значимости вариантных транслокаций t(V;9;22). Ряд авторов считает, что при вовлечении в транслокацию дополнительных хромосом прогноз остается таким же, как и при классической 1(9;22) [1,7]. Другие исследователи полагают, что вариантные транслокации обуславливают худший прогноз [6]. Накопление данных о вариантных перестройках с вовлечением хромосом 9 и 22, встречающихся при ХМЛ, позволит понять патогенетические механизмы течения гемобластоза и проводить прогностическую оценку в каждом конкретном нетипичном случае заболевания.
В настоящем исследовании нами представлен случай хронического миелоидного лейкоза с новой вариантной транслокацией t(7,9,22)(q22; q34; qll).
Материалы и методы исследования. Хромосомный анализ проводили методом стандартного цитогенетического исследования (СЦИ) с использованием рутинного окрашивания красителем Гимза и GTG-бэндинга с разрешением до 350 бэндов на кариотип. Для комплексной оценки кариотипа с целью выявления хромосомных изменений, ассоциированных с ХМЛ, анализировали метафазные пластинки, полученные из костного мозга больного. Культивирование ядерных клеток костного мозга проводили в краткосрочной культуре (24 часа) при температуре 37°C на питательной среде, содержащей RPMI-1640 с глутамином и 20% телячьей эмбриональной сыворотки (Компания «ПанЭко»). Остановку клеточного деления на стадии метафазы производили с помощью колхицина (0,01%), который вносили в среду в количестве 4 мкл при посадке. Гипотонизацию клеток раствором хлорида калия (0,55%) проводили в течение 25 мин при температуре 37 °C. Фиксацию клеток осуществляли трехкратным проведением через охлажденный до -4 °C фиксатор (этанол/ледяная уксусная кислота — 2,5:1). Хромосомные препараты готовили раскапыванием суспензии ядерных фрагментов клеток на влажные охлажденные предметные стекла. Полученные препараты высушивали при температуре 25 °C, окрашивали по методу Гимза с предварительной обработкой 0,25 % раствором трипсина и микроскопировали (микроскоп АХЮ Scope. А1, «Zeiss»). Поиск метафаз осуществляли при увеличении 200 (окуляры PI 10х/23 Zeiss, объектив ЕС Plan-NEOFLUAR20x/05 Ph2 оо/0,17), анализ метафазных пластинок — при увеличении 1000 (окуляры PI 10х/23 Zeiss, объектив С Plan-NEOFLUAR100x/l,3 Oil оо/0,17).
Было проанализировано 35 метафазных пластинок. Идентификацию хромосом проводили в соответствии с международной системой цитогенетической номенклатуры ISCN2009 [8].
Результаты и обсуждение. Клиническое наблюдение. Больному Ш., 1976 г. р., поступившему в состоянии средней тяжести в НИИ гематологии и переливания крови Минздрава РУз (НИИГ и ПК, Ташкент), в июле 2017 года был поставлен диагноз хронического миелоидного лейкоза. До обращения в специализированное учреждение при случайном медицинском обследовании у пациента были выявлены изменения в общем анализе крови. Общий анализ крови больного при поступлении в гематологическое отделение института показал: гемоглобин—126 г/л, эритроциты— 3,9Т012/л, цветной показатель — 0,9, тромбоциты — 404,0-109/л., лейкоциты — 95,0-109/л, бласты — 2 %, миелоциты — 5 %, метамиелобласты — 8 %, палочкоядерные клетки — 11%, сегментоядерные — 66 %, эозинофилы — 2 %, базофилы — 2 %, лимфоциты — 1 %, моноциты — 3 %, СОЭ — 23 мм/ч. Изучение цитологического состава костного мозга показало многоклеточность, бласты—1,8%, лимфоциты — 5,6 %, лейко-эритроцитарный индекс — 9:1, мегакариоциты — в достаточном количестве.
Цитогенетический анализ, проведенный в НИИГиПК М3 РУз, показал, что в 85% [30/35] клеток костного мозга больного присутствовала дериватная хромосома 22 (Ph-хромосома) (Рис. 1А.). Кроме того, при анализе метафазных пластинок были выявлены еще две дериватные хромосомы, одна из которых была идентифицирована как der(9), а другая — как der(7). При классической транслокации 1(9 ;22) дериватная хромосома 9 характеризуется визуальным увеличением светлой эухроматиновой зоны на конце длинного плеча за счет перемещения на него большей части q-плеча хромосомы 22. В случае описываемой нами перестройки q-плечо хромосомы 9 было на 25 % длиннее, чем у ее нормального гомолога вследствие перенесения на него части q-плеча хромосомы 7. Изменение хромосомы 7 цитогенетически определялось как отсутствие крупного терминального фрагмента q-плеча (Рис. 1Б.).
Я •
А.
7 der7 9 der9 It ■ # е I *11
____________________________________________ Б.
I S| | । • 1 l i i
1 2 3 45
. ■ ®. He » # .• • wit Л—Л в в
1II11111
6 7 8 ^9^ 10 1112
TV w w vv w w
13 14
19 20
^Ph
17 1S
Y В.
Puc. 1. A. Kapuomun больного ХМЛ с тремя дериватными хромосомами.
Б. Нормальные и дериватные хромосомы 7 и 9. В. Идеограмма, выполненная с помощью программы ВидеоТесТ-Карио-3.1. Вовлеченные в перестройку хромосомы и их дериваты обозначены стрелками. (Увеличение ><1000)
Относительный размер длины р- и q-плечей дериватов 9-й и 7-й хромосом и их гомологов, не затронутых перестройкой, размер трансло-цированных фрагментов, а также расположение бэндов позволило ориентировочно определить регионы разрывов в хромосомах, участвующих в вариантной транслокации t(7,9,22) (Рис. 2). Локусы разрывов на хромосомах 9 и 22 (соответственно, q34 и ql 1.2) хорошо известны и описаны в литературе. На 7-й хромосоме точка разрыва лежала в области эухроматиновой зоны, расположенной между двумя темноокрашенны-ми гетерохроматиновыми бэндами и идентифицируемой по системе ISCN2009, как локус q22. Анализ метафазных пластинок с помощью программы ВидеоТесТ-Карио-3.1 подтвердил наличие цитогенетической перестройки с вовлечением и 7-й, 9-й и 22-й хромосом — t(7,9,22)(q22; q34; qll) (Рис. IB.).
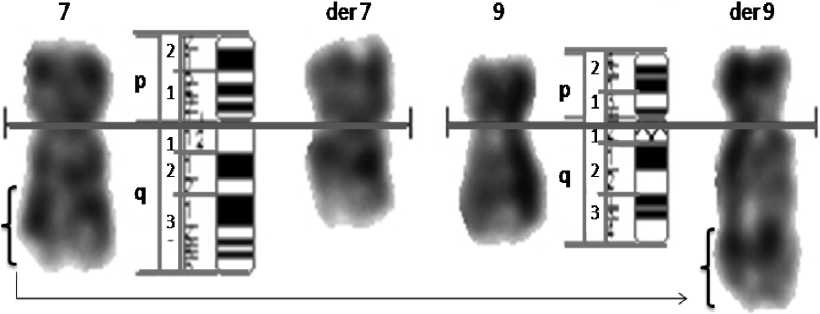
Рис. 2. Идентификация локусов разрывов и транслоцируемых фрагментов на хромосомах 7 и 9, вовлеченных в транслокацию t(7,9,22)(q22; q34; qll) (ISCN2009). (Увеличение xlOOO).
Таким образом, кариотипирование методом СЦИ костного мозга больного ХМЛ в хронической стадии позволило выявить вариантную транслокацию с вовлечением трех хромосом: 7, 9 и 22.
Во всех случаях перестроек с участием хромосом 9 и 22 происходит формирование химерного гена BCR-ABL, кодирующего белок с повышенной тирозинкиназной активностью, который играет ключевую роль в патогенезе ХМЛ. В отличие от дополнительных хромосомных аномалий, возникающих по мере развития ХМЛ и являющихся свидетельством наступления бластного криза, классическая транслокация t(9;22) и вариантные реаранжировки с участием хромосом 9 и 22 являются относительно стабильными хромосомными аномалиями, регистрируемыми при первичной диагностике и сохраняющимися цитогенетически неизмененными в течение заболевания. Однако вопрос о прогностической значимости вариантных транслокаций остается спорным. Возможно, течение заболевания, восприимчивость к терапии и прогноз зависят от степени сбалансированности комплексной вариантной мутации, что связано с потерей или дополнительным внесением генетического материала, а также со структурно-функциональным изменением генов, лежащих в локусах разрывов и отвечающих за пролиферацию и дифференцировку гемопоэтических клеток. Дисбаланс в функционировании генов, как правило, усиливает злокачественные свойства опухолевых клеток. Это выражается в интенсификации передачи опухолевым клеткам сигналов к пролиферации или в ослаблении супрессирующих сигналов, подавлении дифференцировки и апоптоза, приобретении резистентности к противоопухолевым препаратам и других проявлениях.
Новая вариантная реаранжировка 1(7,9,22) (q22; q34; ql 1) была выявлена нами у больного
ХМЛ в хронической стадии на фоне гиперлейкоцитоза, высокого содержания бластных клеток, низкой концентрации лимфоцитов. При этом, несмотря на прием гидреа (1000 мг/д), цитоге-матологические показатели и общее состояние больного продолжали ухудшаться. Ответ на вопрос о прогностической значимости подобных реаранжировок может быть получен при накоплении и систематизации данных по вариантным транслокациям с вовлечением хромосом 9 и 22. Однако анализ данных осложняется уникальностью каждого случая, обусловленной индивидуальным комплексом вовлеченных хромосом и локусов разрывов. Стандартное цитогенетическое исследование, оценивая состояние всего кариотипа, позволяет не только выявлять маркерные и атипичные реаранжирокви, но и определять цитогенетические регионы разрывов, приводящих к мутациям. Выявление данных локусов позволяет предполагать спектр генов, вовлеченных в формирование патогенетического лейкозного клона и, в дальнейшем, сузить поиск молекулярно-генетических маркеров, ассоциированных с вариантом течения ХМЛ и прогнозом.
Заключение. Клинический случай представляет интерес по следующим аспектам. У больного хроническим миелоидным лейкозом описана новая вариантная транслокация с вовлечением хромосом 7, 9 и 22. Хромосомная перестройка t(7,9,22)(q22; q34; qll) выявлена при первичной диагностике у пациента с заболеванием, находящимся в хронической стадии, что позволяет отнести ее к патогенетическим реаранжировкам, ассоциированным с хроническим миелоидным лейкозом. Проведение стандартного цитогенетического исследования при первичной диагностике и в динамике гемобластоза дает возможность выявлять атипичные реаранжирокви, которые могут являться не только диагностическими маркерами, но и обуславливать вариант течения заболевания.
Список литературы Случай рН-положительного хронического миелоидного лейкоза с вариантной транслокацией Т(7;9;22)
- Yokota S., Nakamura Y., Bessho M. A novel five-way translocation t(7;ll;9;22;9)(q22; ql3; q34; ql 1.2; q34) involving Ph chromosome in a patient of chronic myeloid leukemia: a case report // Mol Cytogenet. -2012 May 1,-5(1). -P.20.
- Sessarego M., Fugazza G., Bruzzone R., et al. Complex chromosome rearrangements may locate the bcr/abl fusion gene sites other than 22qll // Haematologica. 2000 Jan. 85(1). P.35-39.
- Batista D. A., Hawkins A., Murphy К. M., Griffin C. A. BCR/ABL rearrangement in two cases of Philadelphia chromosome negative chronic myeloid leukemia: deletion on the derivative chromosome 9 may or not be present // Cancer Genet Cytogenet. 2005 Dec. 163(2). P. 164-167.
- ALAchkar W., Wafa A., Nweder M. S. A complex translocation t(5;9;22) in Philadelphia cells involving the short arm of chromosome 5 in a case of chronic myelogenous leukemia // J Exp Clin Cancer Res. 2007 Sep. 26(3). P.411-415.
- Ikuta K., Torimoto Y, Jimbo J., et al. A novel five-way chromosomal translocation observed in chronic myelogenous leukemia // Cancer Genet Cytogenet. 2008 May. 183(1). P.69-71.
- Kuru D., Tarkan Argiiden Y, Ar M. C., et al. Variant Philadelphia translocations with different breakpoints in six chronic myeloid leukemiapatients // Turk J Haematol. 2011 Sep 5. 28(3). P.186-92.
- Bennour A., Bellaaj H., Ben Youssef Y, et al. Molecular cytogenetic characterization of Philadelphia-negative rearrangements in chronic myeloid leukemia patients // J Cancer Res Clin Oncol. 2011 Sep. 137(9). P.1329- 1336.
- Shaffer L.G., Slovak M.L., Campbell L. J., KargerS., eds. ISCN, 2009. An international systeme for human cytogenetic nomenclature. Basel; 2009.


