Сравнение эффективности плазмид 1 и 3 поколения, кодирующих химерный Т-клеточный рецептор к опухолевому маркеру рака яичников
Автор: Киселева Я.Ю., Большакова О.Б., Кулинич Т.М., Шишкин А.М., Боженко В.К.
Журнал: Вестник Российского научного центра рентгенорадиологии Минздрава России @vestnik-rncrr
Рубрика: Молекулярная медицина
Статья в выпуске: 2 т.21, 2021 года.
Бесплатный доступ
Рак яичников – пятая по частоте причина смерти от рака у женщин и вторая по частоте диагностирования опухоль в гинекологии. Поиск новых эффективных методов лечения рака яичника является актуальной клинической задачей. Одним из наиболее 26 перспективных методов на сегодняшний день является иммунотерапия с использованием CAR-T технологии. Антиген CA125, который имеет высокую экспрессию при раке яичника, может стать мишенью при разработке данных методов терапии. В данной работе представлены результаты разработки метода CAR-T терапии рака яичника с использованием плазмидных конструкций, несущих гены мономолекулярных Т-клеточных рецепторов к СА125. Разработаны и синтезированы три варианта плазмиды, проведены экспериментальные исследования, показавшие правильность и эффективность сборки Т--клеточных рецепторов к СА125 после проведенной трансфекции клеток плазмидными конструкциями, показана эффективность связывания генно-модифицированных клеток с растворенной формой СА125. Было показано, что химерная конструкция р3СА2 (эпитоп Х181) обладает большей эффективностью (72% трансфецированных Т-лимфоцитов приобретают способность связывать СА125) и является более перспективной для дальнейшего исследования.
Онкология, иммунотерапия, химерный антигенный рецептор, плазмида, рак яичников, CAR-T-терапия.
Короткий адрес: https://sciup.org/149135680
IDR: 149135680
Comparison of the efficiency of 1st and 3rd generation plasmids encoding a chimeric T-cell receptor for a tumor marker of ovarian cancer
Ovarian cancer is the fifth most common cause of cancer death in women and the second most commonly diagnosed tumor in gynecology. The search for new effective methods of treating ovarian cancer is an urgent clinical task. One of the most promising methods today is immunotherapy with CAR-T technology. The CA125 antigen, which is highly expressed in ovarian cancer, may be a target in the development of these therapies. This work presents the results of the development of a method for CAR-T therapy for ovarian cancer with plasmid constructs carrying the genes of monomolecular T-cell receptors for CA125. Three plasmid variants were developed and synthesized, experimental studies showed the correctness and efficiency of assembly of T-cell receptors for CA125 after transfection of cells with plasmid constructs. The efficiency of binding of genetically modified cells to the dissolved form of CA125 was demonstrated. The chimeric construct 28 p3CA2 (epitope X181) appeared to be more efficient (72% of transfected T-lymphocytes acquire the ability to bind CA125) and more promising for further research.
Текст научной статьи Сравнение эффективности плазмид 1 и 3 поколения, кодирующих химерный Т-клеточный рецептор к опухолевому маркеру рака яичников
Лечение и рациональная диагностика онкологических заболеваний в настоящее время являются чрезвычайно важной проблемой. Муцин 16 (MUC 16) занимает особую позицию среди белков, являясь не только диагностическим биомаркером, но и терапевтической мишенью [8, 9, 14]. MUC16 представляет собой высокомолекулярный трансмембранный гликопротеин, который обычно экспрессируется на поверхности определенных типов эпителиальных клеток [11]. Являясь представителем семейства муцинов, он содержится в слизи, покрывающей урогенитальные, дыхательные и пищеварительные тракты, а также конъюнктиву и роговицу. MUC16 в совокупности с другими муцинами защищает их от обезвоживания, инфекций и прочих повреждений (химического или физического характера) [6]. Превращение эпителиальных клеток в злокачественные сопутствуется экспрессией большого количества данного вещества на их поверхности [11].
Роберт Бастом и его коллеги первыми обнаружили MUC16. Ими было отмечено, что опухоль-ассоциативный антиген, экспрессирующий в 80% случаев рака яичников, связывается ранее обнаруженным моноклональным антителом OC125 [4]. Впоследствии новый антиген получил название СА125 (cаncer antigen 125) [5].
В настоящее время CA125 хорошо изучен и обширно используется как опухолевый маркер при раке яичников [2]. Он попадает в кровоток благодаря протеолитическому расщеплению и десквамации N-концевого домена MUC16
(sМUС16) с поверхности клеток опухоли. Антигенный эпитоп CA125 обнаруживают в сыворотке крови методом иммуноферментного анализа. Его принято считать лучшим биомаркером эпителиального рака яичников серозного типа. Иммунотерапия при раке яичников – перспективный и прогрессивно развивающийся метод, минимально влияющий на нормальные ткани организма, вследствие своей высокой специфичности. Поэтому поиск новейших подходов, в частности возможность использования CAR-T технологии, является актуальной клинической задачей. Известно, что иммунная система играет важную роль не только в этиологии онкологического заболевания, но и определяет его течение. Ключевой задачей фундаментальной науки является изучение взаимодействия клеток опухоли и иммунной системы, поэтому метод обращения собственного иммунитета против развития злокачественного новообразования может со временем быть представлен, как новый и эффективный способ лечения рака.
Один из таких методов – адоптивная иммунотерапия на основе искусственных (химерных) Т-клеточных рецепторов (CAR-therapy). Она включает введение в организм пациента Т-лимфоцитов, генетически модифицированных ex vivo и несущих на своей поверхности искусственный рецептор заданной специфичности. CAR представляет собой белок слияния и состоит из внеклеточного одноцепочечного вариабельного фрагмента иммуноглобулина scFv (single-chain Fv) и внутриклеточных сигнальных доменов Т-лимфоцитов [12]. В отличие от Т-клеточных рецепторов, которые узнают процессированные антигены в составе главного комплекса гистосовместимости, химерные Т-клеточные рецепторы нацелены на распознавание поверхностных нативных (непроцессированных) антигенов, ассоциированных со злокачественной трансформацией клеток [13].
Технология САR даёт возможность вне тела пациента перепрограммировать его собственные иммунные клетки с целью создания химерного рецептора антигена, который может охотиться за раковыми клетками и эффективно разрушает опухоль.
СAR, сконструированные по такому методу, входящие в состав иммунных эффекторных клеток, позволяют последним приобрести высокую избирательность благодаря добавленному рецептору от моноклональных антител. Полученные таким образом клетки после используются для адоптивной иммунной терапии, которая является разновидностью иммунотерапии рака [10].
Изначально химерные антигенные рецепторы имели в своей структуре нормальные рецепторы T-лимфоцитов, включали в себя цитоплазматическую эффекторную и антиген-распознающую части, а также передаточный фрагмент [3]. В дальнейшем были созданы CAR второго и третьего поколения, которые кроме CD3ζ содержали вспомогательные костимулитрующие домены. Чаще всего CAR второго поколения включают цитоплазматический домен молекулы CD28, расположенный между трансмембранным доменом и сигнальной последовательностью, содержащей ITAM [1, 3, 7]. Третье поколение конструкций допускает присутствие трёх внутриклеточных сигнальных доменов. В них, кроме фрагментов СD28 и СD3 ζ, могут содержаться сигнальные последовательности СD137 / 4-1ВВ, DАP10, СD134 / ОХ-40 и прочие.
Цель данной работы: (1) исследование и выбор оптимальной плазмиды 1 и 3 поколений, содержащей ген мономолекулярного химерного Т-клеточного рецептора к опухолеспецифическому антигену CA125, предназначенной для пассивной иммунотерапии опухолей; (2) оценка функциональности полученных рекомбинантных плазмид на клетках рака молочной железы (МСF-7) и лимфоцитах человека.
Материалы и методы
В работе использованы линии клеток рака яичника человека OVCAR-3, OVKATE и MCF-7 (рак молочной железы, человек), клетки культивировали в стандартных стерильных условиях с использованием среды DMEM (ПанЭко, Россия) при 5% СО2, 37 °С. Ряд экспериментов проведен на лимфоцитах периферической крови человека, полученных от условно здоровых доноров. Выделение фракции лимфоцитов проведено с помощью наслаивания на раствор фиколла-урографина (плотность 1,077 г/см3) (ПанЭко, Россия). Лимфоциты культивировали в стандартных условиях на среде RPMI (ПанЭко, Россия), с содержанием 10% фетальной бычьей сыворотки (ПанЭко, Россия). Т-лимфоциты активировали добавлением в среду интерлейкина-2 (50 ЕД/мл) (Ронколейкин, БИОТЕК, Россия) и фитогемагглютинина (1 мкг/мл) (ФГА, ПанЭко). Моноклональные биотинилированные мышиные антитела (изотип IgG1), способные в растворе связываться с СА125, были предоставлены OOO «XEМА» (Россия, Москва). Структура антител исследована с помощью методов электрофореза белков (SDS-PAGE) с применением технологии изоэлектрического фокусирования (IEF) (Agilent 7100, ФИЗЛАБПРИБОР, Россия).
Трансфекция Т-лимфоцитов человека и клеток MCF-7 проводилась с использованием прибора Amaxa Nucleofector (Lonza) и наборов «Humаn Т-Cеll Nuсlеоfесtоr Kit» (Lоnzа). Для клеток были использованы программы V-024, Т-020 и Т-023, обеспечивающие высокую эффективность трансфекции данных типов клеток.
Оценка экспрессии Z-цепи Т-клеточного рецептора, а также оценка связывания СА125 в растворе были проведены методом проточной цитометрии (Cytomics FC500, Beckman Coulter, USA). Биотинилированные антитела, для плазмиды plCAl - Х75, для плазмиды р3СА2 - Х181, для р3СА3 - Х189 были предоставлены ООО «ХЕМА» (Россия).
Результаты и обсуждение
Создание генно-инженерных конструкций (плазмид), экспрессирующих химерные T-клеточные рецепторы, которые могли распознать антиген СА125 на поверхностях клеток-мишеней, стало важным этапом проделанной работы. Было продемонстрировано, что трансфицированные такой плазмидой лимфоциты периферической крови человека, приобретают свойства экспрессировать на поверхности мономолекулярный Т-клеточный рецептор специфический к СА125.
Работа включала несколько этапов: на первом этапе проводился выбор целевого эпитопа молекулы антигена СА125; на втором этапе были синтезированы конструкции мономолекулярных рецепторов, включающих последовательности, комплементарные к выбранным участкам, и проведено определение правильности сборки рецепторов на поверхности клеток; на третьем этапе выполнено исследование функциональной активности данных конструкций Т-клеточных рецепторов.
Выбор целевого эпитопа СА125
Были созданы моноклональные биотинилированные мышиные антитела (изотип IgG1), способные связаться в растворе с СА125, а именно: Х193, Х189, Х181, Х144, Х75, Х69.
Также были выбраны три клеточные линии OVKATE, OVCAR-3 (рак яичника, человек), MCF-7. Линия OVCAR-3 и линия OVKATE несут на поверхности клеток антиген СА125, а линия MCF-7 не экспрессирует, поэтому ее использовали в качестве контроля. Структура исследуемых антител была изучена с помощью таких методов, как электрофорез белков (SDS-PAGE) и изоэлектрическое фокусирование (IEF).
Помимо этого для всех представленных антител с помощью метода проточной цитофлуориметрии определили связывание с клеточными культурами рака яичников. На основании результатов связывания антител с поверхностными антигенами СА125 было идентифицировано три антитела, демонстрирующих наивысший уровень связывания с линиями клеток OVKATE и OVCAR-3 - Х189, Х181, Х75. С помощью антител полученных к эпитопам СА125 (Х75, Х181, Х189) были разработаны плазмиды, несущие ген химерного мономолекулярного рецептора. В плазмиду рСI было проведено клонирование фрагментов Т-клеточного рецептора: вариабельные фрагменты легких и тяжелых цепей рецептора, комплементарные к соответствующим участкам антител, гибкий шарнирный участок молекулы СD8, фрагмент СD247, являющийся ζ-цепью Т-клеточного рецептора и включающий поверхностный и внутриклеточный домен. На основании структуры (поколения) рецептора данным конструкциям присвоены названия: р1СА1, р3СА2, р3СА3. В таблице 1 представлены описания последовательностей разработанных плазмидных конструкций.
Таблица 1. Структура плазмид, созданных входе исследования
|
№ |
Название |
Сокращен ное название |
Клон антитела scFv |
Шарнир ный участок |
Трансмем бранный домен |
Активаци онные домены |
|
1 |
pCI/CA1-CD8-CD247 (pCI/1C6-CD8-CD247) |
p1CA1 |
X75 |
CD8 |
CD247 |
CD247 |
|
2 |
pC1/3CA2-CARg |
p3CA2 |
X181 |
CD8 |
CD28 |
CD28, CD137, CD247 |
|
3 |
pCI/3CA3-CAR3g |
p3CA3 |
X189 |
CD8 |
CD28 |
CD28, CD137, CD247 |
Оценка функционирования плазмид, кодирующих химерный Т-клеточный рецептор. Исследование поверхностной экспрессии рецептора к СА125 на поверхности клеток MCF-7 после их модификации плазмидами
Клетки линии МСF-7(рак молочной железы человека) не экспрессируют рецепторы к СА125, поэтому появление данных рецепторов на поверхности клеток после внедрения в них плазмидных конструкций может являться показателем правильности сборки Т-клеточного рецептора. Для того, чтобы подтвердить правильность функционирования Т-клеточного рецептора, клетки линии МСF-7
трансфицировали созданными плазмидными конструкциями. Появление после трансфекции иммунореактивных эпитопов ζ-цепи химерного рецептора (СD3ζ) на поверхности клеток МСF-7 является одним из показателей функциональности созданных плазмид. Проверку экспрессии ζ-цепи линии клеток МСF-7 проводили через 24 часа после трансфекции. Для этого клетки обрабатывали меченными антителами к ζ-цепи химерного рецептора и анализировали на проточном цитофлуориметре. Положительный сигнал был обнаружен в клетках, трансфицированных всеми плазмидами, в то время как в не трансфицированных плазмидными конструкциями контрольных препаратах клеток сигнал отсутствовал. Полученные данные указывают на наличие экспрессии химерного иммунорецептора, кодируемого плазмидой р1СА1, и его правильную внутриклеточную сборку. В аналогичных экспериментах с использованием рекомбинантных плазмидных ДНК р2СА2 и р3СА3 (анализ через 24 часа после трансфекции, окрашивание клеток антителами к CD3ζ), экспрессия ζ-цепи была продемонстрирована в 22,3% и 17% клеток соответственно. Это подтверждает правильную сборку Т-клеточных рецепторов, экспрессируемых этими конструкциями. Проведённый после трансфекции плазмидными конструкциями р3СА2 и р3СА3 анализ клеток МСF-7 показал, что кодируемые исследуемой ДНК T-клеточные рецепторы, собираются на поверхности клеток. Это доказывают более высокий уровень экспрессии ζ-цепи по сравнению с рIСА1 и данные по окрашиванию антителами к внутриклеточному фрагменту ζ- цепи. Рисунок 2 показывает результаты связывания трансфицированных клеток с FITC-меченными антителами, полученные с помощью метода проточной цитофлуорометрии. Для всех изученных плазмид сборка химерного Т-клеточного рецептора протекала правильно. Тем не менее, в ходе исследования было установлено, что для каждой плазмидной конструкции свойственны индивидуальные особенности, выраженные в процентном содержании клеток, несущих химерный иммунорецептор и в разных количественных уровнях экспрессии.
Помимо этого, для того чтобы оценить способность трансфицированных клеток MCF-7 связываться с СА125, их инкубировали в течение 30 минут с раствором данного антигена, меченного флуоресцентным красителем FITC (CA125-FITC). Клетки, трансфицированные плазмидами, связывали CA125 в растворе, что было показано после 30 минут инкубации клеток с раствором CA125, меченным FITC. После трансфекции MCF-7 плазмидой р1СА1 положительный сигнал связывания антител был обнаружен у 16,5% клеток в культуре (рисунок 2Б).
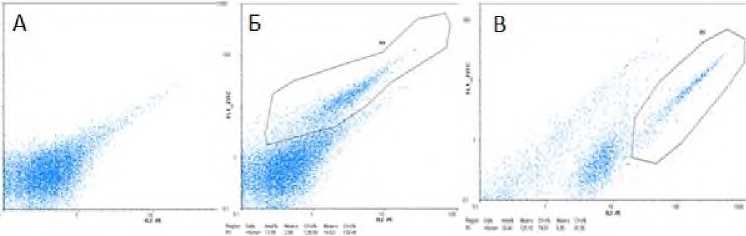
Рисунок 2. Цитофлуориметрический анализ связывания клеток MCF-7, трансфицированных плазмидой p1CA1 через 24 часа после трансфекции. (А) Отрицательный контроль (нетрансфицированные клетки MCF-7). (Б) Клетки MCF-7, трансфицированные плазмидной конструкцией р1СА1, через 24 часа после трансфекции с ФИТЦ-СА125 в растворе. (В) Клетки MCF-7, трансфицированные плазмидной конструкцией р1СА1, после окрашивания FITC-меченными антителами к Z- цепи CD3.
Таким образом, было установлено, что в клетках MCF-7, трансфицированных плазмидой р1СА1, химерный Т-клеточный рецептор экспрессирующийся на их поверхности, способен связать антиген СА125 в растворе, как через 24 часа, так и спустя 48 часов после трансфекции. Исходя из полученных результатов (рисунок 2Б и 2В) был сделан вывод, что клетки, трансфицированные плазмидной конструкцией р1СА1, через 24 часа после трансфекции, экспрессируют поверхностный Т-клеточный рецептор к СА125. При увеличении времени инкубации до 48 часов после трансфекции достоверных изменений в результатах получено не было. При дальнейшем изучении плазмид р3СА2 и р3СА3 было показано, что клетки, трансфицированные этими конструкциями, также спустя 24 и 48 часов после трансфекции, связывают антиген CA125-FITC (Таблица 2). Поэтому можно сделать вывод, что кодируемый всеми исследованными плазмидными конструкциями химерный Т-клеточный рецептор, после проведенной процедуры трансфекции, эффективно экспрессируется на поверхности клеток MCF-7. При исследовании различных вариантов плазмид, кодирующих химерный Т-клеточный рецептор, количественный уровень связывания CA125 с трансфицированными клетками MCF-7 в растворе варьировал в зависимости от выбранной конструкции. Были получены значения относительного уровня связывания FITC-CA125 на поверхности трансфицированных клеток (Таблица 2). Самый высокий уровень связывания СА125 был отмечен в клеточной культуре, трансфицированной плазмидой р3СА2. Анализ проводили через 24 и 48 часов после трансфекции. Стоит отметить, что строгой зависимости уровня связывания FITC-CA125 от времени обнаружено не было.
Таблица 2. Результаты оценки связывания антигена CA125-FITC с клетками линии
MCF-7 генно-модифицированными исследуемыми плазмидными конструкциями
|
Образец (наименование) |
24 часа инкубации |
48 часов инкубации |
|
Количество клеток, несущих поверхностный рецептор к СА125, % |
||
|
MCF-7контроль, нетрансфицированные |
0 |
0 |
|
MCF-7, трансфицированные р1СА1 |
8,3 |
9,2 |
|
MCF-7, трансфицированные р3СА2 |
22,6 |
23,7 |
|
MCF-7, трансфицированные р3СА3 |
17,8 |
16,4 |
Анализ связывания растворимой формы СА125 с лимфоцитами человека, трансфицированными плазмидами p1CA1, р3СА2, р3СА3
После оценки функциональности полученных плазмид, дальнейшее исследование метода иммунотерапии с использованием конструкций химерных Т-клеточных рецепторов к СА125 проводили на лимфоцитах человека. Проанализированные литературные данные свидетельствуют о том, что для повышения уровня экспрессии химерного рецептора и его способности связываться с соответствующим антигеном, а также в целях повышения эффективности трансфекции, рекомендуется предварительная активация лимфоцитов.
В нашем исследовании было проведено сравнение эффективности плазмидных конструкций р1СА1, р3СА2 и р3СА3 при их трансфекции в не активированные и активированные лимфоциты. Активацию проводили рекомбинантным интерлейкином-2 (IL-2) человека (50 ЕД/мл) с параллельной стимуляцией фитогемагглютенином (PHA) в течение 3 суток. По истечении этого срока доля СD3+ Т лимфоцитов в клеточной культуре составляла 60 ± 10%. Последующая трансфекция лимфоцитов человека плазмидными конструкциями методом электропорации была проведена с использованием прибора Amaxa Nucleofector (LonzaEio).
Для того чтобы оценить способность связывать СА125, нестимулированные лимфоциты трансфицировали плазмидами р1СА1, р3СА2 и р3СА3. Затем спустя 24 и 48 часов после трансфекции инкубировали в течение 30 минут с раствором антигена, меченного флуоресцентным красителем FITC (CA125-FITC). Количество клеток, несущих рецептор CA125 на поверхности и связывающих антиген CA125-FITC, оценивали с помощью проточной цитометрии. Проанализировав диаграммы связывания лимфоцитов, которые были трансфицированы исследуемыми плазмидными конструкциями р1СА1, р2СА2, р3СА3 с СА125-НТС, получили 28%, 43% и 36% связывания соответственно. Тем самым было показано, что самый высокий уровень связывания СА125 наблюдается для лимфоцитов, трансфицированных плазмидой р3СА2.
Результаты цитофлуорометрического анализа связывания FITC-CA125 с предварительно активированными IL-2/PHA лимфоцитами, трансфицированными серией плазмидных конструкций, показали, что уровень связывания CA125 активированными клетками значительно превышает уровень связывания с нестимулированными лимфоцитами, трансфицированными теми же плазмидами (р1СА1, р3СА2,р3СА3), и равен 31%, 72% и 56% соответственно. В результате эксперимента было показано, что предварительная активация лимфоцитов, приводит к увеличению экспрессии Т-клеточного рецептора.
Исследования функциональной активности трёх плазмидных конструкций, несущих Т-клеточный рецептор к СА125, продемонстрировали, что разработанные плазмидные конструкции при трансфекции в клетки человека вызывают экспрессию поверхностных рецепторов к СА125. Установлено, что наиболее перспективной для дальнейших исследований является плазмида р3СА2 (pCI/3СА2-CAR3g, антитело Х181), так как она обладает наибольшей функциональностью и эффективностью. Плазмидная конструкция р3СА2 обеспечивает экспрессию функциональных Т-клеточных рецепторов не только на поверхности лимфоцитов человека, но и на клетках линии MCF-7.
Таким образом, проведенное исследование позволило разработать плазмидную конструкцию к опухолевому антигену СА125, что может являться основой для разработки метода иммунотерапии злокачественных новообразований, при которых опухолевые клетки несут на поверхности СА125 (рак яичника, рак легкого).
Список литературы Сравнение эффективности плазмид 1 и 3 поколения, кодирующих химерный Т-клеточный рецептор к опухолевому маркеру рака яичников
- Боженко В. К., Князева А.Д., Киселева Я.Ю. и др. Исследование эффективности различных вариантов химерных Т клеточных рецепторов относительно РЭА позитивных опухолевых клеток. Вестник РНЦРР. 2018. Т. 18. № 2. С. 3 4.
- Сергеева Н.С., Маршутина Н.В. Опухолеассоциированные маркеры в скрининговых программах, направленных на активное выявление рака яичников: реальность, проблемы и перспективы. Практическая онкология. 2010. Т. 11. № 2. С. 110 119.
- Acuto O., Michel F. CD28 mediated co stimulation: a quantitative support for TCR signaling. Nat Rev Immunol. 2003. V. 3. No. 12. P. 939 951. doi: 10.1038/nri1248.
- Bast R. C., Jr., Feeney M., Lazarus H., et al. Reactivity of a monoclonal antibody with human ovarian carcinoma. J Clin Invest. 1981. V. 68. No. 5. P. 1331 1337. doi: 10.1172/JCI110380.
- Bast R. C., Jr., Klug T. L., St John E., et al. A radioimmunoassay using a monoclonal antibody to monitor the course of epithelial ovarian cancer. N Engl J Med. 1983. V. 309. No. 15. P. 883 887. doi: 10.1056/NEJM198310133091503.
- Bottoni P., Scatena R. The Role of CA 125 as Tumor Marker: Biochemical and Clinical Aspects. Adv Exp Med Biol. 2015. V. 867. P. 229 244. doi: 10.1007/978 94 017 7215 0_14.
- Cheng J., Montecalvo A., Kane L.P. Regulation of NF κB induction by TCR/CD28. Immunol Res. 2011. V. 50. No. 2 3. P. 113 117. doi: 10.1007/s12026 011 8216 z.
- Das S., Batra S.K. Understanding the Unique Attributes of MUC16 (CA125): Potential Implications in Targeted Therapy. Cancer Res. 2015. V. 75. No. 22. P. 4669 4674. doi: 10.1158/0008 5472.CAN 15 1050.
- Felder M., Kapur A., Gonzalez--Bosquet J., et al. MUC16 (CA125): tumor biomarker to cancer therapy, a work in progress. Mol Cancer. 2014. V. 13. Article ID 129. doi: 10.1186/1476--4598--13--129.
- Haji--Fatahaliha M., Hosseini M., Akbarian A., et al. CAR--modified T--cell therapy for cancer: an updated review. Artificial Cells Nanomed Biotechnol. 2016 V. 44. No. 6. P. 1339--1349. doi:10.3109/21691401.2015.1052465.
- Haridas D., Ponnusamy M. P., Chugh S., et al. MUC16: molecular analysis and its functional implications in benign and malignant conditions. Faseb J. 2014. V. 28. No. 10. P. 4183--4199. doi: 10.1096/fj.14--257352.
- Jena B., Dotti G., Cooper L.J. Redirecting T--cell specificity by introducing a tumor--specific chimeric antigen receptor. Blood. 2010. V. 116. No. 7. P. 1035--1044. doi: 10.1182/blood--2010--01--043737.
- Klebanoff C.A., Rosenberg S.A., Restifo N.P. Prospects for gene--engineered T--cell immunotherapy for solid cancers. Nat Med. 2016. V. 22. No. 1. P. 26--36. doi: 10.1038/nm.4015.
- Marcos--Silva L., Narimatsu Y., Halim A., et al. Characterization of binding epitopes of CA125 monoclonal antibodies. J Proteome Res. 2014. V. 13. No. 7. P. 3349--3359. doi: 10.1021/pr500215g.


