Сравнение качества жизни, уровня депрессии и тревоги у пациентов со злокачественными образованиями прямой кишки после хирургического лечения с извлечением препарата через естественные отверстия (NOSES) и с мини-лапаротомией
Автор: Ефетов С.К., Цао Ю., Хлусов Д.И., Панова П.Д., Ван Г., Хоробрых Т.В.
Журнал: Московский хирургический журнал @mossj
Рубрика: Онкология
Статья в выпуске: 2 (92), 2025 года.
Бесплатный доступ
Цель исследования. Изучить качество жизни, уровень депрессии и тревоги пациентов после лапароскопических операций по поводу злокачественной опухоли прямой кишки с экстракцией препаратов через естественные отверстия (NOSES) и с выполнением мини-лапаротомии (CL). Материалы и методы. Проспективный анализ результатов лечения пациентов с диагнозом рак прямой кишки выполнен на основании наблюдений пациентов клиники факультетской хирургии № 2 и Второй дочерней больницы Харбинского медицинского университета. Регистрировались и сравнивались предоперационные и послеоперационные результаты стандартизированных опросов: анкета оценки качества жизни (SF-36), шкала депрессии Бека (BDI), тест Спилберга (STAI). Результаты. В исследование были включены данные 30 пациентов после лапароскопической резекции прямой кишки с извлечением препарата через естественные отверстия (NOSES) и через мини-лапаротомию (CL). Через три месяца после операции в группе NOSES отмечались лучшие показатели ролевой функции, физической боли и эмоционального состояния по сравнению с группой CL (все p<0,05). Через шесть месяцев пациенты из группы NOSES демонстрировали лучшие результаты по ролевой, физической, социальной функциям, витальности, эмоциональному состоянию и психическому здоровью (p<0,05) по данным SF-36. Что касается послеоперационной депрессии, пациенты группы NOSES имели лучшие показатели перед выпиской (p=0,037) и через три месяца после операции (p=0,003). По уровню тревожности пациенты группы NOSES имели показатели ниже как по ситуативной (p=0,016), так и по личностной тревожности (p=0,015). Выводы. Данное исследование демонстрирует значительные преимущества послеоперационного качества жизни и психологического самочувствия пациентов после NOSES в сравнении с классической лапароскопической операцией с выполнением мини-лапаротомии.
NOSES, рак прямой кишки, колоректальный рак, минимально инвазивная хирургия, качество жизни, тревожность, депрессия, лапароскопическая хирургия
Короткий адрес: https://sciup.org/142244474
IDR: 142244474 | УДК: 006.617-089 | DOI: 10.17238/2072-3180-2025-2-97-107
Comparing quality of life and psychological status in patients with rectal cancer after natural orifice specimen extraction surgery (NOSES) versus conventional laparoscopic surgery
Introduction. To evaluate and compare the quality of life and psychological status of patients after laparoscopic surgery for rectal cancer with Natural Orifice Specimen Extraction Surgery (NOSES) and with the conventional laparoscopic. Materials and methods of research. This prospective study included patients at Sechenov University and Harbin medical university. Patients were segregated into NOSES group and CL group based on case-match method. QoL was assessed using the short-form 36 health survey (SF-36), Beck anxiety inventory (BAI), and Spielberger state-trait anxiety inventory (STAI) pre-operation, pre-discharge, postoperative 3 months, and postoperative 6 months. Treatment results. A total of 30 patients (15 in NOSES group and 15 in CL group) were included. At three months postoperatively, role function, physical pain, and emotional state were better in the NOSES group than in the CL group (all p<0.05). At six months postoperatively, NOSES group patients with better than CL group patients in role function, physical function, vitality, social function, emotional state, and mental health (p<0.05). As for postoperative depression, patients in the NOSES group were significantly better than patients in the CL group before discharge (p=0.037) and three months after surgery (p=0.003). In terms of anxiety, patients’ state anxiety in the NOSES group were lower than CL group before discharge (p=0.016), and trait anxiety were better than CL group (p=0.015). Conclusion. This research provides compelling evidence that NOSES offers significant advantages in postoperative QoL, psychological well-being, with comparable surgical outcomes of the CL approach.
Текст научной статьи Сравнение качества жизни, уровня депрессии и тревоги у пациентов со злокачественными образованиями прямой кишки после хирургического лечения с извлечением препарата через естественные отверстия (NOSES) и с мини-лапаротомией
Колоректальный рак (КРР) занимает третье место среди наиболее распространенных злокачественных новообразований в мире и является четвертой по значимости причиной смертности от рака [1]. Хирургическое лечение остается основным методом лечения, при этом широко применяются лапароскопические техники [2]. Традиционная лапароскопическая хирургия (CL) обычно требует вспомогательного разреза брюшной стенки для извлечения препарата, что приводит к послеоперационным болям, повышенному риску осложнений в месте разреза и эстетическим проблемам, которые также могут иметь долгосрочные психологические последствия для пациентов.
Операции с извлечением препарата через естественные отверстия (NOSES) сохраняют преимущества лапароскопической хирургии в сочетании с использованием естественных отверстий человека для экстракции препарата, что позволяет избежать вспомогательных разрезов без ущерба для результатов лечения [3].
Несмотря на доказанную эффективность и безопасность NOSES в лечении КРР с точки зрения хирургических результатов [4–5], пациенты часто сталкиваются с послеоперационными психологическими проблемами, такими как депрессия и тревога. Исследования показывают, что психологическое благополучие играет решающую роль в послеоперационном восстановлении пациентов [6].
Материалы и методы
Была собрана проспективная когорта пациентов с низкой локализацией опухолей прямой кишки, которым была проведена радикальная резекция в период с января 2023 года по август 2024 года. Пациенты были набраны из клиники факультетской хирургии № 2 Первого МГМУ им. И.М. Сеченова и отделения колоректальной хирургии Харбинского медицинского университета.
Всем пациентам, соответствующим критериям исследования, была выполнена низкая передняя резекция прямой кишки, и они были разделены на две группы лечения в зависимости от хирургической техники. Первая группа – пациенты после лапароскопической низкой передней резекции прямой кишки с экстракцией препарата через анус (NOSES), вторая группа - пациенты после лапароскопической или роботической операции с мини-лапаротомией для экстракции препарата (CL).
Критерии включения: (1) ИМТ ниже 35 кг/м², (2) подтвержденный диагноз злокачественного образования средне- или нижнеампулярного отделов прямой кишки с помощью колоноскопии и биопсии, (3) по данным предоперационной визуализации протяженность опухоли ≤5,0 см, T-стадия не больше T3, (4) окружной диаметр опухоли менее 5 см , (5) добровольное информированное согласие получено от всех участников , (6) отсутствие стеноза ануса или врожденных пороков развития ануса.
Критерии исключения: (1) необходимость экстренной операции из-за острой кишечной непроходимости, перфорации или клинически значимого кровотечения, (2) необходимость формирования профилактической стомы или наличие стомы по другим причинам, (3) первично-множественный синхронный колоректальный рак или наличие отдаленных метастазов на момент постановки диагноза, (4) пациенты с противопоказаниями для лапароскопического вмешательства, (5) пациенты с неполными клиническими данными или недостаточным наблюдением.
Пациенты были отслежены на протяжении восьми месяцев после операции. После отбора по указанным критериям и минимизации смещения путем сопоставления по полу, возрасту, ИМТ, стадии, локализации и размеру опухоли было сформировано 15 пар пациентов “NOSES-CL” для дальнейшего анализа.
Распределение пациентов
Все операции проводились опытными колоректальными хирургами, имеющими значительный опыт в лапароскопических и роботизированных резекциях КРР (не менее 100 операций). Пациенты были проинформированы о том, что их данные о лечении будут использоваться в исследовательских целях с соблюдением строгих мер конфиденциальности. Исследование было одобрено этическим комитетом Сеченовского университета (протокол заседания Локального этического комитета № 25–22).
Техника операций
В обеих группах (NOSES и CL) операции проводились по стандартизированной методике, включающей тотальную ме-зоректумэктомию (TME) – золотой стандарт для обеспечения полного удаления мезоректума при низких передних резекциях. Все этапы хирургического вмешательства до момента пересечения препарата были одинаковыми в обеих группах и включали в себя: расстановку троакаров, ревизию органов брюшной полости, лимфодиссекцию объемом D2 или D3 в зависимости от стадии заболевания, мобилизацию препаратов в эмбриональных слоях с соблюдением принципом TME, разметку краев резекции.
В группе CL извлечение препарата осуществлялось через мини-лапаротомию, протяженностью от 6 до 10 см, с последующим формированием анастомоза «конец-в-конец» при помощи циркулярного сшивающего аппарата.
В группе NOSES преимущественно применялась модифицированная процедура NOSES 1F [7] или NOSES II. При выполнении NOSES 1F после полной мобилизации препарата кишка промывалась 1 % раствором повидон-йода или бета-дина, в задний проход вставлялся специальный металлический стержень с головкой, заводился в просвет до намеченной проксимальной линии резекции, после чего кишка вместе с опухолью выворачивалась через анус. После этого под визуальным контролем препарат отсекался и формировался ручной двурядный анастомоз конец-в-конец и кишка возвращалась в брюшную полость (рис. 1).
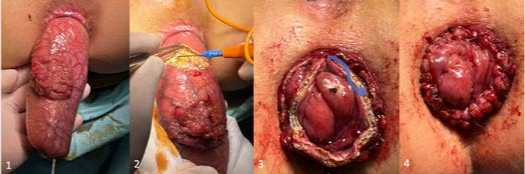
Рис. 1. Трансанальная экстракция NOSES 1F и формирование ручного анастомоза. 1 – момент экстракции, 2 – отсечение препарата, 3 – формирование анастомоза, 4 – финальный вид анастомоза Fig. 1. Transanal extraction NOSES 1F and forming a manual anastomosis. 1 – moment of extraction, 2 – cutting off the preparation, 3 – anastomosis formation, 4 – final view of the anastomosis
При выполнении NOSES II кишка промывалась 1 % раствором повидон-йода или бетадина, на уровне предварительно намеченной дистальной границы резекции, просвет кишки закрывался лигатурой, через задний проход в просвет прямой кишки на окончатом зажиме проводился стерильный рукав до уровня лигатуры, под кишку укладывалась салфетка, пропитанная раствором бетадина, вскрывался просвет кишки с ее пересечением, рукав расправлялся в брюшной полости. Далее окончатым зажимом кишка захватывалась в области лигатуры и плавными движениями выводилась наружу через задний проход. Экстракорпорально препарат отсекался на уровне предварительно намеченной проксимальной границы резекции, в просвет кишки заводилась наковальня циркулярного сшивающего аппарата, фиксировалась киссетным швом, и кишка возвращалась в брюшную полость. Просвет прямой кишки закрывался линейным сшивающим аппаратом, формировался аппаратный анастомоз конец-в-конец или бок-в-конец (рис. 2). Состоятельность анастомоза подтверждалась водно-воздушной пробой.
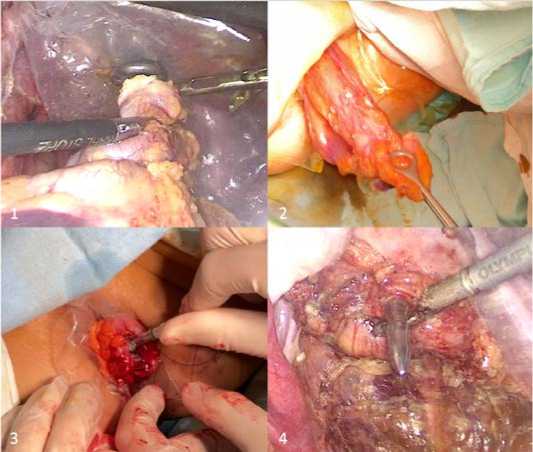
Рис. 2. Трансанальная экстракция NOSES II и формирование аппаратного анастомоза. 1 – рассечение кишки и начало экстракции препарата, 2 – экстракция препарата через анальный канал, 3 – фиксация наковальни сшивающего аппарата и возвращение препарата в брюшную полость, 4 – этап формирования циркулярного аппаратного анастомоза
Fig. 2. Transanal extraction of NOSES II and formation of apparatus anastomosis. 1 – dissection of the intestine and the beginning of drug extraction, 2 – drug extraction through the anal canal, 3 – fixation of the anvil of the stapling device and return of the drug to the abdominal cavity, 4 – stage of circular apparatus anastomosis formation
Статистический анализ
Анализ данных проводился в SPSS for Windows, Version 27.0 (SPSS Inc., Chicago, IL). Для нормально распределенных данных: выражались как среднее ± стандартное отклонение, использовался t-критерий Стьюдента. Для ненормально распределенных данных: выражались как медианы с минимальным и максимальным значениями, использовался критерий Манна-Уитни U. Для категориальных переменных: представлялись в виде пропорций, сравнивались с помощью критерия хи-квадрат или точного теста Фишера. Статистическая значимость определялась при p<0,05, что обеспечивало достоверность выводов.
Результаты
Проведен проспективный сбор данных, включая: базовую информацию о пациентах, хирургические данные, данные послеоперационного восстановления, отчеты о качестве жизни (QoL). Для оценки качества жизни и психологического статуса использовались стандартизированные опросники: SF-36 – опросник из 36 вопросов, оценивающий 8 категорий: Физическая функция (PF), Ролевая функция (RF), Физическая боль (PP), Общее здоровье (GH), Витальность (VT), Социальная функция (SF), Эмоциональное состояние (ES), Психическое здоровье (MH); BDI (шкала депрессии Бека) – шкала из 21 пункта для оценки интенсивности симптомов депрессии; STAI (тест Спилберга) – шкала из 40 пунктов для оценки состояния тревоги (SA) и личностной тревожности (TA).
С января 2023 по август 2024 года было включено 30 пациентов, по 15 в группе NOSES и 15 в группе CL. Предоперационная неоадъювантная химиолучевая терапия назначалась значительно чаще в группе CL (46,7 %) по сравнению с группой NOSES (6,7 %), при этом значение P составило 0,013, что свидетельствует о статистически значимой разнице. Такой результат может быть обусловлен более ранней стадией и меньшими размерами опухоли в группе NOSES. Обе группы были хорошо сопоставимы по основным демографическим и клиническим характеристикам, таким как возраст, пол, ИМТ, классификация ASA, сопутствующие заболевания, размер опухоли, гистологическая стадия T, гистологическая стадия N и стадия TNM, что обеспечило сбалансированное сравнение (табл. 1).
Таблица 1
Основные сведения о пациентах, включенных в исследование
The basic information of included patients
Table 1
|
NOSES (15) |
CL (15) |
P |
|
|
Пол, n (%) Gender, n (%) |
0,715 |
||
|
Мужской Male |
7(46,7) |
8(53,3) |
|
|
Женский Female |
8(53,3) |
7(46,7) |
|
|
Возраст, (года) Age, (years) |
56,18±8,24 |
56,07±6,93 |
0,969 |
|
ИМТ, (кг/м2) BMI, (kg/m2) |
23,55±3,55 |
25,15±4,39 |
0,332 |
|
ASA стадия, n (%) ASA grade, n (%) |
0,068 |
||
|
I/II |
15(100,0) |
12(80,0) |
|
|
III |
0(0,0) |
3(20,0) |
|
|
Неоадъювантная терапия, n (%) Neoadjuvant therapy, n (%) |
1(6,7) |
7(46,7) |
0,013* |
|
Сопутствующие заболевания, n (%) Comorbidities, n (%) |
10(66,7) |
10(66,7) |
1,000 |
Продолжение Таблицы 1
|
Размер опухоли, (см) Tumor size, (cm) |
0,543 |
||
|
<5cm |
13(86,7) |
14(93.3) |
|
|
≥5cm |
2(13.3) |
1(6,7) |
|
|
Патологоанатомическая T стадия, n (%) Pathological T stage, n (%) |
0,231 |
||
|
Tis |
2(13,3) |
0(0,0) |
|
|
T1 |
7(46,7) |
4(26,7) |
|
|
T2 |
2(13,3) |
4(26,7) |
|
|
T3 |
4(26,7) |
7(46,7) |
|
|
Патологоанатомическая N стадия n (%) Pathological N stage, n (%) |
0,666 |
||
|
N0 |
11(73,3) |
12(80,0) |
|
|
N1 |
4(26,7) |
3(20,0) |
|
|
N2 |
0(0,0) |
0(0,0) |
|
|
TNM стадия, n (%) TNM Stage, n (%) |
0,297 |
||
|
0 |
3(20,0) |
0(0,0) |
|
|
I |
5(33,3) |
8(53,3) |
|
|
II |
4(26,7) |
4(26,7) |
|
|
III |
3(20,0) |
3(20,0) |
Время операции в группах NOSES и CL существенно не отличалось: средняя продолжительность операции составила 250,45±61,05 минуты и 299,33±73,12 минуты, соответственно (P=0,084). Интраоперационная кровопотеря также была сопоставима между двумя группами: в группе NOSES она составила в среднем 65,45±60,56 мл, а в группе CL – 90,00±60,36 мл (P=0,316).
Сроки появления первого стула в группе NOSES (1,80±0,94 дня) были короче по сравнению с группой CL (3,55±2,42 дня, P=0,042). Кроме того, достоверно отличалась продолжительность госпитализации пациентов в группе NOSES (7,20±1,26 дня) по сравнению с группой CL (9,80±1,82 дня), P<0,001.
Статистический анализ показал отсутствие значимых различий в общем количестве осложнений между группами (P=0,803). Однако было выявлено существенное различие в частоте несостоятельности анастомозов: в группе NOSES они составили 6,7 %, в то время как в контрольной группе составили 20 % (P=0,598), всем пациентам потребовалось экстренное оперативное вмешательство с ушиванием дефектов анастомозов и формированем стомы. Другие осложнения распределились следующим образом: инфицирование операционной раны: 6,7 % vs 20 % (P=0,598), вентральная грыжа: 6,7 % vs 13,3 % (P=1,000), внутрибрюшная инфекция: 6,7 % vs 13,3 % (P=1,000).
Пациенты в обеих группах продемонстрировали невысокие показатели послеоперационной боли согласно визуальной аналоговой шкале боли (ВАШ) на 1-е, 3-и и 5-е сутки послеоперационного периода. Однако стоит отметить, что в группе NOSES они были менее выражены, особенно на 5-е сутки: 1,55±1,51 vs 3,40±1,84 (Р=0,012) (табл. 2).
Таблица 2
Интраоперационные показатели и краткосрочные результаты
The short-term outcome
Table 2
|
NOSES (15) |
CL (15) |
P |
|
|
Время операции (мин) operation time (min) |
250,45±61,05 |
299,33±73,12 |
0,084 |
|
Интраоперационная кровопотеря (мл) intraoperation bleeding (ml) |
65,45±60,56 |
90,00±60,36 |
0,316 |
|
Хирургическая платформа, n (%) surgical platform, n (%) |
1,000 |
||
|
лапароскопия laparoscopic |
14(90,9) |
15(100) |
|
|
робот robotic |
1(6,7) |
0(0) |
|
|
Тип NOSES, n (%) Type of NOSES, n (%) |
NaN |
||
|
NOSES тип I NOSES type I |
11(73,3) |
0(0) |
|
|
NOSES тип II NOSES type II |
4(26,7) |
0(0) |
|
|
Сроки восстановления перистальтики, (день) Gastrointestinal recovery time, (D) |
1,91±2,88 |
1,20±0,68 |
0,441 |
|
Первый прием пищи, (день) First postoperative oral feeding, (D) |
1,82±0,41 |
2,00±0,00 |
0,167 |
|
Первый послеоперационный стул, (день) First postoperative first flatus, (D) |
1,80±0,94 |
3,55±2,42 |
0,042* |
|
Сроки пребывания в стационаре, (день) Hospital stays, (D) |
7,20±1,26 |
9,80±1,82 |
<0,001* |
Продолжение Таблицы 2
|
Дополнительное использование анальгетиков, n (%) Usage of Additional Analgesics, n (%) |
1(6,7) |
5(33,3) |
0,169 |
|
Несостоятельность анастомоза, n (%) Anastomotic leakage, n (%) |
1(6,7) |
3(20) |
0,598 |
|
Инцизионная инфекция, n (%) Incisional infection, n (%) |
1(6,7) |
3(20) |
0,598 |
|
Инцизионная грыжа, n (%) Incisional hernia, n (%) |
1(6,7) |
2(13,3) |
1,000 |
|
Внутрибрюшная инфекция, n (%) Intra-abdominal infection, n (%) |
1(6,7) |
2(13,3) |
1,000 |
|
Послеоперационная пневмония, n (%) Postoperative pneumonia, n (%) |
0(0) |
0(0) |
NaN |
|
Clavien-Dindo классификация, n (%) Clavien-Dindo classification, n (%) |
NaN |
||
|
класс 1 grade 1 |
0(0) |
2(13,3) |
0,047 |
|
класс 2 grade 2 |
0(0) |
1(6,7) |
|
|
класс 3 grade 3 |
1(6,7) |
2(13,3) |
|
|
Визуальная аналоговая шкала боли VAS pain scale |
|||
|
1-й послеоперационный день Day 1 postoperatively |
2,82±2,09 |
3,87±1,64 |
0,164 |
|
3-й послеоперационный день Day 3 postoperatively |
2,36±1,69 |
3,33±1,50 |
0,135 |
|
5-й послеоперационный день Day 5 postoperatively |
1,55±1,51 |
3,40±1,84 |
0,012* |
операции в группе NOSES были выше показатели RF (ролевая функция), PP (физическая боль) и ES (эмоциональное состояние), все p<0,05. Через шесть месяцев после операции в группе NOSES были лучше показатели RF (ролевая функция), PP (физическая боль), VT (жизнеспособность), SF (социальная функция) и MH (психическое здоровье), все р<0,005. После лечения качество жизни всех пациентов в обеих группах в основном вернулось к норме. Эти результаты доказывают, что у пациентов после NOSES наблюдается значительное улучшение по нескольким параметрам и в то же время лучшие общие результаты, чем у пациентов в группе CL, что способствует повышению общего уровня качества жизни пациентов (табл. 3).
Таблица 3
Результаты исследования качества жизни (SF-36)
The results of quality-of-life (SF-36)
Результаты оценки качества жизни
До операции и перед выпиской существенных различий между двумя группами не было выявлено. Через три месяца после
Table 3
|
Показатели здоровья |
NOSES (15) |
CL (15) |
P |
|
Физическая функция (PF) Physical function (PF) |
|||
|
До операции Pre-operation |
70,91±15,14 |
69,00±14,78 |
0,750 |
|
Перед выпиской Pre-charge |
63,64±31,15 |
60,67±26,92 |
0,797 |
|
Через 3 месяца Postoperative 3 month |
85,91±12,41 |
85,33±6,40 |
0,890 |
|
Через 6 месяцев Postoperative 6 month |
90,00±13,96 |
91,67±11,60 |
0,743 |
|
Ролевое функционирование (RF) Role function (RF) |
|||
|
До операции Pre-operation |
43,18±41,97 |
31,67±43,78 |
0,507 |
|
Перед выпиской Pre-charge |
0,00±0,00 |
5,00±10,35 |
0,082 |
|
Через 3 месяца Postoperative 3 month |
100,00±0,00 |
63,33±41,04 |
0,004* |
|
Через 6 месяцев Postoperative 6 month |
100,00±0,00 |
83,33±24,40 |
0,019* |
|
Физическая боль (PP) Physical Pain (PP) |
|||
|
До операции Pre-operation |
67,27±21,19 |
65,07±19,42 |
0,785 |
|
Перед выпиской Pre-charge |
48,55±21,21 |
46,80±14,92 |
0,818 |
|
Через 3 месяца Postoperative 3 month |
100,00±0,00 |
97,60±3,04 |
0,002* |
|
Через 6 месяцев Postoperative 6 month |
100,00±0,00 |
97,60±3,04 |
0,009* |
|
Общее состояние здоровья (GH) General health (GH) |
|||
|
До операции Pre-operation |
44,64±22,52 |
44,20±23,13 |
0,962 |
|
Перед выпиской Pre-charge |
44,91±28,77 |
38,07±21,88 |
0,497 |
|
Через 3 месяца Postoperative 3 month |
72,09±4,16 |
74,40±10,70 |
0,456 |
|
Через 6 месяцев Postoperative 6 month |
79,36±13,33 |
74,27±11,48 |
0,306 |
|
Жизнеспособность (VT) Vitality (VT) |
|||
|
До операции Pre-operation |
47,27±19,15 |
44,00±17,13 |
0,651 |
|
Перед выпиской Pre-charge |
59,09±24,48 |
53,00±12,51 |
0,462 |
|
Через 3 месяца Postoperative 3 month |
79,55±8,50 |
75,00±7,79 |
0,170 |
|
Через 6 месяцев Postoperative 6 month |
90,00±0,00 |
83,67±7,43 |
0,005* |
|
Социальное функционирование (SF) Social function (SF) |
|||
|
До операции Pre-operation |
63,64±30,34 |
54,17±25,30 |
0,394 |
|
Перед выпиской Pre-charge |
61,41±35,58 |
54,17±20,41 |
0,554 |
|
Через 3 месяца Postoperative 3 month |
75,00±0,00 |
77,50±10,77 |
0,384 |
|
Через 6 месяцев Postoperative 6 month |
100,00±0,00 |
95,00±6,34 |
0,009* |
|
Эмоциональное состояние (ES) Emotional State (ES) |
|||
|
До операции Pre-operation |
33,33±44,72 |
31,11±44,48 |
0,901 |
|
Перед выпиской Pre-charge |
45,45±45,40 |
31,11±44,48 |
0,429 |
|
Через 3 месяца Postoperative 3 month |
100,00±0,00 |
77,78±27,22 |
0,007* |
|
Через 6 месяцев Postoperative 6 month |
100.00±0.00 |
91.11±15.26 |
0.041* |
|
Психическое здоровье (MH) Mental health (MH) |
|
До операции Pre-operation |
65,27±21,87 |
63,60±20,67 |
0,844 |
|
Перед выпиской Pre-charge |
52,36±23,56 |
51,47±21,64 |
0,921 |
|
Через 3 месяца Postoperative 3 month |
81,09±8,02 |
75,73±7,78 |
0,100 |
|
Через 6 месяцев Postoperative 6 month |
95,64±1,21 |
90,40±5,62 |
0,003* |
Послеоперационная депрессия
В предоперационном периоде не было значительной разницы в уровне депрессии между двумя группами. Однако пациенты в группе NOSES перед выпиской (p=0,037) и через шесть месяцев после операции (p=0,003) имели значительно более низкий уровень депрессии, чем пациенты в группе CL. Кроме того, пациенты в обеих группах достигли уровня выраженной депрессии в предоперационном периоде. Перед выпиской из стационара пациенты в группе NOSES были менее подавлены, у них отмечался меньший уровень депрессии, в то время как пациенты в группе CL оставались в депрессии. Через три и шесть месяцев после операции у пациентов обеих групп наблюдалась ремиссия депрессии по мере лечения заболевания и восстановления в послеоперационном периоде. Полученные результаты позволяют предположить, что методика NOSES может значительно снизить уровень депрессии у пациентов в краткосрочной перспективе, что в большей степени способствует их выздоровлению (табл. 4).
Таблица 4
Показатели уровня депрессии (BDI)
The results of depression level (BDI)
Table 4
|
NOSES (15) |
CL (15) |
P |
|
|
До операции Preoperation |
32,00±23,44 |
34,20±23,53 |
0,816 |
|
Перед выпиской predischarge |
15,18±13,00 |
25,80±11,40 |
0,037* |
|
Через 3 месяца postoperative 3 months |
5,09±7,06 |
7,07±5,73 |
0,438 |
|
Через 6 месяцев postoperative 6 months |
0,00±0,00 |
5,33±5,89 |
0,003* |
Послеоперационная тревожность
Пациенты в группе NOSES имели значительно более низкий уровень SA (состояние тревоги), чем пациенты в группе
CL перед выпиской (P=0,016). Пациенты в группе NOSES имели значительно более низкий уровень TA (личностная тревожность), чем пациенты в группе CL через шесть месяцев после операции (P=0,015). Кроме того, мы обнаружили, что пациенты в группе CL имели более высокие показатели по TA и SA, чем пациенты в группе NOSES, после лечения заболевания тревожность снизилась в обеих группах. Эти результаты показывают, что пациенты в группе NOSES имели значительно меньшую предоперационную тревожность, что способствовало скорейшему восстановлению после операции (табл. 5).
Таблица 5
Показатели уровня тревожности (STAI)
The results of anxiety level (STAI)
Table 5
|
NOSES (15) |
CL (15) |
P |
|
|
Состояние тревоги (SA) State anxiety (SA) |
|||
|
До операции Pre-operation |
51,91±10,27 |
54,47±6,55 |
0,479 |
|
Перед выпиской Pre-discharge |
40,64±12,28 |
51,80±9,81 |
0,016* |
|
Через 3 месяца Postoperative 3 months |
38,91±10,45 |
41,60±6,97 |
0,469 |
|
Через 6 месяцев Postoperative 6 months |
41,64±9,10 |
45,53±5,14 |
0,221 |
|
Личностная тревожность (TA) Trait anxiety (TA) |
|||
|
До операции Pre-operation |
44,64±10,17 |
47,47±9,61 |
0,476 |
|
Перед выпиской Pre-discharge |
45,55±10,47 |
49,27±7,16 |
0,324 |
|
Через 3 месяца Postoperative 3 months |
44,09±3,99 |
42,00±3,84 |
0,343 |
|
Через 6 месяцев Postoperative 6 months |
41,18±4,40 |
45,47±3,89 |
0,015* |
Обсуждение
Операция играет важную роль в лечении КРР, и многие пациенты, пережившие КРР, отмечают долгосрочные физические и психосоциальные негативные последствия заболевания, причем боль, тревога и депрессия являются особенно изнурительными долгосрочными симптомами [8]. Широко признано, что методика NOSES уменьшает боль пациента благодаря отсутствию разрезов на поверхности тела [9, 10]. Несколько исследований подтвердили, что уровень тревоги и депрессии может серьезно повлиять на уровень послеоперационного воспаления, а высокий уровень воспаления может сократить время жизни, увеличить риск рецидива и сопутствующих заболеваний [11]. Однако существует пробел в исследовании психологического статуса пациентов с КРР после экстракции препаратов через естественные отверстия. В нашем исследовании психологическая оценка с помощью опросников BDI и STAI показала значительно более низкий уровень депрессии и тревоги в группе NOSES. Это подчеркивает психологические преимущества NOSES, поскольку пациенты, как правило, испытывают меньше стресса во время восстановления. Более быстрое возвращение к привычному образу жизни и меньшая физическая травматичность NOSES, вероятно, являются причиной этих положительных психологических эффектов.
Кроме того, наше исследование продемонстрировало, что NOSES обеспечивает существенные преимущества по нескольким параметрам КЖ, сохраняя при этом онкологическую безопасность и повышая скорость восстановления, что согласуется с данными Zhu et al. [12]. Особенно значительны преимущества в отношении ролевого функционирования, физической боли и эмоционального состояния. В связи с отсутствием разреза на животе, пациент не только не испытывает сильной боли, но и не испытывает беспокойства по поводу внешнего вида, обусловленного разрезом. Исследование [6] подтвердило, что пациенты с более плохим внешним видом послеоперационных рубцов связаны с более высоким уровнем тревоги и депрессии. Помимо внешнего вида, уменьшение боли может помочь пациенту как можно быстрее встать с постели, а ранняя послеоперационная активность может еще больше снизить тревожность пациента и привести к более быстрому восстановлению. Это говорит о том, что NOSES менее инвазивна и способствует более быстрому восстановлению и снижению послеоперационного дискомфорта, что в конечном итоге улучшает общее состояние здоровья и самочувствие, и способствует более быстрому выздоровлению пациента. Экономические последствия этих результатов весьма значительны. Сокращение сроков пребывания в стационаре и ускорение восстановления, связанные с применением NOSES, могут привести к экономии средств как для пациентов, так и для системы здравоохранения. Экономическая эффективность NOSES в сочетании с ее клиническими преимуществами делает ее привлекательной альтернативой методам CL, но не может ее полностью заменить ввиду конкретных показаний к применению.
Интересно также отметить, что частота несостоятельности анастомозов у пациентов в группе NOSES была ниже, чем в группе CL (1 vs 5). Хорошо известно, что несостоятельность анастомоза является очень серьезным, жизнеугрожающим осложнением после низкой передней резекции прямой кишки [13]. Мы преимущественно использовали модифицированный метод NOSES 1F, заключающийся в вытягивании с выворачиванием прямой кишки из тела через анус специальным металлическим стержнем, рассечении кишки и формировании ручного анастомоза экстракорпорально, что может быть причиной снижения частоты несостоятельности анастомозов. Все эти результаты позволяют предположить, что методика NOSES не только снижает частоту тревоги и депрессии у пациентов в послеоперационном периоде, но и в определенной степени уменьшает частоту послеоперационных осложнений у пациентов.
Учитывая наблюдаемое улучшение качества жизни, психологического состояния и сроков восстановления, NOSES имеет потенциал стать предпочтительным методом хирургического лечения КРР с небольшими образованиями. Однако наше исследование имеет ряд ограничений: во-первых, оно не является обобщающим, поскольку проводилось только в 2-х центрах. Во-вторых, комплаентность пациентов определяла количество наблюдений, включенных в исследование. Поэтому для подтверждения полученных результатов необходимы будущие крупные международные многоцентровые рандомизированные контролируемые исследования.
Заключение
Данное исследование предоставляет убедительные доказательства того, что NOSES предлагает значительные преимущества послеоперационного качества жизни, психологического благополучия, при сопоставимых хирургических результатах классической лапароскопической операции с выполнением мини-лапаротомии. Также необходимы долгосрочные исследования для подтверждения устойчивости улучшения КЖ, наблюдаемых в данном исследовании.


