Сравнительная оценка сорбционных материалов для удаления трихотеценов
Автор: Мишина Н.Н., Семенов Э.И., Алеев Д.В., Ерохондина М.А., Валиев А.Р.
Статья в выпуске: 2 т.254, 2023 года.
Бесплатный доступ
Трихотеценовые микотоксины (фумонизин В1 и дезоксиниваленол) это соединения семейства сесквитерпеноидов, продуцируемые грибами рода Fusarium proliferatum и Fusarium verticillioides. Данные микотоксины играют ключевую роль в различных патологических воздействиях на клеточные системы организма и весь организм в целом. Наиболее удобным и эффективным способом нейтрализации их воздействия на организм является использование различных сорбентов. Целью наших исследований было проведение сравнительной оценки различных сорбционных материалов для удаления трихотеценовых микотоксинов в условиях in-vitro . Нами исследовалась способность дрожжевых и растительных β-глюканов, лигнина (сорбентов растительного происхождения), цеолита, шунгита (минеральных сорбентов) связывать трихотеценовые микотоксины фумонизин В1 и дезоксиниваленол. Адсорбцию этих веществ оценивали по методике, имитирующей условия желудочно-кишечного тракта. В результате эксперимента было установлено, что лидерами сорбции к дезоксиниваленолу, являются дрожжевой β-глюкан (щелочной гидролиз) сорбировавший - 94,6 % микотоксина, растительный β-глюкан - 91,5 % и шунгит - 78,4 %. К микотоксину фумонизину В1, наилучшую сорбцию показал шунгит - 98,0 %, цеолит - 77,0 % и лигнин - 64,8 %. Остальные сорбенты проявили себя в меньшей степени. В целом сорбенты растительного происхождения лучше сорбировали дезоксиниваленол, а природные сорбенты показали лучшую сорбционную способность к фумонизину В1.
Дезоксиниваленол, фумонизин в1, in vitro, адсорбция, десорбция, β-глюканы, цеолит, шунгит, лигнины
Короткий адрес: https://sciup.org/142238107
IDR: 142238107 | УДК: 619:615.9:636.5 | DOI: 10.31588/2413_4201_1883_2_254_174
Comparative evaluation of sorption materials for the removal of trichotecens
Trichothecene mycotoxins (fumonisin B1 and deoxynivalenol) are compounds of the sesquiterpenoid family produced by fungi of the genus Fusarium proliferatum and Fusarium verticillioides. These mycotoxins play a key role in various pathological effects on the cellular systems of the body and the whole organism. The most convenient and effective way to neutralize their effects on the body is to use various sorbents. The aim of our research was to conduct a comparative evaluation of various sorption materials for the removal of trichothecene mycotoxins under in vitro conditions. We have studied the ability of yeast and vegetable β-glucans, lignin (sorbents of plant origin), zeolite, shungite (mineral sorbents) to bind trichothecene mycotoxins fumonisin B1 and deoxynivalenol. The adsorption of these substances was assessed by a method that simulates the conditions of the gastrointestinal tract. As a result of the experiment, it was found that the leaders of sorption to deoxynivalenol are yeast β-glucan (alkaline hydrolysis) sorbing - 94.6 % of mycotoxin, vegetable β-glucan - 91.5 % and shungite - 78.4 %. To mycotoxin fumonisin B1, shungite showed the best sorption - 98.0 %, zeolite - 77.0 % and lignin - 64.8 %. Other sorbents showed themselves to a lesser extent. In general, sorbents of plant origin sorbed deoxynivalenol better, and natural sorbents showed better sorption capacity for fumonisin B1.
Текст научной статьи Сравнительная оценка сорбционных материалов для удаления трихотеценов
Трихотеценовые микотоксины – органические соединения семейства сесквитерпеноидов, они содержат в своей структуре 12,13-эпоксидное кольцо, которое способствует их биологической и токсической активности. К трихотеценам относится целый ряд близкородственных соединений, из которых наибольший интерес представляют фумонизин В1 и дезоксиниваленол [11].
Микотоксин фумонизин В1 (FUM, IUPAC name: 2-[2-({19-amino-6-[(3,4-dicarboxybutanoyl) oxy ] – 11, 16, 18-trihydroxy - 5,9 - dimethylicosan - 7- yl}oxy) -2-oxo ethyl]butanedioic аcid) является канцерогенным метаболитом грибов рода Fusarium proliferatum и Fusarium verticillioides [10] , имеет длинную цепочечную углеводородную единицу (аналогичную сфингозину и сфинганину), играющую главную роль в цитотоксическом, иммунодепрессивном, эстрогенном, нейротоксическом, мутагенном и канцерогенном действиях на живой организм [13]. Дезоксиниваленол (DON, IUPAC name: 3,7,15-Trihydroxy-12,13-epoxytricho thec-9-en-8-one ) относится к трихотеценовым микотоксинам типа B, и является наиболее часто обнаруживаемым микотоксином данной группы. В острых, умеренных или низких дозах также вызывает токсическое и иммунотоксическое действие в различных клеточных системах организма [14].
Эффективным и наиболее удобным способом нейтрализации микотоксинов в настоящий момент является использование в качестве терапии соединений с сорбционными свойствами. Для защиты от интоксикации и предотвращения микотоксикозов животных, предложен целый ряд сорбентов различного происхождения. Из-за химических особенностей трихотеценовых микотоксинов в настоящее время нет данных по одновременному исследованию фумонизина В1 и дезоксиниваленола по отношению к сорбционным материалам органического и неорганического происхождения, поэтому актуальность поиска новых сорбентов и их комбинаций остается открытой.
С этой целью нами поставлена задача провести сравнительную оценку различных сорбционных материалов для удаления трихотеценовых микотоксинов в условиях in-vitro .
Материал и методы исследований. Работа выполнена на базе лаборатории микотоксинов отделения токсикологии ФГБНУ «Федеральный центр токсикологической, радиационной и биологической безопасности» (г. Казань). Объектом исследования являлась способность сорбционных материалов связывать трихотеценовые микотоксины: дезоксиниваленол и фумонизин В1 in vitro. В качестве сорбционных материалов
(адсорбентов) использовались: β-глюканы растительного происхождения, Шатрашанского Республики
и дрожжевого цеолит Татарско- месторождения
Татарстан, шунгит
Зажогинского месторождения (Карельский шунгитовый завод, Россия) и лигнин [1, 4, 5, 8, 9, 15]. Дрожжевые β-глюканы получены из хлебопекарных прессованных дрожжей S. cerevisiae. Образцы растительных β-глюканов представлены в виде концентратов, выработанных из овсяных отрубей методом, описанным Гематдиновой В.М. (2018) [1, 3, 6, 12]. В работе использовали 98 % стандарты дезоксиниваленола и фумонизина В1 производства Sigma Aldrich (США), которые растворяли в метаноле с получением исходного раствора (1 мкг/мкл). Адсорбционную способность трихотеценовых микотоксинов оценивали по двухфазной методике, описанной ранее Крюковым В.С. с соавт. (1992) [7]. Измерения проводили в трех повторностях. Содержание микотоксинов определяли методом конкурентного иммуноферментного анализа с помощью тест-систем «Ridascreen» (R-Biopharm, Германия). Модели эксперимента представлены в таблице 1.
Таблица 1 – Схема эксперимента
|
Номер модели |
Название модели in vitro |
|
1 |
Дрожжевой β-глюкан (солевой гидролиз) + дезоксиниваленол |
|
Дрожжевой β-глюкан (солевой гидролиз) + фумонизин В1 |
|
|
2 |
Дрожжевой β-глюкан (щелочной гидролиз) + дезоксиниваленол |
|
Дрожжевой β-глюкан (щелочной гидролиз) + фумонизин В1 |
|
|
3 |
Растительный β-глюкан + дезоксиниваленол |
|
Растительный β-глюкан + фумонизин В1 |
|
|
4 |
Цеолит + дезоксиниваленол |
|
Цеолит + фумонизин В1 |
|
|
5 |
Шунгит + дезоксиниваленол |
|
Шунгит + фумонизин В1 |
|
|
6 |
Лигнин + дезоксиниваленол |
|
Лигнин + фумонизин В1 |
Полученные экспериментальные данные обрабатывали общепринятым методом вариационной статистики с применением критерия достоверности по Стьюденту с использованием специальных программ.
Результат исследований.
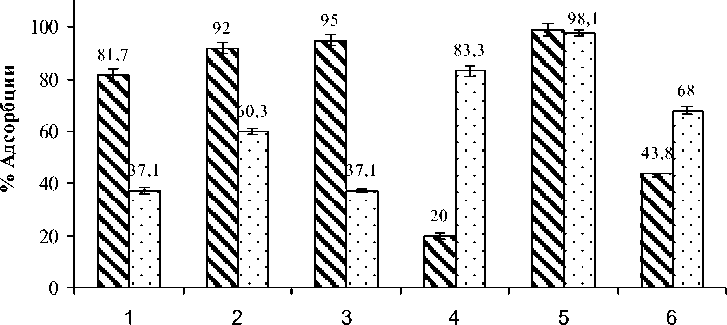
Результаты сравнительной адсорбционной способности группы сорбентов к дезоксиниваленолу и фумонизину В1 в кислой среде (рН=2) при температуре 37 °С (имитация условий желудка) представлены на рисунке 1.
По данным рисунка 1 видно, что в кислой среде (условия желудка) в пятой группе выявлена достаточно высокая сорбция дезоксиниваленола шунгитом и этот показатель составил (99,2±2,5) %. Использование остальных сорбентов показало более низкие результаты. Так, у образцов под номерами 6, 4, 3, 2, 1 адсорбция дезоксиниваленола была ниже на 55,4; 79,2; 4,2; 7,2; 17,5 %, соответственно. Адсорбция фумонизина В1 в этих же условиях выражена сильнее у образцов, имеющих в своем составе силикаты - цеолит (83,3±2,1) % и шунгит (98,1±1,2) %. У остальных образцов установлена адсорбционная способность в следующей последовательности: первой и третьей группах – 37,1 %, во второй группе – 60,3 %, и в шестой группе – 68,0 %.
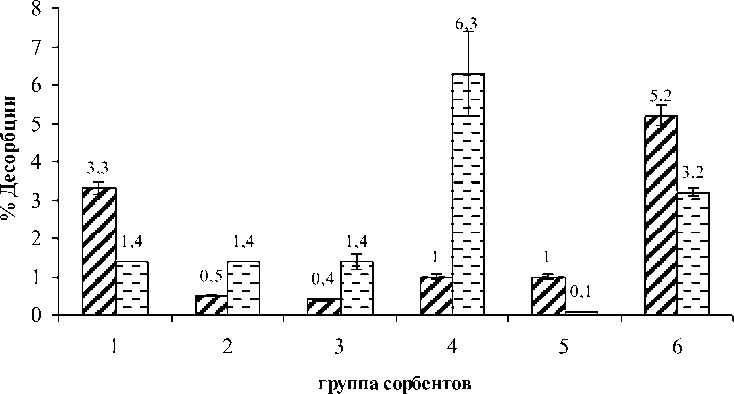
Результаты постановки эксперимента по определению процента десорбции группы сорбентов к дезоксиниваленолу и фумонизину В1 в щелочной среде при рН=8 и температуре 37 °С (условия кишечного тракта) представлены на рисунке 2.
99,2
□ Дезоксиниваленол
□ Фумонизин В1
группа сорбентов
Рисунок 1 – Процент
адсорбции энтеросорбентов
в отношении дезоксиниваленола и
фумонизина В1
и Дезоксиниваленол
□ Фумонизин В1
Рисунок 2 – Процент десорбции энтеросорбентов в отношении дезоксиниваленола и фумонизина В1
Таблица 2 – Истинная сорбция in vitro к трихотеценовым микотоксинам (n=3)
|
Номер модели |
Наименование сорбентов |
Дезоксини-валенол |
Фумонизин В1 |
|
1 |
Дрожжевые β-глюканы (солевой гидролиз) |
78,4±1,2 |
35,7±1,8 |
|
2 |
Растительные β-глюканы |
91,5±2,6 |
58,9±1,6 |
|
3 |
Дрожжевые β-глюканы (щелочной гидролиз) |
94,6±1,1 |
35,7±0,4 |
|
4 |
Цеолит |
19,0±0,9 |
77,0±1,4 |
|
5 |
Шунгит |
98,2±2,1 |
98,0±2,1 |
|
6 |
Лигнин |
38,6±0,8 |
64,8±2,4 |
Результаты исследования процента десорбции показали (рисунок 2), что максимальную десорбцию дезоксиниваленола продемонстрировал лигнин (5,2±0,3) %, чуть ниже β-глюканы
(дрожжевые, солевой гидролиз) – (3,3±0,2) %, у остальных варьировала от 0,4 % до 1 %. Наибольшее количество фумонизина В1 при переходе в условия pH кишечника утратил цеолит – 6,3 %, меньше лигнин 3,2 %, β-глюканы – 1,4 % и шунгит – 0,1 %.
Показатели истинной сорбционной емкости исследуемых групп сорбентов к дезоксиниваленолу и фумонизину В1 представлены в таблице 2.
Из таблицы 2 видно, что способность образцов к элиминации дезоксиниваленола была самой высокой у пятой группы «шунгит» – (98,2±2,1) %, также в первой, второй и третьей группах «β-глюканы различного происхождения» от (94,6±1,1) % до (78,4±1,2) %. Самой низкой была сорбционная способность к дезоксиниваленолу у лигнина (38,6±0,8) % и цеолита (19,0±0,9) %. Количество прочно сорбированного фумонизина В1 установлено в следующей последовательности, у сорбентов первой и третьей группы по 35,7 %, во второй, четвертой, пятой и шестой группах – (58,9±1,6) %, (77,0±1,4) %, (98,0±2,1) %, (64,8±2,4) %, соответственно. По результатам подсчета истинной сорбционной емкости к микотоксинам дезоксиниваленолу и фумонизину В1 с наилучшими показателями лидируют вторая (растительный β-глюкан) и пятая (шунгит) модели.
Заключение. Учитывая числовые значения показателей сорбции к трихотеценовому микотоксину дезоксиниваленолу, лидерами являются дрожжевой β-глюкан (щелочной гидролиз) сорбировавший – 94,6 % микотоксина, растительный β-глюкан – 91,5 % и шунгит – 78,4 %. К микотоксину фумонизину В1 наилучшую сорбцию показал шунгит – 98,0 %, цеолит – 77,0 % и лигнин – 64,8 %. Остальные сорбенты проявили себя в меньшей степени. В целом сорбенты растительного происхождения лучше сорбировали дезоксиниваленол, а природные сорбенты показали лучшую сорбционную способность к фумонизину В1.
Резюме
Трихотеценовые микотоксины (фумонизин В1 и дезоксиниваленол) это соединения семейства сесквитерпеноидов, продуцируемые грибами рода Fusarium proliferatum и Fusarium verticillioides. Данные микотоксины играют ключевую роль в различных патологических воздействиях на клеточные системы организма и весь организм в целом. Наиболее удобным и эффективным способом нейтрализации их воздействия на организм является использование различных сорбентов. Целью наших исследований было проведение сравнительной оценки различных сорбционных материалов для удаления трихотеценовых микотоксинов в условиях in-vitro . Нами исследовалась способность дрожжевых и растительных β-глюканов, лигнина (сорбентов растительного происхождения), цеолита, шунгита (минеральных сорбентов) связывать трихотеценовые микотоксины фумонизин В1 и дезоксиниваленол. Адсорбцию этих веществ оценивали по методике, имитирующей условия желудочно-кишечного тракта. В результате эксперимента было установлено, что лидерами сорбции к дезоксиниваленолу, являются дрожжевой β-глюкан (щелочной гидролиз) сорбировавший – 94,6 % микотоксина, растительный β-глюкан – 91,5 % и шунгит – 78,4 %. К микотоксину фумонизину В1, наилучшую сорбцию показал шунгит – 98,0 %, цеолит – 77,0 % и лигнин – 64,8 %. Остальные сорбенты проявили себя в меньшей степени. В целом сорбенты растительного происхождения лучше сорбировали дезоксиниваленол, а природные сорбенты показали лучшую сорбционную способность к фумонизину В1.
Список литературы Сравнительная оценка сорбционных материалов для удаления трихотеценов
- Адсорбция микотоксинов техническими лигнинами / З. А. Канарская, А. В. Канарский, Ю. Г. Хабаров [и др.] // Химия растительного сырья. – 2011. – № 1. – С. 59-63.
- Гематдинова, В. М. Получение концентрата бета-глюкана из овсяных отрубей для функциональных продуктов питания / В. М. Гематдинова, З. А. Канарская, А. В. Канарский // Пищевая промышленность. – 2018. – № 3. – С. 19-22.
- Грачева, О. А. Продуктивность, качество мяса и яиц кур-несушек при скармливании «Янтовета» / О. А. Грачева, Л. Ф. Якупова // Ученые записки Казанской государственной академии ветеринарной медицины им. Н. Э. Баумана. – 2016. – Т. 226. – № 2. – С. 48-51.
- Изучение сорбционной активности биосорбентов по отношению к Т-2 токсину / А. Ш. Садыкова, Е. Ю. Тарасова, Л. Е. Матросова [и др.] // Ветеринарный врач. – 2021. – № 3. – С.45-52.
- Изучение сорбционной активности потенциальных средств профилактики микотоксинов в отношении афлатоксинов / Е. Ю. Тарасова, Э. И. Семенов. Л. Е. Матросова [и др.] // Ветеринарный врач. – 2020. – № 2. – С. 51-58.
- Камалиев, А. Р. Ветеринарно- санитарная оценка качества мяса кроликов после применения полисахаридного препарата «Гемив» / А. Р. Камалиев, Р. А. Асрутдинова, М. Г. Сагитова [и др.] // Ученые записки Казанской государственной академии ветеринарной медицины им. Н. Э. Баумана. – 2015. – Т. 223. – № 3. – С. 87-90.
- Мишина, Н. Н. Профилактическая эффективность лигнин- и полисахаридсодержащих энтеросорбентов при сочетанном Т-2 токсикозе: специальность 16.00.04 «Ветеринарная фармакология с токсикологией»: автореф. дис. … канд. биол. наук / Мишина Наиля Наримановна. – Казань, 2009. – 24 с.
- Обоснование введения в рацион животных комбинации сорбентов неорганической и органической природы при Т-2 токсикозе / Н. Н. Мишина, Э. И. Семенов, К. Х. Папуниди [и др.] // Ветеринарный врач. – 2019. – № 2. – С. 30-37.
- Перфилова, К. В. Обоснование компонентного состава комплексного средства «Цеапитокс» в отношении Т-2 токсина в опытах in vitro / К. В. Перфилова, Н. Н. Мишина, Э. И. Семенов // Ученые записки Казанской государственной академии ветеринарной медицины им. Н. Э. Баумана. – 2021. – Т. 247. – № 3. – С. 208–212.
- Потехина, Р. М. Грибы рода Aspergillus – возбудители болезней животных и птиц / Р. М. Потехина, Е. Ю. Тарасова, Л. Е. Матросова – Казань: Федеральный центр токсикологической, радиационной и биологической безопасности, 2020. – 21 с.
- Экспериментальный сочетанный микотоксикоз свиней на фоне инфекционной нагрузки / Э. И. Семенов, Л. Е. Матросова, С. А. Танасева [и др.] // Сельскохозяйственная биология. – 2022. – Т. 57. – № 2. – С. 371-383.
- Catalli, A. Chitin and β-glucan polysaccharides as immunomodulators of airway inflammation and atopic disease / A. Catalli, M. Kulka // Metabolic & Immune Drug Discovery. – 2010. – Vol. 4. – P. 175-189.
- Juan-Garcia, A. Cytotoxicity, genotoxicity and disturbance of cell cycle in HepG2 cells exposed to OTA and BEA: single and combined actions Toxins / A. Juan-Garcia, J. Tolosa, C Juan, M.J. Ruiz // Toxins. – 2019. – Vol. 11 (6). – Р. 341.
- Krysinska-Traczyk, E. Levels of fungi and mycotoxins in the samples of grain dust collected from five various cereal crops in eastern Poland / E. Krysinska-Traczyk, J. Perkowski, J. Dutkiewicz // Ann. Agric. Environ. Med. – 2007. – Nо 14 – P. 159-167.
- Liu, Q. Zheng Lignins: biosynthesis and biological functions in plants / Q. Liu, L. Luo, L. Zheng // Int. J. Mol. Sci. – 2018. – Nо 19. – P. 335.


