Сравнительная оценка возможности заселения клеточного материала в матриксы, изготовленные методами электроспиннинга и аэродинамического формирования в турбулентном газовом потоке
Автор: Афанасьев С.А., Муслимова Э.Ф., Нащекина Ю.А., Никонов П.О., Роговская Ю.В., Больбасов Е.Н., Твердохлебов С.И.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: В помощь практическому врачу
Статья в выпуске: 3 т.32, 2017 года.
Бесплатный доступ
Введение. Методы электроспиннинга и аэродинамического формирования (АЭРДФ) в газовом потоке позволяют изготавливать синтетические структуры, подобные межклеточным матриксам. Но важной является оценка пригодности таких структур для заселения клеточным материалом. Материал и методы. Рассмотрено 2 типа матрикса из полимолочной кислоты. Матрикс № 1 получен методом электро-спиннинга, матрикс № 2 - методом АЭРДФ. Структуру матриксов оценивали на электронном микроскопе. В матриксы методом динамического заселения вносили стромальные клетки костного мозга (СККМ) кролика с последующим (3 суток) культивированием матриксов в СО2-инкубаторе при 37 °С. Присутствие клеток в матриксах оценивали с помощью флуоресцентной микроскопии. Данные представляли как среднее ± стандартное отклонение. Результаты. Матрикс № 1 сформирован волокнами правильной цилиндрической формы (диаметр 1,5±0,7 мкм) без собственного рельефа. Средняя пористость составила 67±3%. В структуре матрикса № 2 имеются жгуты (диаметр 27,5±17,4 мкм), сформированные направленными волокнами (диаметр 0,44±0,14 мкм) с развитым рельефом поверхности. Средняя пористость составила 55±3% (р function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Нетканые материалы, электроспиннинг, аэродинамическое формирование, культура клеток
Короткий адрес: https://sciup.org/149125174
IDR: 149125174 | DOI: 10.29001/2073-8552-2017-32-3-71-76
Comparative assessment of the possibility of cellular material collection to matrixes obtained by methods of electrospinning and aerodynamic formation in a turbulent gas flow
Introduction. Methods of electrospinning and aerodynamic formation in the gas stream allow the fabrication of synthetic structures similar to intercellular matrices. But it is important to assess the suitability of such structures for colonization by cellular material. Materials and Methods. Porous matrices of polylactic acid are used. Matrix No. 1 was obtained by the method of electrospinning, matrix No. 2 - by the method of aerodynamic formation. The structure of the matrices was examined on an electron microscope. The matrices were dynamically populated with stromal cells from the rabbit’s bone marrow, then matrices were cultured for 3 days in a CO2 incubator at 37 °C. Cells were detected by fluorescence microscopy. Data were presented as mean ± standard deviation. Results. The matrices differed in structure. Matrix No. 1 was formed by fibers of regular cylindrical shape (diameter 1.5±0.7 μm) without its own relief. The average porosity was 67±3%. In the structure of matrix No.2 it was possible to single out a macrolevel represented by wisps (diameter 27.5±17.4 μm) formed by directed fibers (diameter 0.44±0.14 μm) with developed surface relief. The average porosity was 55±3% (p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Сравнительная оценка возможности заселения клеточного материала в матриксы, изготовленные методами электроспиннинга и аэродинамического формирования в турбулентном газовом потоке
Работы в области клеточных технологий тесным образом связывают в себе фундаментальные и прикладные аспекты. Именно это обстоятельство может обеспечить успех их практической реализации, в том числе в направлении регенеративной медицины [1]. Так, очевидно, что биомеханический подход к регенерации костной ткани, основанный на применении методик накостного и чре-скостного остеосинтеза, при многих патологиях достиг предела своих возможностей [2, 3]. Дальнейшее совершенствование возможно при использовании тканевой инженерии и факторов, способных индуцировать процесс регенерации ткани [4].
Одним из ключевых элементов, необходимых для успешной реализации стратегии тканевой инженерии, являются искусственно созданные тканевые эквиваленты (матриксы, scaffolds), в пределах которых тем или иным способом возможно наращивать объем ткани. Искусственные матриксы формируют субстрат и определяют форму и комплекс свойств восстанавливаемой ткани или органа. Волокнистые матриксы — наиболее перспективный тип для регенерации костной ткани, они изготовлены из композиционных материалов на основе биорезорбируемых полимеров и фосфатов кальция [5]. Такие матриксы обладают высокой эластичностью, достаточной механической прочностью, высокой открытой пористостью, что не только способствует протеканию процессов интеграции костной ткани с матриксом с образованием системы «кар-кас-костная ткань», но и обеспечивает возможность насыщения такого каркаса фармакологическими препаратами и клеточными материалами [6].
Среди многочисленных методов изготовления волокнистых композиционных матриксов [7] наибольшее внимание исследователей привлекают два способа их формирования — электроспиннинг [8] и АЭРДФ в турбулентном газовом потоке [9].
Следует отметить, что для приложений тканевой инженерии одним из определяющих свойств матрикса является его способность к заселению клетками. Таким образом, цель исследования: оценить пригодность матриксов, сформированных методами электроспиннинга и АЭРДФ, для заселения клеточным материалом.
Материал и методы
Для исследований использованы два типа пористых матриксов диаметром 20 мм и толщиной 150 мкм, изготовленных из композиционного материала на основе полимолочной кислоты PURASORB® PL 38 (Purac, Нидерланды) и мелкодисперсного гидроксиапатита (Ca10(PO4)6(OH)2) дисперсностью <40 мкм, полученного из биогенного сырья методом высокотемпературного отжига с последующей многократной промывкой и просеиванием (кафедра «Технологии силикатов и наноматериалов» ТПУ). Композитный материал готовили растворением полимолочной кислоты (4 масс. %) в хлороформе («Экрос», Россия) в герметичном реакторе при комнатной температуре и постоянном перемешивании. Далее в раствор добавляли дисперсию порошка гидроксиапатита в хлороформе таким образом, чтобы массовое содержание неорганической фазы по отношению к полимолочной кислоте составило 25 вес. %.
Матрикс № 1 получен методом электроспиннинга на установке NANON-NF 01 (Япония) при следующих параметрах: размер сборочного коллектора — длина 200 мм, диаметр — 100 мм, частота вращения — 50 об/мин, игла — 18 G, расход полимерного раствора — 3,5 мл/ч, расстояние от иглы до сборочного коллектора — 16 см, напряжение — 25 кВ. Матрикс № 2 получен методом АЭРДФ на установке собственной конструкции. Формирование структуры матрикса осуществлялось при следующем режиме: давление сжатого воздуха — 3,5 атм, расход раствора полимера — 30 мкл/мин, диаметр сопла для пода- чи полимерного раствора — 0,7 мм, диаметр сопла для подачи сжатого воздуха — 1 мм, расстояние от сопла до сборочного коллектора — 400 мм.
Исследование структуры матриксов проводили на электронном микроскопе ESEM Quanta 400 FEG (FEI, США), используя режим низкого вакуума в атмосфере паров воды. Изображения получали при следующих условиях: остаточное давление в камере — 60 Па, ускоряющее напряжение — 20 кВ, ток пучка — 3,5 мкА.
Матриксы заселяли клеточным материалом методом динамического заселения [10, 11]. С помощью перистальтического насоса через матриксы пропускали 15 мл суспензии, содержащей 0,6 x 10 5 кл/мл стромальных клеток костного мозга (СККМ) кролика. Заселенные клетками матриксы помещали в среду DMEM (Gibco, США), содержащую 1% HEPES буфера, 10% эмбриональной бычьей сыворотки, 1% L-глутамина, 100 ед/мл пенициллина, 0,1 мкг/мл стрептомицина, 0,1 мкг/мл амфотерицина В (Sigma Aldrich, США), и культивировали в течение 3 суток в СО2-инкубаторе при температуре 37 °С. Ранее было показано, что количество клеток вокруг матрикса, появляющихся в первые 3 суток культивирования, является объективным показателем эффективности посева клеточного материала [10].
Присутствие клеток в структуре матриксов оценивали с помощью флуоресцентной микроскопии. Для этого матриксы помещали в раствор ядерного красителя Dapi на 45 мин, затем промывали в буфере PBS, переносили на стекло и исследовали с помощью микроскопа Axio Imager M2 (Carl Zeiss, Германия) при следующих параметрах: Excition Wavelength, 353 Emission Wavelength 465, х400. В 2D-режиме количество клеток считали на площади 348,79 х 263,03 мкм. Изображения 3D были получены с помощью камеры Axocam503 mono и программного обеспечения ZEN 2 pro (функция Z-stek). Каждый объект был исследован на толщину 19,8 мкм (37 фотографий). Для определения количества клеток в 3D-режиме клетки тоже считали на площади 348,79 х 263,03 мкм, но в каждой из 37 фотографий. Подсчет клеток проводили в 10 случайных полях зрения.
Статистическую обработку результатов исследований проводили с использованием пакета программ STATISTICA (StatSoft, Dell). Для оценки нормальности распределения использовали критерий Колмогорова– Смирнова. Во всех случаях мы имели нормальное распределение и для оценки значимости различий выборок использовали t-критерий Стьюдента. Критический уровень значимости p принимался равным 0,05. Данные представляли как среднее ± стандартное отклонение.
Результаты
Согласно данным микроскопического исследования, матриксы существенно отличались друг от друга по своей структуре. Матрикс № 1 был сформирован отдельными волокнами правильной цилиндрической формы средним диаметром 1,5±0,7 мкм, хаотически перепутанными между собой. На поверхности волокон отсутствовал собственный рельеф (рис. 1а). При значительном увеличении (рис. 1б) в структуре обнаруживались единичные включения частиц гидроксиапатита средним диаметром 1,8±0,6 мкм. Средняя пористость сформированного матрикса составила 67±3%.

Рис. 1а Рис. 1б
Рис. 1. Структура матрикса, сформированного методом электроспиннинга
Примечание: а — увеличение 500x; б — увеличение 5000x.

Матрикс № 2 отличался более сложной пространственной организацией. В ней можно выделить макроуровень, который представлен жгутами средним диаметром 27,5±17,4 мкм (рис. 2а). Эти жгуты в свою очередь сформированы направленными волокнами (рис. 2б). Диаметр волокон составлял в среднем 0,44±0,14 мкм, что значимо (р<0,05) меньше, чем в матриксе, полученном методом электроспиннинга. Еще одной особенностью этих волокон являлось то, что у них присутствовал развитый рельеф поверхности. Средняя пористость матрикса № 2 была значимо (р<0,05) меньше, чем матрикса № 1 и составила 55±3%. В структуре матрикса № 2 присутствовали и частицы гидроксиапатита, они были распределены более равномерно с отсутствием значи- тельных скоплений. Значительное количество частиц гидроксиапатита расположено между волокнами. Однако присутствуют частицы, которые, как и в матриксе № 1, заключены в структуру волокна. Площадь свободной поверхности матрикса № 2 превышала площадь свободной поверхности матрикса № 1 не менее чем в 8 раз.

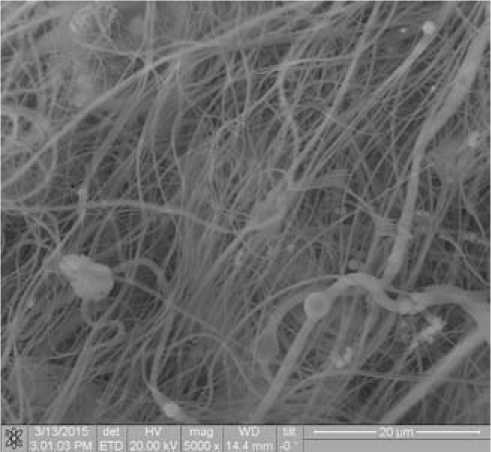
Рис. 2б
Рис. 2а
Рис. 2. Структура матрикса, сформированного методом АЭРДФ Примечание: а — увеличение 300x; б — увеличение 5000x.
Далее была проведена оценка пригодности матриксов для заселения клеточным материалом. Оказалось, что рассматриваемые матриксы статистически значимо (р<0,05) различались по среднему количеству выявленных клеток. Так, для матрикса № 1 это значение составило 56±9 клеток против 81±6 клеток для матрикса № 2
в 2D-режиме. В 3D-режиме различие между матриксами было еще более явным (рис. 3). В матриксе № 1 среднее число выявляемых клеток составляло 120±40, тогда как в матриксе № 2 этот показатель был уже почти в 2 раза выше и составлял 215±18 клеток.
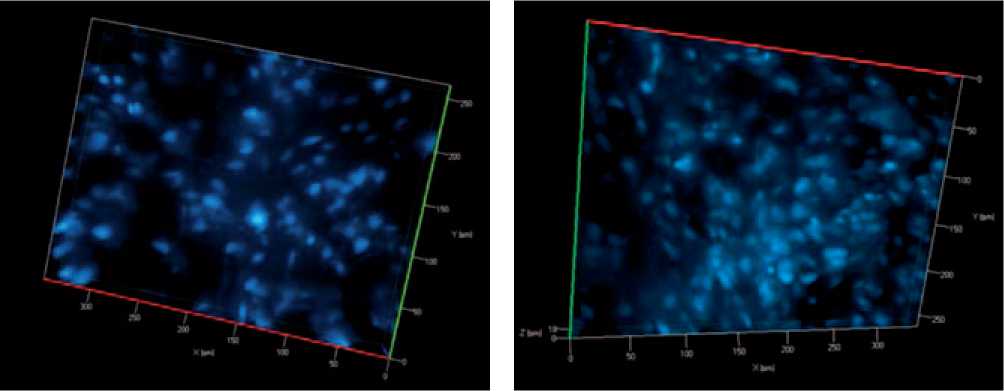
Рис. 3б
Рис. 3а
Рис. 3. Типичный вид 3D-изображения клеток, заселенных в матриксы на основе полимолочной кислоты (ядерный краситель Dapi, увеличение 400х)
Примечание: а — матрикс, сформированный методом электроспиннинга; б — матрикс, сформированный методом АРДФ.
Обсуждение
Проведена сравнительная оценка структуры матриксов, полученных методом электроспиннинга и методом АЭРДФ. Сформированные нетканые материалы существенно отличались по своей структуре. Так, матрикс № 2, полученный методом АЭРДФ, отличался более сложной пространственной организацией, меньшим средним диаметром волокон и большей площадью свободной поверхности, чем матрикс № 1, сформированный методом электроспиннинга.
Обнаруженные различия в морфологии рассматриваемых матриксов можно объяснить особенностями процесса формирования волокон, из которых они образованы. Действительно, в случае электроспиннинга происходит расщепление струи прядильного раствора на некотором расстоянии от сопла из-за высокой концентрации одноименных электрических зарядов. Процесс расщепления струи прядильного раствора носит многократный характер и продолжается до тех пор, пока капиллярное давление на поверхности дочерних струй прядильного раствора не скомпенсирует электрические силы или струя при испарении растворителя не превратится в твердое волокно [12, 13]. При использовании метода АЭРДФ струя прядильного раствора ускоряется и растягивается высокоскоростным газовым потоком. В зоне газового потока, отличающегося высокой турбулентностью, происходит изгиб и запутывание струи, что увеличивает вероятность перепутывания соседних струй [14, 15]. Это приводит к образованию волокон сложной пространственной организации. В дополнение к этому струя прядильного раствора подвергается растягивающим воздействиям со стороны потока твердых частиц, которые способны покидать струю за счет кинетической энергии и вытягивать за собой прядильный раствор, становясь центрами создания дочерних струй. Наличие такого механизма в свою очередь является мощным фактором уменьшения диаметра формируемых волокон.
Далее была проведена оценка возможности заселения матриксов СККМ. Надо отметить, что в работе был использован динамический способ заселения клеток. Данный метод обеспечивает распределение клеток по всему объему матрикса в отличие от статического способа заселения, при котором суспензию клеток наносят на поверхность материала [10, 11].
Полученные результаты свидетельствуют о том, что СККМ успешно фиксировались в объеме рассматриваемых матриксов. Этот факт является подтверждением того, что оба типа матриксов биосовместимы. Однако мы обнаружили, что матрикс, полученный методом АЭРДФ, в равных условиях способен адгезировать значимо большее количество СККМ. Такой результат, по всей видимости, обусловлен более высоким значением площади свободной поверхности. Кроме того, известно, что поверхности с большей шероховатостью являются предпочтительными для адгезии клеток [16], можно предположить, что развитая поверхность волокон, сформированных методом АЭРДФ, стимулирует прикрепление клеток. Также на более эффективное заселение клеток в матрикс № 2 могло повлиять наличие в его структуре свободных частиц фосфатов кальция, так как насыщение жидкости вокруг частиц и порового пространства матрикса биологически активными ионами кальция и фосфора оказывает синергетический эффект и усиливает адгезию.
Таким образом, в отличие от метода электроспиннинга метод АЭРДФ в газовом потоке позволяет получать матриксы с более оптимальной пространственной организацией, что обеспечивает их лучшее заселение клеточным материалом.
Финансирование: исследование поддержано Российским научным фондом (проект № 16-13-10239).
Список литературы Сравнительная оценка возможности заселения клеточного материала в матриксы, изготовленные методами электроспиннинга и аэродинамического формирования в турбулентном газовом потоке
- Попов С.В., Рябов В.В., Суслова Т.Е. и соавт. Фундаментальные и прикладные аспекты клеточных технологий в кардиологии и кардиохирургии // Бюллетень СО РАМН. - 2008. - Т. 28(4). - С. 5-15.
- Aranovich A., Popkov A., Barbier D., Popkov D. Femoral lengthening by combined technique in melorheostosis: a case report // Eur. Orthop. Traumatol. - 2014. - Vol. 5. - P. 175-179- DOI: 10.1007/s12570-013-0220-4
- Popkov D., Journeau P., Popkov A. et al. Ollier's disease limb lenghtening: Should intramedullary nailing be combined with circular external fixation? // Orthop. Traumatol. Surg. Res. - 2010. - Vol. 96. - P. 348-353- DOI: 10.1016/j.otsr.2010.01.002
- Petite H., Viateau V., Bensaïd W. et al. Tissue-engineered bone regeneration // Nat. Biotechnol. - 2000. - Vol. 18. - P. 959-963- DOI: 10.1038/79449
- Boccaccini A.R., Blaker J.J. Bioactive composite materials for tissue engineering scaffolds // Expert Rev. Med. Devices. - 2005. - No. 2. - P. 2303-2317- DOI: 10.1586/17434440.2.3.303
- Santoro M., Shah S.R., Walker J.L., Mikos A.G. Poly(lactic acid) nanofibrous scaffolds for tissue engineering // Adv. Drug Deliv. Rev. - 2016. - Vol. 107. - P. 206-212-
- DOI: 10.1016/j.addr.2016.04.019
- Tamayol A., Akbari M., Annabi N. et al. Fiber-based tissue engineering: Progress, challenges, and opportunities // Biotechnol. Adv. - 2013. - Vol. 31. - P. 669-687-
- DOI: 10.1016/j.biotechadv.2012.11.007
- Jiang T., Carbone E.J., Lo K.W.-H., Laurencin C.T. Electrospinning of Polymer Nanofibers for Tissue Regeneration // Prog. Polym. Sci. - 2014. - Vol. 46. - P. 1-24-
- DOI: 10.1016/j.progpolymsci.2014.12.001
- Daristotle J.L., Behrens A.M., Sandler A.D., Kofinas P. A Review of the Fundamental Principles and Applications of Solution Blow Spinning // ACS Appl. Mater. Interfaces. - 2016. - No. 8. - P. 34951-34963- 10.1021/ acsami.6b12994.
- DOI: 10.1021/acsami.6b12994
- Нащекина Ю.А., Никонов П.О., Михайлов В.М. и др. Зависимость заполнения стромальными клетками костного мозга трехмерной матрицы от способа посева клеток и типа модификации поверхности матрицы // Цитология. - 2014. - Т. 56(4). - С. 283-290.
- Nashchekina Y.A., Nikonov P.O., Mikhailov V.M. et al. Distribution of bone-marrow stromal cells in a 3D scaffold depending on the seeding method and the scaffold inside a surface modification // Cell tissue biol. - 2014. - Vol. 8(4). - P. 313-320.
- Filatov Y., Budyka A., Kirichenko V. Electrospinning of Micro- and Nanofibers: Fundamentals in Separation and Filtration Processes. - New York: Begell House Inc., 2007. - 404 p.
- Reneker D.H., Chun I. Nanometre diameter fibres of polymer, produced by electrospinning // Nanotechnology. - 1996. - Vol. 7(3). - P. 216-223.
- Daristotle J.L., Behrens A.M., Sandler A.D. et al. A Review of the Fundamental Principles and Applications of Solution Blow Spinning // ACS Appl. Mater. Interfaces. - 2016. - Vol. 8(51). - P. 34951-34963.
- Tomecka E., Wojasinski M., Jastrzebska E. et al. Poly(l-lactic acid) and polyurethane nanofibers fabricated by solution blow spinning as potential substrates for cardiac cell culture // Mater. Sci. Eng. C. - 2017. - Vol. 75. - P. 305-316.
- Faia-Torres A.B., Charnley M., Goren T. et al. Osteogenic differentiation of human mesenchymal stem cells in the absence of osteogenic supplements: A surface-roughness gradient study // Acta Biomater. - 2015. - Vol. 28. - P. 64-75.


