Сравнительное изучение реактогенности и антигенной активности коммерческих адъювантов в составе эмульсионной вакцины против хламидиоза животных
Автор: Заева Н.С., Евстифеев В.В., Яковлев С. И., Хусаинов Ф.М., Садыкова С.В.
Рубрика: Ветеринария
Статья в выпуске: 3 т.263, 2025 года.
Бесплатный доступ
В статье представлены результаты сравнительного изучения реактогенности и антигенной активности коммерческих адъювантов «БС-50», «БС-60», «БС-70», «CORALVAC RZ 506» и «CORALVAC RZ 528» и их сравнение с эталонным адъювантом «МЛА-70» в составе эмульсионной вакцины против хламидиоза животных. В качестве лабораторной модели для исследований использовались морские свинки. Оценка реактогенности вакцин проводилась ежедневно, в течение первых 10 суток после иммунизации. В ходе проведения клинических осмотров животных, фиксировались и учитывались: общая температура тела, общее состояние, потребность в корме и переносимость вакцин животными. Результаты сравнительного изучения реактогенности вакцин на основе различных адъювантов позволили установить отсутствие местных реакций у лабораторных животных на введение биопрепаратов. Серологические исследования проводили каждые 30 суток после вакцинации на протяжение пяти месяцев. Было установлено, что все исследуемые вакцины, изготовленные с применением различных адъювантов, вызывают выработку комплементсвязывающих хламидийных антител у лабораторных животных. Наиболее высокие показатели антигенной активности были выявлены в группах морских свинок, иммунизированных биопрепаратами, изготовленными на основе адъюванта «БС-60» и эталонного адъюванта «МЛА-70». Самые низкие результаты показали биопрепараты на основе адъювантов «CORALVAC RZ». Полученные результаты говорят о том, что адъювант «БС-60» оказался наиболее оптимальным из всех исследуемых препаратов, соответствующих требованиям надлежащей производственной практики. Поэтому в дальнейшем, доклинические и клинические испытания, рекомендуется проводить с использованием адъюванта «БС-60».
Вакцина, хламидиоз, адъювант, антигенная активность, реактогенность
Короткий адрес: https://sciup.org/142246287
IDR: 142246287 | УДК: 619:616.98:578 | DOI: 10.31588/2413_4201_1883_3_263_25
Comparative study of reactogenicity and antigenic activity of commercial adjuvants in emulsion vaccine against animal chlamydia in animal
The article presents the results of a comparative study of reactogenicity and antigen activity of commercial adjuvants BS-50, BS-60, BS-70, CORALVAC RZ 506 and CORALVAC RZ 528 and their comparison with the reference adjuvant MLA-70 in emulsion vaccine against chlamydia in animals. Guinea pigs were used as a laboratory model for the studies. The vaccine reactogenicity was assessed daily during the first 10 days after immunization. During clinical examinations of animals, the following were recorded and taken into account: general body temperature, general condition, appetite and vaccine tolerance of animals. The results of a comparative study of vaccines reactogenicity based on various adjuvants made it possible to establish the absence of local reactions in laboratory animals to the introduction of biopreparations. Serological studies were carried out every 30 days after vaccination for five months. It was found that all the studied vaccines manufactured using various adjuvants cause the production of complement-fixing chlamydial antibodies in laboratory animals. The highest rates of antigen activity were found in groups of guinea pigs immunized with biopreparations on the basis of BS-60 adjuvant and the reference adjuvant MLA-70. The lowest results were shown by biopreparations based on CORALVAC RZ adjuvants. The obtained results indicate that BS-60 adjuvant turned out to be the most optimal of all the studied drugs that meet the requirements of good manufacturing practice. Therefore, in the future, preclinical and clinical trials are recommended to be carried out using BS-60 adjuvant.
Текст научной статьи Сравнительное изучение реактогенности и антигенной активности коммерческих адъювантов в составе эмульсионной вакцины против хламидиоза животных
Несмотря на то, что хламидии чувствительны к ряду антибактериальных препаратов, таких как тетрациклины, макролиды и фторхинолоны, особенности их жизненного цикла существенно снижают эффективность применения антибиотиков для лечения инфицированных животных на фермах в условиях вспышки заболевания. Поэтому для эффективной профилактики хламидиоза сельскохозяйственных животных обязательно использование средств специфической профилактики [5, 6].
Тем не менее, несмотря на разнообразие существующих средств профилактики хламидиоза, их усовершенствование и создание новых вакцин является актуальной задачей [7].
Доказано, что для повышения иммуногенности обязательным при создании инактивированных вакцин является использование масляных адъювантов [8, 9, 10]. Однако, стандарты надлежащей производственной практики, ограничивают использование ряда веществ и субстанций, а также продуктов из них произведенных, без соблюдения требований GMP, что практически исключает возможность производства собственных адъювантов и предполагает замену их на готовые продукты, произведенные по стандартам GMP.
Положение осложняется тем, что почти все такие адъюванты являлись импортируемыми из-за рубежа продуктами и в настоящее время требуется их замещение на аналоги. Поэтому подбор новых адъювантов для создания и повышения качества вакцин на сегодняшний день является актуальной задачей.
Целью исследования явилось сравнительное изучение реактогенности и антигенной активности коммерческих адъювантов в составе эмульсионной вакцины против хламидиоза животных.
Условия, материалы и методы. Исследовательская работа проходила на базе лаборатории хламидийных инфекций ФГБНУ «ФЦТРБ-ВНИВИ».
Оценка реактогенности вакцин проводилась ежедневно, в течение первых 10 суток после иммунизации. В ходе проведения клинических осмотров животных фиксировались и учитывались: общее состояние, температура тела, аппетит животных, переносимость вакцин.
Антиген для создания экспериментальных вакцин был изготовлен из следующих штаммов: штамм Chlamydia psittaci «АМК-16», штамм Chlamydia psittaci «250» и штамм Chlamydia psittaci «РС-85».
Путем эмульгирования антигена с адъювантами при соответствующих режимах в лабораторных условиях было изготовлено шесть экспериментальных эмульсионных вакцинных препарата.
Адъюванты, для эмульгирования с антигеном, были взяты в различных пропорциях, соответственно их характеристикам:
-
- «БС-50» эмульгировали с антигеном в соотношении 50/50;
-
- «БС-60» эмульгировали с антигеном в
соотношении 60/40;
-
- «БС-70» эмульгировали с антигеном в
соотношении 70/30;
-
- «CORALVAC RZ 506» эмульгировали с антигеном в соотношении 60/40;
-
- «CORALVAC RZ 528» эмульгировали с антигеном в соотношении 70/30;
-
- «МЛА-70» эмульгировали с антигеном в соотношении 70/30.
Вакцины представляли собой обратную эмульсию типа «вода в масле».
Оценка антигенной активности вакцин проводилась в реакции связывания комплемента (РСК). Для этого 28 морских свинок разделили на семь групп по четыре животных в каждой: шесть экспериментальных групп и одна контрольная (контрольной группе не вводились препараты). Всех животных иммунизировали экспериментальными вакцинами внутримышечно в область внутренней поверхности бедра в дозе 0,5 см3.
Серологические исследования проводили в РСК на 30, 60 и 90, 120 и 150 сутки после иммунизации морских свинок.
Серологические исследования проводили с применением диагностической тест-системы: «Набор антигенов и сывороток для серологической диагностики хламидиозов сельскохозяйственных животных» (г. Казань). Технологические режимы постановки РСК соответствовали инструкции используемого диагностикума.
Результаты и обсуждение . В ходе проведения ежедневных клинических осмотров иммунизированных морских свинок никаких патологий у животных шести групп выявлено не было, животные были активны и не отказывались от корма. На протяжение двух недель, после введения вакцин, у некоторых иммунизированных животных наблюдали небольшие припухлости в месте введения биопрепаратов, которые полностью рассасывались к 12-15 суткам, что является допустимым для эмульсионных вакцин.
В таблице 1 представлены результаты постановки реакции связывания комплемента с сыворотками крови морских свинок, полученных на 30, 60, 90, 120 и 150 сутки после иммунизации экспериментальными вакцинами на основе различных адъювантов.
Таблица 1 – Результаты исследований сывороток крови вакцинированных морских свинок в РСК
|
Номер группы |
Адъювант |
Номер животного |
Титр антител в РСК |
||||
|
30 сут |
60 сут |
90 сут |
120 сут |
150 сут |
|||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
1 |
БС-50 |
1 |
1:20 |
1:20 |
1:40 |
1:10 |
1:10 |
|
2 |
1:20 |
1:20 |
1:20 |
1:20 |
1:20 |
||
|
3 |
1:20 |
1:80 |
1:20 |
1:20 |
1:10 |
||
|
4 |
1:80 |
1:40 |
1:40 |
1:40 |
1:20 |
||
|
Средний титр антител |
1:35 |
1:40 |
1:30 |
1:22,5 |
1:15 |
||
|
2 |
БС-60 |
5 |
1:80 |
1:20 |
1:20 |
1:10 |
1:10 |
|
6 |
1:80 |
1:80 |
1:80 |
1:40 |
1:40 |
||
|
7 |
1:20 |
1:40 |
1:20 |
1:20 |
1:10 |
||
|
8 |
1:20 |
1:40 |
1:80 |
1:80 |
1:80 |
||
|
Средний титр антител |
1:50 |
1:45 |
1:50 |
1:37,5 |
1:35 |
||
|
3 |
БС-70 |
9 |
1:20 |
1:10 |
1:10 |
1:10 |
1:10 |
|
10 |
1:20 |
1:20 |
1:40 |
1:40 |
1:20 |
||
|
11 |
1:20 |
1:20 |
1:20 |
1:20 |
1:20 |
||
|
12 |
1:40 |
1:80 |
1:40 |
1:20 |
1:10 |
||
|
Средний титр антител |
1:25 |
1:32 |
1:27 |
1:22,5 |
1:15 |
||
Продолжение Таблицы 1
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
4 |
«CORALVAC RZ 506» |
13 |
1:10 |
1:40 |
1:20 |
1:20 |
1:10 |
|
14 |
1:10 |
1:10 |
1:10 |
1:5 |
1:5 |
||
|
15 |
1:20 |
1:40 |
1:40 |
1:20 |
1:10 |
||
|
16 |
1:10 |
1:20 |
1:20 |
1:10 |
1:10 |
||
|
Средний титр антител |
1:12,5 |
1:27,5 |
1:22,5 |
1:13,7 |
1:8,7 |
||
|
5 |
«CORALVAC RZ 528» |
17 |
1:5 |
1:20 |
1:10 |
1:5 |
1:5 |
|
18 |
1:5 |
1:40 |
1:40 |
1:20 |
1:5 |
||
|
19 |
1:10 |
1:40 |
1:40 |
1:20 |
1:10 |
||
|
20 |
1:10 |
1:10 |
1:10 |
1:5 |
1:5 |
||
|
Средний титр антител |
1:7,5 |
1:27,5 |
1:25 |
1:12,5 |
1:6,2 |
||
|
6 |
«МЛА-70» |
21 |
1:80 |
1:80 |
1:80 |
1:80 |
1:40 |
|
22 |
1:20 |
1:20 |
1:20 |
1:20 |
1:20 |
||
|
23 |
1:80 |
1:80 |
1:80 |
1:40 |
1:40 |
||
|
24 |
1:20 |
1:40 |
1:20 |
1:20 |
1:20 |
||
|
Средний титр антител |
1:50 |
1:55 |
1:50 |
1:40 |
1:30 |
||
Как видно из таблицы 1, на 30 сутки после вакцинации животных экспериментальными сериями вакцин, сыворотки крови всех морских свинок реагировали со специфическим хламидийным антигеном в РСК. Однако следует отметить, что их концентрация в крови иммунизированных животных разных групп значительно отличалась.
В группах морских свинок, иммунизированных вакцинами, изготовленными из адъювантов «БС-50», «БС-70», «CORALVAC RZ 506», «CORALVAC RZ 528» и «МЛА-70» максимальная концентрация комплементсвязыва-ющих антител была выявлена на 60 сутки после вакцинации. В первой группе на второй месяц после вакцинации уровень противохла-мидийных антител находился в пределах титров от 1:20 до 1:80. Далее наблюдали плавное снижение их концентрации. К 90 суткам исследования концентрация хламидийных иммуноглобулинов варьировалась в пределах титров 1:20 – 1:40. Минимальная концентрация специфических хламидийных антител в сыворотках крови животных была выявлена на 150 сутки после вакцинации и варьировалась в пределах титров от 1:10 до 1:120.
Во второй группе животных иммунизированных вакциной, изготовленной с применением адъюванта «БС-60» максимальные значения титров специфических противохлами-дийных антител были выявлены на 30 и 90 сутки после вакцинации и варьировались в пределах титров от 1:20 до 1:80. Концентрация комплементсвязывающих антител на 150 сутки после вакцинации находилась в пределах титров 1:10 – 1:80.
В третьей группе животных (адъювант «БС -70») уровень хламидийных антител на 60 сутки находился в пределах титров 1:10 – 1:80. Далее концентрация специфических иммуноглобулинов начала снижаться и к 150 суткам после вакцинации варьировалась в пределах титров 1:10 – 1:20.
Наименьшие уровни специфических противохламидийных антител на протяжении всего исследования были зафиксированы в группах морских свинок, иммунизированных вакцинами с адъювантами серии «CORALVAC RZ». В обеих группах на 60 сутки после вакцинации концентрация проти-вохламидийных иммуноглобулинов находилась в пределах титров 1:10 – 1:40. Далее концентрация хламидийных антител в обеих группах плавно снижалась. В четвертой группе морских свинок, иммунизированных вакциной, изготовленной с применением адъюванта «CORALVAC RZ 506» уровень комплемент-связывающих антител на 120 сутки варьировался в пределах титров 1:5 – 1:20. К 150 суткам концентрация противохламидийных антител в сыворотках крови иммунизированных животных еще снизилась и находилась в пределах титров 1:5 – 1:10.
В пятой группе лабораторных животных (адъювант ««CORALVAC RZ 528») концентрация специфических иммуноглобулинов на 120 и 150 сутки после вакцинации находилась в пределах титров 1:5 – 1:20 и 1:5 – 1:10 соответственно.
В шестой группе морских свинок, иммунизированных биопрепаратом, изготовленным из эталонного адъюванта «МЛА-70» были выявлены самые максимальные титры специфических противохламидийных антител. Их концентрация, на протяжение всего исследования находилась в пределах титров 1:20 – 1:80. Максимальный титр был выявлен на 60 сутки после вакцинации. Далее концентрация специфических антител снижалась. На 150 сутки после вакцинации уровень специфических антител варьировался в пределах титров от 1:20 до 1:40.
На рисунке 1 представлены средние титры комплементсвязывающих противо-хламидийных антител по группам вакцин, изготовленных с применением адъювантов серии БС и эталонного адъюванта «МЛА-70».
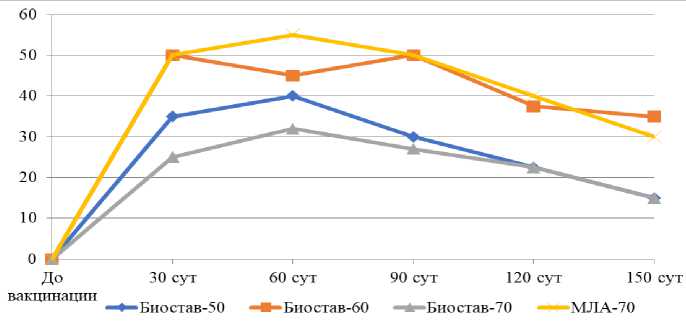
Рисунок 1 – Динамика накопления комплементсвязывающих хламидийных антител в сыворотках крови морских свинок, иммунизированных эталонной вакциной и экспериментальными биопрепаратами на основе адъюванта серии «БС»
Из рисунка 1 видно, что среди вакцин, изготовленных с применением адъювантов серии «БС», самые низкие средние титры специфических хламидийных антител были выявлены в группе животных, иммунизированных препаратом на основе адъюванта «БС-70». На 30 сутки после иммунизации средний титр антител составил 1:25. К 60 суткам был выявлен максимальный уровень специфических хламидийных антител, который равнялся 1:32. Последующие три месяца наблюдали снижение уровня специфических иммуноглобулинов. На 90, 120 и 150 сутки исследования средние титры противохламидийных антител были равны 1:27, 1:22,5 и 1:15 соответственно.
В группе «БС-50» показатели средних титров антител на протяжение первых 90 суток после введения биопрепарата были немного выше и равнялись 1:35 на 30 сутки, 1:40 на 60 сутки и 1:30 на 90 сутки. На протяжении последующих двух месяцев средние титры антител находились в пределах 1:22,5 и 1:15 на 120 и 150 сутки соответственно.
В группах морских свинок, иммунизированных вакцинами, изготовленными из адъювантов «БС-60» и «МЛА-70» на протяжение всего исследования уровень специфических противохламидийных антител был значительно выше, чем в группах животных иммунизированных вакцинами, изготовленными с применением адъювантов «БС-50» и «БС -70». На 30 сутки после введения биопрепаратов в обеих группах средний титр антител равнялся титру 1:50. На 60 сутки после вакцинации в группе морских свинок иммунизированных вакциной с адъювантом «БС-60» средний титр составил 1:45, тогда как в группе животных иммунизированных вакциной с адъювантом «МЛА-70» средний титр составил 1:55. На третий месяц после иммунизации средние титры специфических антител в группах «БС-60» и «МЛА-70» были равны 1:50. К 120 суткам средние титры комплементсвязываю-щих антител в группе «БС-60» имели значение 1:37,5, а в группе «МЛА-70» 1:40. На 150 сутки исследования средний титр специфических иммуноглобулинов в обеих группах снизился, но все равно оставался на достаточно высоком уровне, а именно 1:35 в группе «БС-60» и 1:30 в группе «МЛА-70».
На рисунке 2 представлены средние титры специфических противохламидийных антител в группах лабораторных животных, иммунизированных вакцинами, изготовленными с применением адъювантов CORALVAC RZ 528», «CORALVAC RZ 506» и эталонного адъюванта «МЛА-70».
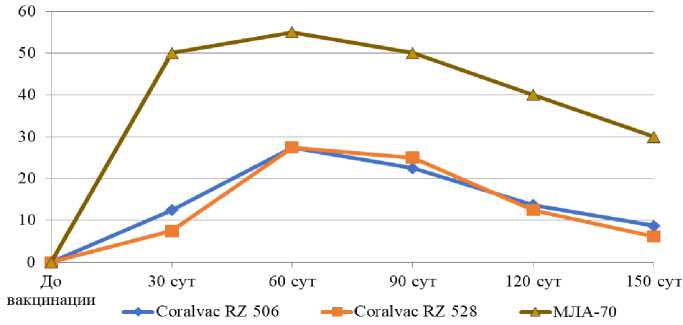
Рисунок 2 – Динамика накопления комплементсвязывающих хламидийных антител в сыворотках крови морских свинок, иммунизированных эталонной вакциной и экспериментальными биопрепаратами на основе адъюванта серии «CORALVAC RZ»
На протяжение 150 суток исследования концентрация комплементсвязывающих хламидийных антител в сыворотках крови морских свинок, иммунизированных экспериментальными вакцинами, изготовленными с применением адъювантов серии «CORALVAC RZ была значительно ниже аналогичных показателей антигенной активности вакцины, изготовленной с использованием эталонного адъюванта «МЛА-70».
Из рисунка 2 можно сделать вывод, что значительной разницы в средних титрах хламидийных антител в группах животных привитыми биопрепаратами на основе адъювантов «CORALVAC RZ 506» и «CORALVAC RZ 528». На 60 сутки был выявлен максимальный средний титр антител в обеих группах -1:27,5. На протяжении последующих трех месяцев концентрация специфических иммуноглобулинов в крови иммунизированных животных плавно снижалась. Средний титр антител на 90 сутки равнялся 1:22,5 и 1:25, на 120 сутки 1:13,7 и 1:12,5, а к 150 суткам исследования были зафиксированы минимальные значения — 1:8,7 и 1:6,2 в группах «CORALVAC RZ 506» и
«CORALVAC RZ 528» соответственно.
Выводы. Как показали проведенные исследования, изготовленные экспериментальные серии хламидийных вакцин на основе адъювантов серии «БС», «CORALVAC RZ» и эталонного адъюванта «МЛА-70» являются ареактогенными и обладают способностью вызывать выработку противохламидийных антител в крови лабораторных животных после их иммунизации.
При оценке антигенной активности экспериментальных серий эмульсионных вакцин было установлено, что наиболее высокий титр специфических антител наблюдался в группе животных, иммунизированных вакциной, изготовленной на основе адъюванта «БС-60».
Полученные результаты говорят о том, что адъювант «БС-60» оказался наиболее оптимальным из всех исследуемых препаратов, соответствующих требованиям надлежащей производственной практики. Поэтому в дальнейшем, изготовление экспериментальных серий вакцины против хламидиозадля доклинических и клинических испытаний, рекомендуется проводить с использованием адъюванта «БС-60».


