Сравнительный анализ эффективности применения обогащенной тромбоцитами плазмы и гиалуронатов при лечении остеоартрита коленного сустава: метаанализ исследований с шестимесячным наблюдением
Автор: Приезжева Е.С., Сивкова Н.И., Жиляков А.В., Волокитина Е.A.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Обзорная статья
Статья в выпуске: 1 т.32, 2026 года.
Бесплатный доступ
Введение. В научной литературе представлено множество исследований, сравнивающих эффективность применения PRP-терапии, или обогащенной тромбоцитами плазмы (ОТП), и препаратов гиалуроновой кислоты (ГК) при остеоартрите коленного сустава, однако результаты носят противоречивый характер из-за методологических ограничений и высокой неоднородности протоколов лечения. Цель работы — сравнить данные научных исследований об эффективности применения ОТП и препаратов ГК средней молекулярной массы в лечении больных остеоартритом коленного сустава. Материалы и методы. Проведен поиск рандомизированных контролируемых исследований в базах PubMed, Embase и Cochrane Library за 2017–2024 гг. по следующим ключевым словам: osteoarthritis, knee joint, intra-articular injections, platelet-rich plasma, hyaluronic acid, WOMAC, meta-analysis. Включены исследования, в которых рассматривали пациентов с диагнозом «остеоартрит коленного сустава» любой степени тяжести, получавших внутрисуставные инъекции ОТП или ГК с оценкой выраженности болевого синдрома по шкале WOMAC. После строгого отбора включены четыре исследования с идентичными протоколами лечения. Результаты. В метаанализ включены данные 333 пациентов (164 в группе ОТП и 169 в группе ГК). Средний балл выраженности болевого синдрома по WOMAC через шесть месяцев от начала лечения (внутрисуставное введение) составил 4,52 (SD = 1,59) в группе ОТП и 4,95 (SD = 2,07) в группе ГК. Размер эффекта Hedges'g: 0,26 (95 % ДИ: –0,61–1,14; p = 0,336). Публикационное смещение отсутствовало (тест Эггера, p = 0,06). Обсуждение. В результате нашего исследования значимых различий между применением ОТП и ГК не выявлено, что противоречит ряду предыдущих метаанализов. Возможно, данный факт обусловлен использованием при нашем анализе более строгих критериев включения и оценкой препаратов ГК только средней молекулярной массы. Заключение. Проведенный метаанализ, направленный на сравнительную оценку эффективности применения ОТП и ГК средней молекулярной массы при лечении пациентов с остеоартритом коленного сустава, не выявил статистически значимых различий между группами при оценке выраженности болевого синдрома по шкале WOMAC через шесть месяцев от начала лечения, что свидетельствует о сопоставимой эффективности данных методов терапии.
Гиалуроновая кислота, богатая тромбоцитами плазма, инъекции, внутрисуставные, остеоартрит, коленный сустав, измерение боли, результаты лечения, метаанализ
Короткий адрес: https://sciup.org/142247058
IDR: 142247058 | УДК: 616.728.3-002-08:615.38:547.995.15:615.036 | DOI: 10.18019/1028-4427-2026-32-1-132-143
Efficacy of platelet-rich plasma in the treatment of pain syndrome in knee osteoarthritis: a meta-analysis of the studies with a 6-month follow-up
Introduction The scientific literature database contains numerous studies comparing the efficacy of platelet-rich plasma (PRP) and hyaluronic acid (HA) preparations in knee osteoarthritis, but the results are contradictory due to methodological limitations and high heterogeneity of treatment protocols. Purpose To compare the data from scientific studies on the effectiveness of using PRP and medium molecular weight HA preparations in the treatment of patients with knee osteoarthritis. Materials and methods A search of randomized controlled trials was conducted in PubMed, Embase, and the Cochrane Library published in the period 2017–2024 using the following keywords: osteoarthritis, knee joint, intra-articular injections, platelet-rich plasma, hyaluronic acid, WOMAC, and meta-analysis. Studies that examined patients diagnosed with knee osteoarthritis of any severity who received intra-articular injections of PRP or HA and assessed pain using the WOMAC were reviewed. After rigorous selection, four studies with identical treatment protocols were included. Results The meta-analysis included 4 studies involving 333 patients (164 in the PRP group and 169 in the HA group). The mean WOMAC pain score at 6 months after the start of treatment was 4.52 (SD = 1.59) in the PRP group and 4.95 (SD = 2.07) in the HA group. The effect size of Hedges' g was 0.26 (95 % CI: –0.61 to 1.14; p = 0.336). Egger's test did not reveal a statistically significant publication bias (p = 0.06). Discussion Our study revealed no significant differences between the use of PRP and HA, which contradicts several previous meta-analyses. This may be due to the use of more stringent inclusion criteria in our analysis and the evaluation of HA preparations with only medium molecular weight. Conclusion This meta-analysis was aimed to compare the effectiveness of using PRP and medium molecular weight HA in the treatment of patients with knee osteoarthritis and did not reveal statistically significant differences between the groups in severity of pain using the WOMAC system six months after the start of treatment, which indicates comparable effectiveness of these therapy methods.
Текст научной статьи Сравнительный анализ эффективности применения обогащенной тромбоцитами плазмы и гиалуронатов при лечении остеоартрита коленного сустава: метаанализ исследований с шестимесячным наблюдением
Остеоартрит (ОА) коленного сустава является распространенным дегенеративно-дистрофическим заболеванием с прогрессирующим разрушением суставного хряща, поражением субхондральной кости, синовиальной оболочки и связочного аппарата, а также одной из ведущих причин хронической боли и инвалидности среди взрослого населения во всем мире [1]. Проблема диагностики и лечения ОА крупных суставов социально значима, поскольку заболевание приводит к значительному снижению качества жизни, ограничению повседневной активности, потере трудоспособности. По данным эпидемиологических исследований, распространенность ОА коленного сустава среди взрослого населения варьирует от 10 до 30 %, причем заболеваемость чаще встречается у женщин и лиц пожилого возраста [2]. Основными симптомами ОА являются боль, скованность, хромота и ограничение подвижности, что существенно снижает качество жизни пациентов.
На сегодняшний день для лечения пациентов с ОА используют как консервативные, так и хирургические методы. Консервативное лечение направлено на уменьшение болевого синдрома, улучшение функции сустава и замедление прогрессирования заболевания. К числу консервативных методов относится медикаментозная терапия, включающая применение нестероидных противовоспалительных препаратов (НПВП), анальгетиков, симптоматических препаратов замедленного действия, а также физиотерапия, лечебная физкультура, ортезирование и внутрисуставные инъекции [3, 4]. Современные хирургические методы, такие как высокие корригирующие остеотомии и тотальное эндопротезирование, эффективны при поздних стадиях заболевания при наличии деформаций сустава, значительного ограничения подвижности и выраженного болевого синдрома. Однако хирургическое вмешательство сопряжено с такими рисками, как инфекционные осложнения, тромбоэмболия и развитие нестабильности эндопротеза. Реабилитационный период после операции не всегда приводит к полному восстановлению функции сустава.
При ранних стадиях заболевания консервативное лечение является предпочтительным. На сегодняшний день при консервативном лечении широко применяют внутрисуставные инъекции гиалуроновой кислоты (ГК). ГК является естественным компонентом синовиальной жидкости, обеспечивает смазку, амортизацию и питание суставного хряща. Введение экзогенной ГК может улучшить вязкоэластичные свойства синовиальной жидкости, а также стимулировать естественные процессы восстановления, способствуя регенерации хрящевой ткани и поддерживая гомеостаз синовиальной среды [5, 6]. ГК уменьшает болевой синдром, снижает воспаление и улучшает подвижность сустава. Однако эффект от инъекций ГК носит временный характер, — от нескольких недель до нескольких месяцев.
В последние годы в лечении пациентов с ОА коленного сустава стали применять обогащенную тромбоцитами плазму (ОТП), которая представляет собой аутологичный биологический препарат, получаемый из крови самого пациента путем центрифугирования. ОТП отличается высокой концентрацией тромбоцитов, которые при активации выделяют разнообразные факторы роста, стимулирующие регенерацию хрящевой ткани [7, 8]. Инъекции ОТП способны уменьшить болевой синдром, улучшить функцию сустава и замедлить прогрессирование дегенеративных изменений. Клинические исследования S.A. Raeissadat et al. и G. Filardo et al. показали, что инъекции ОТП существенно уменьшают боль и улучшают подвижность сустава по сравнению с контрольными группами, при этом эффект сохраняется в течение 6–12 месяцев после лечения [9, 10].
В научной литературе представлено множество исследований, направленных на сравнение эффективности ОТП (PRP-терапии) и препаратов ГК при ОА коленного сустава. Тем не менее, результаты исследований остаются противоречивыми из-за методологических ограничений, таких как отсутствие стандартизированных протоколов, небольшие размеры выборок, недостаточное ослепление и кратковременное наблюдение [11–13]. Кроме того, выявлена высокая неоднородность протоколов приготовления ОТП, существуют различия в концентрации тромбоцитов, в методах активации и алгоритмах внутрисуставного введения, а также в частоте и продолжительности курсов лечения. Эти факторы существенно затрудняют сопоставление результатов исследований и являются основными источниками противоречий при сравнении эффективности применения ОТП и ГК при ОА коленного сустава [14]. Ожидается, что результаты нашего исследования позволят определить, какой из методов обеспечивает более выраженное и длительное купирование болевого синдрома при ОА коленного сустава, что имеет критически важное значение для выбора оптимальной стратегии лечения.
Цель работы — сравнить данные научных исследований об эффективности применения ОТП и препаратов ГК средней молекулярной массы в лечении больных остеоартритом коленного сустава.
МАТЕРИАЛЫ И МЕТОДЫ
Метаанализ проведен в соответствии с рекомендациями PRISMA (англ.: Preferred Reporting Items for Systematic Reviews and Meta-Analyses). Протокол исследования зарегистрирован в международном реестре PROSPERO. Поиск литературы проведен в трех основных электронных базах данных PubMed, Embase, и Cochrane Library за период с января 2018 г. по декабрь 2024 г. Поисковая стратегия включа- ла комбинацию следующих MeSH-терминов и ключевых слов: osteoarthritis, knee joint, intra-articular injections, platelet-rich plasma, hyaluronic acid, WOMAC, meta-analysis. Термины объединяли с помощью булевых операторов AND/OR для создания оптимальной поисковой строки. Дополнительно проведен «ручной» поиск по спискам источников отобранных статей. Выраженность болевого синдрома в анализируемых исследованиях оценивали по шкале WOMAC через шесть месяцев от начала применения внутрисуставных инъекций при ОА коленного сустава.
Критерии включения и исключения
Критерии включения статей в исследование: пациенты с подтвержденным диагнозом «остеоартрит коленного сустава» любой степени тяжести; вмешательства — инъекции ОТП (для группы лечения) и инъекции ГК (контрольная группа); основные исходы — оценка выраженности болевого синдром по шкале WOMAC через шесть месяцев; вторичные исходы — по шкалам IKDC, Леккена и VAS. Для анализа отобраны только рандомизированные контролируемые клинические исследования.
Критерии исключения : исследования пациентов с билатеральным остеоартритом коленного сустава, а также нерандомизированные исследования и публикации, из которых невозможно извлечь данные для анализа.
Отбор публикаций проводили в четыре этапа:
-
1. Идентификация: найдено 192 публикации в электронных базах данных; дополнительно выявлено четыре публикации из других источников; общее количество идентифицированных публикаций — 196.
-
2. Скрининг: на этом этапе два независимых исследователя проводили первичный скрининг по названиям и аннотациям выявленных статей с целью исключения нерелевантных публикаций на основании следующих критериев: отсутствие данных о целевых вмешательствах, популяция, не соответствующая теме исследования, результаты, не связанные с задачами анализа. После удаления дубликатов осталось 170 публикаций. Все публикации прошли скрининг по заголовкам и аннотациям. Критериям включения соответствовали 11 полнотекстовых статей, на этапе скрининга из исследования исключено 159 публикаций.
-
3. Окончательный отбор: полные тексты статей, прошедших первичный отбор, анализировали на соответствие критериям включения и исключения; в случае разногласий между исследователями вопрос решали путём обсуждения, а при необходимости привлекали третьего исследователя для вынесения окончательного решения.
-
4. Итог: четыре исследования соответствовали всем критериям включения и были использованы для количественного синтеза (метаанализа).
Публикации исключали по следующим причинам: отсутствие данных по шкале WOMAC через шесть месяцев наблюдения ( n = 2); отсутствие данных по общему показателю WOMAC ( n = 1); отсутствие контрольной группы в дизайне исследования ( n = 2); обзорные статьи без оригинальных данных ( n = 2).
Процесс отбора исследований схематически представлен на диаграмме PRISMA (рис. 1).
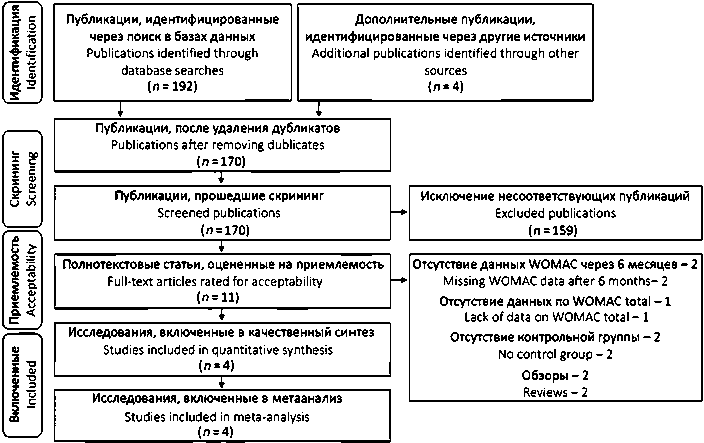
Рис. 1. Блок-схема PRISMA процесса отбора исследований для включения в метаанализ эффективности внутрисуставных инъекций при остеоартрите коленного сустава
Извлечение данных
Извлечение данных проводили два независимых исследователя с использованием стандартизированной формы, включающей следующие данные: автор, год публикации, страна, количество участников, возраст, пол, индекс массы тела (ИМТ), классификация, длительность наблюдения, дозировка и количество инъекций. Параметр WOMAC выбран для оценки эффективности лечения, поскольку является общепризнанным комплексным показателем, охватывающим данные о болевом синдроме и функциональных ограничениях у пациентов с ОА. Если в публикации приведены не абсолютные значения, а относительные (например, разница в значениях WOMAC между началом исследования и через шесть месяцев), данные пересчитывали в абсолютные значения, что унифицировало результаты и обеспечивало их корректное обобщение. В частности, такое действие выполнено с данными статьи S.A. Raeissadat [9]. Также для унифицирования результатов все временные значения, измеренные в месяцах или днях, конвертированы в недели. Остальные сведения, такие как демографические характеристики и дозировки, были необходимы для контроля потенциальных факторов, влияющих на результаты, и для оценки однородности исследуемых групп.
Оценка риска систематической ошибки
Оценку риска систематической ошибки проводили независимо два исследователя с использованием Кокрановского инструмента оценки риска смещения. Были рассмотрены такие аспекты, как генерация случайной последовательности, скрытое распределение, ослепление участников и персонала, неполные данные о результатах, а также избирательность публикаций. Данный подход позволял минимизировать предвзятость и увеличить надежность полученных данных.
Статистический анализ
Для анализа данных использовался программный пакет Stata 12.0 (StataCorp., College Station, TX, США). Основные результаты (болевые ощущения и функции по шкале WOMAC) рассчитывали с использованием стандартного среднего различия (SMD) с 95 % доверительным интервалом. Использование SMD выбрано для учета различий в масштабах измерений между исследованиями, что делает его предпочтительным методом для метаанализа данных из источников, применявших различные шкалы оценки. Неоднородность оценивали с использованием статистики I² с показателями 25 %, 50 % и 75 %, интерпретируемыми как низкий, средний и высокий уровни гетерогенности, соответственно. Для проведения метаанализа использовали метод случайных эффектов, который учитывает потенциальную неоднородность между исследованиями и позволяет делать более обобщённые выводы. Значение p < 0,05 считали статистически значимым, что обеспечивало достаточную уверенность в результатах анализа.
РЕЗУЛЬТАТЫ
Включенные в метаанализ исследования охватывали данные о 333 пациентах, получавших лечение при ОА коленного сустава: 164 пациента в группе ОТП и 169 пациентов в группе ГК.
Метаанализ показал отсутствие статистически значимой разницы в исходном уровне боли между группами ОТП и ГК (Hedges'g = 0,25, стандартная ошибка = 0,20, 95 % ДИ: –0,38 – 0,88; p = 0,205). Среднее значение уровня болевых ощущений исходно различно ввиду искажения восприятия болевых ощущений в зависимости от исследуемой исходной стадии заболевания, а также наличия сопутствующих отягчающих патологических состояний. Так, в некоторых публикациях данные о степени тяжести основного заболевания либо не представлены, либо представлены частично. Исходные данные по показателю WOMAC (боль) по каждому исследованию представлены в табл. 1.
Таблица 1
Сравнение средних значений по шкале WOMAC (боль) перед началом терапии
|
Автор, год, номер источника |
ОТП |
ГК |
Вес исследования, % |
Доля случаев (95 % ДИ) |
||||
|
M |
SD |
Всего пациентов |
M |
SD |
Всего пациентов |
|||
|
Duymus T.M., 2017 [20] |
15,40 |
2 |
33 |
16,6 |
1,10 |
34 |
23,15 |
0,74 [0,25;1,25] |
|
Raeissadat S.A., 2021 [9] |
9,69 |
1,30 |
52 |
9,44 |
1,60 |
49 |
27,25 |
0,00 [–0,39;0,39] |
|
Su K., 2018 [21] |
9,57 |
1,45 |
25 |
9,60 |
1,19 |
30 |
21,86 |
–0,17 [–0,71;0,37] |
|
Wang Y.C., 2022 [22] |
4,2 |
0,42 |
54 |
4,38 |
0,43 |
56 |
27,75 |
0,42 [0,04;0,80] |
Примечание : M — среднее значение; SD — стандартное отклонение; ДИ — доверительный интервал.
Через шесть месяцев после начала лечения средний балл боли по шкале WOMAC (боль) снизился как в группе ОТП, так и в группе ГК. Средний балл боли составил 4,52 (SD = 1,59) в группе ОТП и 4,95 (SD = 2,07) в группе ГК. Однако разница между группами по уровню боли через шесть месяцев не достигла статистической значимости ( p = 0,336). Размер эффекта Hedges'g составил 0,26 (95 % ДИ: –0,61 – 1,14). Результаты по каждому исследованию, включенному в метаанализ, представлены в табл. 2.
Таблица 2
Сравнение средних значений по шкале WOMAC (боль) через шесть месяцев от начала лечения
|
Автор, год, номер источника |
ОТП |
ГК |
Вес исследования, % |
Доля случаев (95 % ДИ) |
||||
|
M |
SD |
Всего пациентов |
M |
SD |
Всего пациентов |
|||
|
Duymus T.M., 2017 [20] |
9,4 |
1,70 |
33 |
9,7 |
1,60 |
34 |
24,43 |
0,18 [–0,30;0,67] |
|
Raeissadat S.A., 2021 [9] |
4,69 |
0,90 |
52 |
5,64 |
0,70 |
49 |
26,44 |
0,12 [–0,27;0,51] |
|
Su K., 2018 [21] |
4,7 |
0,70 |
25 |
5,56 |
0,82 |
30 |
22,35 |
1,10 [0,54;1,70] |
|
Wang Y.C., 2022 [22] |
2,87 |
0,35 |
54 |
2,79 |
0,38 |
56 |
26,78 |
–0,22 [–0,60;0,16] |
Примечание : M — среднее значение; SD — стандартное отклонение; ДИ — доверительный интервал.
При анализе результатов исследования S.A. Raeissadat et al. обращает на себя внимание система количественной оценки эффективности терапии, где изменения показателей болевого синдрома по шкале WOMAC представлены в виде отрицательных значений относительно исходного уровня, что потребовало применения метода стандартизации данных для обеспечения сопоставимости результатов [9].
Метаанализ показал, что через шесть месяцев после начала лечения величина эффекта Hedges’g по общему значению WOMAC увеличилась до 0,79 по сравнению с исходным уровнем. Однако данный эффект не был статистически значимым ( p = 0,282).
Для оценки возможного публикационного смещения использован тест Эггера, результаты которого представлены в табл. 3.
Таблица 3
Результаты теста Эггера
|
Параметр |
Оценка |
Стандартная ошибка |
95 % ДИ |
|
Константа (Intercept) |
11,14 |
3,48 |
0,05–22,23 |
|
Наклон (Slope) |
–2,26 |
0,77 |
–4,70–0,18 |
Примечание : t-критерий = 3,20; p -значение = 0,086.
Тест Эггера не выявил статистически значимого публикационного смещения ( p = 0,086), что графически подтверждено на рис. 2.
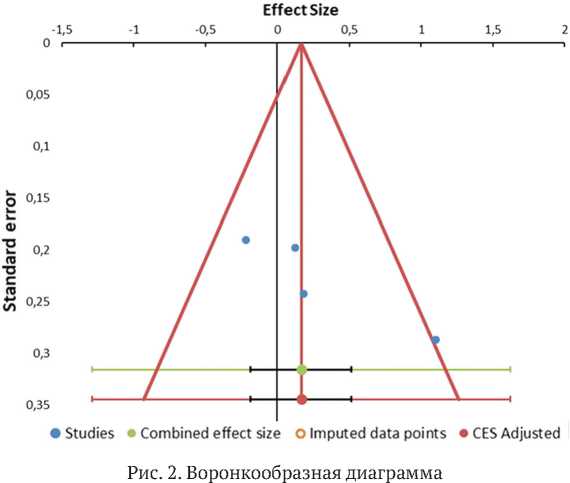
Воронкообразная диаграмма — графический метод оценки публикационного смещения. В идеальном случае, когда публикационное смещение отсутствует, точки на диаграмме должны быть распределены симметрично вокруг вертикальной линии, проходящей через суммарный размер эффекта. Асимметрия воронкообразной диаграммы может свидетельствовать о публикационном смещении. В настоящем метаанализе воронкообразная диаграмма выглядит относительно симметричной, что может свидетельствовать об отсутствии публикационного смещения и коррелирует с результатами теста Эггера.
ОБСУЖДЕНИЕ
Цель данного метаанализа состояла в оценке эффективности применения ОТП по сравнению с ГК в снижении болевого синдрома при ОА коленного сустава через шесть месяцев после начала лечения. Включенные данные обследования 333 пациентов из четырех рандомизированных контролируемых исследований на основе анализа показателя WOMAC (оценка боли) не выявили статистически значимых различий между двумя методами, что подчеркивает необходимость более глубокого анализа факторов, влияющих на исходы лечения. Возможно, что такие факторы, как особенности пациентов и методологические различия в подходах, могли повлиять на результаты, сглаживая потенциальные различия.
Эффективность применения ОТП и ГК может зависеть от тяжести ОА: пациенты с ранней стадией заболевания часто реагируют на оба метода лечения одинаково хорошо, при поздних стадиях ОА реакция на введение ОТП и ГК может отличаться. Включение в метаанализ информации о пациентах с разной степенью тяжести ОА могло привести к тому, что различия в эффективности ОТП и ГК были нивелированы. Например, исследования с участием пациентов с начальной стадией остеоартрита показали, что инъекции ГК менее эффективны у пациентов с более тяжелыми стадиями заболевания [15–22].
Индивидуальные характеристики пациента, такие как возраст, пол, генетическая предрасположенность, сопутствующие заболевания, образ жизни и уровень физической активности, также могут оказывать влияние на результат применения ОТП и ГК [23–28]. Пациенты пожилого возраста часто имеют замедленный регенеративный потенциал, что снижает эффективность ОТП. Мужчины и женщины по-разному реагируют на лечение из-за различий в гормональном фоне. Генетическая предрасположенность также влияет на способность тканей к восстановлению. Пациенты с сопутствующими заболеваниями, такими как диабет, могут иметь повышенный уровень воспалительных реакций, что ухудшает результаты лечения. Образ жизни, включая уровень физической активности, также критически важен: активные пациенты могут лучше реагировать на терапию за счет улучшенного кровообращения и метаболизма, а пациенты с ожирением или сахарным диабетом реагируют хуже из-за выраженности воспалительного процесса в суставах.
Авторы анализируемых публикаций не всегда учитывали генетическую предрасположенность и индивидуальные различия в регенеративном потенциале, что могло повлиять на точность результатов. Важно проводить исследования, которые принимают во внимание особенности пациентов, чтобы определить, кому из них терапия ОТП или ГК может принести наибольшую пользу, и каким образом можно персонализировать лечение [29, 30].
Отсутствие стандартизации протоколов приготовления и введения ОТП также является важным фактором, влияющим на результаты лечения. Для стандартизации протоколов необходимо определить оптимальные параметры центрифугирования, концентрацию тромбоцитов и содержание лейкоцитов, а также единообразные методы введения ОТП. Введение стандартизированных инструкций позволит снизить вариабельность и повысить сопоставимость результатов между исследованиями. В рассматриваемых публикациях использованы различные методы приготовления ОТП и центрифугирования, с различной концентрацией тромбоцитов и лейкоцитов [29–32]. K. Su et al. [21] применяли ОТП без лейкоцитов, тогда как другие исследователи использовали ОТП с различным содержанием лейкоцитов, что могло влиять на результаты, так как лейкоциты способствуют развитию воспалительных реакций [26]. Также различие методов введения ОТП (объем и количество инъекций, интервалы между ними) могло сказаться на степени эффективности лечения [32–34]. Использование разных антикоагулянтов также могло повлиять на биологическую активность ОТП [19, 24, 36].
Качество плазмы, получаемой для ОТП, может различаться в зависимости от оборудования и методов, применяемых в лабораториях. Даже небольшие изменения в скорости или времени центрифугирования могут существенно изменить состав конечного продукта, что напрямую влияет на эффективность лечения [37]. Важно стандартизировать не только основные этапы приготовления ОТП, но и вспомогательные процессы, такие как сбор образцов и их обработка. Введение стандартизированных рекомендаций для подготовки пациента также может снизить вариабельность результатов. Например, прием антикоагулянтов или других препаратов до процедуры может изменять реактивность тромбоцитов и тем самым повлиять на результат лечения [38–40].
Методы введения ОТП зависят от техники врача, места инъекции (внутрисуставная или периартику-лярная) и даже глубины введения [41]. Это еще один аспект, требующий стандартизации. Разработка детальных рекомендаций по технике инъекций могла бы минимизировать эти различия и способствовать повышению воспроизводимости результатов лечения. Таким образом, необходимость стандартизации охватывает весь процесс от подготовки плазмы до взаимодействия с пациентом и выполнения процедуры, требует комплексного подхода и участия специалистов из разных областей, — клиницистов, исследователей и реабилитологов.
Ограничением данного метаанализа является небольшое количество включенных исследований (всего четыре), что снижает статистическую мощность и увеличивает риск случайных ошибок. Небольшое количество исследований увеличивает вероятность того, что результаты могут быть случайными и не отражать истинную картину эффективности методов лечения. Для повышения статистической надежности необходимо провести более масштабные исследования, чтобы обеспечить достаточную для достоверных выводов выборку. Высокая гетерогенность (I2 = 79,74 %) свидетельствует о значительных различиях в дизайне исследований, характеристиках пациентов и применяемых методах лечения [32, 35–39, 42]: возраст участников, стадия ОА, наличие сопутствующих заболеваний, уровень физической активности. Усугубить неоднородность данных могли и различия в методах приготовления и введения ОТП. Разные подходы к отбору пациентов также внесли свою лепту: в одних исследованиях участвовали пациенты с минимальными симптомами, в других — с тяжелыми формами остеоартрита [40–47].
Некоторые исследования оказывали значительное влияние на общий эффект [21, 22], вероятно, из-за различий в методологии и стадии заболевания участников. Это подчеркивает необходимость проведения анализа чувствительности, который позволил бы выявить источники гетерогенности и их вклад в результаты метаанализа. Неоднородность также может быть связана с методами оценки эффективности лечения, использование разных шкал для оценки боли и функциональности затрудняет сопоставление результатов [48–51]. Для устранения этих недостатков необходимы крупные, хорошо спланированные исследования с более однородными характеристиками участников и стандартизированными протоколами лечения.
Следует учитывать и потенциальное публикационное смещение, так как результаты с положительными исходами публикуют чаще, чем нейтральные или отрицательные. Это приводит к искажению представления об эффективности вмешательств. Проведение регистрации протоколов исследований и обеспечение прозрачности исследований могут помочь снизить риск публикационного смещения и улучшить качество метаанализов [52]. Для повышения статистической мощности и достоверности результатов необходимы крупные многоцентровые исследования, которые позволят собрать больше данных и предоставить более надежные выводы [37, 53–55].
Данный метаанализ оценивал эффект лечения через шесть месяцев после начала инъекционной терапии, однако для выявления более устойчивых различий между группами требуется более длительное наблюдение (12 месяцев и более). Длительное наблюдение позволит обнаружить отложенные эффекты, которые не проявляются в краткосрочной перспективе, а также оценить стабильность достигнутых улучшений и потенциальные долгосрочные изменения в состоянии хрящевой ткани. Исследования показали, что эффект от ОТП может сохраняться дольше, чем от ГК, особенно при наблюдении свыше шести месяцев [56–58]. Такие исследования помогут оценить возможные отложенные побочные эффекты и изменения в структуре хрящевой ткани и определить, возможно ли накопление положительных эффектов при повторных инъекциях [38, 47, 58–62].
Повторные курсы терапии могут усиливать регенеративный эффект и улучшать клинические результаты. Долгосрочные исследования помогут лучше понять, как индивидуальные факторы, такие как генетическая предрасположенность и уровень физической активности, влияют на продолжительность и стабильность эффекта лечения [63–66]. Кроме уменьшения боли, следует также оценивать изменения в хрящевой ткани, улучшение подвижности суставов и общее качество жизни пациентов.
Для оценки возможного публикационного смещения в метаанализе использованы тесты Эггера и Begg&Mazumdar, которые не выявили статистически значимого смещения ( p = 0,06 для теста Эггера). Анализ методом Trim and Fill также подтвердил стабильность результатов. Однако стоит помнить, что у этих методов есть ограничения, и их интерпретация должна проводиться осторожно [41]. Необходимо применять дополнительные подходы для минимизации предвзятости и обеспечения максимальной достоверности и устойчивости выводов.
Дальнейшие исследования должны быть направлены на несколько ключевых аспектов. Во-первых, необходимо изучить влияние тяжести остеоартрита на эффективность ОТП и ГК, стратифицируя пациентов по степени тяжести, чтобы разработать более таргетированные стратегии лечения. Во-вторых, следует учитывать индивидуальные факторы (возраст, пол, индекс массы тела, сопутствующие заболевания, образ жизни и генетическая предрасположенность) для создания персонализированных подходов к терапии [44, 67, 68].
Необходимы стандартизированные протоколы приготовления и введения ОТП для снижения неоднородности данных и более точной оценки эффективности терапии. Важно стандартизировать все этапы процесса — от сбора и обработки крови до параметров центрифугирования и методов введения [16]. Стандартизация должна включать контроль за качеством плазмы, концентрацией тромбоцитов, содержанием лейкоцитов и использованием антикоагулянтов. Рекомендации по подготовке пациентов перед процедурой также могут улучшить воспроизводимость результатов.
Наконец, требуется проведение крупных, многоцентровых исследований с длительным периодом наблюдения, чтобы оценить долгосрочные эффекты ОТП и ГК, а также их влияние на функциональные показатели и качество жизни пациентов [69–71]. Такие исследования должны быть направлены на выявление преимуществ комбинированного лечения и изучение влияния повторных курсов терапии.
Таким образом, основная цель консервативного лечения при ОА — стабилизация дегенеративно-воспалительных процессов в суставе, которая сможет способствовать продлению сроков работоспособности сустава и отдалению сроков выполнения тотальной артропластики [72]. Именно в этом ключе многоцентровые исследования помогут улучшить понимание механизмов действия ОТП и ГК и способствовать разработке рекомендаций, направленных на повышение эффективности лечения и улучшение качества жизни пациентов с ОА.
ЗАКЛЮЧЕНИЕ
Метаанализ сравнительной оценки эффективности применения ОТП и ГК средней молекулярной массы при лечении больных ОА коленного сустава не выявил статистически значимых различий между группами пациентов при оценке выраженности болевого синдрома по шкале WOMAC через шесть месяцев от начала лечения, что свидетельствует о сопоставимой эффективности данных методов терапии.
Однако необходимо учитывать ограниченное количество включенных в анализ исследований, высокую гетерогенность между ними и отсутствие стандартизированных протоколов приготовления и введения ОТП. Для более точной сравнительной оценки эффективности ОТП и ГК необходимы дальнейшие крупные, хорошо спланированные исследования с длительным периодом наблюдения, учетом тяжести заболевания, особенностей пациентов и стандартизированными методами приготовления и введения ОТП.


