Средняя лобэктомия при немелкоклеточном раке легкого: эффективность и отдаленные результаты
Автор: Аксарин А.А., Тер-ованесов М.Д., Мордовский А.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 2 (48), 2016 года.
Бесплатный доступ
В статье оценена эффективность средней лобэктомии при немелкоклеточном раке легкого (НМРЛ) по сравнению с другими лобэктомиями и билобэктомией. Пятилетняя выживаемость была выше при билобэктомии - 74,9%, чем при средней лобэктомии - 64,1% и других лобэктомиях - 62,0%. Выполнение систематической лимфодиссекции привело к снижению количества внутригрудных рецидивов. Предпочтение при хирургическом лечении НМРЛ с поражением средней доли следует отдавать органосохраняющим операциям (средняя лобэктомия, билобэктомия) с выполнением обязательной систематической лимфодиссекцией.
Немелкоклеточный рак легкого (нмрл), хирургическое лечение, средняя лобэктомия, систематическая лимфодиссекция
Короткий адрес: https://sciup.org/142211250
IDR: 142211250 | УДК: 616.24-006.6-089:616.42-089.87
Pulmonary middle lobectomy for non-small cell lung cancer: prognostic implications and effectiveness
The paper evaluated the effectiveness of middle lobectomy for non-small cell lung cancer (NSCLC) compared with lobectomy and other bilobektomiey. Five-year survival was higher in bilobektomii - 74.9%, than in the middle lobectomy - 64.1% and other lobectomy - 62.0%. Implementation of systematic lymphadenectomy resulted in a decrease in the number of intrathoracic relapses. Preference in the surgical treatment of NSCLC with the defeat of the average share should be given to breast-conserving surgery (middle lobectomy, bilobektomiya) with the implementation of a mandatory systematic lymphadenectomy.. Key words: non-small cell lung cancer (NSCLC), surgery, lobectomy average, systematic lymph node dissection.
Текст научной статьи Средняя лобэктомия при немелкоклеточном раке легкого: эффективность и отдаленные результаты
Рак легкого является одной из самых распространенных злокачественных опухолей. Хирургическое лечение является краеугольным камнем в лечении немелкоклеточного рака легкого (НМРЛ), особенно на ранних стадиях заболевания [1, 2]. Лобэктомия в настоящее время считается золотым стандартом хирургической лечения НМРЛ. Средняя лобэктомия (СЛЭ) считается одной из наиболее распространенных форм лобэктомии, несмотря на уникальные анатомические особенности средней доли. Средняя доля является самой маленькой, между двумя большими верхней и нижней долями и ее лимфатический дренаж является непредсказуемым. По данным ряда авторов при локализации опухоли в средней доле происходит раннее вовлечение соседних долей через межсегментарные вены [3]. Лимфатический дренаж от средней доли предполагает впадение лимфатических сосудов в перибронхиальные, паратрахе-альные, претрахеальные, околопищеводные, субкариналь-ные (бифуркационные) [4]. Исходя из этих особенностей, ряд авторов [5–8] считают, что опухоли, локализующиеся в средней доле, ухудшают прогноз заболевания. С целью оценки эффективности средней лобэктомии мы провели сравнение результатов лечения по сравнению с другими видами лобэктомии (верхней и нижней). Поскольку при поражении средней доли нередко выполняется другой вид резекции легкого - билобэктомия, мы также сравнили результаты лечения при выполнении средней лобэктомии и билобэктомии.
Цель исследования
Оценка эффективности средней лобэктомии при НМРЛ.
Материалы и методы
Клинический материл для исследования, составили 492 больных с НМРЛ, которым была выполнена лобэктомия или билобэктомия (при локализации опухоли в средней доле) в лечебных онкологических учреждениях Югры в период с 1999 по 2011г., и наблюдавшиеся до 1.01.2015 г. Спе-
циального отбора больных для выполнения исследования не проводилось.
Среди пациентов преобладали представители мужского пола 396 (80,5%) над женским полом – 96 (19,5%). Средний возраст соответствовал 55,0 лет. Все пациенты были с I – IIIA стадией. Статистически значимых возрастных отличий в зависимости от распространенности процесса не наблюдалось.
Тридцатидневная летальность после операции составила 1,2%. Критериями включения были диагноз НМРЛ, патологической стадии I–IIIA, отсутствие второго первичного рака другой локализации в течение последующих 5 лет, R0 резекция с помощью стандартной лобэктомии или билобэктомии (при локализации опухоли в средней доле). Пациенты были разделены на три группы в зависимости от вида операции: средняя лобэктомия при раке средней доли (СЛЭ), билобэктомия (БЛЭ) при раке средней доли и контрольная группа верхняя и нижняя лобэктомия при другой локализации рака легкого (ЛЭ). Пациенты с послеоперационным диагнозом НМРЛ с поражением средостенных лимфоузлов (N2) получили адьювантную химиотерапии или химиолучевое лечение в большинстве случаев: 41 из 66 (62,1%). Предоперационное обследование включало анализы крови, обзорную рентгенографию органов грудной клетки, компьютерную томографию органов грудной клетки, ультразвуковое исследование брюшной полости и оценку функции внешнего дыхания [9].
Стадирование заболевания у пациентов осуществлялось в соответствие с 6 классификацией Международной ассоциации по изучению рака легких и патологической классификации Всемирной организацией здравоохранения [10]. Были оценены в качестве возможных прогностических факторов: пол, возраст, гистология опухоли, патологическая стадия опухоли, диаметр, критерии T и N.
В группу больных с лобэктомией включались пациенты, которым была выполнена раздельная обработка сосудов, бронха, а также отсутствие опухолевых клеток по краю резекции бронха или в междолевой щели с моноблочной лим-фодиссекцией. В группу больных с билобэктомией были взяты пациенты с раком средней доли согласно тем же хирургическим принципам, описанным для лобэктомия.
Сведения о больных систематизированы в базе данных Microsoft Excel. Полученные данные подвергались статистической обработке. Выживаемость была рассчитана методом Каплан-Мейера. Статистическая значимость различий между группами определялась с помощью лог-ранг теста. Все статистические анализы были двусторонними и проводились с использованием пакета SPSS (версия 17.0 для Windows).
Результаты
СЛЭ была выполнена у 18 больных (3,7%), билобэктомия у 13 (2,6%) и лобэктомия у 461 (93,7%). Среди пациен- тов преобладали представители мужского пола 396 (80,5%) над женским полом – 96 (19,5%). Распределение больных в зависимости от объема выполненной операции, пола возраста, гистологической структуры опухоли, критериев T и N, стадии представлено в таблице 1.
Распределение по возрасту и полу было схожее в трех группах. Гистологическая структура была схожа в группах СЛЭ и ЛЭ с преобладанием плоскоклеточного рака (44,4% и 44,7%). В группе БЛЭ преобладал железистый рак (53,8%). Средний диаметр опухоли был 3,12, 3,77 и 3,67 см в группах СЛЭ, БЛЭ и ЛЭ соответственно. Меньшей стадии были опухоли в группах СЛЭ и БЛЭ по сравнению с контрольной группой (ЛЭ). По критерию pT1 опухоли были 72,2% в СЛЭ группе (14/18), 53,8% в БЛЭ группе (7/13) и 42,7% в контрольной группе (197/461). По критерию pN1-2 распределение было следующее: 22,2% (4/18) в группе СЛЭ, 15,4% (2/13) в группе БЛЭ и 30,7% (140/461) в контрольной группе. В IIIA стадию пациенты оперировались только в группе СЛЭ (16,7%) и контрольной группе (14,5%).
Нами проведена сравнительная оценка непосредственных и отдаленных результатов операций при раке легкого с различным объемом лимфодиссекции. Мы использовали следующую классификацию медиастинальной лимфодис-секции (P. Goldstraw):
-
1. Медиастинальная лимфодиссекция не выполнялась.
-
2. Системная биопсия (СБ) (удалялись только пораженные лимфоузлы или трахеобронхиальные и субкариналь-ные сигнальные средостенные лимфоузлы).
-
3. Систематическая лимфодиссекция (СЛД) (ипсилатеральная радикальная лимфодиссекция – 1 – 10 группы лимфоузлов по классификации T. Naruke).
-
4. Двусторонняя (ипси- и контралатеральная) лимфо-диссекция.
В нашем исследовании выполнялись первые три варианта лимфодиссекции. Характеристика больных по уровню поражения лимфатического коллектора и объему выполненной лимфодиссекции представлена в таблице 2.
Метастатическое поражение лимфоузлов в группе СЛЭ было в 22,2% (4/18), в группе БЛЭ в 15,4% (2/13) и в 30,7% (140/461) в контрольной группе. В целом различные объемы лимфодиссекции были выполнены в 50,0% в группе СЛЭ, в 92,3% в группе БЛЭ и в 74,7% в контрольной группе. При этом систематическая лимфодиссекция была выполнена в 22,2% в группе СЛЭ, в 61,5% в группе БЛЭ и в 49,5% в контрольной группе. Аналогичные показатели были при правосторонней локализации опухоли в контрольной группе.
-
У пациентов с СЛЭ поражение лимфоузлов уровня pN2 было выявлено в четырех случаях: у трех в сублобарных лимфоузлах, у одного в паратрахеальном лимфоузле. У одного пациента из этой группы были поражены верхние междолевые лимфоузлы. У пациентов с БЛЭ в одном случае
Таблица 1
|
Параметры |
СЛЭ (n-18) n (%) |
БЛЭ (n-13) n (%) |
ЛЭ (n-461) n (%) |
|
Возраст < 66 лет 66-74 года |
15 (83,3) 3 (16,7) |
12 (92,3) 1 (7,7) |
397 (86,1) 64 (13,9) |
|
Пол мужской женский |
13 (72,2) 5 (27,8) |
9 (69,2) 4 (30,8) |
374 (81,1) 87 (18,9) |
|
Гистология плоскоклеточный аденокарцинома другой |
8 (44,4) 7 (38,9) 3 (16,7) |
4 (30,8) 7 (53,8) 2 (15,4) |
206 (44,7) 206 (44,7) 49 (10,6) |
|
Размер опухоли (см) |
3,12±1,91 |
3,77±1,87 |
3,67±2,11 |
|
рT T 1 T 2 T 3 |
13 (72,2) 5 (27,8) |
7 (53,8) 6 (46,7) |
197 (42,7) 244 (52,9) 20 (4,4) |
|
pN N0 N1 N2 |
14 (77,8) 1 (5,5) 3 (16,7) |
11 (84,6) 2 (15,4) - |
321 (69,6) 77 (16,7) 63 (13,7) |
|
Cтадия IA-IB IIA-IIB IIIA |
14 (77,8) 1 (5,5) 3 (16,7) |
11 (84,6) 2 (15,4) |
309 (67,0) 85 (18,5) 67 (14,5) |
Таблица 2
|
Параметры |
СЛЭ (n-18) n (%) |
БЛЭ (n-13) n (%) |
ЛЭ (n-461) n (%) |
|
pN N0 |
14 (77,8) |
11 (84,6) |
321 (69,6) |
|
N1 |
1 (5,5) |
2 (15,4) |
77 (16,7) |
|
N2 |
3 (16,7) |
– |
63 (13,7) |
|
Лимфодиссекция без лимфодиссекции |
9 (50,0) |
1 (7,7) |
117 (25,4) |
|
СБ |
5 (27,8) |
4 (30,8) |
116 (25,2) |
|
СЛД |
4 (22,2) |
8 (61,5) |
228 (49,5) |
|
Правосторонняя локализация |
СЛЭ (n-18) |
БЛЭ (n-13) |
ЛЭ (n-256) |
|
pN N0 |
14 (77,8) |
11 (84,6) |
176 (68,8) |
|
N1 |
1 (5,5) |
2 (15,4) |
41 (16,0) |
|
N2 |
3 (16,7) |
– |
39 (15,2) |
|
Лимфодиссекция без лимфодиссекции |
9 (50,0) |
1 (7,7) |
68 (26,6) |
|
СБ |
5 (27,8) |
4 (30,8) |
56 (21,9) |
|
СЛД |
4 (22,2) |
8 (61,5) |
132 (51,6) |
Клинические и патологические характеристики пациентов по группам исследования
Распределение больных по критерию pN и объему лимфодиссекции
выявлено поражение верхних междолевых лимфоузлов во втором – поражение верхних и нижних междолевых лимфоузлов.
Отдаленные результаты были прослежены до 1.01.2015г. В конце периода наблюдения, 203 пациента (41,3%) умерли. Летальный исход наступил у 7 из 18 (38,9%) в группе СЛЭ, у 3 из 13 (23,1%) в группе БЛЭ и 193 из 461 (41,9%) в контрольной группе. Пятилетняя общая выживаемость составила 64,1% в группе СЛЭ, 74,9% в группе БЛЭ и 62,0% в контрольной группе (ЛЭ).
Отдаленные результаты лечения в зависимости от выполненного объема оперативного лечения приведены на рисунке 1.
Пятилетняя выживаемость была выше при БЛЭ – 74,9%, чем при СЛЭ – 64,1% и ЛЭ – 62,0%. Однако данное различие было статистически незначимым (р=0,268).
Для устранения потенциальных отличий в лимфаденэктомии в зависимости от стороны поражения, мы провели анализ отдаленных результатов для правосторонней локализации опухоли.
В конце периода наблюдения, 114 пациентов из 287 (39,7%) с правосторонней локализацией опухоли умерли. Летальный исход наступил у 7 из 18 (38,9%) в группе СЛЭ, у 3 из 13 (23,1%) в группе БЛЭ и 104 из 287 (36,2%) в контрольной группе. Пятилетняя общая выживаемость составила 64,1% в группе СЛЭ, 74,9% в группе БЛЭ и 62,9% в контрольной группе (рис. 2). Различия в выживаемости при правосторонней локализации опухоли также были статистически незначимыми (р=0,293).
Прогрессирование заболевания было у 131 пациента. Уровень рецидива заболевания был 27,7% (5/18), 15,4% (2/13) и 26,9% (124/461) в группах СЛЭ, БЛЭ и ЛЭ соответственно. Внутригрудные рецидивы выявлены в 15,4% (2/18), 0 (0/13) и 6,3% (29/461) в группах СЛЭ, БЛЭ и ЛЭ соответственно. При этом внутригрудные рецидивы возникли у пациентов с СЛЭ, которым не выполнили медиастинальную лимфодиссекцию. В группе больных с ЛЭ, которым выполнили СЛД, внутри-грудные рецидивы развились только в 2,2% (5/228). Отдаленные метастазы были диагностированы в 16,7% (3/18), 15,4% (2/13) и 20,6% (95/461) при СЛЭ, БЛЭ и ЛЭ соответственно.
Многофакторный анализ показал три независимых прогностических фактора, влияющих на отдаленные результаты: возраст (р=0,01), патологическая стадия (р<0,01), пол (р=0,008). При этом результаты в группах СЛЭ и ЛЭ были очень схожими.
Размер опухоли, сторона поражения, дифференцировка опухоли, общее число пораженных лимфоузлов не имели прогностическое значение на выживаемость.
Обсуждение
Среди небольшого количества сообщений, касающихся прогноза НМРЛ с локализацией в средней доле, ни один из
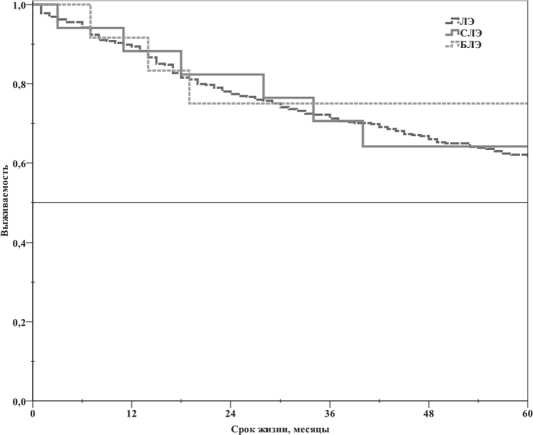
Рис. 1. Отдаленные результаты лечения исследуемой популяции пациентов. СЛЭ – средняя лобэктомия. БЛЭ – билобэктомия, ЛЭ – лобэктомия
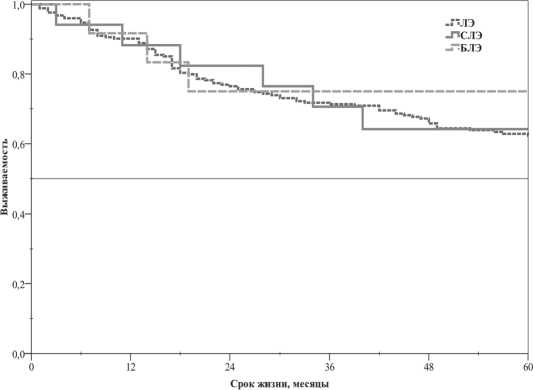
Рис. 2. Отдаленные результаты лечения исследуемой популяции пациентов с правосторонней локализацией опухоли. СЛЭ - средняя лобэктомия. БЛЭ – билобэктомия, ЛЭ – лобэктомия них ориентирован на эффективность стандартной средней лобэктомии. Настоящее исследование включает в себя 18 СЛЭ, представляющих 3,7% всех анатомических резекций легкого, выполненных в онкологических учреждениях Югры за исследуемый период. Этот показатель соответствует данным литературы [4–7], хотя в них предлагались более широкие резекции легкого, чем СЛЭ.
В нашей серии, 5-летняя общая выживаемость после СЛЭ составила 64,1%. H. Miura et al. [5] сообщили о 31 случае НМРЛ с различными объемами оперативного лечения вплоть до пневмонэктомии. Разницы в выживаемости в за- висимости от локализации опухоли в средней или других долях авторами не было получено. Однако частота эксплоративных торакотомий при поражении средней доли была выше из-за распространения опухоли на соседние доли и диссеминацией по плевре. В недавно опубликованном ретроспективном исследовании 13650 пациентов с Т1-2 НМРЛ, перенесших резекцию, B.A. Whitson et al. [11] исследовали прогностическое значение локализации опухоли. Разницы в ОВ не было выявлено, хотя при многофакторном анализе рак-специфическая смертность была выше у пациентов, перенесших СЛЭ. В нашем исследовании ОВ при СЛЭ была аналогична с контрольной группой, однако уступила группе пациентов, перенесших БЛЭ. При этом разница была статистически незначимая. Поскольку зоны лимфодиссекции существенно отличаются от стороны грудной клетки, мы провели анализ для правосторонней локализации опухоли.
Пятилетняя ОВ при правосторонней локализацией опухоли была идентичная при СЛЭ и в контрольной группе (ЛЭ), однако была лучше в группе БЛЭ.
Возможное объяснение либо в неоптимальной лимфо-диссекции, выполненной в группе СЛЭ или анатомические особенности, присущие средней доли (например, ранняя инфильтрация висцеральной плевры), в результате чего СЛЭ уступает БЛЭ в онкологической эффективности.
В исследовании M.S. Ludwig et al. отмечено прогностическое значение объема лимфодиссекция [12]: в большом исследовании при I стадии НМРЛ отмечена значимая корреляция между выживанием и количеством резецированных лимфатических узлов.
На возможность поражения верхнедолевых лимфоузлов (9.2%) сообщается в исследовании M. Sato et al. [13]. Y. Sakao et al. [14] изучили прогностическое влияние метастатического поражения различных групп лимфоузлов у 45 пациентов с pN1-2 поражением при НМРЛ средней доли. Среди pN1 групп лимфатических узлов, прилегающих к среднедолевому бронху, худший прогноз был при поражении нижних междолевых лимфоузлов. При поражении медиастинальных лимфоузлов отрицательное прогностическое влияние на ОВ была при поражении наивысших средостенных лимфоузлов.
Выводы
Полученные нами результаты с одной стороны указывают на преимущество билобэктомии по сравнению с СЛЭ, с другой стороны общая выживаемость при СЛЭ аналогична при выполнении лобэктомии при поражении опухолью верхней или нижней доли. По нашему мнению СЛЭ следует применять при небольших (T1-2) опухолях, не прорастающих в соседние доли с обязательной СЛД. Оптимальным хирургическим лечением более крупных опухолей средней доли с прорастанием в соседнюю долю будет билобэктомия с СЛД. Полученные нами результаты требуют проведения дополнительного проспективного исследования с целью оценки эффективности объема хирургического лечения при НМРЛ средней доли.
Список литературы Средняя лобэктомия при немелкоклеточном раке легкого: эффективность и отдаленные результаты
- Трахтенберг А.Х., Чиссов В.И. Рак легкого: руководство, атлас. ГЭОТАР-Медиа, 2009. С. 484
- Manser R., Wright G., Hart D., Byrnes G., Campbell D.A. Surgery for early stage non-small cell lung cancer//Cochrane Database Syst Rev 2005;1:CD004699.
- Rivera C., Mordant P., Pricopi C., Arame A., Foucault C., Dujon A. et al. Is the rate of pneumonectomy higher in right middle lobe lung cancer than in other right-sided locations?//Ann Thorac Surg 2014;97:402-7.
- Riquet M., Dupont P., hidden G., Debesse B. Lymphatic drainage of the middle lobe of the adult lung.//Surg Radiol Anat 1990;12:231-3.
- Miura H., Kato H., Konaka C., Usuda J., Uchida O., Taira O. Primary Lung Cancer of the middle lobe. Is its prognosis poor?//Lung Cancer 1996;14:273-9.
- Peleg H., Antkowiak J.G., Lane W.W., Regal A.M., Takita H. Prognosis after resection of non-small cell lung cancer of the right middle lobe//J Surg Oncol 1987;35:230-4.
- Freise G., Gabler A., Liebig S. Bronchial carcinoma and longterm survival. Retrospective study of 433 patients who underwent resection//Thorax 1978;33:228-34.
- Bedini A.V., Cataldo I., Valente M., Alloisio M., Pastorino U., Ravasi G. Surgical prognosis in stage I bronchogenic carcinoma of the middle lobe//Scand J Thorac Cardiovasc Surg 1989;23:283-4.
- Colice G.L., Shafazand S, Griffin J.P., Keenan R., Bolliger C.T. American College of Chest Physicians. Physiologic evaluation of the patient with lung cancer being considered for resectional surgery: ACCP evidenced-based clinical practice guidelines (2nd edition)//Chest 2007;132(3 Suppl):S161-77.
- Travis W.D., Colby T.V., Corrin B., Shimosato Y., Brambilla E. Histological Typing of Lung and Pleural Tumors, World Health Organization International Histological Classification of Tumors. Berlin: Springer, 1999.
- Whitson B.A., Groth S.S., Andrade R.S., Habermann E.B., Maddaus M.A., D'Cunha J. T1/T2 non-small-cell lung cancer treated by lobectomy: does tumor anatomic location matter?//J Surg Res 2012;177:185-90.
- Ludwig M.S., Goodman M., Miller D.L., Johnstone P.A. Postoperative survival and the number of lymph nodes sampled during resection of node-negative non-small cell lung cancer//Chest 2005;128:1545.
- Sato M., Saito Y., Aikawa H., Sakurada A., Sagawa M., Tanita T. et al. Involvement of the #12u lymph nodes around the upper lobe bronchi in patients with lungcancer of the right middle lobe, right lower lobe, or left lower lobe//Surg Today 1999;29:238-42.
- Sakao Y., Okumura S., Mingyon M., Uehara H., ishikawa Y., Nakagawa K. The impact of superior mediastinal lymph node metastases on prognosis in non-small cell lung cancer located in the right middle lobe//J Thorac Oncol 2011;6:494-9.


