Структурно-функциональное состояние гемоглобина у телят-гипотрофиков (Bos taurus) под влиянием препарата интерамина
Автор: Шабунин С.В., Востроилова Г.А., Паршин П.А., Сулин В.Ю., Мартынова А.В., Хохлова Н.А., Шабанов Д.И., Пархоменко Ю.С., Вели А.А.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Тканевые препараты
Статья в выпуске: 2 т.60, 2025 года.
Бесплатный доступ
Коррекция морфофункциональной незрелости телят с признаками антенатальной гипотрофии и коморбидными патологиям остается одной из актуальных проблем в животноводстве. Структурно-функциональные изменения гемоглобина (Hb) служат важными диагностическими критериями физиологического состояния животного в процессе роста. У телят-гипотрофиков наблюдается нарушение обменных процессов и кислородтранспортной функции крови, что способно приводить к замедлению замены фетального гемоглобина (HbF) на дефинитивный гемоглобин взрослых животных (HbA). Коррекция таких состояний с помощью различных препаратов и механизмы их действия продолжают оставаться предметом изучения. Мы впервые выявили влияние препарата интерамин, содержащего гидрофильную криофракцию селезенки крупного рогатого скота, рекомбинантные видоспецифичные (бычьи) альфа- и гамма-интерфероны (IFN-α и IFN-γ) и витамины А, Е, на состояние кроветворной системы у телят-гипотрофиков, которое оценивали по спектральным характеристикам гемоглобина в гемолизате периферической крови. Содержание фетального гемоглобина в крови телят определяли спектрофотометрически по локальным максимумам светопоглощения растворов гемоглобина в ультрафиолетовом диапазоне. С использованием базы данных Uniprot проведен сравнительный анализ ароматических аминокислотных остатков в первичной структуре β- и γ-субъединиц гемоглобинов Bos taurus и установлено различие в количественном содержании триптофана в обеих молекулах. В результате исследования впервые установлены изменения максимумов светопоглощения в УФ-диапазоне гемоглобина телят-гипотрофиков при применении интерамина. При подкожном введении новорожденным телятам-гипотрофикам интерамина в дозе 1 мл/10 кг массы животного впервые зарегистрировано смещение локального максимума светопоглощения гемоглобина в УФ-диапазоне от 270 нм к 275 нм. При этом такое изменение локальных максимумов наблюдалось уже на 7-е сут у телят-гипотрофиков, которым начали вводить комплексный препарат, в то время как применение препарата сравнения - Биферона-Б телятам-гипотрофикам по такой же схеме индуцировало смещение локального максимума светопоглощения гемоглобина только к 30-м сут неонатального развития и не наблюдалось к этому времени у телят-гипотрофиков без применения препаратов. Основываясь на данных литературы, предложен гипотетический механизм обнаруженных явлений. Возможно, что интерамин благодаря иммуномодулирующему эффекту ускоряет замещение фетального гемоглобина на дефинитивный у телят-гипотрофиков и оказывает корректирующее действие на кислородтранспортную функцию крови.
Телята-гипотрофики, фетальный гемоглобин, уф-спектры поглощения, иммуномодуляция, тканевые препараты, рекомбинантные интерфероны, интерамин, ароматические аминокислоты
Короткий адрес: https://sciup.org/142245115
IDR: 142245115 | УДК: 636.28:619:615.36 | DOI: 10.15389/agrobiology.2025.2.382rus
Structure and functional state of hemoglobin in hypotrophic calves (Bos taurus) as influenced by Interamin, a complex drug
Correction of morphofunctional immaturity of calves with signs of antenatal hypotrophy and comorbid pathologies remains one of the urgent problems in animal husbandry. Structural and functional changes in hemoglobin (Hb) serve as important diagnostic criteria for the physiological state of an animal during growth. Hypotrophic calves have disorders of metabolic and oxygen transport function of the blood, which can lead to a slowdown in the replacement of fetal hemoglobin (HbF) with definitive hemoglobin (HbA) of adult animals. Correction of such conditions using various drugs and their mechanisms of action continue to be the subject of study. We have revealed for the first time the effect of the preparation Interamin, containing hydrophilic cryofraction of cattle spleen, recombinant species-specific (bovine) alpha- and gamma-interferons (IFN-α and IFN-γ) and vitamins A, E, on the state of the hematopoietic system in hypotrophic calves, which was assessed by the spectral characteristics of hemoglobin in the hemolysate of peripheral blood. Using the Uniprot database, a comparative analysis of aromatic amino acid residues in the primary structure of β- and γ-subunits of Bos taurus hemoglobin was carried out and a difference in the quantitative content of tryptophan in both molecules was established. As a result of the study, changes in the maximum light absorption in the UV range of hemoglobin in hypotrophic calves were established for the first time when using interamin. When interamin was administered subcutaneously to newborn hypotrophic calves at a dose of 1 ml/10 kg of animal weight, a shift in the local maximum of hemoglobin light absorption in the UV range from 270 nm to 275 nm was registered for the first time. Moreover, such a change in local maxima was observed already on the 7th day in hypotrophic calves that began to be administered the complex drug. While the use of the comparison drug Biferon B to hypotrophic calves in the same scheme induced a shift in the local maximum of hemoglobin light absorption only by the 30th day of neonatal development and was not observed by this time in hypotrophic calves without the use of drugs. Based on literature data, hypothetical mechanisms of the observed phenomena are proposed. It is possible that interamin, due to its immunomodulatory effect, accelerates the replacement of fetal hemoglobin with definitive hemoglobin in hypotrophic calves and has a corrective effect on the oxygen-transport function of the blood.
Текст научной статьи Структурно-функциональное состояние гемоглобина у телят-гипотрофиков (Bos taurus) под влиянием препарата интерамина
Перинатальные патологии у крупного рогатого скота, возникающие вследствие дисфункции системы мать—плацента—плод, остаются одним из негативных факторов в животноводстве (1). Клинически такие патологии проявляются рождением морфологически и функционально незрелого потомства с признаками антенатальной гипотрофии и коморбидных нарушений — анемии и иммунодефицитов (2, 3). В связи с высокими экономическими затратами при воспроизводстве крупного рогатого скота коррекция морфофункциональных патологий у молодняка и его дальнейшее использование в хозяйственном процессе представляется актуальной задачей (1).
Фетальный гемоглобин (HbF, fetal) — главный гемоглобин плода. Глобиновая часть HbF структурно представлена двумя α - и двумя γ -цепями. Экспрессия фетального гемоглобина служит ткане- и стадийно-специфическим маркером онтогенеза у крупных млекопитающих (4). У новорожденного теленка доля HbF составляет около 70 %. Затем в течение примерно
60 сут неонатального периода фетальный гемоглобин замещается на дефинитивный (HbA, adult) (5-7). При патологиях, сопряженных с нарушением обменных процессов и кислородтранспортной функции крови, к которым относят анемию новорожденных телят, в неонатальном периоде у животных наблюдается высокое содержание HbF и происходит замедление процессов его замены на взрослый гемоглобин (8, 9). В условиях гипоксии на фоне значительного усиления эритропоэза возникает адаптивная реакция эритроцитов, связанная с активацией гена γ -цепи глобина (фетальной γ -субъеди-ницы) индуцируемым гипоксией фактором 1 (hypoxia-inducible factor 1, HIF-1), что приводит к повышению количества HbF (9-11). В связи с этим выявление HbF в крови может быть использовано для диагностики патологий, сопряженных с гипоксией (12, 13).
Таким образом, структурно-функциональные изменения гемоглобина (Hb) рассматриваются как начальные проявления ряда патологических процессов и важные критерии физиологического состояния животного в процессе роста (14). При этом закономерности изменения форм гемоглобина у животных как при патологии, так и при ее фармакокоррекции остаются до конца не выясненными.
В представленной работе нами впервые проведен сравнительный анализ спектров поглощения гемоглобина телят-гипотрофиков в неонатольный период при курсовом применении комплексного препарата интерамина. Исследуемый комплексный препарат интерамин (разработан в ФГБНУ Всероссийский научно-исследовательский ветеринарный институт патологии, фармакологии и терапии) содержит гидрофильную криофракцию селезенки крупного рогатого скота, рекомбинантные видоспецифичные (бычьи) альфа- и гамма-интерфероны (IFN- α и IFN- γ ) и витамины А и Е. В качестве препарата сравнения мы использовали Биферон-Б (разработка ООО Научно-производственный центр «ПроБиоТех», Республика Беларусь), учитывая сходство действующих веществ, входящих в его состав и содержащихся в исследуемом нами препарате, и присутствие цитокинового компонента (в 1 см3 биопрепарата содержится не менее 1,0½104 МЕ суммарной антивирусной активности смеси белков альфа- и гамма-интерферонов бычьих рекомбинантных).
Цель работы заключалась в определении влияния комплексного препарата интерамина на структурно-функциональное состояние гемоглобина и содержание фетального гемоглобина в крови телят-гипотрофиков как показателя развития кроветворной системы.
Методика. Эксперимент проводили на телятах красно-пестрой масти голштинской породы ( n = 40), принадлежащих ООО «ЭкониваАгро» (с. Коршево, Бобровский р-н, Воронежская обл.). Отобранных животных с признаками антенатальной гипотрофии 2-й степени разделили по принципу парных аналогов на три группы по 10 гол. в каждой. В IV группу вошли 10 телят-нормотрофиков. Условия опыта соответствовали действующим международным и российским законодательным актам (Директива 2010/63/EU от 22.09.2010; Европейская конвенция ETS 123, Strasbourg, 1986; ГОСТ 332162014), а также требованиям биоэтической комиссии ФГБНУ ВНИВИПФиТ.
Телятам из I группы ( n = 10, гипотрофики) вводили подкожно комплексный препарат интерамин (1 мл на 10 кг массы животного, 4-кратно, 1-е, 3-и, 8-14-е, 18-24-е сут жизни), телятам из II группы ( n = 10, телята-гипотрофики) — подкожно препарат Биферон-Б по той же схеме; в III ( n = 10, контроль 1, телята-гипотрофики) и IV ( n = 10, контроль 2, телята-нормотрофики) группах препараты не применяли.
У всех телят на 1-е, 7-е и 30-е сут жизни в утреннее время до кормления брали кровь в объеме 10 мл из яремной вены с помощью вакуумной системы отбора в пробирки с К3 EDTA. Полученные образцы помещали в термостабильный контейнер с температурой +4-6 °С и транспортировали до места исследования в течение 2 ч с момента отбора.
Для получения водных растворов гемоглобина венозную кровь (2 мл) разбавляли до 10 мл изотоническим раствором NaCl (154 мМ). Суспензию эритроцитов центрифугировали (10 мин, 5500 об/мин, +12 ° С), супернатант удаляли. Процедуру отмывания эритроцитов в 10 мл физиологического раствора повторяли трижды. После осмотического гемолиза 0,5 мл отмытых эритроцитов в 5,5 мл дистиллированной воды в течение 20 мин мембраны эритроцитов осаждали центрифугированием при 5500 об/мин 30 мин. После центрифугирования супернатант, содержащий гемоглобин, переносили в пробирки и разбавляли до рабочих концентраций, используя 0,01 М фосфатный буфер (рН = 7,0) (8).
Спектры поглощения водных растворов гемоглобина регистрировали на спектрофотометре Shimadzu UV-1700 (PC) («Shimadzu», Япония) в диапазоне длин волн 240-320 нм со спектральной шириной щели 1 нм и шагом сканирования 0,1 нм.
Статистическая обработка данных включала расчет средних значений длин волн локальных максимумов УФ-светопоглощения ( М) и их среднеквадратического отклонения ( ± SD). Для обоснования межгрупповых различий локальных максимумов УФ-светопоглощения в области 270 нм и 275 нм использовали критерий χ 2 для многопольных таблиц. В результатах исследования представлены межгрупповые различия локальных максимумов УФ-светопоглощения гемоглобина в области 270 нм и 275 нм для критического χ 2 = 16,27 при df = 3 на уровне значимости p < 0,001.
Результаты. Анализ базы данных Uniprot аминокислотных последовательностей в первичной структуре у-глобина HbF и р-субъединицы HbA показал различия по остаткам 22 аминокислот, в том числе по ароматическим аминокислотам, которые относят к хромофорам II типа, обладающим светопоглощением в УФ-диапазоне (табл.).
Количественные различия в содержании ароматических аминокислотных остатков в р -субъединице дефинитивного гемоглобина HbA и у -субъединице фетального гемоглобина HbF коров ( Bos taurus ), оказывающие влияющие на спектральные свойства в УФ-диапазоне
Субъединица Phe Tyr Trp
Р -Субъединица HbA 10 2 2
у -Субъединица HbF 10 2 1
Примечание. Показатели получены с использованием базы данных Uniprot
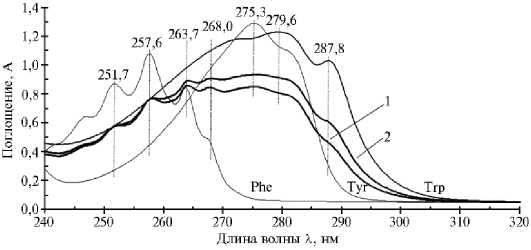
Рис. 1. Характерные спектры светопоглощения (A — оптическая плотность) 0,01 М водных растворов фенилаланина (Phe) , тирозина (Tyr) и триптофана (Trp) и аддитивных моделей у-субъеди-ницы HbF (Phe+Tyr+Trp) (1) и р-субъединицы HbA (Phe+Tyr+Trp+Trp) (2 ), определяющие особенности светопоглощения HbF и HbA. Спектрофотометр Shimadzu UV 1700 (PC) («Shimadzu», Япония).
Поскольку максимум светопоглощения в области 240-300 нм обусловлен суперпозицией хромофоров боковых групп ароматических и гетероциклических аминокислотных остатков, входящих в состав гемоглобина (15), мы провели спектральный анализ водных растворов этих аминокислот. В результате зарегистрированы максимумы светопоглощения водных растворов (pH = 7,0) ароматических аминокислот при следующих длинах волн: для фенилаланина (Phe) λ max = 257,6 нм с двумя выраженными пиками в области 251,5 нм и 263,7 нм, для тирозина (Tyr) λ max = 275.,3 нм, для триптофана (Trp) λ max = 279,6 нм и пиком при 287,8 нм (рис. 1).
По результатам сравнительного анализа УФ-спектров водных растворов ароматических аминокислот и их аддитивных спектров можно предположить, что пики при 251,7 нм, 257,6 нм и 263,7 нм обусловлены светопоглоще-нием фенилаланина. Локальные максимумы с длинами волн λ max = 268,0 нм и λ max = 275,3 нм и перегибы при λ = 279,6 нм и λ = 287,8 нм формируются как суперпозиции максимумов светопоглощения тирозина и триптофана (см. рис. 1).
Учитывая, что γ -субъединица фетального бычьего гемоглобина содержит только один остаток триптофана, а в β -субъединице взрослого бычьего гемоглобина два остатка триптофана, можно предположить, что УФ-спектры растворов фетального и взрослого гемоглобинов будут иметь разные максимумы светопоглощения в области 240-320 нм.
Ранее мы выявили различия спектральных характеристик водных растворов оксигемоглобина телят в неонатальный период при нормотрофическом и гипотрофическом развитии (8). К возрасту 1 мес у клинически здоровых телят-нормотрофиков максимум УФ-светопоглощения в коротковолновом диапазоне смещается к 274,8 нм и приближается к параметрам HbA. У телят с гипотрофическим развитием по данным спектрального анализа максимум спектра поглощения не изменяется и соответствует 269,8 нм, что, по нашему мнению, свидетельствует о сохранении в эритроцитах телят-гипотрофиков фетального гемоглобина (8). Снижение интенсивности све-топоглощения в коротковолновом диапазоне у телят с гипотрофией, по всей видимости, связано с развитием анемии.
Проведенный нами анализ спектров поглощения водных растворов гемоглобина телят в ранний постнатальный период (до 30 сут) в диапазоне длин волн 240-320 нм выявил два локальных максимума в области около 270 нм и 275 нм. Таким образом, мы получили подтверждение, что к 30-м сут развития у телят-нормотрофиков локальный максимум поглощения водных растворов гемоглобина в диапазоне длин волн 240-320 нм, отражающий структурные свойства Hb, смещался от 270 нм к 275 нм. Основываясь на аддитивной модели спектров гемоглобина, мы предполагаем, что первый локальный максимум в области 270 нм коррелирует с содержанием фетального гемоглобина HbF, второй в области 275 нм — дефинитивного HbA (8, 15).
На основании сравнительного анализа локальных максимумов в области 270 нм было установлено, что у телят-нормотрофиков и телят-гипо-трофиков, получавших Биферон-Б, указанный пик исчезает к 30-м сут развития. У гипотрофиков, получавших интерамин, максимум при λ max = 270 нм не регистрировался с 7-х сут развития. Учитывая связь между локальным максимумом в области 270 нм и наличием в крови фетального гемоглобина, можно предположить, что у нормотрофиков и гипотрофиков, которым вводили Биферон-Б, к 30-м сут жизни происходит постепенная замена HbF на взрослый гемоглобин HbA. У гипотрофиков, получавших интерамин, этот процесс ускоряется (рис. 2).
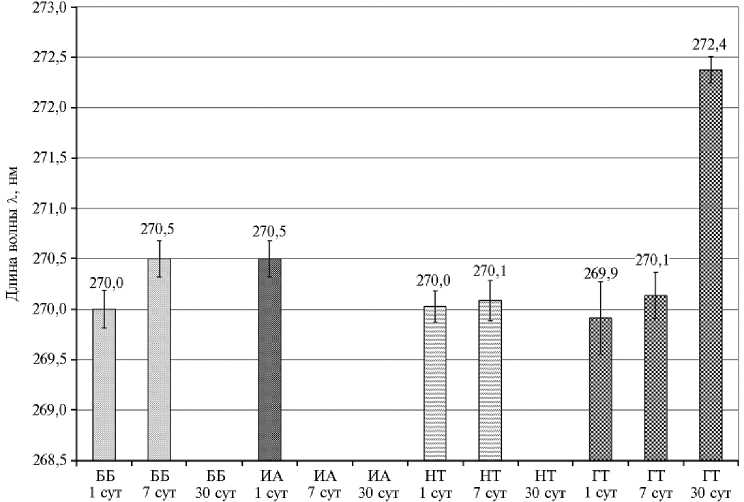
Рис. 2. Влияние гипотрофии и ее фармакокоррекции интерамином или Бифероном-Б на положение локальных максимумов светопоглощения водных растворов Hb в диапазоне длин волн 268272 нм : ИА — интерамин (I группа, n = 10); ББ — Биферон-Б (II группа, n = 10); ГТ — телята-гипотрофики (III группа, n = 10); НТ — телята-нормотрофики (IV группа, n = 10); 1, 7, 30 сут — время после начала применения препаратов; спектрофотометр Shimadzu UV 1700 (PC) («Shimadzu», Япония) ( M ±SD, телята красно-пестрой масти голштинской породы, Воронежская обл., 2022 год).
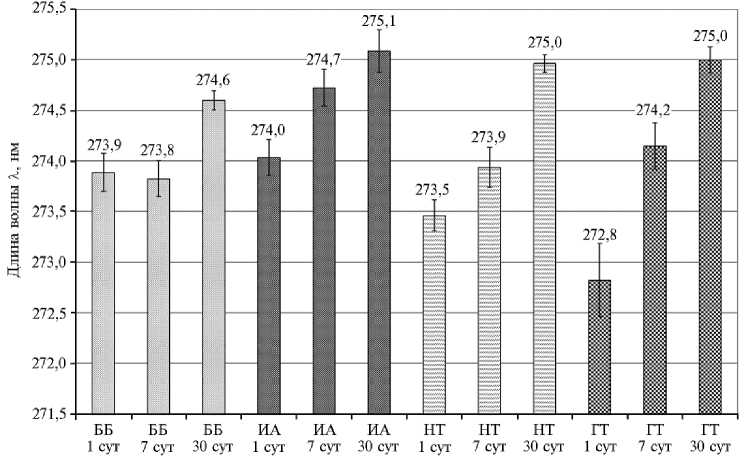
Рис. 3. Влияние гипотрофии и ее фармакокоррекции интерамином или Бифероном-Б на положение локальных максимумов светопоглощения водных растворов Hb в диапазоне длин волн 273275 нм : ИА — интерамин (I группа, n = 10); ББ — Биферон-Б (II группа, n = 10); ГТ — телята-гипотрофики (III группа, n = 10); НТ — телята-нормотрофики (IV группа, n = 10); 1, 7, 30 сут — время после начала применения препаратов; спектрофотометр Shimadzu UV 1700 (PC) («Shimadzu», Япония) ( M ±SD, телята красно-пестрой масти голштинской породы, Воронежская обл., 2022 год).
Сравнительный анализ второго локального максимума в области 275 нм показал, что у нормотрофиков (IV группа) и гипотрофиков (I группа) 386
при использовании интерамина, в отличие от животных, которые получали Биферон-Б (II группа), этот пик становится выраженным уже к 7-м сут развития. У нормотрофиков (IV группа) и гипотрофиков (III группа) локальный максимум в области 275 нм регистрировался к 30-м сут (рис. 3).
Таким образом, сравнение спектров поглощения водных растворов гемоглобина показало, что локальный максимум в области 270 нм у телят-нормотрофиков (IV группа) не регистрируется к 30-м сут жизни (см. рис. 2), а у телят-гипотрофиков (I группа) применение интерамина нивелирует первый локальный максимум в области 270 нм к 7-м сут и ускоряет смещение локальных максимумов в область 275 нм, которое происходит также на 7-е сут жизни (см. рис. 3). Анализ спектров в диапазоне длин волн 250-290 нм в целом позволяет заключить, что у телят-гипотрофиков интерамин сокращает сроки замены фетального гемоглобина на взрослый HbA.
У многих видов животных, в том числе у крупного рогатого скота, в неонатальный период онтогенеза в эритроцитах происходит переключение синтеза γ -цепи гемоглобина на β -цепь, благодаря чему число эритроцитов, продуцирующих HbF, постепенно уменьшается, в то время как число эритроцитов, синтезирующих HbA, возрастает (16). Конститутивность работы систем транскрипции и регуляции транскрипции генов Hb позволяет предполагать сходство этих процессов у многих животных разных видов (17). У млекопитающих наиболее изученным белком — репрессором синтеза γ -цепи гемоглобина является белок BCL11A (B cell lymphoma 11A), который способен изменять экспрессию генов через ремоделирование хроматина благодаря наличию в структуре BCL11A мотивов типа «цинковые пальцы». Помимо регуляции синтеза гемоглобинов, BCL11A влияет на развитие мозга, а также функционирование гематопоэтических и иммунных клеток. Исследования in vitro и in vivo показывают постепенное повышение активности BCL11A и его трансляции de novo в эритроидных клетках после рождения (16). Многие другие транскрипционные факторы (GATA1, KLF1, SOX6 и MYB6) и регуляторные микроРНК также способны влиять на транскрипцию γ - и β -цепи гемоглобинов и образование HbF как непосредственно, так и через воздействие на BCL11A (16-19). На синтез HbF также влияет парциальное давление O 2 в тканях. Так, в исследовании на эритропоэтических стволовых клетках человека in vitro при снижении содержания O 2 выявлено значимое повышение числа эритроцитов, содержащих HbF (20). Вероятно, такие изменения регулируются действием HIF-1 α , поскольку показано его влияние на некоторые транскрипционные факторы и медиаторы при эритропоэзе, например EPO (Erythropoietin) (21).
Одним из ключевых регуляторов многих эритроидных генов служит транскрипционный фактор KLF1 (Kruppel-like factor 1), который значительно повышает экспрессию β-цепей гемоглобинов и активирует белок-репрессор синтеза γ-цепи BCL11A (22). Исследования продемонстрировали отсутствие прямой зависимости экспрессии KLF1 от парциального давления О2 и действия HIF-1α (20). Таким образом, KLF1 потенциально мог бы выступать в качестве переключателя синтеза HbF на синтез HbA даже в условиях локальной гипоксии, поскольку сверхэкспрессия KLF1 приводит к более раннему переключению экспрессии генов γ-цепи гемоглобинов на экспрессию генов β-цепи (23). Кроме того, KLF1 является регулятором множества клеточных метаболических путей (клеточный цикл, апоптоз, регулирование цитоскелета, синтез гемма), необходим для дефинитивного эритропоэза и определяет первичный ответ клеток на стрессовые воздействия, активируя системы антитоксической защиты (цитохом P450-оксидо- редуктазу) (17). При этом увеличение экспрессии KLF1 возможно при воздействии активатора эритропоэза EPO (24).
Таким образом, задержка в переключении с синтеза γ -цепи на синтез β -цепь в эритроидных клетках у телят-гипотрофиков может быть вызвана состоянием анемии и гипоксии, поскольку антенатальная гипотрофия телят сопровождается нарушениями в кровеносной системе животных. Наблюдается диссеминированное внутрисосудистое свертывание крови, гипохромия и другие патологические состояния, которые возникают вследствие дисфункции кроветворных органов и трансмембранной потери гемоглобина (25). В свою очередь, нарушения в системе транспортировки кислорода могут поддерживаться воспалительной супрессией нормального эритропоэза со стороны иммунной системы (21). Так, IFN- β репрессирует развитие эритроидных клеток (26), а провоспалительный фактор TNF- α способен ингибировать эритропоэз посредством различных механизмов, например ингибируя экспрессию GATA1-зависимых генов, что приводит к снижению дифференцировки эритроцитов, регулируя экспрессию мРНК ЕРО в почках, блокируя передачу сигнала от HIF-1 α при HIF-1 α -индуцированной экспрессии ЕРО (21). При этом факторы регуляции транскрипции TGF β и SCF (Stem Cell Factor) индуцируют синтез γ -цепей гемоглобина и образование HbF (27). Поскольку при гипотрофии у новорожденных телят наблюдаются нарушения функций иммунной системы с образованием большого количества провоспалительных цитокинов и снижением содержания иммуннорегуля-торов (28), число эритроцитов c HbF у таких животных может оставаться высоким. Вероятные причины этого — продолжающаяся гипоксия, воспалительная репрессия ЕРО-индуцированного эритропоэза, сохранение продукции HIF-1 α , TGF β и SCF, что в эритроидных клетках приводит к снижению экспрессии KLF1 и уменьшению активности BCL11A, вследствие чего не подавляется синтез γ -цепей гемоглобина.
В настоящее время остается не до конца выясненным механизм воздействия интерамина на организм телят. Полученные данные позволяют предполагать влияние IFN- α и IFN- γ , поскольку применение содержащего их препарата Биферон-Б также приводило к коррекции положения характерных для HbF максимумов в спектре поглощения у телят-гипотрофиков. В то же время ускоренное по сравнению с нормотрофиками исчезновение пиков, характерных для HbF, уже на 7-е сут может свидетельствовать о иммуномодуляции и активации кроветворения и антиоксидантной системы интерамином благодаря тканевому компоненту препарата (29). Таким образом, возможно, интерамин благодаря своему влиянию на эритропоэз может индуцировать переключение экспрессии с γ -цепи гемоглобинов на β -цепи. Сообщалось, что такие иммуномодуляторы, как рапамицин, ресвератрол, талидомид, индуцировали образование HbF, подавляя или стимулируя эритропоэз (30). Тканевой иммуномодулирующий препарат аминоселетон на основе селезенки крупного рогатого скота также стимулировал эритропоэз и активность антиоксидантной защиты у коров и свиней (29). Иммунокорректоры Пролам и Иммунофан индуцировали снижение количества TNF α , но увеличивали концентрацию IL1 β в плазме крови у телят-гипотро-фиков. При этом наблюдались некоторые различия в уровнях других цитокинов при иммунном ответе (28).
Различия в действии препаратов на эритропоэз и продукцию цитокинов свидетельствуют о существовании разных механизмов, обеспечивающих иммуномодулирующий эффект и успешную коррекцию патологий крови и обмена кислорода. Один из гипотетических механизмов улучшения состояния телят при анемии и гипоксии под влиянием корректирующих препаратов предполагает прямое изменение концентрации цитокинов, например 388
снижение продукции TNF α , приводящее к увеличению синтеза EPO, стимуляции нормального эритропоэза, повышению парциального давления О 2 в тканях и, в итоге, к синтезу преимущественно HbA. Другим таким механизмом, вероятно, может выступать усиление стресс-индуцированного эритропоэза в SEP (stress erythroid progenitors), которые находятся в селезенке и обеспечивают альтернативные клеточные ответы при воздействии цитокинов (21). Так, провоспалительные цитокины TNF α и IL1 β увеличивают in vitro пролиферацию SEP (в отличие от эритроидных предшественников в костном мозге), а IFN- γ вовлечен в рекрутирование моноцитов для расширения ниши SEP в селезенке (21). Возможно, активность стресс-ин-дуцированного эритропоэза, которую стимулируют препараты-иммунномо-дуляторы, способна в некоторой степени компенсировать супрессию эритропоэза, вызванную острым воспалением, и улучшать состояние телят-гипо-трофиков при анемии и гипоксии, что снизит продукцию HIF-1 α и приведет к переключению программ транскрипции в клетках-предшественниках эритроцитов c синтеза HbF на HbA.
В наибольшей степени проблемы индуцированного гипоксией изменения содержания HbF и HbA в крови в настоящее время изучены у человека (13, 18, 31). Известно, что ряд таких факторов, как гестационный возраст, морфофункциональная зрелость ребенка, особенности внутриутробного развития, характер родоразрешения, течение периода ранней адаптации и воздействие токсических веществ оказывают влияние на сроки смены гемоглобина новорожденных детей (18, 31). Однако данных о причинах задержки смены HbF на HbA у новорожденных все еще недостаточно. Плацентарная недостаточность и хроническая внутриутробная гипоксия, которые могут сопровождать патологические состояния во время беременности, позволяют сделать заключение о неблагоприятном влиянии гипоксических состояний на эритропоэз плода (31). У новорожденных, подвергавшихся хронической внутриматочной гипоксии, и недоношенных детей наблюдалось достоверное увеличение содержания HbF в крови, при этом определение гемоглобинов различных форм может быть использовано в качестве чувствительного маркера при диагностике патологий кислородтранспортной системы и терапии пациентов в состоянии гипоксии (32, 33). Интересно, что условия высокогорной гипоксии вызывали созревание эритроцитов, содержащих HbF, у здоровых взрослых людей, а возвращение к нор-моксии приводило к статистически значимому снижению количества HbF уже через 72 ч (34). При этом процессы синтеза γ - и β -цепей гемоглобина зависели от содержания HIF-1 α и EPO в крови (34).
Представленные результаты исследования могут косвенно свидетельствовать в пользу полученных нами данных, поскольку демонстрируют диагностическую значимость определения HbF при некоторых патологиях кровеносной системы новорожденных, важную роль эритропоэза, выступающего в качестве компенсаторного механизма при гипоксических состояниях, а также возможность относительно быстрой замены HbF на HbA при достижении нормоксии.
Вместе с тем предложенные механизмы действия интерамина и других препаратов-иммуномодуляторов на процессы кроветворения и кисло-родообмена у коров изучены не в полной мере и во многом остаются гипотетическими. У телят недостаточно исследованы системы регуляции факторов транскрипции при эритропоэзе, в частности их сходство с такими системами у других млекопитающих. Также важно выяснить, можно ли использовать концентрацию HbF в крови телят-гипотрофиков в качестве маркера анемии и состояния системы кислородообмена. Эти вопросы пред- ставляют научно-практический интерес и требуют дальнейшего изучения.
Итак, мы впервые оценили влияние комплексного препарата инте-рамина на морфофункциональное состояние гемоглобинов незрелого молодняка крупного рогатого скота с признаками антенатальной гипотрофии и коморбидными патологиями (анемии, иммунодефицит, гипоксия). Установленные различия в УФ-спектрах гемоглобинов в положении локальных максимумов светопоглощения при длине волны 270 и 275 нм, соответствующих присутствию в крови фетального и дефинитивного гемоглобинов, свидетельствуют о том, что у телят-гипотрофиков интерамин ускоряет замещение фетального гемоглобина на дефинитивный уже на 7-е сут (в сравнении с телятами-гипотрофиками без лечения и получавшими препарат сравнения Биферона-Б). Обнаруженные изменения, которые происходят под действием интерамина, указывают на нормализацию кислородтранспортной функции крови у телят с гипотрофическим развитием. Эти процессы, по нашему мнению, могут происходить как вследствие прямого влияния компонентов интерамина на эритропоэз, так и через иммуномодулирующее действие исследуемого препарата за счет снижения содержания провоспалительных цитокинов в организме телят.


