Сверхупругие безникелевые сплавы титана как материалы для дентальных имплантатов (экспериментальное обоснование)
Автор: Олесова Валентина Николаевна, Узунян Наринэ Адольфовна, Хафизов Раис Габбасович, Иванов Александр Сергеевич, Олесов Егор Евгеньевич, Шумаков Филипп Геннадиевич
Журнал: Клиническая практика @clinpractice
Рубрика: Фундаментальная медицина
Статья в выпуске: 2 т.9, 2018 года.
Бесплатный доступ
Сверхэластичные сплавы титана (титан-ниобий-цирконий и титан-ниобий-тантал) более выгодны по сравнению с титаном для зубных имплантатов благодаря своим физико-механическим свойствам, более близким к свойствам костной ткани. Были проведены морфологические исследования на животных биосовместимости этих сплавов по сравнению с титаном. Контроль взаимодействия образцов титанового сплава с костной тканью проводили в моменты времени 30 и 90 дней; В качестве методов исследования использовались сканирующая электронная микроскопия и микрозондовый элементный анализ ткани вдоль границы с титановыми сплавами. Близость морфологического рисунка и элементного состава костной ткани вдоль границы с титаном и суперэластичными сплавами титана показана как на контрольном периоде 30 дней (при контакте со сплавами обнаружена плохо минерализованная соединительная ткань), так и на 90 дни (граница с титановыми сплавами покрыта минерализованной костной тканью, сходной по своему составу с окружающей костной тканью).
Короткий адрес: https://sciup.org/143166576
IDR: 143166576
Superelastic nickel-free titanium alloys as materials for dental implants (experimental study)
Superelastic alloys of titanium (titanium-niobium-zirconium and titanium-niobium-tantalum) are more favorable in comparison with titanium for dental implants due to their physico-mechanical properties closer to those of bone tissue. Animal morphological studies of the biocompatibility of these alloys in comparison with titanium have been carried out. The control of the titanium alloy samples' interaction with bone tissue was performed at the time points of 30 and 90 days; scanning electron microscopy and microprobe element analysis of tissue along the boundary with titanium alloys were used as the methods of investigation. The proximity of the morphological pattern and elemental composition of bone tissue along the border with titanium and superelastic alloys of titanium is shown, both at the control period of 30 days (in contact with alloys, a poorly mineralized connective tissue is found) and at 90 days (the border with titanium alloys is covered with mineralized bone tissue, similar in its composition to the surrounding bone tissue).
Текст научной статьи Сверхупругие безникелевые сплавы титана как материалы для дентальных имплантатов (экспериментальное обоснование)
Поиск новых конструкционных материалов для дентальных имплантатов не прекращается, несмотря на превосходную биосовместимость титановых сплавов и керамики [1–3]. Это обусловлено значительной разницей физико-механических свойств имплантатов и воспринимающей костной ткани, способной привести к перегрузке последней, особенно при недостаточном количестве имплантатов. В настоящее время проводятся комплексные исследования по обоснованию для целей имплантологии сверхупругих титано- вых сплавов, таких как титан-ниобий-тантал Ti-22Nb-6Ta и титан-ниобий-цирконий Ti-22Nb-6Zr, полученных методом литья в НИТУ «МИСиС» [4–8]. Наряду со свойствами сверхупругости, присущими никелиду титана (Ti-50Ni), новые титановые сплавы не имеют в своем составе никеля.
Цель исследования – экспериментальное морфологическое изучение остеоинтеграции безникелевых сверхупругих титановых сплавов Ti-22Nb-6Ta и Ti-22Nb-6Zr.

МАТЕРИАЛ И МЕТОДЫ
Способность к остеоинтеграции сверхэластичных сплавов Ti-22Nb-6Ta и Ti-22Nb-6Zr оценивали в сопоставлении со сплавом титана на экспериментальных животных в Казанском федеральном университете (лаборатория лазерной конфокальной микроскопии Междисциплинарного центра аналитической микроскопии, Междисциплинарный центр коллективного пользования КФУ). Кроликам породы серый великан числом 18 животных со средней массой тела 2500 г под внутримышечным 2% роме-таровым наркозом производили разрез длиной 4 см в поднижнечелюстной области, скелетировали поверхность челюсти и формировали отверстия диаметром 4 мм и глубиной 2 мм с последующим введением в костное ложе с усилием образцов сплавов, после обработки раны 3% раствором перекиси водорода ее послойно ушивали. Животных выводили из опыта в сроки 30 и 90 суток внутримышечным введением 6 мл калипсола, производили забор костных блоков, которые помещали в раствор 10% нейтрального формалина; проводили рентгенологический контроль на аппарате PanExam+ (Kavo). Предварительный просмотр костных блоков осуществляли посредством оптического микроскопа при увеличении ×50, ×100 и ×200. Зону контакта костной ткани с образцами из титановых сплавов анализировали на автоэмиссионном высокоразрешающем сканирующем электронном микроскопе Merlin (CarlZeiss) после обработки блоков в вакуумной установке Q 150TES (QuorumTechnologies) для нанесения проводящего слоя сплава Au/Pd в соотношении 80/20 толщиной 15 нм методом катодного распыления. Микроскоп оснащен спектрометром энергетической дисперсии AZtec X-Max (OxfordInstruments) с разрешением спектрометра 127 эВ; точность изме- рения 0,01–1%. Элементный рентгеновский микро-зондовый анализ в сопровождении спектрограммы проводили на электронном микроанализаторе EVO GM (CarlZeiss) при ускоряющем напряжении 20 кэВ и рабочем отрезке 10 мм с использованием набoра эталoнов для количественнoго микрoанализа; глубина зондирования порядка 1 мкм; предел обнаружения элементов 1500×2000 ррм.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Взаимодействие с костной тканью образцов сверхэластичных сплавов титан-ниобий-тантал и титан-ниобий-цирконий демонстрирует в эксперименте их остеоинтегративные свойства. Через 30 суток после интеграции образцов титан-ниобий-циркония между ними и костной тканью в некоторых местах по линии контакта при увеличении в сканирующем электронном микроскопе в 50, 100, 500 раз выявляется щель размером до 20 мкм. На большем протяжении контакта с имплантатом выявлены обширные участки ткани, покрывающей края образцов титан-ниобий-циркония (рис. 1). Элементный микрозондовый анализ состава ткани за границами образца сплава позволил идентифицировать ее как костную ткань, поскольку содержание Ca и P среди 8 анализируемых элементов превалировало (соответственно 44,27 и 12,89 вес.%); содержание С и O – 30,33 и 12,22 вес.%. В зонах «нарастания» ткани на образцы титан-ниобий-циркония основные элементы – углерод (72,45 вес.%), а также кислород (13,45 вес.%), что расценивается как соединительная ткань (рис. 2, таблица). Через 90 суток поверхность образцов титан-ниобий-циркония полностью покрывается минерализованной костной тканью, о чем свидетельствует микроэлементный анализ, показывающий следующий состав: Ca 27,27, P 13,77, C 29,68, O 25,84 вес.% (рис. 3, 4).
Рис. 1. Граница контакта костной ткани с образцом из титан-ниобий-циркония (срок эксперимента 30 суток, ув. ×100)
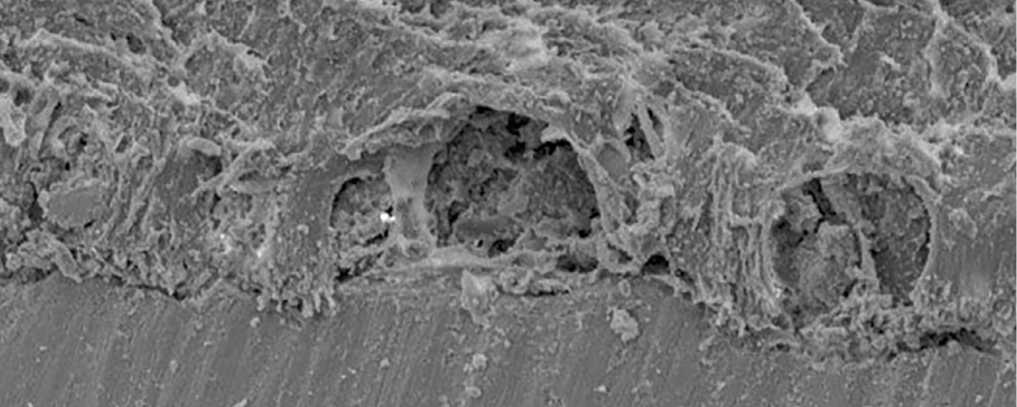
ATATATAT ▼
▼ATAT


Электронно-микроскопическая картина и микро-зондовый элементный анализ в эксперименте при использовании титан-ниобий-тантала показывают результаты, близкие к эксперименту при использовании титан-ниобий циркония.
Присутствие титана в костной ткани на сроке контроля 30 суток также сопровождается наличием щели между металлическим образцом имплантата и костной тканью до 10 мкм. При большем увеличении выявляются многочисленные зоны нарастания на металл тканей со стороны костного ложа. Эта ткань по элементному составу в основном С 61,12 вес.% и O 21,67 вес.% (таблица, рис. 5), тогда как ткань на некотором расстоянии от границы с металлическим имплантатом состоит в основном из Ca, P, С и О соответственно 48,21, 15,01, 25,48 и 8,87 вес.%. На сроке контроля 90 суток образцы из титана полностью покрыты минерализованной костной тканью составом: Ca 26,49, P 13,76, C 27,83, O 29,60 вес.% (таблица, рис. 6).
Рис. 2. Спектрограмма элементного микрозондового анализа ткани в контакте с образцом из титан-ниобий-циркония (срок эксперимента 30 суток)
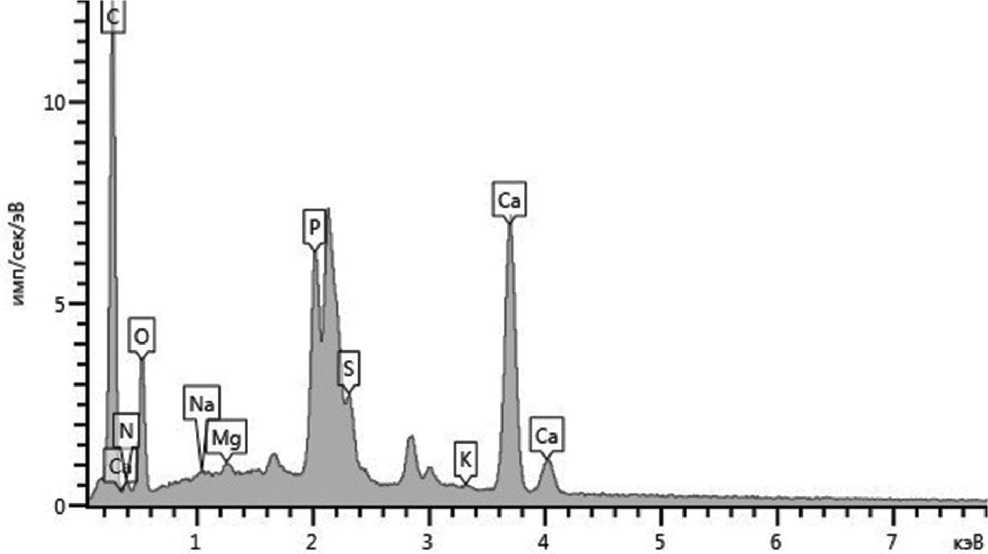
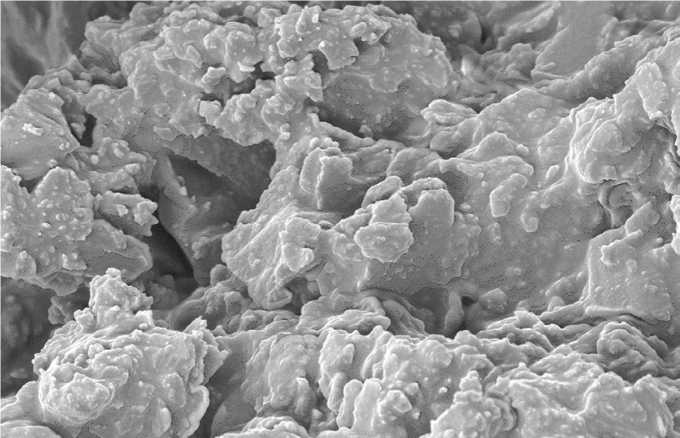
Рис. 3. Костная ткань в контакте с образцом из титан-ниобий-циркония (срок эксперимента 90 суток, ув. ×5000)
иническая!?™» оактика:^
Рис. 4. Спектрограмма элементного микрозондового анализа костной ткани в контакте с ти-тан-ниобий-цирконием (срок эксперимента 90 дней)
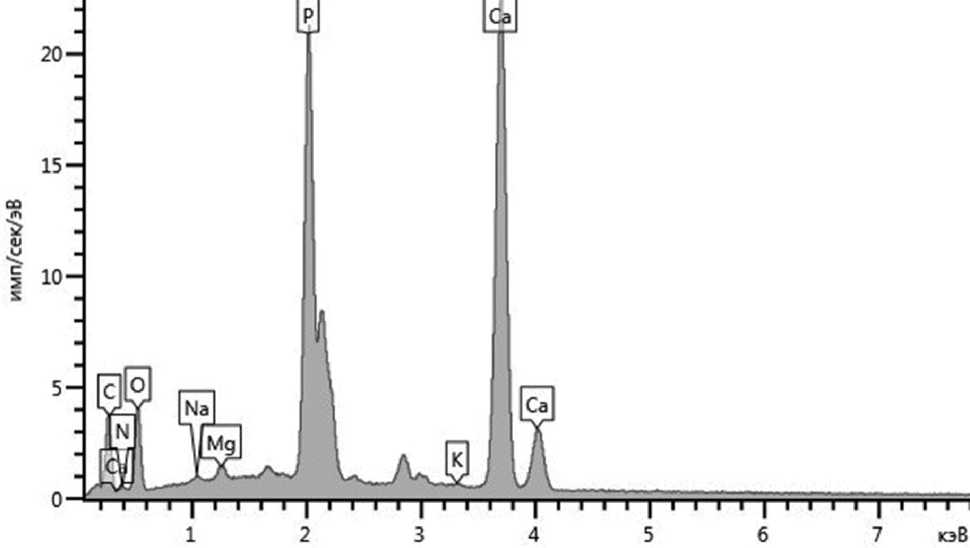
Рис. 5. Граница контакта костной ткани с титаном (срок эксперимента 30 суток, ув. ×100)
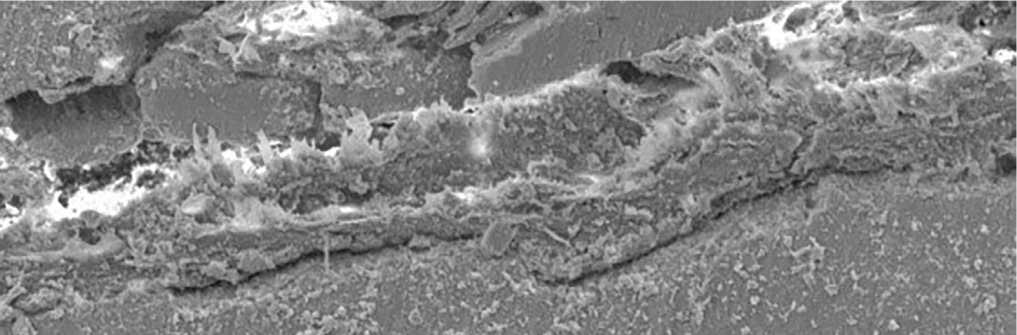

Рис. 6. Костная ткань в контакте с титаном (срок эксперимента 90 суток, ув. ×5000)

Результаты элементного микрозондового анализа ткани по границе образцов титан-ниобий-циркония и титана (вес.%)
|
Элемент |
Ti-22Nb-6Zr |
TiGrade 4 |
Название эталона |
||
|
30 суток |
90 суток |
30 суток |
90 суток |
||
|
С |
72,45 |
29,68 |
61,12 |
27,83 |
С Vit |
|
N |
9,49 |
2,56 |
3,01 |
0,00 |
BN |
|
О |
13,45 |
25,84 |
21,67 |
29,60 |
SiO2 |
|
Na |
0 |
0,26 |
0,10 |
0,34 |
Albite |
|
Mg |
0,11 |
0,51 |
0,20 |
0,69 |
MgO |
|
Р |
0,81 |
13,77 |
3,76 |
13,76 |
GaP |
|
S |
1,66 |
0 |
1,69 |
1,14 |
FeS2 |
|
К |
0,10 |
0,11 |
0,08 |
0,15 |
KBr |
|
Са |
1,94 |
27,27 |
8,37 |
26,49 |
Wollastonite |
|
Сумма |
100,00 |
100,0 |
100,00 |
100,00 |
— |
ЗАКЛЮЧЕНИЕ
В эксперименте на животных образцы дентальных имплантатов из сплавов титан-ниобий-цирко-ния и титан-ниобий-тантала интегрируются костной тканью, как и титан. Остеоинтеграция образцов дентальных имплантатов из сверхупругих сплавов завершается через 90 суток пребывания в костной ткани, сопровождается минерализацией со- единительной ткани на границе со сплавами, формирующейся в начальный период после введения образцов сплавов в костную ткань. Электронномикроскопический анализ и элементный микрозон-довый анализ позволяют ранжировать сплавы по степени остеоинтеграции: титан, титан-ниобий-цир-коний, титан-ниобий-тантал.
Список литературы Сверхупругие безникелевые сплавы титана как материалы для дентальных имплантатов (экспериментальное обоснование)
- Загорский В.А., Робустова Т.Г. Протезирование зубов на имплантатах. 2-е изд., доп. М: Бином, 2016.
- Кулаков А.А., Лосев Ф.Ф., Гветадзе Р.Ш. Зубная имплантация: основные принципы, современные достижения. М: МИА, 2006.
- Лебеденко И.Ю., Арутюнов С.Д., Ряховский А.Н. и др. Ортопедическая стоматология: Национальное руководство. М: ГЭОТАР-Медиа, 2016.
- Григорьян А.С., Филонов М.Р., Архипов А.В. и др. Возможности применения сплава титана с памятью упругости в стоматологии//Стоматология. 2013. № 1. С. 4-8.
- Жукова Ю.С., Петржик М.И., Прокошкин С.Д. Оценка кристаллографического ресурса деформации при обратимом мартенситном превращении β в α'' в титановых сплавах с эффектом памяти формы//Металлы. 2010. № 6. С. 77-84.
- Клопотов А.А., Гюнтер В.Э., Марченко Е.С., Байгонакова Г.А. Влияние термической обработки на физические и структурные свойства сплава TI50NI47,7MO0,3V 2 с эффектами памяти формы//Известия высших учебных заведений. Физика. 2015. № 58 (7-2). С. 68-74.
- Сысолятин П.Г., Гюнтер В.Э., Сысолятин С.П. и др. Имплантаты с памятью формы в челюстно-лицевой хирургии. Томск: Изд-во МИЦ, 2012.
- Olesov E.E., Shugailov I.A., Mirgazizov M.Z. et al. Experimental study of changes in the electric potential of implants made of titanium alloys under the influence of functional dynamic load//Research Journal of Pharmaceutical, Biological and Chemical Sciences September. 2016. No. 7(5). P. 1118-1124.


