Термодинамические расчеты параметров состояния гидротермальной среды для моделирования процесса зарождения биосферы
Автор: Компаниченко В.Н., Авченко О.В.
Журнал: Региональные проблемы @regionalnye-problemy
Рубрика: Биология. Экология
Статья в выпуске: 2 т.18, 2015 года.
Бесплатный доступ
В контексте гидротермального сценария зарождения биосферы выполнены термодинамические расчеты равновесий в гидротермальном растворе, включающие твердую, жидкую и газообразную фазы. В качестве исходных эталонов взяты реальные составы архейского метабазита и хлоридно-натрового термального раствора из кальдеры Узон на Камчатке. Расчеты проводились при температурах от 25 до 150є, давлении от 1 до 50 бар, и соотношении вода-порода от 1000 до 0,05. Результаты показывают наличие больших колебаний химизма жидкой фазы при изменении данных параметров. Это доказывает существование значительных флуктуаций параметров гидротермального раствора при его подъеме к поверхности. Такие флуктуации рассматриваются как важное условие возникновения простейших форм жизни на ранней Земле.
Гидротермальная система, гидрохимический состав, давление, температура, расчет, флуктуация, зарождение биосферы
Короткий адрес: https://sciup.org/14328903
IDR: 14328903 | УДК: 551.23:550.4
Thermodynamic calculations of the parameters of hydrothermal environment in the modeling of biosphere origin
Elaborating a hydrothermal scenario of the biosphere origin, it was made thermodynamic calculations of balances in hydrothermal solution, including its solid, liquid and gaseous phases. For the initial standards it has been taken real structures of the Archaean meta-basic rock and chloride-sodium thermal solution from the Uzon caldera in Kamchatka. The calculations were made at temperatures from 25 to 150є, pressure - from 1 to 50 bars, and the water-rock ratio from 1000 to 0,05. Their results show considerable fluctuations in chemism of the liquid phase at the parameters change. It means that hydrothermal solution is characterized by considerable fluctuations of the parameters during its rise to the surface. Such fluctuations are considered as an important condition for the emergence of primary forms of a life on the early Earth.
Текст научной статьи Термодинамические расчеты параметров состояния гидротермальной среды для моделирования процесса зарождения биосферы
После опубликования первой гипотезы о возникновении первичных микроорганизмов на Земле в районах горячих источников на дне океанов [11] появилось множество работ, рассматривающих гидротермальную среду как материнскую для биосферы. В настоящее время гидротермальные системы и океан (вне областей выхода термальных источников) рассматриваются как две альтернативные среды зарождения жизни на ранней Земле. Гидротермальный сценарий зарождения биосферы имеет несколько версий. Одни исследователи считают наиболее подходящей средой области разгрузки кислых перегретых (до 300–400º С) флюидов в осевых частях срединно-океанических хребтов [11], другие – умеренно-высокотемпературные (100–110º С) источники щелочного состава на склонах хребтов [21], третьи – выходы термальных растворов на континентах [20]. По-разному рассматриваются и биогеохимические аспекты процесса возникновения первичных форм жизни в гидротермальной среде [12].
Одним из вариантов гидротермального сценария является инверсионный подход к зарождению биосферы [6, 16]. В его основе лежит представление о термодинамической инверсии предбиологи- ческих микросистем как о решающем моменте в их трансформации в первичные формы жизни. Согласно данному подходу, инверсия могла произойти только в далеких от равновесия условиях и обязательно при существенных колебаниях параметров в материнской среде. Этим предложенный подход отличается от всех других подходов к проблеме зарождения биосферы, в которых допускается возникновение первичных форм жизни и в стабильной среде. Вытекающая из него необходимость колебательных условий указывает на гидротермальные системы (включая области их выхода в открытые или подземные водоемы) как на наиболее благоприятную среду для зарождения жизни, в отличие от океана с его достаточно статичными условиями.
До настоящего времени практически все лабораторные эксперименты по предбиологической химии в мире, за редкими исключениями, проводились в стабильных условиях. Однако для проверки и дальнейшего развития инверсионной модели необходимо проведение экспериментов в лабораторных установках, где будут созданы режимы флуктуаций, моделирующие природную гидротермальную среду. Для этого должен быть исследован характер колебаний термодинамических и физико- химических параметров в различных гидротермальных системах и изучены влияющие на этот процесс геологические факторы. Хотя данных по режимам таких колебаний в мировой литературе накопилось немало, до сих пор они не привлекались для решения проблемы зарождения биосферы.
В принципе, возможны два подхода к изучению флуктуаций параметров в гидротермальных системах – на основе их прямого мониторинга и через термодинамические расчеты. В рамках первого подхода нами была исследована динамика давления пароводяной смеси в Верхне-Мутновской гидротермальной системе на Камчатке, где выявлено наличие макро- и микроколебаний, и охарактеризованы их периоды и амплитуды [7, 17]. Также рассчитаны коэффициенты корреляции между температурой и давлением, которые варьируют в разных скважинах от 0,89 до 0,99. В гидротермальной системе Мура (Словения) установлены почти синхронные колебания температуры, давления и концентраций целого ряда компонентов [18]. Периоды таких достаточно регулярных колебаний составляют около 70 мин.
Для объяснения отмеченных флуктуаций выдвигаются различные причины. Так, сложные колебания давления пароводяной смеси в Мутновской гидротермальной системе могут инициироваться периодическим усилением эндогенной активности Мутновского и Горелого вулканов, находящихся на расстоянии до нескольких километров от термальных полей [7]. Последнее извержение Мутнов-ского вулкана произошло по геологическим меркам недавно – в 2000 г. Другой причиной гидродинамических аномалий могут быть обильные осадки после засушливого периода; в этом случае проникновение холодных вод по трещинам усыхания в резервуар имеет следствием последующее набухание гидротермально-измененных пород и запечатывание водопроводящих трещин. Одна из гидродинамических аномалий, установленных в скважине № 30 Мутновского поля в течение 1996– 1997 гг., по времени совпадает с началом периода сильных дождей [5]. Еще одна возможная причина связана с высокой региональной сейсмичностью Камчатского полуострова. В частности, две из трех наиболее ярко выраженных гидродинамических аномалий, выявленных в ходе мониторинга давления в скважине № 30 в 1996–1997 гг., были отчетливо связаны с землетрясениями магнитудой 4,1 и 4,5 балла [4]. Наличие связи между гидродинамическим режимом и сейсмическими явлениями устанавливались и в других регионах мира [9, 22].
Таким образом, генетическая интерпретация установленных режимов флуктуаций термодинами- ческих и физико-химических параметров в гидротермальных системах носит достаточно вариабельный характер. Из этого вытекает, что причины таких колебаний остаются недостаточно выясненными. При этом в ряде случаев между колебаниями различных параметров устанавливаются высокие корреляционные зависимости (например, в гидротермальной системе Мура в Словении), что свидетельствует о наличии каких-то общих причин, инициирующих постоянную изменчивость гидротермальной среды. В этой связи нами предпринята попытка на основе термодинамических расчетов создать обобщенную модель гидротермальной системы в вертикальном диапазоне от поверхности до глубины порядка 1 км, ориентированную на выявление корреляционных зависимостей между термодинамическими и физико-химическими параметрами в восходящем потоке флюидов в верхней части земной коры. При этом такая модель должна учитывать особенности гидротермального процесса на ранней Земле, что делает возможным ее использование при разработке гидротермального сценария зарождения биосферы.
Характеристика термодинамической модели
Согласно имеющимся многочисленным данным, в самую раннюю архейскую эру геологической эволюции Земли состав магматических пород варьировал от основного до ультраосновного. Такие составы характеризовались относительно низкими содержаниями кремнезема (35–50%) и высокими – окислов железа, кальция и магния. В настоящее время подобные породы широко представлены в океанической коре и в зоне перехода от океана к континенту (в частно6сти, на полуострове Камчатка). В связи с этим, в расчетную модель взаимодействия «флюид-порода» были заложены следующие характеристики. В качестве эталона породы был выбран архейский метабазит, типичный для ранних этапов развития Земли. Его химический состав приведен в табл. 1. По минералогическому составу это гранат-амфибол-двупироксено-вый кристаллосланец из охотского метаморфического комплекса [1]. За основу состава флюида в одной из серии расчетов был взят хлоридно-натро-вый раствор пробы 81-D4U, отобранной нами из кипящего водяного котла в центральной части кальдеры Узон (Камчатка) и имеющей pH 5,1. Растворы подобного состава, связанные с вулканизмом основного и среднего ряда, также должны были быть широко распространены на ранней Земле. Согласно классической зональности гидротермальных полей на Камчатке, именно высокотемпературные хлоридно-натровые воды наиболее тесно пространственно связаны с магматическими оча-
Состав архейского метабазита (в %), выбранного для модели взаимодействия гидротермального флюида с горной породой [1]
Таблица 1
В расчетной модели вода (1 кг) поступает в ме-табазит и взаимодействует с ним в условиях давления (Р) и температуры (Т), типичных для приповерхностных областей земной коры: от температуры 25º С и давления 1 бар (поверхность) до 150º С и 50 бар (глубина в несколько сотен метров), включая промежуточные значения температуры (100, 125, 150º С) и давления (10 бар). Соотношение вода–порода менялось по массе от 1000 до 0,05, т.е. от открытых полостей жидкости в крупных трещинах или межслойных пространствах до растворов в мелких порах. Первая серия расчетов проведена без добавления углекислого газа, вторая – с добавкой 2 молей CO2. Расчет модели проводился методом минимизации потенциала Гиббса на программном комплексе «Селектор». Подробное описание этого комплекса с построением различных термодинамических моделей дается в двух монографиях [2, 8]. Моделирование проводилось на основе термодинамической базы [15] и с учетом моделей твердых растворов. База данных по моделям твердых растворов, по сравнению с работой [3], была существенно переработана и расширена за счет новых моделей орто- и клиноамфиболов, биотита, клинопироксена, ильменита, шпинели, опубликованных в работах [13, 14, 23–25]. Газовый флюид моделировался идеальной смесью реальных газов H2O, CO2, CH4, CO, H2, O2, причем зависимость термодинамических характеристик газов от давления вычислялась по модифицированному Б.И. Ли и М.Г. Кеслером [19] уравнению состояния Бенедикта-Вебба-Рубина. В целом модель включала: 119 компонентов, входящих в раствор (анионы, катионы и нейтральные комплексы); 97 компонентов, составляющих твердые фазы; 19 газовых компонентов. В твердых фазах, которые по расчетным данным выпадали в осадок, находились следующие минералы: хлорит (Chl), гетит (Gth), каолинит (Kao), кварц (Q), рутил (Ru), кальцит (Cc), ильменит (Ilm), гранат (гроссуляр-андрадит) (Gr), микроклин (Mic), мусковит (Mu), пренит (Pre), сфен (Sph), альбит (Ab), хлоритоид (Ctd). Расчеты флюида проводились с расчетом коэффициентов активности компонентов раствора по уравнению Дебая-Хюккеля.
Таким образом, выбранные для расчетов геофизические и геохимические параметры гидротермальных систем охватывают весь основной диапазон условий, в пределах которых, согласно инверсионному варианту гидротермального сценария зарождения биосферы, наиболее вероятно возникли первичные формы жизни на ранней Земле.
Результаты термодинамических расчетов
Результаты расчетов сведены в 20 таблиц. В двух первых из них приведена общая минерализация (мг/кг H 2 O) водного раствора при взаимодействии воды с метабазитом (табл. 2, 3). В качестве переменных параметров были использованы: а) различные весовые соотношения воды (W) и горной породы (R); б) различные Р-Т условия, включающие значения температуры 25, 100, 125 и 150ºС и давления 1, 10 и 50 бар. В табл. 2 показаны расчеты без добавления CO 2 в систему, в табл. 3 – с добавлением 2 молей CO 2 . Как видно из табл. 2, при всех указанных Р-Т условиях общая минерализация варьирует незначительно: около 3 г/л при превалировании воды над породой (или равенстве их объемов). Только в поровых растворах она возрастает до примерно 5,4 г/л. Наблюдается также некоторое расхождение между расчетными и экспериментальными данными по общей минерализации в условиях на поверхности, но оно невелико. Добавление в систему 2 молей CO 2 существенно меняет результаты при соотношениях вода-порода от 10 до 100 (табл. 3). Ключевым фактором здесь становится величина давления. При максимальном значении давления 50 бар общая минерализация возрастает в несколько раз и колеблется в пределах 7,6–13,6 г/л.
В остальных 18 таблицах приведена информация по рН, Eh и составу основных катионов и анионов в растворе в двух сериях расчетов – с добавлением и без добавления CO 2 (по 9 таблиц в каж-
Таблица 2
Общая минерализация (мг/кг H2O) водного раствора при взаимодействии воды с метабазитом при различных весовых соотношениях воды (W) и горной породы (R) и указанных Р-Т, без добавления 2 молей CO2 в систему
|
W/R |
Градусы, Бары |
25°, 1 |
25°, 10 |
25°, 50 |
100°, 10 |
100°, 50 |
125°, 10 |
125°, 50 |
150°, 10 |
150°, 50 |
|
R=0 |
Общая минерализация |
2925 3741* |
2925 |
2925 |
2960 |
2960 |
2984 |
2985 |
3016 |
3018 |
|
1000 |
Общая минерализация |
2926 |
2926 |
2926 |
2970 |
2970 |
2996 |
2996 |
3026 |
3028 |
|
100 |
Общая минерализация |
2906 |
2900 |
2899 |
2977 |
2978 |
3000 |
3003 |
3040 |
3043 |
|
10 |
Общая минерализация |
2972 |
2961 |
2963 |
2933 |
2994 |
3019 |
3020 |
3051 |
3053 |
|
1 |
Общая минерализация |
3101 |
3089 |
3092 |
3117 |
3119 |
3142 |
3142 |
3175 |
3176 |
|
0,05 |
Общая минерализация |
5390 |
5409 |
5410 |
5402 |
5405 |
5410 |
5411 |
5424 |
5425 |
Примечание: * – экспериментальное значение общей минерализации из анализа воды в пробе 81-D4U дой серии). Значения в каждой таблице рассчитаны для определенных Р-Т условий. В нижней части таблиц даются твердые фазы, которые уходят в осадок. Ниже для примера показаны две таблицы из разных серий расчетов при температуре 25º С и давлении 1 бар, отражающие условия на поверхности (табл. 4 и 5). Даже из простого взгляда на таблицы видно, насколько сильно концентрации компонентов зависят от соотношения воды и породы. В табл. 4, иллюстрирующей условия без добавления CO2, концентрации большинства компонентов отличаются в несколько раз; стабильно только поведение кремнезема и галогенов (F-, Cl-). Различие в содержаниях СаCO3 и CO3-2 еще больше и составляет 2–3 порядка. Однако для иона HCO3- оно небольшое – до 200%. С уменьшением отношения W/R состав флюида эволюционирует от нейтрального (6,3) до щелочного (9,4–9,6). При этом окислительно-восстановительный потенциал меняется от слабо отрицательных значений (между -0,15 и –0,25) до слабо положительных (между 0,07 и 0,16). При добавлении в систему 2 молей CO2 отмеченные отличия проявляются сильнее (табл. 5). Концентрации F- и Cl- тоже начинают меняться – в поровых растворах они возрастают вдвое. Состав раствора варьирует уже от кислого (pH=4) до щелочного (p =9,3). Окислительно-восстановительный потенциал переходит в область слабо положительных значений (от 0,02 до 0,4), его величина достигает максимума при R=0(0,4) и плавно снижается к поровым растворам (0,08).
На рис. 1 показано изменение pH с уменьшением соотношения вода-порода (W/R) при стабильном давлении 10 бар и различных температурах 25, 100, 125 и 150º С в двух системах: без добавления и с добавлением 2 молей CO 2 . В первой системе при максимальной температуре 150º С величина pH обнаруживает минимальную изменчивость и варьирует около нейтральных значений (pH=6–7), слегка увеличиваясь с увеличением доли породы в системе (W/R от 100 до 0,05). На фоне снижения температуры контрастность значений pH растет, достигая максимума при температуре 25º С: от 6,3 в чисто водной среде до 9,3–9,5 при W/R 10–0,05. Но особенно высока изменчивость pH в системе с добавлением 2 молей CO 2 . В ней проявляются те же тенденции, но гораздо более ярко: от кислых растворов (pH=3,5) до щелочных (pH=9,2–9,4) при температуре 25º С. Примерно такая же картина изменения pH выявляется в ходе снижения не только температуры, но и давления в системе (рис. 2). На фоне уменьшения интенсивных термодинамических параметров (150º С – 50 бар, 100º С – 10 бар, 25º С – 1 бар) состав растворов эволюционирует от нейтральных к щелочным при повышенной доле породы в системе (W/R 100–0,05). Добавление 2
Таблица 3
Общая минерализация (мг/кг H2O) водного раствора при взаимодействии воды с метабазитом при различных весовых соотношениях воды (W) и горной породы (R), c добавлением 2 молей CO2 в систему
|
W/R |
Градусы. Бары |
25°, 1 |
25°, 10 |
25°, 50 |
100°, 10 |
100°. 50 |
125°, 10 |
125°, 50 |
150°, 10 |
150°, 50 |
|
R=0 |
Общая минерализация |
2927 |
2950 |
2983 |
2980 |
3007 |
3000 |
3032 |
3040 |
3067 |
|
1000 |
Общая минерализация |
2963 |
2996 |
3046 |
ЗОЮ |
3039 |
3034 |
3060 |
3068 |
3094 |
|
100 |
Общая минерализация |
4001 |
6766 |
6768 |
4287 |
5261 |
3995 |
4665 |
3836 |
4282 |
|
10 |
Общая минерализация |
2941 |
11592 |
13613 |
3056 |
11047 |
3110 |
10020 |
3182 |
7636 |
|
1 |
Общая минерализация |
3070 |
3081 |
3107 |
3151 |
3163 |
3209 |
3223 |
3281 |
3282 |
|
0,05 |
Общая минерализация |
5374 |
5407 |
5493 |
5415 |
5438 |
5445 |
5466 |
5485 |
5504 |
Таблица 4
|
5 ^ о о СО о х за 2 га § 5 В § g & £ у о S о X 1 3 >^ 8 g о У о га га S о ? У к О m га Cd сч д о к и &15 g 5 S <^ Cd № ю 8 cd а Н CD 2 ц 2 m ° to Kt О со га о S ю й to Я -н о к S ^ ” § &; &« га а & cd И Л -^ О ^ а 5 S S & в 8 Ё =§ cd га В Л у £ § у S |
^ н cd ^ |
d d |
г- °^ со 40 |
40^ О |
1 |
1 |
1 |
|||||||
|
+П3 d |
СМ о П ш СО 00 |
СП in со |
сМ in |
40 о |
40 о |
|||||||||
|
Xi |
; in |
П 40 |
со |
in |
in |
СП |
||||||||
|
cd о |
П С4 о |
СМ^ |
40 |
40, (М |
со ri |
40 |
5 и |
+ |
+ |
|||||
|
5 У о У У < |
о GO |
— ш <М 40 СП СО |
со СП |
П о сп |
(М сп |
о сп |
О 40 ш |
< |
||||||
|
о о |
СП 40 |
СО in |
М |
ЯГ |
я' |
ri |
хп |
+ |
+ |
|||||
|
U- |
г- |
г^ |
г^ |
г^ |
г^ |
V £ |
+ |
|||||||
|
о |
о ш О 40 Г1 СО |
о о П |
о о П |
о о Г1 |
ш *п Г1 |
ш 04 (М |
У ^ |
|||||||
|
6 о |
о о о |
ri со о' |
04 о |
СП |
СП |
in o' |
и § |
+ |
+ |
+ |
+ |
+ |
||
|
3 3 У CD У о CD га я и d |
6' от |
•П |
in |
in |
in |
in |
(М^ in |
5 |
+ |
+ |
+ |
|||
|
о cd Z |
об |
со |
■п |
CS o' |
o' СП |
Е |
||||||||
|
ш т |
in ri о |
и |
+ |
+ |
||||||||||
|
о GO cd и |
га- |
40х |
СП ш |
CM ОО |
сп ОО |
СП |
3 02 |
|||||||
|
о х |
40 40 40 40 со СО |
in |
о СМ |
co о |
со о |
rl |
о |
+ |
+ |
+ |
+ |
+ |
||
|
о и и |
чГ o' |
о о |
о |
40 o' |
40 o' |
40 o' |
о ^ |
|||||||
|
И |
м |
in о^ со |
о? |
40 04 |
04" |
5 |
||||||||
|
X и |
ш о |
in см о |
40 о |
о o' |
о о' |
со о о' |
и |
+ |
+ |
+ |
+ |
|||
|
1 |
о d |
о о о |
о о |
о |
in о o' |
о о о |
о о |
о |
in о^ о |
|||||
|
S о |
5 |
1 |
rit о |
40^ 04 |
in |
СП |
04 |
||||||
|
d d |
ОО о^ o' |
1 |
1 |
1 |
1 |
। |
|||||||
|
cd d |
СМ ш ОО |
ОО |
СП о |
04 |
Г1 ri о |
ri 40 |
|||||||
|
V |
С4 О |
СП |
04 о |
'—1 |
О О |
||||||||
|
и |
40^ о |
^ |
3 |
о |
40^ об' |
■0 и |
|||||||
|
5 га о S X < |
О О) |
СП |
СП |
о |
04 |
СМ |
о in |
< |
|||||
|
о и X |
ОО 4о" |
04 40 |
М |
г? ri |
& со |
||||||||
|
L |
in |
м- 40^ |
Г-; |
04 |
СП |
<У £ |
+ |
+ |
|||||
|
и |
о о СМ |
о О СМ |
о о СМ |
о СМ |
40 in СМ |
о о СМ СМ |
= |
+ |
+ |
||||
|
о и |
1 |
04 о о о о o' |
чГ о |
ОО' о |
со о |
40 in о" |
V i |
+ |
+ |
||||
|
5 3 У О 3 (D я |
д' |
in |
in |
in |
in |
in |
in |
5 |
|||||
|
и d |
ОО |
ОО |
o' |
со ОС |
о |
40^ О |
Е |
||||||
|
хЛ X |
ш о |
1 |
1 |
। |
1 |
। |
CD и |
+ |
+ |
+ |
|||
|
6 CZ) cd и |
со |
40 |
CM |
in |
in |
Й |
□ |
+ |
1 |
1 |
1 |
||
|
о m d |
40 40 |
40 40 |
со |
40 in |
in |
СМ |
о |
+ |
+ |
+ |
+ |
||
|
д и О |
04 о о о о о |
о |
40 40 o' |
40 40 o' |
40 40 o' |
о сз ^ |
+ |
+ |
|||||
|
D- |
о. |
ГЧ |
ОО 4о" |
о? |
о? |
04' |
■с 5 |
1 |
1 |
1 |
|||
|
^ Щ |
Г1 о o' |
о |
СП о |
o' |
o' |
00 О o' |
и |
+ |
+ |
+ |
+ |
||
|
о cd |
о о о |
о о |
о |
0 o' |
о о о |
о о |
о |
о |
|||||
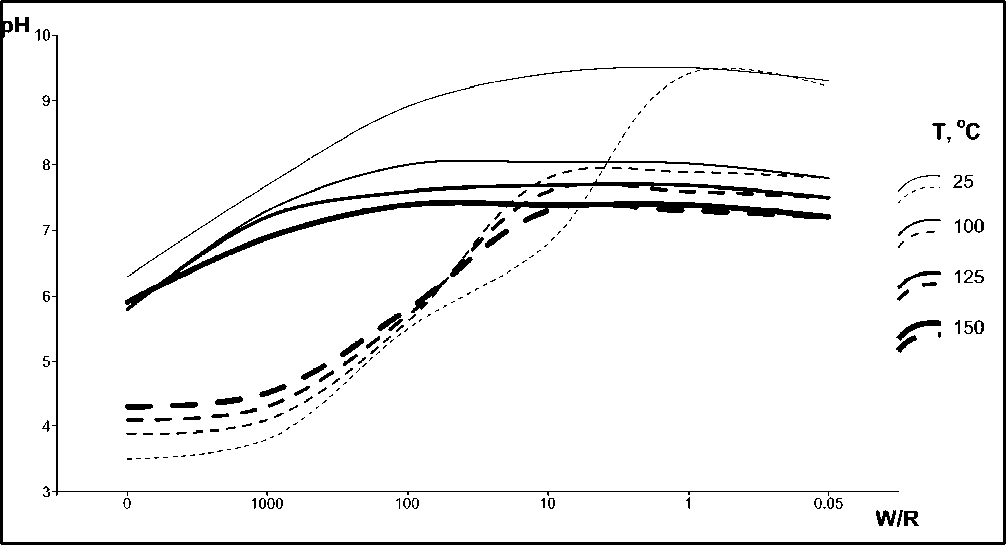
Рис. 1. Значения рН в зависимости от температуры и соотношения W/R при стабильном давлении (10 бар) без добавления 2 молей СО2
молей CO2 точно так же приводит к увеличению контрастности состава растворов – от кислых (pH=4) до щелочных (pH=9,3). Правда, в этом случае появляется и отличие, заключающееся в появлении двух пиков на кривой роста кислотности-щелочности при температуре 25º С, которые приходятся на значения W/R = 1000 и 10. Это отличие отчетливо иллюстрирует нелинейность процессов, протекающих в гидротермальных системах.
На вышеприведенных рис. 1 и 2 было продемонстрировано общее изменение химизма растворов в зависимости от термодинамических параметров, соотношения вода-порода и наличия/отсут-ствия молей CO 2 в системе. Для более детального
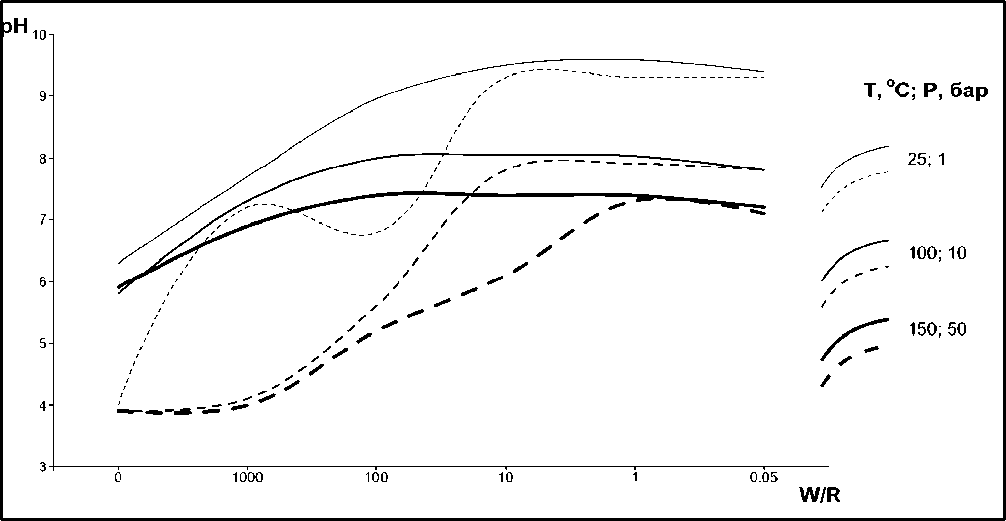
Рис. 2. Значения рН в зависимости от температуры и соотношения W/R при стабильном давлении (10 бар) с добавлением 2 молей СО2
отображения особенностей химического состава нами были выбраны 5 компонентов, поведение которых представляется наиболее информативным: изменение их концентраций является значительным (в отличие от почти постоянных содержаний кремнезема и галогенов), но и не чрезмерно большим (как наблюдающееся для СаCO 3 и CO 3 -2 ). Среди отобранных компонентов есть нейтральные молекулы (CaSO 4 , NaCl), катионы (Ca +2 , K + ) и анион (HCO 3 - ). Изменение их концентраций в зависимости от соотношения вода-порода при температуре 150ºС и давлении 10 бар показано на рис. 3. На нем видно, что только концентрации HCO 3 - непрерывно возрастают с увеличением доли породы в системе, остальные компоненты ведут себя по-разному. Пик содержания хлорида натрия приходится на равное соотношение воды и породы, при этом заметнее оно снижается с увеличением водной составляющей. Молекула CaSO 4 , а также катионы Ca +2 и K + проявляют сходные тенденции: их содержания минимальны при относительно сопоставимом соотношении вода-порода (W/R=100–1) и увеличиваются в системах с большим преобладанием одной либо другой составляющей.
Эти же компоненты показаны на рис. 4, который иллюстрирует изменение их концентраций в зависимости от температуры при постоянном давлении 10 бар и отношении вода–порода равном 100. Как и на предыдущем графике, наименьшие вариации обнаруживает анион HCO3-, концентрации которого плавно снижаются от 5,2 до 2,7 мг/кг на фоне падения температуры. На этом же фоне со- держания хлорида натрия и особенно катиона калия стремительно падают, в то время как концентрации катиона кальция и его сульфата, напротив, в целом возрастают.
Интерпретация результатов и выводы
Проведенные нами термодинамические расчеты равновесий в гидротермальном растворе показывают наличие больших вариаций значений параметров, которые зависят от Р-Т условий и соотношений жидкой, твердой и газообразной фаз. С уменьшением соотношения вода-порода в системе pH раствора может меняться от кислого до щелочного (при фиксированной температуре и давлении). Концентрации нейтральных молекул, так же как анионов и катионов, в разных РТ условиях и меняющемся W/R отношении могут отличаться в десятки раз. Добавление в систему вода-порода газовой фазы (углекислота) существенно изменяет ее, приводя к повышению кислотности и уменьшению вариаций содержаний многих компонентов. При этом общая минерализация может увеличиваться в несколько раз при росте давления.
В реальных природных условиях гидротермальных систем растворы мигрируют из глубоких областей земной коры к поверхности в термоградиентном поле Земли. Вертикальные градиенты температуры и давления в областях вулканической и гидротермальной активности очень велики. Например, прямые замеры в скважине 30 Мутновского геотермального месторождения на Камчатке показали значения температуры на глубине 950 м в 230º С и давления в 27 бар (до начала его эксплуа-
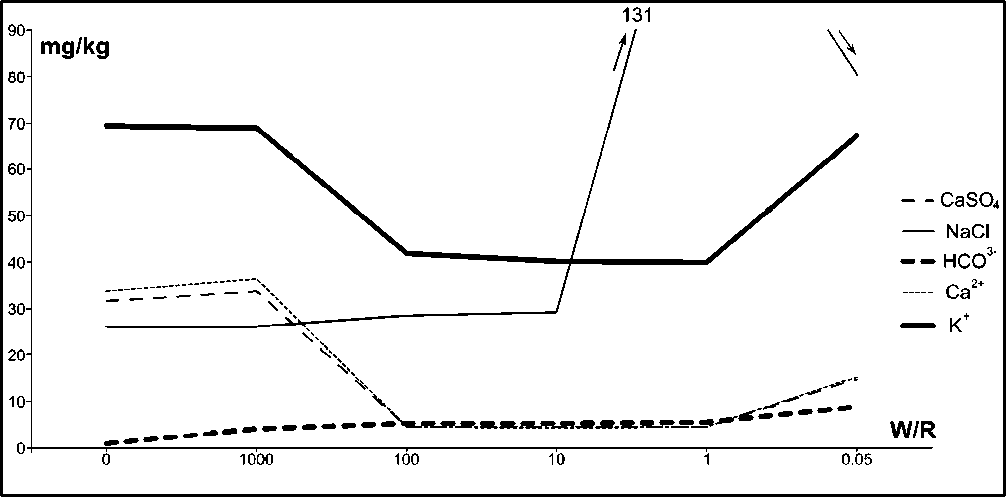
Рис. 3. Концентрации CaSО4, NaCl, НСО3-, Са+2, К+ при разных соотношениях W/R и стабильных температуре (150°С) и давлении (10 бар), без добавления 2 молей СО2
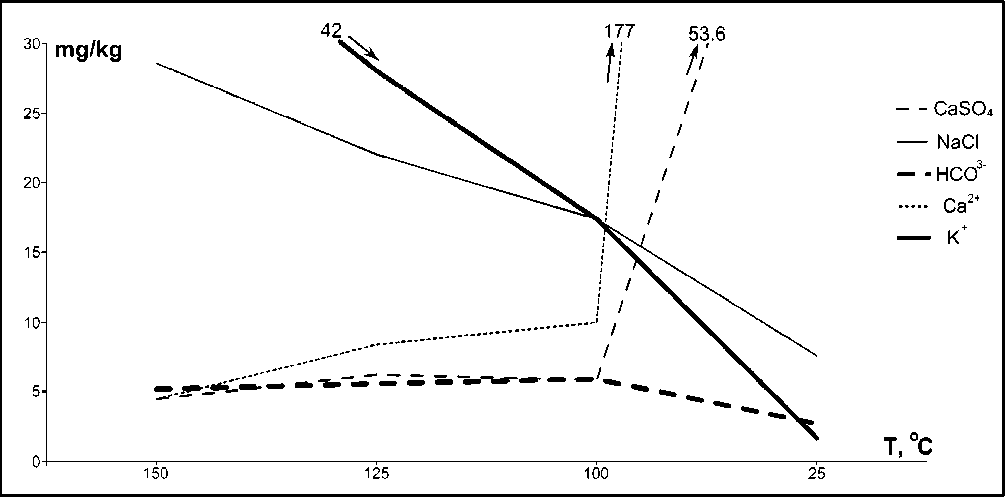
Рис. 4. Концентрации CaSО4, NaCl, НСО3-, Са+2, К+ при разной температуре и стабильном соотношении W/R (100) и давлении (10 бар), без добавления 2 молей СО2
тации – 45 бар), а на поверхности в устье данной скважины – 120º С и 2 бара [5, 7]. При движении к поверхности флюиды проходят через открытые пространства (крупные трещины и пустоты), зоны дробления с сопоставимым соотношением жидкой и твердой фаз и поры. Из результатов проведенного исследования следует, что в таких условиях неизбежна постоянная перестройка состава и структуры растворов, сопровождаемая концентрационными колебаниями. При этом в естественной среде такая изменчивость, несомненно, имеет гораздо более сложный характер, чем продемонстрированная на основе результатов проведенного исследования. Из всего многообразия горных пород и газов, присутствующих в верхней части земной коры, мы включили в исследованную систему только метабазит и углекислоту. Тем не менее, из проведенных расчетов вытекает принципиальная изменчивость гидротермальной среды, проявляющаяся в наличии разнообразных разноранговых флуктуаций.
Рассматривая результаты проведенного исследования в контексте инверсионного подхода к зарождению биосферы, можно отметить следующее. Данный подход постулирует необходимость существенных колебаний термодинамических и физико-химических параметров в материнской среде. Такие колебания являются естественными для гидротермальных систем, что подтверждается приведенными данными. Это отличает их от океана с его достаточно стабильными условиями, в котором имеют место только слабые флуктуации, связан- ные с морскими течениями или суточными колебаниями температуры. Таким образом, гидротермальные системы (их подповерхностные области, а также зоны разгрузки на дне океанов и на континентах) могут рассматриваться в качестве наиболее вероятной среды для возникновения первичных форм жизни.
Список литературы Термодинамические расчеты параметров состояния гидротермальной среды для моделирования процесса зарождения биосферы
- Авченко О.В. Петрология Охотского метаморфического комплекса. М.: Наука, 1977.
- Авченко О.В., Чудненко К.В., Александров И.А. Основы физико-химического моделирования минеральных систем. М.: Наука, 2009. 229 с.
- Авченко О.В., Чудненко К.В., Александров И.А., Худоложкин В.О. Адаптация программного комплекса «Селектор_С» к решению проблем петрогенезиса метаморфических пород//Геохимия. 2011. № 2. С.149-164.
- Кирюхин А.В., Лесных М.Д., Поляков А.Ю. Естественный гидродинамический режим Мутновского геотермального резервуара и его связь с сейсмической активностью//Вулканология и сейсмология. 2002. №1. С. 51-60.
- Кирюхин А.В., Москалев Л.К., Поляков А.Ю., Чернев И.И. Изменение термогидродинамического и газогидрохимического режима резервуара в процессе эксплуатации Мутновского геотермального месторождения//XVIII Совещание по подземным водам Сибири и Дальнего Востока. Иркутск, 2006. С. 267-271.
- Компаниченко В.Н. Этапы перехода от доклеточных органических микросистем к первичным сообществам прокариот//Известия РАН. Сер. биологическая. 2011. № 5. С. 630-640.
- Компаниченко В.Н., Шлюфман К.В. Амплитудно-частотная характеристика колебаний давления пароводяной смеси в Верхне-Мутновской гидротермальной системе//Вулканология и сейсмология. 2013. № 5. С. 51-58.
- Чудненко К.В. Термодинамическое моделирование в геохимии: теория, алгоритмы, программное обеспечение, приложения. Новосибирск: Академическое издательство «Гео», 2010. 287с.
- Brown Kevin M., Tryon Michael D., DeShon Heather R., Dorman LeRoy M. and Schwartz Susan Y. Correlated transient fluid pulsing and seismic tremor in the Costa Rica subduction zone//Earth and Planetary Science Letters. 2005. Vol. 238, N 1-2. P. 189-203.
- Cleaves HJ., Aubrey AD., Bada JL. An evaluation of critical parameters for abiotic peptide synthesis in submarine hydrothermal systems//Origins of Life and Evolution of Biospheres. 2009. Vol. 39. P. 109-126.
- Corliss JB., Baross JA., Hoffman SE. An hypothesis concerning the relationship between submarine hot springs and the origin of life on the Earth//Oceanological Acta. 1981. SP 4. P. 59-69.
- Deamer DW. Prebiotic amphiphilic compounds. In: Seckbach J (ed) Origins. Kluwer, Netherlands, 2004. P. 75-89.
- Diener J.F.A., Powell R., White R.W., Holland T.J.B. A new thermodynamic model for clino-and orthoamphiboles in the system Na2O-CaO-FeO-MgO-Al2O3-SiO2-H2O-O//Journal of Meta-morphic Geology. 2007. Vol. 25. P. 631-656.
- Green E., Holland T.J.B., Powell R. An order disorder model for omphacitic pyroxenes in the system jadeite -diopside -hedenbergite -acmite, with applications to eclogitic rocks//American Mineralogist. 2007. Vol. 92, N 7. P. 1181-1189.
- Holland T.J.B., Powell R. An internally consistent thermodynamic data set for phases of petrological interest//Journal of Metamorphic Geology. 1998. Vol. 16, N 3. P. 309-343.
- Kompanichenko V.N. Inversion concept of the origin of life//Origins of Life and Evolution of Biospheres. 2012. Vol. 42 (2-3). P. 153-178.
- Kompanichenko V.N., Poturay V.A., Shlufman K.V. Hydrothermal systems of Kamchatka are models of the prebiotic environment. Origin of Life and Evolution of Biospheres. 2015. DOI 10.1007/s11084-015-9429-2.
- Kralj Pt., Kralj Pol. Thermal and mineral waters in north-eastern Slovenia//Environmental Geology. 2000. Vol. 39, N 5. P. 488-498.
- Lee B.I., Kesler M.G. Generalized thermodynamic correlations based on three parameter corresponding//AICHEJ. 1975. Vol. 21, N 3. P. 510-527.
- Marshall WL. Hydrothermal synthesis of amino acids//Geochimical et Cosmochimical Acta. 1994. Vol. 58. P. 2099-2106.
- Martin W, Russell JM. On the origin of biochemistry at an alkaline hydrothermal vent//Philosophical Transactions of Royal Society B. 2007. Vol. 362. P. 1887-1925.
- Stefansson V. The Krafla geothermal field, North-East Iceland//Geothermal Systems: Principles and Case Histories. New York: Perhamon Press, 1981. P. 271-294.
- Tajcmanova L., Connolly J.A.D., Cesare B. A thermodynamic model for titanium and ferric iron solution in biotite//Journal of Metamorphic Geology. 2009. Vol. 27. P. 153-165.
- White R.W., Powell R., Clarke G.L. The interpretation of reaction textures in Fe_rich metapelitic granulites of the Musgrave Block, central Australia: constraints from mineral equilibria calculations in the system K2O-FeO-MgO-Al2O3-SiO2-H2O-TiO2-Fe2O3//Journal of Metamorphic Geology. 2002. Vol. 20. P. 41-55.
- White R.W., Pomroy N.E., Powell R. An in situ metatexite-diatexite transition in upper amphibolite facies rocks from Broken Hill, Australia//Journal of Metamorphic Geology. 2005. Vol. 23. P. 579-602.


