Успешное лечение сепсиса после трансплантации печени у ВИЧ-положительного пациента с множественными сопутствующими заболеваниями: клинический случай
Автор: Казымов Б.И., Алекберов К.Ф., Ядрихинская М.С., Кузнецова А.Д., Петрова А.О., Шемакин С.Ю.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Клинический случай
Статья в выпуске: 2 т.15, 2025 года.
Бесплатный доступ
Введение. Исторически ВИЧ-инфицированным пациентам долгое время отказывали в трансплантации печени из-за опасений худших результатов по сравнению с неинфицированным населением. Благодаря достижениям в области антиретровирусной терапии и улучшенному пониманию иммунологического состояния этих пациентов, трансплантация стала жизнеспособным вариантом лечения. Описание случая. В данном отчёте описывается 56-летний ВИЧ-положительный мужчина с множественными сопутствующими заболеваниями, перенёсший трансплантацию печени по поводу терминальной стадии заболевания печени вследствие хронического гепатита В. Ранний посттрансплантационный период осложнился тяжёлым сепсисом, полиорганной недостаточностью и дисфункцией трансплантата. Методы лечения. Комплексная терапия включала длительную вазопрессорную поддержку, заместительную почечную терапию, многократные переливания крови и целенаправленную антимикробную терапию. Результаты. Пациент был успешно вылечен и выписан в стабильном состоянии с функционирующим трансплантатом. Заключение. Этот случай демонстрирует, что даже тяжёлые инфекционные осложнения после трансплантации печени у полиморбидных ВИЧ-положительных пациентов могут быть успешно излечены при соответствующем мультидисциплинарном интенсивном лечении.
ВИЧ-инфекция, Трансплантация печени, Сепсис, Полиорганная недостаточность, Иммуносупрессивная терапия, Антиретровирусная терапия, Посттрансплантационные осложнения, Гепатит B, Интенсивная терапия, Гемодиафильтрация
Короткий адрес: https://sciup.org/143184264
IDR: 143184264 | УДК: 616.36-089.843+616.94+616.98:578.828.6 | DOI: 10.20340/vmi-rvz.2025.2.CASE.3
Successful Management of Sepsis Following Liver Transplantation in an HIV-Positive Patient with Multiple Comorbidities: a case report
Introduction. Historically, HIV-infected patients were denied liver transplantation due to concerns about poorer outcomes compared to the non-infected population. Due to advances in antiretroviral therapy and improved understanding of the immunological status of these patients, transplantation has become a viable treatment option. Case Description. This report describes a 56-year-old HIV-positive man with multiple comorbidities who underwent liver transplantation for end-stage liver disease due to chronic hepatitis B. The early post-transplantation period was complicated by severe sepsis, multiple organ failure, and graft dysfunction. Treatment Methods. Comprehensive therapy included prolonged vasopressor support, renal replacement therapy, multiple blood transfusions, and targeted antimicrobial therapy. Results. The patient was successfully treated and discharged in stable condition with a functioning graft. Conclusion. This case demonstrates that even severe infectious complications after liver transplantation in polymorbid HIV-positive patients can be successfully treated with appropriate multidisciplinary intensive care.
Текст научной статьи Успешное лечение сепсиса после трансплантации печени у ВИЧ-положительного пациента с множественными сопутствующими заболеваниями: клинический случай
Появление высокоактивной антиретровирусной терапии (ВААРТ) кардинально трансформировало парадигму ведения пациентов с ВИЧ-инфекцией, переведя патологию из категории фатальных в разряд хронических заболеваний, что инициировало фундаментальный пересмотр стратегии трансплан-тологической помощи данному контингенту [1, 2]. Эпидемиологическая конвергенция ВИЧ-инфекции и вирусных гепатитов В и С, обусловленная общностью путей трансмиссии, детерминирует экспоненциальный рост когорты ВИЧ-позитивных пациентов с терминальной гепатопатией, нуждающихся в трансплантации печени [3, 4]. Клиникоэкспериментальные исследования демонстрируют, что ВИЧ-инфекция потенцирует фибротическую трансформацию печёночной паренхимы, при этом терминальная печёночная недостаточность и гепатоцеллюлярная карцинома являются доминирующими факторами летальности в популяции ВИЧ-инфицированных пациентов [5, 6] с аннуализиро-ванным риском летального исхода вследствие гепа-топатии, достигающим 50% [7, 8].
Традиционно, фундаментальными контраргументами к выполнению трансплантации ВИЧ-серопозитивным реципиентам являлись опасения акселерации прогрессирования ВИЧ-инфекции и повышенной чувствительности к генерализованным инфекционным осложнениям, в особенности сепсису, ассоциированным с исходной иммунологической компрометацией [9]. Сепсис остаётся одним из наиболее девастирующих и потенциально фатальных осложнений в постоперационном периоде трансплантации печени, особенно у иммунодефицитных пациентов [3, 10]. Предикторами повышенного риска генерализованной инфекции у ВИЧ-позитивных реципиентов являются базисная иммунологическая дисфункция, полиморбидность и ятрогенная иммуносупрессия, необходимая для профилактики отторжения аллотрансплантата [2, 9].
Вопреки исторически сложившемуся скептицизму, современные многоцентровые исследования демонстрируют обнадеживающие показатели выживаемости среди тщательно селектированных ВИЧ-положительных реципиентов печёночного трансплантата [3, 10]. Эффективная терапия посттрансплантационного сепсиса в данной когорте пациентов базируется на мультидисциплинарном подходе, включающем своевременную идентификацию инфекционного агента, таргетную антимикробную терапию и комплексную органопротективную поддержку. Российская школа трансплантации печени ВИЧ-инфицированным пациентам находится в стадии методологического становления, при этом предварительные результаты свидетельствуют о перспек- тивности данного интервенционного подхода при условии оптимальной селекции кандидатов [11].
Настоящий клинический случай представляет собой всесторонний анализ успешного ведения тяжелого сепсиса у полиморбидного ВИЧ-позитивного пациента в постоперационном периоде трансплантации печени, иллюстрирующий, что адекватная интенсивная терапия способна нивелировать даже витальные инфекционные осложнения у данной категории высокорисковых пациентов.
Клинический случай
Информация о пациенте
Пациент А., 56 лет, мужчина (рост 186 см, вес 100 кг) с недавно диагностированной ВИЧ-инфекцией (январь 2022 г.) и положительной серологией на Treponema pallidum. В анамнезе гипертоническая болезнь с преимущественным поражением сердца (стадия 2, степень 2, сердечнососудистый риск 4), ожирение и сахарный диабет 2 типа (целевой уровень HbA1c < 7,0%).
Клинические данные
Пациент первоначально был госпитализирован по поводу COVID-19, который осложнился двусторонней пневмонией (КТ степени 3), дыхательной недостаточностью (степень 2), интоксикационным и цитолитическим синдромами, а также септическим шоком.
В декабре 2022 года поступил в отделение трансплантации печени с декомпенсированным циррозом печени вследствие хронического вирусного гепатита В. Функция печени была значительно нарушена: класс C по Чайлд-Пью (15 баллов), шкала MELD 36. У пациента наблюдалась портальная гипертензия, проявляющаяся расширением воротной и селезёночной вен, гепатоспленомегалией, асци- том (2 степени), варикозным расширением вен пищевода (2 степени) и портальной гастропатией. Также имелись гиперспленизм с тромбоцитопенией и панцитопенией, а также печёночная недостаточность (гипопротеинемия, гипоальбуминемия, гипокоагуляция и энцефалопатия 1 степени). Дополнительные находки включали гранулирующую рану перианальной области после удаления остроконечных кондиллом, наружно-внутренний геморрой с кровотечением в анамнезе.
Диагностическая оценка
При поступлении пациент жаловался на одышку, дискомфорт в правом подреберье, увеличение живота и желтуху. Его состояние было расценено как тяжёлое с признаками печёночной недостаточности.
Терапевтическое вмешательство
Пациенту была выполнена трансплантация печени. Ранний послеоперационный период протекал относительно без особенностей, с уровнями АЛТ/АСТ 376/428 Ед/л в первый день. Он получал инфузионную терапию, антибактериальное лечение, иммуносупрессию и заместительную терапию.
Наблюдение и исходы: лечение сепсиса
В течение первой недели после трансплантации произошла дисфункция и отторжение трансплантата. Впоследствии у пациента развился тяжёлый сепсис с полиорганной недостаточностью. Клинические проявления включали гемодинамическую нестабильность, требующую вазопрессорной поддержки, острое повреждение почек, требующее заместительной почечной терапии, коагулопатию, требующую многократных переливаний крови и плазмы, и дыхательную недостаточность.
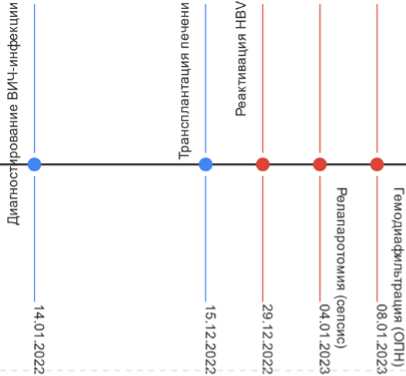
Н Первичная диагностика ■ Трансплантация
В Отдаленные осложнения
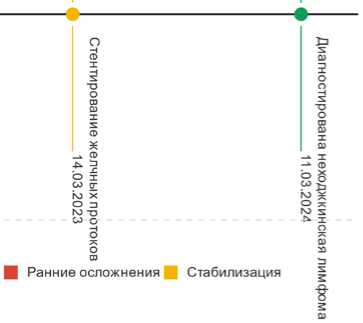
Рисунок 1. Временная диаграмма ключевых событий у пациента А
Figure 1. Time diagram of key events in patient A
Комплексное лечение сепсиса
Комплексный подход к лечению сепсиса у ВИЧ-положительного пациента после трансплантации печени включал несколько взаимосвязанных направлений терапии. Антимикробная терапия была начата эмпирически с комбинации меропенема (1 г каждые 8 часов внутривенно) и ванкомицина (1 г каждые 12 часов внутривенно), а после выявления возбудителей - Klebsiella pneumoniae и Enterococcus faecium - продолжена целенаправленно с учётом чувствительности; профилактически также были назначены флуконазол (400 мг в/в один раз в день) и ко-тримоксазол (480 мг ежедневно). Для поддержания гемодинамики применялась непрерывная инфузия норадреналина (0,15-0,5 мкг/кг/мин) для удержания среднего артериального давления выше 65 мм рт. ст., при рефрактерной гипотензии добавлялся вазопрессин (0,03 Ед/мин), проводился тщательный мониторинг центрального венозного давления и сердечного выброса, а также обеспечивалось поддержание внутрисосудистого объёма контролируемыми инфузиями кристаллоидов и альбумина.
Учитывая развитие острого повреждения почек с олигурией и повышением креатинина до 320 мкмоль/л, была инициирована продлённая вено-венозная гемодиафильтрация с последующим переходом на интермиттирующий гемодиализ по мере стабилизации состояния, при этом особое внимание уделялось коррекции электролитных нарушений, особенно гиперкалиемии. Нутритивная поддержка осуществлялась через назоеюнальный зонд (высокобелковая формула, 30 ккал/кг/день) с мониторингом гликемического профиля и поддержанием уровня глюкозы 8-10 ммоль/л, при недостаточности энтерального питания дополнительно применялось парентеральное. Критически важным компонентом была санация очагов инфекции, включавшая хирургический дебридмент инфицированных тканей передней брюшной стенки, установку VAC-системы для улучшения заживления раны и удаления инфекционного экссудата, а также регулярные повторные санации под анестезией.
Особенностью ведения данного пациента стала необходимость балансирования иммуносупрессии -дозы такролимуса были временно уменьшены (с целевой концентрацией 5-7 нг/мл во время сепсиса), доза микофенолата мофетила снижена на 50%, но при этом базовая иммуносупрессия поддерживалась метилпреднизолоном (8 мг/день) для предотвращения отторжения трансплантата; после разрешения сепсиса происходило постепенное возвращение к стандартным дозировкам. Для профилактики осложнений интенсивной терапии применялась ранняя мобилизация, компрессионные чулки, низкомолекулярный гепарин, специализиро- ванный противопролежневый матрас с регулярной сменой положения тела и регулярная санация полости рта. Антиретровирусная терапия также требовала временной коррекции с учётом множественных лекарственных взаимодействий с иммуно-супрессантами и антибиотиками, проводился регулярный мониторинг количества CD4-лимфоцитов и вирусной нагрузки ВИЧ, а для оптимизации подхода привлекался специалист по ВИЧ-инфекции.
Состояние пациента постепенно стабилизировалось на фоне этого интенсивного лечебного подхода. Через два месяца после операции было выполнено иссечение некротических участков передней брюшной стенки после ранее наложенной VAC-системы и наложены вторичные швы для окончательного закрытия раны.
Инструментальные исследования
Ультразвуковое исследование артерий и вен гепатобилиарной зоны
Воротная вена: 1,3 см, кровоток сохранён, линейная скорость кровотока 0,28 м/с.
Печеночная артерия: 0,4 см, линейная скорость кровотока 0,36 м/с, индекс резистентности 0,64.
Печёночная вена: 0,8 см, линейная скорость кровотока 0,24 м/с.
Результаты указывали на удовлетворительную гемодинамику печёночного трансплантата, несмотря на тяжёлый септический эпизод.
Ультразвуковое исследование органов брюшной полости
Нормально функционирующий трансплантат.
Лабораторные показатели при выписке:
МНО: 0,99.
Протромбиновое время: 11,6 с.
АЧТВ: 30,4 с.
Тромбоциты: 410×10^9/л.
Гемоглобин: 94 г/л.
Эритроциты: 3,19×10^12/л.
Вирус гепатита В: положительный.
Эти значения продемонстрировали замечательное восстановление функции печени и разрешение коагулопатии, которая присутствовала во время септического эпизода. Пациент был выписан в удовлетворительном состоянии с нормально функционирующим трансплантатом и инструкциями о наблюдении у местного хирурга и гепатолога.
Дальнейшее течение
Пациент поддерживал стабильную функцию трансплантата во время контрольных визитов. Через год после трансплантации он был госпитализирован в гематологическое отделение с лимфопролиферативными изменениями. Хотя это позднее осложнение не было напрямую связано с более ранним септическим эпизодом, оно подчеркивает продолжающиеся иммунологические проблемы в этой группе пациентов.
Обсуждение
Сепсис у ВИЧ-положительных реципиентов трансплантата печени
Сепсис представляет одну из наиболее значимых проблем в посттрансплантационном периоде для ВИЧ-положительных пациентов. Риск тяжёлой инфекции существенно повышен из-за нескольких факторов: предсуществующей иммунной дисфункции, связанной с ВИЧ-инфекцией [12, 13, 14], дополнительной иммуносупрессии, необходимой для предотвращения отторжения трансплантата [15, 16], и часто присутствующих сопутствующих заболеваний [4, 17]. В данном случае у пациента имелись множественные факторы риска, включая ВИЧ-инфекцию, коинфекцию гепатитом В [18, 19], сахарный диабет, ожирение и предшествующую инфекцию COVID-19 с тяжёлой пневмонией.
Российский опыт трансплантации печени ВИЧ-положительным пациентам всё ещё развивается. Недавнее исследование Новрузбекова М.С. и соавт. описало пять ВИЧ-инфицированных реципиентов, перенёсших трансплантацию печени в России между 2018 и 2022 годами, при этом четверо пациентов выжили и достигли стабильного состояния в отдалённом периоде [11]. Их анализ показал, что муль-тидисциплинарный подход, включающий специалистов по ВИЧ-инфекции, был необходим для успешных исходов.
Принципы лечения посттрансплантационного сепсиса
Этот случай иллюстрирует несколько ключевых принципов в лечении сепсиса после трансплантации печени у ВИЧ-положительных пациентов:
-
1. Раннее распознавание и вмешательство. Быстрая идентификация сепсиса критически важна для начала своевременного лечения [20, 21]. У нашего пациента развитие полиорганной дисфункции в первую неделю после трансплантации вызвало немедленную эскалацию помощи.
-
2. Микробиологическая диагностика. Получение соответствующих посевов перед началом анти-биотикотерапии и последующая коррекция лечения на основе результатов тестирования антимикробной чувствительности необходимы для эффективного контроля инфекции [22, 23]. В данном случае повторные бактериологические культуры направляли коррекцию антибиотического режима.
-
3. Мультидисциплинарный подход. Успешное лечение требовало сотрудничества между трансплантологами, специалистами по инфекционным заболеваниям, реаниматологами, нефрологами и специалистами по ВИЧ-инфекции [3, 9]. Этот скоординированный подход позволил сбалансированно управлять как иммуносупрессией, так и инфекцией.
-
4. Тщательная коррекция иммуносупрессии. Одним из наиболее сложных аспектов лечения сеп-
- сиса у реципиентов трансплантатов является балансирование необходимости предотвращения отторжения с контролем инфекции [15, 24]. Слишком большое снижение иммуносупрессии может привести к потере трансплантата, в то время как недостаточное снижение может препятствовать разрешению инфекции. У нашего пациента иммуносупрессия была тщательно скорректирована при мониторинге функции трансплантата.
-
5. Агрессивный контроль источника инфекции. Хирургическое вмешательство при инфицированных тканях, как показано некрэктомией и VAC-терапией в этом случае, часто необходимо для контроля источника инфекции [20, 21].
-
6. Поддерживающая терапия. Интенсивные поддерживающие меры, включая вазопрессорную терапию, заместительную почечную терапию и переливания компонентов крови, были критически важны для поддержания функции органов во время лечения инфекции [25, 26].
Барьеры и проблемы
Существует несколько барьеров для оптимального лечения ВИЧ-положительных реципиентов трансплантатов с сепсисом [11, 17]. Во-первых, опыт работы с этой специфической группой пациентов ограничен, особенно в регионах, где программы трансплантации для ВИЧ-положительных пациентов относительно новы. Во-вторых, лекарственные взаимодействия между антиретровирусными препаратами, иммуносупрессантами и антимикробными средствами усложняют фармацевтическое ведение [9, 10]. В-третьих, стигма, связанная с ВИЧ-инфекцией, может по-прежнему влиять на клинические решения в некоторых условиях [2, 6].
Несмотря на эти проблемы, данный случай демонстрирует, что при соответствующем интенсивном лечении и мультидисциплинарном подходе даже тяжёлый сепсис у полиморбидного ВИЧ-положительного реципиента печёночного трансплантата может быть успешно вылечен, приводя к сохранению трансплантата и выживанию пациента [10, 27].
Заключение
Данный случай демонстрирует успешное лечение тяжёлого сепсиса у ВИЧ-положительного пациента с множественными сопутствующими заболеваниями после трансплантации печени. Несмотря на развитие полиорганной недостаточности и дисфункции трансплантата в раннем посттрансплантационном периоде, интенсивное мультидисциплинарное лечение привело к разрешению инфекции, сохранению трансплантата и выживанию пациента до выписки.
Из этого опыта можно извлечь несколько ключевых уроков. Во-первых, ВИЧ-положительный статус не должен рассматриваться как абсолютное противопоказание к трансплантации печени, даже у паци- ентов со значительными сопутствующими заболеваниями [1, 3, 10]. Во-вторых, хотя посттрансплантационный сепсис в этой популяции представляет существенные проблемы, агрессивное и скоординированное лечение может привести к благоприятным исходам [26, 27]. В-третьих, мультидисципли-нарный подход с участием специалистов по трансплантации, реаниматологов, специалистов по инфекционным заболеваниям и ВИЧ-инфекции необходим для навигации по сложным взаимодействиям между ВИЧ-инфекцией, иммуносупрессией и сепсисом [9, 11].
По мере роста опыта трансплантации печени у ВИЧ-положительных пациентов в России и во всем мире, вероятно, появятся стандартизированные протоколы профилактики и лечения сепсиса в этой уникальной популяции. Этот случай дополняет растущую совокупность доказательств того, что даже тяжёлые инфекционные осложнения могут быть преодолены при соответствующем интенсивном лечении [2, 3, 11], предлагая надежду на расширение доступа к трансплантации для ВИЧ-положительных пациентов с терминальной стадией заболевания печени.


