Влияние Helicobacter pylori на содержание провоспалительных Т-клеточных цитокинов и продуцирующих их субпопуляций
Автор: Цыганова М.И., Талаева М.В., Талаев В.Ю., Неумоина Н.В., Перфилова К.М., Мохонова Е.В., Лапин В.А., Мелентьев Д.А.
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Экспериментальные модели и инструментальные исследования для оценки риска в гигиене и эпидемиологии
Статья в выпуске: 3 (23), 2018 года.
Бесплатный доступ
Резюме: Helicobacter pylori - распространенный патогенный микроорганизм, проникающий в слизистую желудка и двенадцатиперстную кишку и способствующий развитию заболеваний желудочно-кишечного тракта, в том числе и онкологического характера. Данный возбудитель склонен к длительному хроническому персистированию в организме, часто не сопровождающемуся какими-либо выраженными симптомами, что сильно затрудняет его своевременное обнаружение. Анализ риска возникновения и развития различных патологий, ассоциированных с Helicobacter pylori, показывает, что значительную роль в их протекании играет характер иммунного ответа, развивающегося после инфицирования. Существуют данные, что Helicobacter pylori способен влиять на защитные иммунные реакции, смещая их баланс в сторону иммуносупрессивной составляющей, например, повышения содержания Т-регуляторных клеток и вырабатываемых ими цитокинов. Однако существуют также данные о том, что параллельно Helicobacter pylori способен вызывать ответные реакции провоспалительного характера, включающие в себя пути, ассоциированные с Т-хелперными клетками 1-го и 17-го типа...
Лимфоциты, т-хелперные клетки, дифференцировка, костимуляция, антитела, проточная цитофлюорометрия, клеточные культуры, т-helpers
Короткий адрес: https://sciup.org/142215928
IDR: 142215928 | УДК: 616.98: | DOI: 10.21668/health.risk/2018.3.13
Influence exerted by Helicobacter pylori on concentrations of anti-inflammatory Т-cell cytokines and sunpopulations that produce them
Helicobacter pylori is a widely spread pathogenic microorganism. It penetrates the mucous tunic of the stomach and the duodenum and causes diseases in the gastrointestinal tract, including oncologic ones. This agent is able to be chronically persistent in a body and frequently there are no apparent symptoms of it; therefore, it is difficult to detect this pathogen in due time. Risk analysis related to occurrence and development of various pathologies associated with Helicobacter pylori, revealed that their clinical course was to a great extent determined by an immune response that emerged after infection. There are data that Helicobacter pylori is able to influence protective immune reactions making their balance to move to an increase in immune-suppressive components, for example, increased concentrations of T-regulatory cells and cytokines produced by them. However, some data can be found on Helicobacter pylori ability to induce anti-inflammatory responses which include those associated with T-helpers of the 1st and 17th types...
Текст научной статьи Влияние Helicobacter pylori на содержание провоспалительных Т-клеточных цитокинов и продуцирующих их субпопуляций
Вследствие этого оценка провоспалительного действия H. pylori и механизмов, определяющих склонность возбудителя как к регуляторному, так и провоспалительному действию представляется актуальной научно-практической задачей. Кроме того, значительный интерес представляет предварительно показанная для H. pylori возможность напрямую, без участия антигенпрезентирующих клеток (АПК) влиять по крайней мере на некоторые субпопуляции Т-клеток человека.
Целью работы была оценка способности H. pylori стимулировать образование INF-γ, IL-17A и Th17 в условиях прямого контакта между бактериями и Т-клетками, без участия АПК.
37 °С, в течение 7 суток. Идентификацию H. pylori осуществляли на основании культуральных и морфологических признаков.
Для оценки влияния H. pylori на дифференцировку лимфоцитов производилось сокультивирова-ние лимфоцитов с различными концентрациями бактерий (последовательно использовались соотношения лимфоцитов к H. pylori 1:10, 1:20, 1:50) в течение 18 часов в условиях: 5 % CO 2 , 37 °С, среда RPMI-1640 (Gibco, США) с добавлением 10%-ной эмбриональной телячьей сыворотки и 0,3 г/л L-глутамина («Панэко», Россия). Часть лимфоцитов со-культивировалась с бактериями в присутствии дополнительных стимуляторов – моноклональных антител к молекуле CD3 (1 мкг/мл, eBioscience, США), имитирующих воздействие на Т-клеточный рецептор, или смеси антител к CD3 и CD28 (1 мкг/мл, eBioscience, США, и 3 мкг/мл, Beckman Coulter, Франция), имитирующих воздействие АПК на Т-клетки. Имелись следующие культуры: лимфоциты с добавлением H. pylori , но без добавления стимулирующих антител; лимфоциты с добавлением антител к CD3 и без добавления бактерий; лимфоциты с добавлением антител к CD3 и с добавлением H. pylori ; лимфоциты с добавлением антител к CD3 и CD28, и без добавления H. pylori ; и лимфоциты с добавлением антител к CD3 и CD28 и добавлением H. pylori . Последний вариант добавлялся с целью оценить степень влияния, оказываемого на характер стимуляции непосредственным присутствием возбудителя. Эксперименты для всех соотношений лимфоцитов и бактерий проводились отдельно. Негативными контролями для всех вариантов культур служили лимфоциты без добавления H. pylori и стимулирующих антител.
По истечении 18 часов в культурах цитофлюорометрически оценивалось содержание Th17 как клеток фенотипа CD4+CD161+ и CD4+IL-17A+. Для окрашивания указанных маркеров применялись антитела к CD4, меченные FITC, антитела к CD161, меченные PE, антитела к IL-17A, меченные PE, все – производства eBioscience, США. Пермеабилизацию мембран, необходимую для мечения IL-17A, производили набором реагентов Fix/Perm Concentrate и Perm Buffer (eBioscience, США), согласно инструкциям производителя. Анализ осуществляли на ци-тофлюориметре FacsCalibur (Beckton Dickinson, США). Активность Th1 определялась путем измерения концентрации INF-γ в надосадках культур методом ИФА («Вектор-Бест», Россия). Для статистической обработки данных использовался критерий Ньюмена–Кейлса.
Результаты и их обсуждение. Одним из важных моментов в реализации иммунного ответа является повышение уровня INF-γ. Как активатор макрофагов этот цитокин задействован в непосредственном ответе на инфекционные атаки, кроме того, он усиливает эффекты интерферонов α и β, способствует развитию иммунного ответа по Th1-типу и обладает способностью стимулировать активность антигенпрезентирующих клеток [22]. Как можно видеть на рис. 1, добавление H. pylori к суспензии выделенных лимфоцитов как без дополнительных стимуляторов, так и в совокупности с антителами к CD3 или CD3/CD28 приводило к статистически достоверному повышению продукции INF-γ.
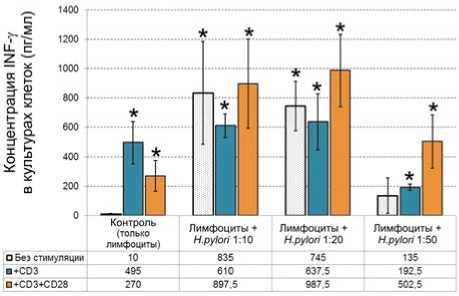
Рис. 1. Влияние H. pylory на продукцию INF-γ. Варианты стимуляции обозначены под диаграммой. Контроль – лимфоциты без добавления бактерий и антител, * – достоверные отличия от контроля ( p <0,05)
Данные о влиянии H. pylori на дифференцировку лимфоцитов в сторону Th17 и приобретении ими фенотипа CD4+CD161+ при отсутствии в культурах дендритных клеток представлены на рис. 2 и 3.
Как можно видеть, совместное культивирование H. pylori и Т-клеток в течение 18 часов не приводило к повышению числа CD4+CD161+-клеток. Среднее содержание их в культурах без стимуляции бактериями составляло 20,065 ± 0,72 % от всех CD4+-клеток, при добавлении H. pylori к отвечающим лимфоцитам в соотношении 10:1 составляло 22,15 ± 1,49 %. При этом содержание этих клеток
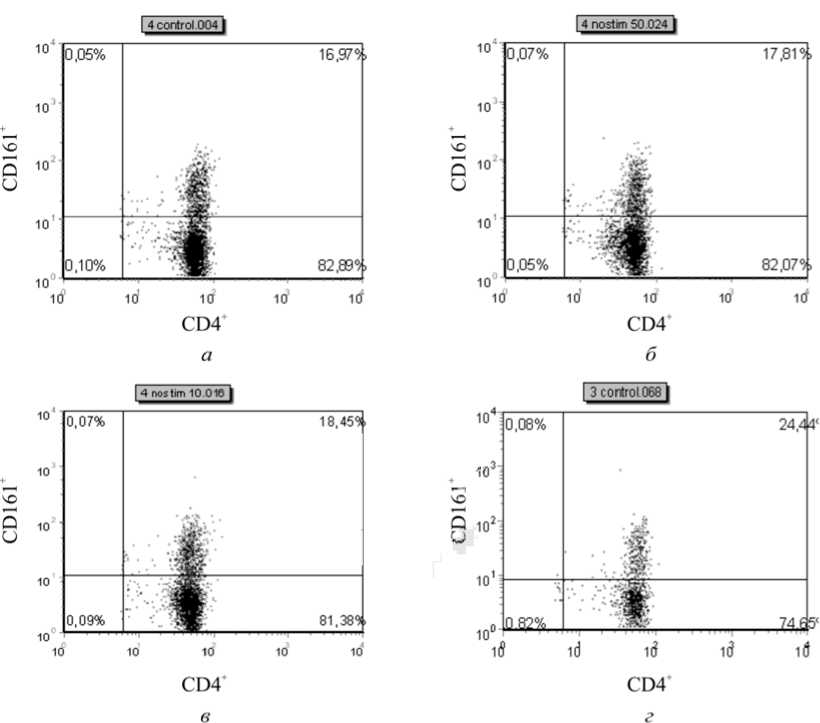
Рис. 2. Содержание CD4+CD161+-клеток в культуре Т-лимфоцитов при прямом сокультивировании с H. pylori без дополнительной стимуляции, в % от общего количества CD4+ клеток (данные репрезентативного эксперимента): а – контрольная суспензия лимфоцитов без добавления H. pylori , б – сокультивирование с H. pylori в соотношении 1:10, в , г – сокультивирование с H. pylori в соотношении 1:20 и 1:50 соответственно. Процентное содержание клеток указано в углах квадрантов
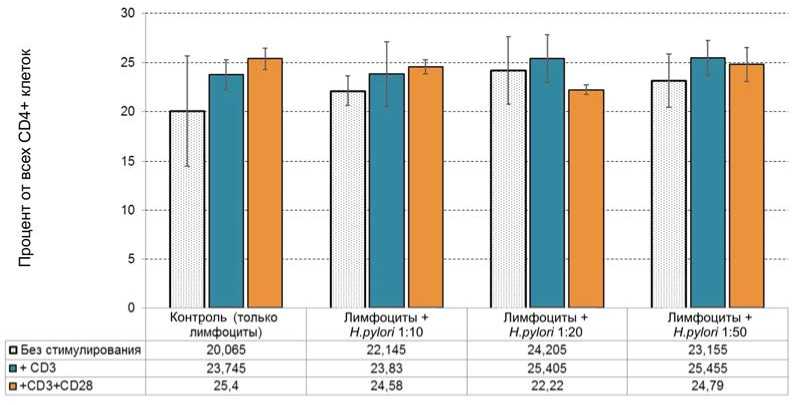
Рис. 3. Влияние H. pylory на содержание CD4+CD161+-клеток. Варианты стимуляции обозначены под диаграммой. Контроль – лимфоциты без добавления бактерий и антител
Содержание IL-17А+СD4+ клеток в условиях сокультивирования с H. pylory и/или дополнительной стимуляции антителами к CD3 и CD28
в культурах с соотношением клеток 1:20 и 1:50 также было практически не отличимо от контрольных значений нестимулированных лимфоцитов (для соотношения 20:1 содержание составило 24,2 ± 3,41 %, а для соотношения 50:1 – 23,15 ± 2,73 %.).
Для проверки значимости костимуляции нами были поставлены дополнительные эксперименты с добавлением стимулирующих антител к молекулам CD3 и CD3+CD28, предоставляющих Т-клеткам сигнал, подобный стимуляции от антигенпрезентирующих клеток. В культуре Т-лимфоцитов без H. pylori но с добавлением антител к CD3 содержание CD4+CD161+-клеток составило 23,745 ± 7,3 %. В то же время при добавлении и H. pylori, и антител к CD3 содержание CD4+CD161+-клеток составило 23,83 ± 3,30 % для соотношения 1:10, 25,4 ± 2,42 % для соотношения 1:20 и 25,4 ± 1,75 % для соотношения 1:50.
Молекула CD161 при ее коэкспрессии с молекулой CD4 широко используются в мировой научной практике как маркер популяции Th17. Однако наличие мембранных фенотипических маркеров не гарантирует функциональной способности отвечающих клеток к продукции IL-17A – основной функции Th17. Также, по мнению некоторых авторов, оценка содержания Th17 по наличию внутриклеточного IL-17A или его продукции является более надежным методом, чем применение CD161. Учитывая вышеизложенное, было оценено содержание внутриклеточного IL-17А в культурах лимфоцитов, отвечающих на H. pylory . Для этого произвели пермеабилизацию мембран отвечающих клеток и окрашивание их моноклональными антителами к IL-17A. Было установлено, что в применяющихся условиях культивирования большинство клеток не повышают экспрессию IL-17А (таблица).
Так, ни в одном из применяемых вариантов стимуляции и соотношений отвечающих клеток и бактерий содержание IL-17А+-клеток не превышало 0,5 % от всех CD4+-клеток пробы, что не отличается от нормального содержания IL-17+-клеток в крови человека [23–25].
Выводы. Прямое сокультивирование выделенных Т-лимфоцитов с H. pylori способствует резкому повышению продукции INF-γ, что в условиях данного эксперимента может с большой вероятностью свидетельствовать об активации Th1. Однако процент содержания Тh17, определяемых и как CD4+CD161+, и как CD4+IL17A+ в таких условиях сколько-нибудь значимо не изменяется. Можно предположить, что ответная реакция Т-хелперов на прямой контакт с H. pylori при ее провоспалитель-ном течении проходит по Th1-типу, без существенного вовлечения Th17. Механизм же, определяющий способность H. pylori стимулировать активность как Th1, так и T-reg (что было показано нами ранее), требует дополнительного исследования. В целом механизмы и действующие агенты, с помощью которых может осуществляться прямое воздействие патогенов на выбор преобладающего типа иммунного ответа, по мнению авторов, представляют значительный фундаментальный и практический интерес, поскольку потенциально могут быть использованы при разработке лекарственных средств, направляющих иммунный ответ в благоприятную сторону. Также значимы они и для оценки риска развития гиперстимулированных форм иммунного ответа у пациентов, инфицированных H. pylori .
Финансирование. Исследование не имело спонсорской поддержки.
Список литературы Влияние Helicobacter pylori на содержание провоспалительных Т-клеточных цитокинов и продуцирующих их субпопуляций
- Inflammatory bowel diseases: review of known environmental protective and risk factors involved/K.W.J. van der Sloot, M. Amini, V. Peters, G. Dijkstra, B.Z. Alizadeh//Inflamm Bowel Dis. -2017. -Vol. 9. -P. 1499-1509.
- Pachathundikandi S.K., Müller A., Backert S. Inflammasome activation by Helicobacter pylori and its Implications for persistence and immunity//Curr. Top. Microbiol. Immunol. -2016. -Vol. 397. -P. 117-131.
- Helicobacter pylori polyclonally activates murine CD4+ T-cells in the absence of antigen-presenting cells/C. Rosenplenter, F. Sommer, P. Kleemann, A. Belkovets, A. Schmidt, M. Lohoff//Eur. J. Immunol. -2007. -Vol. 37, № 7. -P. 1905-1915.
- Microbes and viruses are bugging the gut in celiac disease. Are they friends or foes?/A. Lerner, M. Arleevskaya, A. Schmiedl, T. Matthias//Front Microbiol. -2017. -Vol. 8. -P. 1392.
- Chen Y., Blaser M.J. Helicobacter pylori colonization is inversely associated with childhood asthma//J. Infect. Dis. -2008. -Vol. 198. -P. 553-560.
- Diagnosis of Helicobacter pylori infection is associated with lower prevalence and subsequent incidence of Crohn's disease/L.E. Bartels, P. Jepsen, L.A. Christensen, L.U. Gerdes, H. Vilstrup, J.F. Dahlerup//Journal of Crohn's and Colitis. -2016. -Vol. 10, № 4. -P. 443-448.
- Helicobacter pylori infection prevents allergic asthma in mouse models through the induction of regulatory T cells/I.C. Arnold, N. Dehzad, S. Reuter, H. Martin, B. Becher, C. Taube, A. Mьller//Journal Clin. Invest. -2011. -Vol. 121, № 8. -P. 3088-3093.
- The effect of Helicobacter pylori on asthma and allergy/A. Amedei, G. Codolo, G. Del Prete, M. de Bernard, M.M. D'Elios//Journal Asthma. Allergy. -2010. -Vol. 3. -P. 139-147.
- Lymphocytes in the human gastric mucosa during Helicobacter pylori have a T-helper cell 1 phenotype/K.B. Bamford, X. Fan, Sh.E. Crowe, J.F. Leary, W.K. Gourley, G.K. Luthra, E.G. Brooks, D.Y. Graham, V.E. Reyes, P.B. Ernst//Gastroenterology. -1998. -Vol. 114, № 3. -P. 482-492.
- Tarkkanen J., Kosunen T.U, Saksela E. Contact of lymphocytes with Helicobacter pylori augments natural killer cell activity and Induces Production of Gamma Interferon//Infection and immunity. -1993. -Vol. 61, № 7. -P. 3012-3016.
- Tsai H.-F., Hsu P.-N. Interplay between Helicobacter pylori and immune cells in immune pathogenesis of gastric inflammation and mucosal pathology//Cellular & Molecular Immunology. -2010. -Vol. 7. -P. 255-259.
- Влияние Helicobacter pylori на дифференцировку Т-регуляторных клеток/А.В. Матвеичев, М.В. Талаева, В.Ю. Талаев, Н.В. Неумоина, К.М. Перфилова, Д.Г. Лапаев, Е.В. Мохонова, М.И. Цыганова, В.Н. Коптелова, З.И. Никитина, В.А. Лапин, Д.А. Мелентьев//Анализ риска здоровью. -2017. -№ 1. -С. 21-28.
- Human peripheral and gastric lymphocyte responses to Helicobacter pylori NapA and AphC differ in infected and uninfected individuals/H.J. Windle, Y.S. Ang, V. Athie-Morales, R.McManus, D.Kelleher//Gut. -2005. -Vol. 54, № 1. -P. 25-32.
- Involvement of Toll-like receptors on Helicobacter pylori-induced immunity/R. Kдbisch, R. MejнasLuque, M. Gerhard, C. Prinz//PLoS One. -2014. -Vol. 9, № 8. -P. e104804.
- Shiu J., Blanchard T.G. Dendritic cell function in the host response to Helicobacter pylori infection of the gastric mucosa//Pathog. Dis. -2013. -Vol. 67, № 1. -P. 46-53.
- Interleukin-17C in human Helicobacter pylori gastritis/S. Tanaka, H. Nagashima, M. Cruz, T. Uchida, T. Uotani, J.A. Jimйnez Abreu, V. Mahachai, R. Vilaichone, T. Ratanachu-ek, L. Tshering, D.Y. Graham, Y. Yamaoka//Infect Immun. -2017. -Vol. 85, № 10. -P. e00389-e00417.
- Permin H., Andersen L.P. Inflammation, immunity, and vaccines for Helicobacter infection//Helicobacter. -2005. -Vol. 10, № 1. -P. 21-25.
- Pre-differentiated Th1 and Th17 effector T cells in autoimmune gastritis: ag-specific regulatory T cells are more potent suppressors than polyclonal regulatory T cells/E.N. Huter, G.H. Stummvoll., R.J. DiPaolo D.D. Glass, E.M. Shevach//Int. Immunopharmacol. -2009. -Vol. 9, № 5. -P. 540-545.
- Правада Н.С., Будрицкий А.М. Комплексная терапия с применением иммунотропных препаратов при туберкулезе и система интерферона-гамма//Вестник Витебского государственного медицинского университета. -2015. -Т. 14, № 4. -С. 5-14.
- Th1-Th17 ratio as a new insight in rheumatoid arthritis disease/H. Bazzazi, M. Aghaei, A. Memarian, H. Asgarian-Omran, N.Behnampour, Y.Yasdani//Iran J. Allergy Asthma Immunol. -2018. -Vol. 17, № 1. -P. 68-77.
- Роль Helicobacter Pylori при развитии экстрагастродуоденальных заболеваний/Э.А. Бардахчьян, С.Ю. Ломов, Н.Г. Харланова, Н.В. Камнева//Экспериментальная и клиническая гастроэнтерология. -2005. -№ 3. -С. 20-27.
- Интерферон-γ: биологическая функция и значение для диагностики клеточного иммунного ответа/А.А. Луцкий, А.А. Жирков, Д.Ю. Лобзин, М. Рао, Л.А. Алексеева, М. Мейрер, Ю.В. Лобзин//Журнал инфектологии. -2015. -Т. 7, № 4. -С. 10-22.
- Percentages of CD4+CD161+ and CD4-CD8-CD161+ T сells in the synovial fluid are correlated with disease activity in rheumatoid arthritis/J. Miao, K. Zhang, F. Qiu, T. Li, M. Lv, N. Guo, Q. Han, P. Zhu//Mediators Inflamm. -2015. -Vol. 2015. -P ID 563713.
- Rheumatoid synovial fluid interleukin-17-producing CD4 T cells have abundant tumor necrosis factor-alpha co-expression, but little interleukin-22 and interleukin-23R expression/L.D. Church, A.D. Filer, E. Hidalgo, K.A. Howlett, A.M.C. Thomas, S. Rapecki, D. Scheel-Toellner, C.D. Buckley, K. Raza//Arthritis Res. Ther. -2010. -Vol. 12, № 5. -P. R184.
- Shen H., Goodall J.C, Hill Gaston H.J.S. Frequency and phenotype of peripheral blood Th17 cells in ankylosing spondylitis and rheumatoid arthritis//Arthritis & rheumatism. -2009. -Vol. 60, № 6. -P. 1647-1656.


