Влияние некоторых солей на растворимость лактозы
Автор: Гнездилова А.И., Шохалов В.А., Шохалова В.Н., Ефанова Е.А.
Журнал: Молочнохозяйственный вестник @vestnik-molochnoe
Статья в выпуске: 4 (60), 2025 года.
Бесплатный доступ
В работе экспериментально изучена растворимость лактозы и вязкость насыщенных растворов в присутствии хлоридов натрия и кальция и бикарбоната натрия. Установлено, что соли кальция обладают меньшей растворяющей способностью по сравнению с солями натрия. В небольших количествах (менее 5%) соли кальция способны снижать растворимость лактозы и интенсифицировать процесс кристаллизации. Анион хлора является более сильным мелассообразователем по сравнению с анионом углекислоты. Установленные закономерности следует учитывать в промышленном производстве молочного сахара.
Лактоза, растворимость, коэффициент насыщения, вязкость
Короткий адрес: https://sciup.org/149150043
IDR: 149150043 | УДК: 637.345 | DOI: 10.52231/2225-4269_2025_4_172
Effect of some salts on lactose solubility
The present work studies experimentally lactose solubility and the viscosity of saturated solutions in the presence of sodium and calcium chlorides as well as sodium bicarbonate. It has been established that calcium salts have lower dissolving capacity compared to sodium salts. In small amounts (less than 5%), calcium salts can reduce lactose solubility and intensify the crystallization process. The chloride anion is a stronger molasses former than the carbon dioxide anion. The established patterns should be taken into account in industrial manufacturing of milk sugar.
Текст научной статьи Влияние некоторых солей на растворимость лактозы
Актуальность
Основными параметрами, влияющими на процесс кристаллизации лактозы, являются: пересыщение, температура, гидромеханические условия, а также наличие в пересыщенных растворах примесей (несахаров).
Примеси могут содержаться в исходном сырье или попадать в раствор на стадиях технологической обработки, например, при очистке молочной сыворотки реагентами.
В настоящее время для очистки молочной сыворотки эффективно применяются баро- и электромембранные методы, такие как ультра-и нанофильтрация, обратный осмос и электродиализ [1–5]. Наряду с ними широко используются химические способы: кислотный, щелочной, кислотно-щелочной, хлор-кальциевый и безреагентный [6].
Например, при щелочном или кислотно-щелочном способе в сыворотку добавляют 10%-ный раствор гидроксида натрия или 10%-ный раствор гидрокарбоната натрия. Хлор-кальциевый способ предполагает внесение 20%-ного раствора хлорида кальция. Для повышения эффективности очистки сыворотки от белков и снижения затрат авторы [7] предложили метод раскисления 10%-ным раствором гидроксида натрия до pH 6,5–7,2 с последующим добавлением 40%-ного раствора хлорида кальция в количестве 0,1–0,4 г/л. Кроме того, хлорид натрия попадает в молочную сыворотку в процессе производства сыра (при посолке). Также был разработан способ раскисления и очистки творожной сыворотки сухими реагентами: оксидом или гидроксидом кальция [8].
В результате в пересыщенный раствор лактозы могут попадать катионы натрия и кальция, а также анионы хлора и углекислоты.
В связи с этим представляет интерес исследовать влияние этих ионов на растворимость лактозы, а следовательно, на процесс кристаллизации и выход молочного сахара.
Влияние некоторых примесей на растворимость лактозы изучалось в работах [9–14]. Исследования [9] показали, что растворимость лактозы в сывороточном пермеате выше, чем в воде. В лактозо-белковых смесях растворимость также отличается от растворимости в чистой воде [10, 11]. В работе [12] изучено влияние белков и показано, что растворимость зависит от их концентрации: с увеличением содержания белков растворимость лактозы сначала возрастает, а затем стабилизируется.
Одним из объяснений повышенной растворимости лактозы может быть образование комплексов [13]. Например, лактоза образует нерастворимый комплекс с кальцием. Гидроксид бария также образует комплекс с лактозой, но он менее устойчив, чем комплекс кальций-лактоза [14]. Существенное влияние на растворимость лактозы и её кристаллизацию оказывают минеральные соли. Так, хлорид лития снижает рас- творимость и увеличивает скорость роста кристаллов, в то время как гидрофосфат калия действует противоположным образом [15].
В работе [16] определялась растворимость лактозы в присутствии некоторых солей. Было установлено, что в области низких концентраций соли снижали растворимость, однако при дальнейшем увеличении их концентрации наблюдался некоторый рост растворимости лактозы.
Таким образом, растворимость лактозы напрямую влияет на пересыщение раствора, что, в свою очередь, определяет ход процесса кристаллизации, выход и качество готового молочного сахара.
Целью работы является экспериментальное изучение растворимости лактозы и вязкости насыщенных растворов в присутствии катионов натрия и кальция и анионов хлора и углекислоты.
Методы исследования
Для определения растворимости лактозы готовили ее насыщенные растворы. Для этого в термостатируемый стакан при температуре 20 ± 0,5 °C вносили навеску лактозы и при непрерывном перемешивании постепенно добавляли из термостатируемой пипетки водный раствор соли концентрацией 0–20 %. Процесс вели до полного растворения кристаллов,котороеконтролироваливизуальнопоисчезновениютвердой фазы. Время достижения насыщения составляло 6–10 часов. Состав насыщенного раствора лактозы определяли по массовой доле сухих веществ, измеренной на рефрактометре. Растворимость, выраженную в виде моногидрата лактозы, пересчитывали на безводную форму с учетом соотношения их молекулярных масс. Вязкость насыщенных растворов измеряли с помощью вискозиметра Гепплера. Все опыты проводили в трехкратной повторности; их результаты представлены в таблице 1.
Таблица 1 – Состав насыщенных растворов лактозы в присутствии некоторых примесей при 200С, % масс
|
NaHCО3 |
NaCl |
CaCl2 |
Лактоза |
Вода |
Вязкость, μ·103 Па.с |
|
- |
- |
- |
16,1 |
83,90 |
1,71 |
|
1,70 |
- |
- |
14,70 |
83,60 |
1,72 |
|
3,40 |
- |
- |
14,55 |
82,05 |
1,80 |
|
6,70 |
- |
- |
15,72 |
77,58 |
1,90 |
|
14,71 |
- |
- |
17,28 |
68,01 |
2,98 |
|
- |
- |
2,50 |
14,67 |
82,83 |
1,74 |
|
- |
- |
5,03 |
12,68 |
82,29 |
1,97 |
|
- |
- |
9,20 |
12,79 |
78,01 |
2,32 |
|
- |
- |
19,68 |
15,50 |
64,82 |
4,32 |
|
- |
1,34 |
- |
15,32 |
83,34 |
1,71 |
|
- |
2,65 |
- |
15,30 |
82,05 |
1,85 |
|
- |
5,24 |
- |
16,00 |
78,76 |
1,90 |
|
- |
12,30 |
- |
16,88 |
70,82 |
2,36 |
Для оценки растворимости лактозы по экспериментальным данным (таблица 1) был рассчитан коэффициент насыщения. Коэффициент насыщения, как известно, учитывает влияние различных примесей на растворимость лактозы и рассчитывается как отношение:
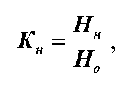
где н . - растворимость лактозы в данном растворителе, кг/кг воды;
H - растворимость лактозы в воде при той же температуре, кг/кг воды.
Коэффициент насыщения Кн и его зависимость от концентрации добавок в растворителе (Нс) представлена на рисунке 1.
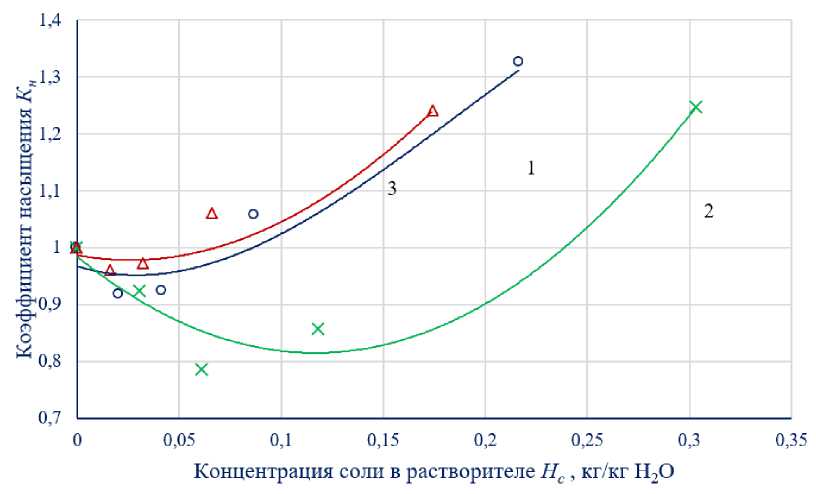
Рисунок 1 – Влияние некоторых солей на коэффициент насыщения Кн : 1 – NaHCО3; 2 – CaCl2; 3 – NaCl.
Согласно рисунку 1, с ростом концентрации солей в растворителе коэффициент насыщения сначала уменьшается, а затем возрастает. Первоначальное снижение растворимости связано с гидратацией ионов электролитов. Как указано в [16], гидратационная способность катионов усиливается в ряду Na ⁺ → Ca² ⁺ , причем соли кальция обладают наибольшим водоотнимающим эффектом. Последующее повышение растворимости при дальнейшем увеличении концентрации солей, вероятно, объясняется процессами комплексообразования и ассоциацией ионов с формированием общих гидратных оболочек [16, 17]. Эти процессы высвобождают часть молекул воды, которые затем участвуют в растворении лактозы.
Установленные закономерности по изменению коэффициента насыщения Кн были описаны с помощью уравнения:
KH = 1 — агНс + a2Hc — a3Hj ,
где Нс. – содержание соли в растворителе, кг/кг Н2О;
а 1 ,а 2, а 3 – коэффициенты.
Значения коэффициентов а 1 ,а 2 ,а 3 в уравнении (2) представлены в таблице 2.
Таблица 2 - Значение коэффициентов в уравнении (2)
|
Коэффициент |
NaHCО3 |
NaCl |
CaCl2 |
|
а1 |
1,0931 |
0,6653 |
5,604 |
|
а2 |
20,273 |
12,951 |
44,774 |
|
а3 |
36,339 |
4,4513 |
78,363 |
С использованием коэффициентов из уравнения (2) был рассчитан коэффициент насыщения. Расчётные значения удовлетворительно согласуются с экспериментальными данными, демонстрируя среднее относительное отклонение ±3,66%.
Вязкость оказывает значительное влияние на процесс кристаллизации и, особенно на стадию зарождения новой фазы. Результаты экспериментальных данных по вязкости (таблица 1) были представлены графически на рисунке 2.
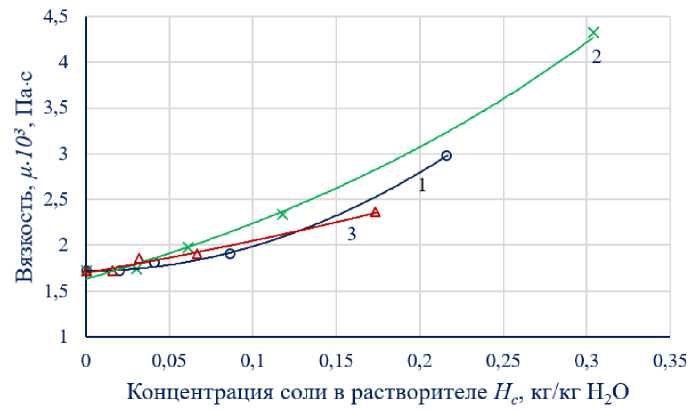
Рисунок 2 – Влияние некоторых солей на вязкость насыщенных растворов лактозы μ :
1 – NaHCО3; 2 – CaCl2; 3 – NaCl.
Исследование вязкости насыщенных растворов лактозы в присутствии солей также выявило две характерные области (рисунок 2). В первой области, при низких концентрациях солей (Нс), вязкость растет незначительно. Во второй области с ростом концентрации наблюдается более интенсивное увеличение вязкости. При этом вязкость насыщенного раствора лактозы с хлоридом кальция хлорида кальция (CaCl₂) возрастает в наибольшей степени.
Экспериментальные данные по вязкости μ насыщенных растворов были аппроксимированы с помощью уравнения:
ц = 1,71 ■ Ю"3 ■ ехр (С-Нс\
где μ – динамический коэффициент вязкости насыщенных растворов лактозы в присутствии добавок, Па<;
Н с - содержание соли в растворителе, кг/кг Н 2 О;
С– коэффициент.
Значения коэффициента С в уравнении (3) представлены в таблице 3.
Таблица 3-Значения коэффициента к в уравнении (3)
|
Добавка |
NaHCО3 |
NaCl |
CaCl2 |
|
Коэффициент С |
2,65 |
1,88 |
3,16 |
По уравнению (2) были рассчитаны значения вязкости насыщенных растворов лактозы в присутствии солей, среднее относительное отклонение расчетных значений от экспериментальных составило ±3,73 %.
Выводы
-
1 .Соли кальция обладают меньшей растворяющей способностью по сравнению с солями натрия.
-
2 .В небольших количествах (менее 5%) соли кальция способны снижать растворимость лактозы и интенсифицировать процесс кристаллизации.
-
3 Анион хлора является более сильным мелассообразователем по сравнению с анионом углекислоты.
-
4 . Установленные закономерности следует учитывать в промышленном производстве молочного сахара.


