Влияние посола сельди на физико-химические и функциональные свойства коллагеновых гидролизатов, полученных из ее кожи
Автор: Рудова Е. А., Куприна Е. Э., Боброва К. В.
Журнал: Вестник Мурманского государственного технического университета @vestnik-mstu
Рубрика: Биотехнология продуктов питания и биологически активных веществ. Пищевые системы
Статья в выпуске: 3 т.28, 2025 года.
Бесплатный доступ
Продукты гидролиза кожи – отходы производства пресервов из сельди соленой – имеют высокий потенциал использования в пищевой промышленности и сельском хозяйстве в качестве добавок, повышающих пищевую ценность продуктов питания и кормов. В работе проведено сравнительное исследование свойств гидролизатов из кожи атлантической сельди соленой и свежемороженой. Гидролиз сырья проводился в среде католита, полученного в результате электролиза воды. Степень гидролиза гидролизата из кожи сельди свежемороженой составила 38,7 0,1 %, из кожи сельди соленой – 52,2 0,2 %. Гидролизат из кожи сельди свежемороженой показал большую пенообразующую способность, чем гидролизат из кожи сельди соленой, 233 3 и 167 3 % соответственно. Однако гидролизат из кожи сельди соленой образовывал более стабильные при хранении пену и жировую эмульсию, что дало возможность рекомендовать его к использованию в эмульсионных продуктах питания. В обоих гидролизатах обнаружены аминокислоты: пролин, глицин, аланин и глутаминовая кислота. Рассчитано содержание коллагена в гидролизатах из кожи сельди соленой и свежемороженой, которое составило 25,1 0,5 и 18,7 0,4 мг/мл соответственно, что позволило рекомендовать гидролизаты, полученные предложенным способом, в качестве добавок, повышающих пищевую ценность продуктов питания и кормов.
Гидролизат коллагена, электрохимический гидролиз, переработка рыбных отходов, сельдь атлантическая, посол сельди, collagen hydrolysate, electrochemical hydrolysis, fish waste processing, Atlantic herring, herring ambassador
Короткий адрес: https://sciup.org/142245684
IDR: 142245684 | УДК: 664.959.5 | DOI: 10.21443/1560-9278-2025-28-3-348-359
Текст статьи Влияние посола сельди на физико-химические и функциональные свойства коллагеновых гидролизатов, полученных из ее кожи
e-mail: , ORCID:
*Saint Petersburg State Institute of Technology (Technical University), Saint Petersburg, Russia; e-mail: , ORCID:
В условиях санкций обеспечение населения РФ продуктами питания собственного производства становится особенно актуальным. Несмотря на то что масштабное производство продуктов питания в крупных городах России было развито уже в XIX в. ( Виноходов, 2025 ) в 90-х годах XX в. из-за развала СССР многие из них были утеряны, в том числе и рыбоперерабатывающие предприятия, поэтому модернизация и обеспечение безотходного цикла производства на них весьма насущны. На территории РФ у потребителей пользуются спросом пресервы из сельди соленой ( Дементьева и др., 2015 ). При их производстве на рыбоперерабатывающих предприятиях образуются отходы, из которых около 10 % приходится на кожу ( Салтанова и др., 2011; Левковская, 2021 ).
Одним из вариантов решения проблемы утилизации кожи сельди является ее переработка в белковый гидролизат ( Байдалинова и др., 2018 ). Преимуществом данного решения является возможность дальнейшего использования гидролизата в пищевой промышленности или сельском хозяйстве для увеличения пищевой ценности продуктов питания и кормов ( Цибизова, 2010; Бодрякова и др., 2022; Мезенова и др., 2015 ). Это становится возможным благодаря высокому содержанию белков в коже сельди, которое колеблется от 14,0 до 20,5 % ( Петров и др., 2012 ). Большая часть белков кожи сельди приходится на коллаген ( Красакова и др., 2018 ), богатый пролином, глицином, аланином, глутаминовой и аспарагиновой кислотами, а также содержащий ценные незаменимые аминокислоты: валин, лизин и лейцин ( Антипова и др., 2019 ). Достоинством переработки кожи сельди гидролизом является переход биологически активных веществ в форму, которая легко усваивается организмом ( Цибизова, 2010 ).
Существуют различные способы гидролиза коллагенсодержащего сырья: ферментативный ( Ярочкин и др., 2012 ), щелочной ( Кременевская и др., 2023 ), кислотный ( Тихонова и др., 2009 ), экстракционный ( Петров и др., 2012 ), электрохимический. Последний способ предполагает взаимодействие сырья с водными растворами электролитов (католитов), полученных в результате электролиза воды в условиях постоянного электрического поля ( Куприна, 2007 ). Особенностями католитов является присутствие в них не только гидроксил ионов, но и восстановительного потенциала, влияющего особым образом на гидролиз тканей.
Электрохимический метод, в отличие от других, не предусматривает использование агрессивных химических реагентов, действует мягко и позволяет избежать потерь биологически активных веществ, в том числе аминокислот ( Кириллов, 2016 ). Поэтому именно электрохимическому гидролизу и отдано предпочтение в данной работе.
Свойства получаемого белкового гидролизата зависят от различных факторов, в том числе от качества кожи. Поэтому актуальным вопросом является изучение влияния на свойства гидролизатов такого фактора, как посол сельди.
Между рыбой и рассолом осуществляется взаимный диффузионно-осмотический перенос влаги и соли ( Димова и др., 2006 ). Также посол сопровождается сложными биохимическими превращениями, в ходе которых происходит изменение природной структуры белков, жиров и экстрактивных веществ, а также их расщепление ( Цибизова, 2010; Альшевская и др., 2021 ).
Научной новизной работы является исследование физико-химических и функциональных характеристик гидролизатов, полученных из отхода производства – кожи сельди атлантической, с использованием католита.
Цель работы – сравнительное исследование свойств гидролизатов из кожи сельди свежемороженой и соленой, полученных с использованием католитов. Для достижения данной цели ставились задачи: изучить кинетику процесса получения католитов, наработать гидролизаты из кожи сельди свежемороженой и соленой, исследовать их физико-химические и функциональные свойства.
Материалы и методы
Сельдь свежемороженая произведена компанией "Любо". Рыба была добыта на Фарерских островах в ноябре 2024 г. В 100 г продукта содержится 17,96 ± 0,05 г белка и 9,04 ± 0,11 г жира. Сельдь изготовлена по требованиям ЕАЭС, номер сертификата N RU Д-RU.РА01.В.02829/251.
Сельдь слабосоленая произведена компанией ООО "Лакифиш". Рыба выловлена в Атлантическом океане в сентябре 2024 г. В 100 г продукта содержится 20,71 ± 0,06 г белка и 14,22 ± 0,13 г жира. Продукт изготовлен по техническим условиям СТО 34313236-007-20242.
Лабораторный электролизер состоит из сульфокатионнообменной мембраны, стального анода и катода из платинированного титана.
Кожу сельди различных способов обработки – сельди атлантической свежемороженой и слабосоленой – получали путем обесшкуривания целой рыбы, далее кожу измельчали до размера частиц не более 10–3 м.
Определение содержания хлорида натрия, влаги, белковых соединений и липидов в коже проводили по ГОСТ 7636-853.
Католит для гидролиза кожи получали согласно последовательности действий:
-
1. Подготовлены 1,0 ± 0,1 % растворы электролитов: NaCl и Na2SO4.
-
2. В электролизер введены электролиты из п.1: в катодную камеру – раствор NaCl, в анодную – Na2SО4. Электролиз растворов проводили при постоянных значениях напряжения и силы тока. Напряжение поддерживали на уровне 14,0 ± 0,1 В. Для изучения кинетики электролиза определяли глубину протекания процессов, с заданной периодичностью осуществляли отбор проб из катодной камеры, измеряя их окислительновосстановительный и водородный потенциалы с использованием рН-метра-милливольтметра модели рН-150МИ. Электролиз завершали по достижении рН ≥ 12,0 ± 0,2.
Гидролиз кожи сельди осуществляли по методике:
-
1. В емкость из термостойкого стекла помещали измельченную кожу и раствор католита в пропорции 1 : 5 (таким образом, гидромодуль получаемого гидролизата 1 : 5). На водяной бане суспензию нагревали до 90 ± 5 °С. При этой температуре смесь выдерживали в течение 60 ± 5 мин, затем охлаждали до комнатной температуры.
-
2. Для удаления нерастворившейся в католите фракции суспензию центрифугировали в течение 30–35 мин при скорости вращения ротора ≥ 3 000 об/мин.
-
3. Затем при помощи хладагентов температуру осветленного раствора снижали до 1–2 °С. При такой температуре жир застывал, в то время как гидролизат сохранял жидкое состояние.
-
4. Далее жировую фракцию отделяли от гидролизата декантацией.
После проведения гидролиза кожи сельди определяли массы полученных фракций.
Перед исследованием свойств гидролизатов их нейтрализовали 15 % HCl до рН 7,0 ± 0,2.
Определение жироэмульгирующей способности проводили в соответствии с модифицированной методикой: равные объемы по 25,0 ± 0,5 мл нейтрализованного гидролизата и дезодорированного подсолнечного масла смешивали в блендере в течение 5 мин для получения однородной эмульсии. В мерном цилиндре в течение суток при температуре 20–25 °С отстаивали полученную смесь. После отстаивания измеряли два показателя: объем масла, которое образовало эмульсию, и объем масла, которое не вошло в состав эмульсии. Жироэмульгирующую способность, выраженную в процентах, рассчитывали как отношение объема эмульгированного масла к общему объему использованного масла4.
Для определения пенообразующей способности использовали модифицированную методику: брали 25,0 ± 0,5 мл нейтрализованного гидролизата и взбивали его в блендере в течение 120–130 с. После этого измеряли, во сколько раз увеличился объем после взбивания по сравнению с изначальным объемом5.
Для оценки устойчивости пены вычисляли отношение объема пены через 30–35 мин после взбивания к объему пены сразу после взбивания.
Содержание аминокислот, входящих в состав белковых гидролизатов, исследовалось методами бумажной хроматографии в соответствии с методическими указаниями "Определение белков и аминокислот в микробной биомассе"6.
Массовая доля пролина оценивалась с помощью методики определения количества аминокислот хроматографическим методом, изложенным в методических указаниях "Определение белков и аминокислот в микробной биомассе"7.
Определение содержания аминного азота в коже свежемороженой и соленой сельди осуществляли методом формольного титрования водных вытяжек из нее в соответствии с методикой пособия "Методы исследования рыбы и рыбных продуктов"8.
Массовую долю аминного азота в процентах Nao для кожи сельди вычисляли по формуле (1)
Nao
V X K X 0,0014 X V X V x 100 m x V x V
где V 1 – объем раствора гидроксида натрия с концентрацией 0,1 моль/дм3, израсходованный на титрование исследуемого образца, см3; V 2 – объем водной вытяжки в мерной колбе, см3; V 3 – объем водной вытяжки, взятый для осаждения белков, см3; V 4 – объем водной вытяжки, взятый для осаждения белков с учетом объема трихлоруксусной кислоты, см3; V 5 – объем фильтрата, взятого на титрование, см3; K – коэффициент пересчета на точный раствор гидроксида натрия с концентрацией 0,1 моль/дм3; m – навеска исследуемого образца, г.
Определение содержания аминного азота в гидролизатах осуществлялось методом формольного титрования9.
Массовую долю аминного азота в процентах N a для гидролизатов вычисляли по формуле (2)
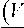
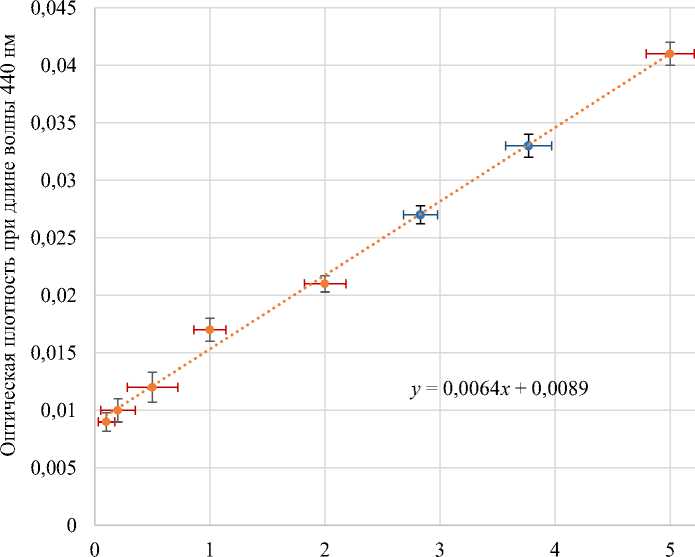
- V )x K x 0,28 X 100
N a
)-----------,------------, (2)
m X 1000
где V – объем раствора гидроксида натрия с концентрацией 0,02 моль/дм3, израсходованный на титрование исследуемого образца, см3; V 1 – объем раствора гидроксида натрия с концентрацией 0,02 моль/дм3, израсходованный на титрование контрольного образца, см3; K – коэффициент пересчета на точный раствор гидроксида натрия с концентрацией 0,02 моль/дм3; 0,28 – количество аминного азота, соответствующее 1 см3 раствора гидроксида натрия с концентрацией 0,02 моль/дм3; 1 000 – коэффициент пересчета мг в г; m – навеска жидкого исследуемого образца, г.
Для определения степени гидролиза использовали формулу (3)
NA =
N a ■ L - N ao N o - N ao
X 100,
где NA – степень гидролиза, %; N о – величина общего азота в сырье; N a – величина аминного азота в гидролизате; Nao – величина аминного азота в сырье до гидролиза; L – коэффициент, характеризующий разбавление исходного сырья.
Результаты и обсуждение
В табл. 1 представлены результаты исследований влияния посола на состав кожи сельди атлантической.
Таблица 1. Состав кожи атлантической сельди соленой и свежемороженой Table 1. The composition of skin of Atlantic herring salted and freshly frozen
|
Анализируемое вещество |
Содержание анализируемого вещества, % |
|
|
Кожа сельди соленой |
Кожа сельди свежемороженой |
|
|
Хлорид натрия |
3,8 ± 0,2 |
0,6 ± 0,1 |
|
Водная фракция |
49,4 ± 0,3 |
52,5 ± 0,3 |
|
Жировая фракция |
24,1 ± 0,2 |
26,0 ± 0,4 |
|
Белковые вещества |
16,3 ± 0,1 |
18,2 ± 0,2 |
|
Аминный азот |
0,16 ± 0,01 |
0,12 ± 0,01 |
Из данных табл. 1 следует, что в результате посола уменьшилось содержание влаги, жира и белковых веществ в коже, что может быть обусловлено, с одной стороны, диффузией хлорида натрия в мышечную ткань, а, с другой стороны, потерей влаги ( Левковская, 2021 ).
Гидролиз кожи проводился в среде католита. Кинетические зависимости значений pH и Eh католита от времени проведения электролиза представлены на рис. 1 и 2. Из данных кинетических кривых следует, что требуемые значения pH 12,1 ± 0,2 и Eh 755 ± 10 мВ были достигнуты за 15 мин электролиза. В работе ( Кириллов, 2016 ) установлено, что наиболее эффективно гидролиз коллагенсодержащего сырья реализуется при указанных физико-химических характеристиках католита.
По предложенной методике из кожи сельди свежемороженой и кожи сельди соленой были получены два гидролизата по 300,0 ± 0,5 мл каждый. Гидролизаты - суспензии с небольшим количеством примесей -разделены на составляющие: жир, нерастворимый остаток и гидролизат. Выходы фракций представлены в табл. 2.
Время, мин
Рис. 1. Зависимость водородного потенциала католита от времени электролиза Fig. 1. Dependence of the hydrogen potential of the catholyte on the electrolysis time
Время, мин
0 2 4 6 8 10 12 14 16
Eh, мВ
окислительно-восстановительного потенциала католита от времени электролиза
Fig. 2. Dependence of the redox potential of the electrolyte on the electrolysis time
Таблица 2. Выходы фракций нутриентов кожи после гидролиза Table 2. Yields of skin nutrient fractions after hydrolysis
|
Фракция |
Содержание фракции, % |
|
|
Образец гидролизата кожи сельди свежемороженой |
Образец гидролизата кожи сельди соленой |
|
|
Гидролизат |
86,9 ± 2,0 |
88,1 ± 2,2 |
|
Жир |
11,1 ± 0,2 |
7,4 ± 0,1 |
|
Нерастворимый остаток |
1,6 ± 0,3 |
1,2 ± 0,1 |
Из данных табл. 2 следует, что посол приводит к снижению содержания жировой фракции в гидролизатах.
Результаты исследования функциональных свойств (жироэмульгирующей и пенообразующей способности) полученных гидролизатов представлены в табл. 3.
Таблица 3. Функциональные свойства гидролизатов из кожи сельди разных способов обработки Table 3. Functional properties of hydrolysates of herring skin obtained by different processing methods
|
Сырье, из которого получен гидролизат |
Функциональные свойства гидролизата |
||
|
Жироэмульгирующая способность, % |
Пенообразующая способность, % |
Устойчивость пены, % |
|
|
Кожа сельди свежемороженой |
100 ± 1 |
233 ± 3 |
86 ± 1 |
|
Кожа сельди соленой |
99 ± 1 |
167 ± 3 |
95 ± 2 |
Жироэмульгирующие способности гидролизатов, полученных из кожи сельди свежемороженой и соленой, существенно не отличаются друг от друга (табл. 3), так же и не отличается внешний вид эмульсий (рис. 3). Для определения стабильности эмульсий их отстаивали при температуре 20–25 °С в течение семи дней. Было обнаружено, что образец с гидролизатом из кожи сельди соленой сохранял более однородную структуру (рис. 4).

а б
Рис. 3. Эмульсии гидролизатов с растительным маслом: а – из свежемороженой кожи, б – из соленой кожи Fig. 3. Emulsions of hydrolysates with vegetable oil: a – from freshly frozen skin, б – from salted skin
Из представленных данных можно сделать вывод, что гидролизат из кожи сельди свежемороженой обладает более высокой способностью к пенообразованию, однако пены и эмульсии, полученные с использованием гидролизата из кожи сельди соленой, оказываются более устойчивыми и стабильными.

а
б
Рис. 4. Эмульсии после отстаивания в течение 7 дней: а – свежемороженая кожа, б – соленая кожа Fig. 4. Emulsions after settling for 7 days: a – freshly frozen skin, б – salted skin
Для оценки аминокислотного состава белковых гидролизатов из кожи сельди свежемороженой и соленой осуществлена их хроматография на бумаге. Было проведено 2 хроматографических анализа.
В результате рассчитаны факторы разделения (Rf) аминокислот-свидетелей и аминокислот белковых гидролизатов – табл. 4 и 5.
Таблица 4. Факторы разделения аминокислот белковых гидролизатов из кожи сельди, определенные по хроматограммам на бумажных дисках
Table 4. Amino acid separation factors of protein hydrolysates from herring skin determined by chromatograms on paper discs
|
Анализируемая аминокислота |
Значение фактора разделения Rf |
|
|
Хроматограмма с исследуемым раствором – гидролизатом из кожи сельди свежемороженой |
Хроматограмма с исследуемым раствором – гидролизатом из кожи сельди соленой |
|
|
Аминокислота-свидетель глицин |
0,63 |
0,53 |
|
Аминокислота-свидетель аланин |
0,80 |
0,77 |
|
Исследуемый раствор, первая аминокислота |
0,56 |
0,57 |
|
Исследуемый раствор, вторая аминокислота |
0,73 |
0,84 |
Таблица 5. Факторы разделения аминокислот белковых гидролизатов из кожи сельди, определенные по хроматограмме на бумаге
Table 5. Amino acid separation factors of protein hydrolysates from herring skin determined by chromatogram on paper
|
Значение фактора разделения Rf |
|||||
|
Аминокислоты-свидетели |
Аминокислоты исследуемого гидролизата из кожи сельди свежемороженой |
Аминокислоты исследуемого гидролизата из кожи сельди соленой |
|||
|
Лизин |
0,22 |
Первая аминокислота |
0,18 |
Первая аминокислота |
0,18 |
|
Аспарагиновая кислота |
0,32 |
Вторая аминокислота |
0,28 |
Вторая аминокислота |
0,28 |
|
Глутаминовая кислота |
0,39 |
Третья аминокислота |
0,39 |
Третья аминокислота |
0,40 |
|
Пролин |
0,46 |
Четвертая аминокислота |
0,46 |
Четвертая аминокислота |
0,49 |
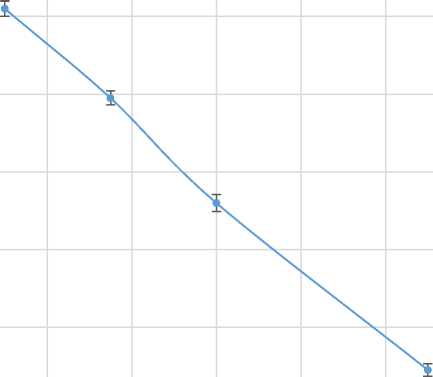
Из данных табл. 4 и 5 следует, что в гидролизатах из кожи соленой и свежемороженой сельди присутствуют ценные аминокислоты: глицин, аланин, пролин и глутаминовая кислота. Учитывая, что пролин является специфической аминокислотой для коллагена ( Антипова и др., 2015; Болгова, 2015 ), с целью определения содержания коллагена в исследуемых гидролизатах проведено количественное определение пролина с помощью бумажной хроматографии. Для этого построен калибровочный график при различных концентрациях пролина, приведенный на рис. 5.
Концентрация пролина, мг/мл
Рис. 5. Калибровочный график зависимости оптической плотности от различных концентраций пролина. Оранжевые точки – калибровочный график. Синие точки – исследуемый гидролизат
Fig. 5. Calibration graph of optical density dependence on different concentrations of proline.
The orange dots are a calibration graph. The blue dots are the hydrolysate under study
По калибровачному графику было определено, что в гидролизате из кожи сельди свежемороженой содержится 3,77 ± 0,20 мг/мл пролина, а в гидролизате из кожи сельди соленой – 2,83 ± 0,15 мг/мл пролина. Так как коллаген по литературным данным содержит около 15 % пролина в своем составе ( Krane, 2008 ), установлено, что содержание коллагена в гидролизате из кожи свежемороженой сельди составило 25,1 ± 0,5 мг/мл, а в гидролизате из кожи соленой сельди – 18,7 ± 0,4 мг/мл.
Для оценки степени гидролиза были определены массовые доли аминного азота в исследуемых гидролизатах (табл. 6).
Таблица 6. Массовая доля аминного азота в исходном сырье и в коллагеновых гидролизатах Table 6. Mass fraction of amino nitrogen in the raw material and in collagen hydrolysates
|
Анализируемое сырье |
Массовая доля аминного азота, % |
|
|
Сельдь свежемороженая |
Сельдь соленая |
|
|
Кожа |
0,12 ± 0,01 |
0,16 ± 0,01 |
|
Гидролизат |
0,20 ± 0,01 |
0,24 ± 0,01 |
Из данных табл. 6 следует, что в результате гидролиза с использованием католита содержание аминного азота в образцах (c учетом разбавления исходного сырья в 6 раз) увеличилось в 9–10 раз. Степень гидролиза, рассчитанная по формуле 3, составила для гидролизата из кожи сельди свежемороженой 38,7 ± 0,1 %, для гидролизата из кожи сельди соленой – 52,2 ± 0,2 %. При этом степень растворения коллагена близка к 99 % (табл. 2).
Заключение
В рамках исследования проанализирован состав кожи сельди соленой и свежемороженой. Установлено, что в результате посола в коже увеличилось содержание хлорида натрия в 6 раз и составило 3,8 %, при этом содержание водной, жировой фракций и белковых веществ снизилось на 3,1; 1,9 и 2,1 % соответственно, что обусловлено диффузией последних в тузлук.
Изучена кинетика изменения pH и Eh католита в процессе его наработки, показано, что требуемые значения pH 12,1 ± 0,2 и Eh 755 ± 10 мВ были достигнуты за 15 мин электролиза.
Установлено, что гидролизат из кожи сельди свежемороженой имел большую пенообразующую способность, чем гидролизат из кожи сельди соленой, 233 ± 3 и 167 ± 3 % соответственно. Однако гидролизат из кожи сельди соленой образовывал более стабильные пену и эмульсию, устойчивость пены гидролизата из кожи сельди свежемороженой составила 86 ± 1 %, гидролизата из кожи сельди соленой – 95 ± 1 %. Большая устойчивость пены и жировой эмульсии, полученных с использованием гидролизата из кожи сельди соленой, вероятно, обусловлена влиянием соли на стабильность систем. Таким образом, гидролизат из кожи сельди соленой можно рекомендовать для использования в производстве эмульсионных продуктов.
В обоих гидролизатах при помощи метода хроматографии на бумаге были обнаружены такие аминокислоты, как пролин, глицин, аланин и глутаминовая кислота. По содержанию пролина в гидролизатах из кожи сельди соленой (2,83 ± 0,15 мг/мл) и свежемороженой (3,77 ± 0,20 мг/мл) рассчитано содержание коллагена в гидролизатах – 25,1 ± 0,5 и 18,7 ± 0,4 мг/мл соответственно, что свидетельствует о наличии пищевой ценности полученных гидролизатов.
Методом формольного титрования были определены массовые доли аминного азота в исходном сырье и полученных гидролизатах, выявлено, что в результате гидролиза с использованием католита содержание аминного азота в образцах увеличилось в 9–10 раз. Степень гидролиза в гидролизате из кожи сельди свежемороженой составила 38,7 ± 0,1 %, в гидролизате из кожи сельди соленой – 52,2 ± 0,2 %, что, вероятно, обусловлено ферментативным гидролизом, происходящим при посоле под действием катепсинов рыбы ( Ахмедова и др., 2016 ).
Таким образом, установлено, что изменения в составе кожи сельди после посола привели к снижению пенообразующей способности гидролизатов из кожи, однако обеспечили повышение устойчивости пен и эмульсий, а также привели к снижению общего содержания белков в гидролизатах и повышению их степени гидролиза.
Коллагеновые гидролизаты из вторичных сырьевых ресурсов, содержащие большое количество пептидов и аминокислот, перспективны для использования в различных сферах пищевой промышленности и сельском хозяйстве. Однако для конкретной области применения необходимо учитывать фактор влияния способа обработки исходного сырья на свойства конечного продукта.


